解题方法
1 . 无机化合物X与Y均由三种相同短周期的非金属元素组成(X比Y的相对分子质量大),常温下均为无色液体,易水解,均产生酸性白雾。取1.35gX与足量水完全反应,向反应后的溶液中滴加1.00 mol·L-1的NaOH溶液40.0mL恰好反应,溶液呈中性,继续滴加BaCl2溶液至过量,产生不溶于稀盐酸的2.33g白色沉淀。Y水解得到两种产物,其物质的量之比1:2,且产物之一能使品红溶液褪色。请回答:
(1)X的化学式______________ 。白色沉淀属于_____________ (填“强”、“弱”或“非”)电解质。
(2)Y与水反应的化学方程式_________________ 。
(3)二元化合物Z能与X化合生成Y。一定条件下,0.030 mol Z与足量氨反应生成0.92gA(原子个数之比1:1,其相对分子量为184)和淡黄色单质B及离子化合物M,且M的水溶液的pH<7。将0.92gA隔绝空气加强热可得到0.64gB和气体单质C。
①写出Z与足量氨反应的化学方程式____________ 。
②亚硝酸钠和M固体在加热条件下_____________ (填“可能”或“不能”)发生反应,判断理由是_________________ 。
③请设计检验离子化合物M中阳离子的实验方案:_________________ 。
(1)X的化学式
(2)Y与水反应的化学方程式
(3)二元化合物Z能与X化合生成Y。一定条件下,0.030 mol Z与足量氨反应生成0.92gA(原子个数之比1:1,其相对分子量为184)和淡黄色单质B及离子化合物M,且M的水溶液的pH<7。将0.92gA隔绝空气加强热可得到0.64gB和气体单质C。
①写出Z与足量氨反应的化学方程式
②亚硝酸钠和M固体在加热条件下
③请设计检验离子化合物M中阳离子的实验方案:
您最近一年使用:0次
名校
2 . 高锰酸钾是锰的重要化合物和常用的氧化剂。以下是工业上用软锰矿制备高锰酸钾的一种工艺流程:
(1) KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列_____ 物质相似。
A.75%酒精 B.双氧水 C.苯酚 D.“84”消毒液(NaClO溶液)
(2)操作Ⅰ的名称是________ ;操作Ⅱ是根据KMnO4和K2CO3两物质在__________ (填性质)上差异,采用 __________ (填操作步骤)、趁热过滤得到KMnO4粗晶体的。
(3)上述流程中可以循环使用的物质有石灰、CO2、____ 和____ (写化学式)。
(4) 向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是_______ 。
(5) 铋酸钠(NaBiO3,不溶于水)用于定性检验酸性溶液中Mn2+的存在(铋元素的还原产物为Bi3+,Mn的氧化产物为+7价),写出反应的离子方程式:__________________ 。
(6) 写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:________________ 。
(7)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得_____ mol KMnO4。

(1) KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列
A.75%酒精 B.双氧水 C.苯酚 D.“84”消毒液(NaClO溶液)
(2)操作Ⅰ的名称是
(3)上述流程中可以循环使用的物质有石灰、CO2、
(4) 向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是
(5) 铋酸钠(NaBiO3,不溶于水)用于定性检验酸性溶液中Mn2+的存在(铋元素的还原产物为Bi3+,Mn的氧化产物为+7价),写出反应的离子方程式:
(6) 写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:
(7)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得
您最近一年使用:0次
2019-09-24更新
|
1216次组卷
|
3卷引用:湖北省宜昌市部分示范高中教学协作体2020届高三9月联考化学试题
3 . 含有a mol FeI2的溶液中,通入x mol Cl2。下列各项为通入Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是
| A.x≤a,2I−+Cl2=I2+2Cl− |
| B.x=1.2a,10Fe2++14I−+12Cl2=10Fe3++7I2+24Cl− |
| C.x=1.4a,4Fe2++10I−+7Cl2=4Fe3++5I2+14Cl− |
| D.x≥1.5a,2Fe2++4I−+3Cl2=2Fe3++2I2+6Cl− |
您最近一年使用:0次
2019-07-07更新
|
1335次组卷
|
3卷引用:辽宁省凤城市第一中学2018-2019学年高二6月月考化学试题
名校
4 . 汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3=K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则下列判断不正确的是
| A.生成44.8L N2(标准状况) |
| B.有0.25 mol KNO3被还原 |
| C.转移电子的物质的量为1.75mol |
| D.被氧化的N原子的物质的量为3.75mol |
您最近一年使用:0次
2019-07-05更新
|
9182次组卷
|
8卷引用:黑龙江省鹤岗市第一中学2020-2021学年高二6月月考化学试题
名校
5 . 碱性锌锰电池的工作原理:Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2,其中的电解质溶液是KOH溶液。某课题组用废旧铁壳无汞碱性锌锰电池为原料,制备一种新型材料——MnxZn(1−x)Fe2O4,其工艺流程如图所示:
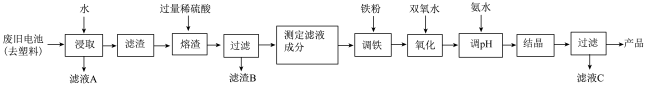
(1)已知MnxZn(1−x)Fe2O4中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中的锰相同,则铁元素的化合价为___________ 。
(2)滤液A中溶质的电子式为___________ 。
(3)“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将+3价锰的化合物全部还原成Mn2+,写出该反应的离子方程式:___________________________________ 。
(4)“调铁”工序的目的是调整滤液中铁离子的总浓度,使其中金属元素的物质的量之比与产品的化学式MnxZn(1−x)Fe2O4相符合。
①写出“调铁”工序中发生反应的离子方程式:__________________ 、_______________ 。
②若测得滤液的成分为c(Mn2+)+c(Zn2+)=a mol·L−1,c(Fe2+)+c(Fe3+)=b mol·L−1,滤液体积为1m3,“调铁”工序中,需加入的铁粉质量为___________ kg(忽略溶液体积变化,用含a、b的代数式表示)。
(5)在“氧化”工序中,加入双氧水的目的是_________________ ,生产过程中发现实际消耗双氧水的量大于理论值,其可能原因除温度外,主要是______________________ 。
(6)用氨水“调pH”后,经“结晶”、“过滤”可得到产品和滤液C(C为正盐),从滤液C中还可分离出一种氮肥,该氮肥的溶液中离子浓度由大到小的排序为_____________ 。

(1)已知MnxZn(1−x)Fe2O4中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中的锰相同,则铁元素的化合价为
(2)滤液A中溶质的电子式为
(3)“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将+3价锰的化合物全部还原成Mn2+,写出该反应的离子方程式:
(4)“调铁”工序的目的是调整滤液中铁离子的总浓度,使其中金属元素的物质的量之比与产品的化学式MnxZn(1−x)Fe2O4相符合。
①写出“调铁”工序中发生反应的离子方程式:
②若测得滤液的成分为c(Mn2+)+c(Zn2+)=a mol·L−1,c(Fe2+)+c(Fe3+)=b mol·L−1,滤液体积为1m3,“调铁”工序中,需加入的铁粉质量为
(5)在“氧化”工序中,加入双氧水的目的是
(6)用氨水“调pH”后,经“结晶”、“过滤”可得到产品和滤液C(C为正盐),从滤液C中还可分离出一种氮肥,该氮肥的溶液中离子浓度由大到小的排序为
您最近一年使用:0次
2019-07-04更新
|
255次组卷
|
2卷引用:四川省成都市蒲江县蒲江中学2021-2022学年高二下学期5月月考化学试题
真题
名校
6 . 聚合硫酸铁[Fe(OH)SO4]n能用作净水剂(絮凝剂),可由绿矾(FeSO4·7H2O)和KClO3在水溶液中反应得到。下列说法不正确 的是
| A.KClO3作氧化剂,每生成1 mol [Fe(OH)SO4]n消耗6/n mol KClO3 |
| B.生成聚合硫酸铁后,水溶液的pH增大 |
| C.聚合硫酸铁可在水中形成氢氧化铁胶体而净水 |
| D.在相同条件下,Fe3+比[Fe(OH)]2+的水解能力更强 |
您最近一年使用:0次
2019-04-12更新
|
5924次组卷
|
36卷引用:湖南省长沙市第一中学2020届高三第一次月考化学试题
湖南省长沙市第一中学2020届高三第一次月考化学试题江西省宜春市奉新县第一中学2020届高三上学期第二次月考化学试题黑龙江省牡丹江市第一高级中学2020届高三10月月考化学试题江西省吉安市五校2019-2020学年高二上学期第二次联考化学试题安徽省池州市第一中学2020-2021学年高二12月月考化学试题上海交通大学附属中学2021届高三下学期3月月考化学试题湖南省长沙市雅礼中学2022-2023学年高三上学期第五次月考化学试题湖南省株洲市第四中学2023届高三第六次月考化学试题重庆市万州第二高级中学2022-2023学年高三下学期5月月考化学试题北京市第八十中学2024届高三上学期10月月考化学试题化学江苏省扬州市宝应区2023-2024学年曹甸高级中学高三上学期9月化学试卷2019年4月浙江省普通高校招生选考科目考试化学试题福建省华安一中2018-2019学年高二下学期期末考试化学试题河北省邯郸市2019-2020学年高三上学期期中考试化学试题2020届高考化学小题狂练(全国通用版)专练5 氧化还原反应辽宁省抚顺市第一中学2020届高三上学期期中考试化学试题2020届高三化学化学二轮复习——高考常考题:氧化还原反应的实际应用【精编选择25题】专题1.3 氧化还原反应(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升(已下线)专题六 元素化合物的性质、应用及转化(真题汇编)-2020年高考二轮模块化复习之《元素化合物》名师讲案与提分特训(已下线)小题必刷08 氧化还原反应的规律及应用——2021年高考化学一轮复习小题必刷(通用版)广东省佛山市第一中学2020-2021学年高二上学期期中考试化学(选考)试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)课时17 铁及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)3.3.1 盐类的水解-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)专题05.元素及其化合物-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)考向26 盐类的水解-备战2022年高考化学一轮复习考点微专题(已下线)考点04 氧化还原反应-备战2022年高考化学学霸纠错(全国通用)(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)考点14 铁及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)第三章 金属及其化合物 第13讲 铁及其重要化合物(已下线)题型27 铁及其化合物的性质、用途及相关计算新疆喀什地区伽师县2022-2023学年高三上学期11月期中考试化学试题(已下线)2019年高考浙江卷化学试题变式题(单选题21-25)
7 . I.在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)一定温度下,向1 L 0.l mol·L-1 CH3 COOH溶液中加入0.1 molCH3COONa固体,溶液中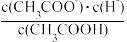
_______ (填“增大”、“减小”或“不变”);溶液中各微粒浓度由大到小的顺序为:_______
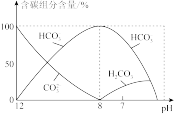
(2)常温下,向20 ml0.1mol/LNa2CO3溶液中逐滴加入0.1mol/LHCl溶液40 mL,溶液中含碳元素的微粒(CO2)因逸出未画出)物质的量分数随溶液pH变化的情况如下:
回答下列问题:
①所得溶液中含量最多的三种微粒的物质的量浓度的大小关系为_______
②已知在25℃时,CO 水解反应的平衡常数即水解常数Kh=2×10-4mol/L,当溶液中c(HCO
水解反应的平衡常数即水解常数Kh=2×10-4mol/L,当溶液中c(HCO ):c(CO
):c(CO )=2:1时,溶液的pH=
)=2:1时,溶液的pH=_______ 。
Ⅱ.金属表面处理、皮革鞣制、印染等都可能造成铬污染。六价铬比三价铬毒性强,更易被人体吸收且在体内蓄积。工业上处理酸性含Cr2O 废水的方法如下:
废水的方法如下:
(1)向含Cr2O 的酸性废水中加入FeSO4溶液,使Cr2O72-全部转化为Cr3+。写出该反应的离子方程式:
的酸性废水中加入FeSO4溶液,使Cr2O72-全部转化为Cr3+。写出该反应的离子方程式:_______ 。
(2)调节溶液的pH,使Cr3+完全沉淀。25℃时,若调节溶液的pH=8,则溶液中残余Cr3+的物质的量浓度为_______ mol/L(已知25℃时,Ksp[Cr(OH) 3]=6.3×10-31)。
(3)铬元素总浓度的测定:准确移取25.00 mL含Cr2O72-和Cr3+的酸性废水,向其中加入足量的(NH4)2S2O8溶液将Cr3+氧化成Cr2O ,煮沸除去过量的(NH4)2S2O8;向上述溶液中加入过量的KI溶液,充分反应后,以淀粉为指示剂,向其中滴加0.015 mol/L的Na2 S2O3标准溶液,终点时消耗Na2S2O3溶液20.00 ml)。计算废水中铬元素总浓度
,煮沸除去过量的(NH4)2S2O8;向上述溶液中加入过量的KI溶液,充分反应后,以淀粉为指示剂,向其中滴加0.015 mol/L的Na2 S2O3标准溶液,终点时消耗Na2S2O3溶液20.00 ml)。计算废水中铬元素总浓度_______ (单位:mg/L,写出计算过程)。 已知测定过程中发生的反应如下:
①2Cr3++3S2O +7H2O= Cr2O
+7H2O= Cr2O +6SO
+6SO +14H+
+14H+
②Cr2O +6I-+14H+=2Cr3++3I2+7H2O
+6I-+14H+=2Cr3++3I2+7H2O
③I2+ S2O = 2I-+ S4O
= 2I-+ S4O
(1)一定温度下,向1 L 0.l mol·L-1 CH3 COOH溶液中加入0.1 molCH3COONa固体,溶液中
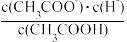
(2)常温下,向20 ml0.1mol/LNa2CO3溶液中逐滴加入0.1mol/LHCl溶液40 mL,溶液中含碳元素的微粒(CO2)因逸出未画出)物质的量分数随溶液pH变化的情况如下:

回答下列问题:
①所得溶液中含量最多的三种微粒的物质的量浓度的大小关系为
②已知在25℃时,CO
 水解反应的平衡常数即水解常数Kh=2×10-4mol/L,当溶液中c(HCO
水解反应的平衡常数即水解常数Kh=2×10-4mol/L,当溶液中c(HCO ):c(CO
):c(CO )=2:1时,溶液的pH=
)=2:1时,溶液的pH=Ⅱ.金属表面处理、皮革鞣制、印染等都可能造成铬污染。六价铬比三价铬毒性强,更易被人体吸收且在体内蓄积。工业上处理酸性含Cr2O
 废水的方法如下:
废水的方法如下:(1)向含Cr2O
 的酸性废水中加入FeSO4溶液,使Cr2O72-全部转化为Cr3+。写出该反应的离子方程式:
的酸性废水中加入FeSO4溶液,使Cr2O72-全部转化为Cr3+。写出该反应的离子方程式:(2)调节溶液的pH,使Cr3+完全沉淀。25℃时,若调节溶液的pH=8,则溶液中残余Cr3+的物质的量浓度为
(3)铬元素总浓度的测定:准确移取25.00 mL含Cr2O72-和Cr3+的酸性废水,向其中加入足量的(NH4)2S2O8溶液将Cr3+氧化成Cr2O
 ,煮沸除去过量的(NH4)2S2O8;向上述溶液中加入过量的KI溶液,充分反应后,以淀粉为指示剂,向其中滴加0.015 mol/L的Na2 S2O3标准溶液,终点时消耗Na2S2O3溶液20.00 ml)。计算废水中铬元素总浓度
,煮沸除去过量的(NH4)2S2O8;向上述溶液中加入过量的KI溶液,充分反应后,以淀粉为指示剂,向其中滴加0.015 mol/L的Na2 S2O3标准溶液,终点时消耗Na2S2O3溶液20.00 ml)。计算废水中铬元素总浓度①2Cr3++3S2O
 +7H2O= Cr2O
+7H2O= Cr2O +6SO
+6SO +14H+
+14H+②Cr2O
 +6I-+14H+=2Cr3++3I2+7H2O
+6I-+14H+=2Cr3++3I2+7H2O③I2+ S2O
 = 2I-+ S4O
= 2I-+ S4O
您最近一年使用:0次
8 . 碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2,该反应的还原产物为_______ 。
(2)上述浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中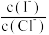 为:
为:_______ ,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
(3)已知反应2HI(g) =H2(g) + I2(g)的ΔH= +11kJ·mol-1,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为_______ kJ。
(4)Bodensteins研究了下列反应:2HI(g)⇌H2(g) + I2(g)
在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
①根据上述实验结果,该反应的平衡常数K的计算式为:_______ 。
②上述反应中,正反应速率为v正= k正·x2(HI),逆反应速率为v逆=k逆·x(H2)·x(I2),其中k正、k逆为速率常数,则k逆为_______ (以K和k正表示)。若k正 = 0.0027min-1,在t=40min时,v正=_______ min-1
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为_______ (填字母)

(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2,该反应的还原产物为
(2)上述浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中
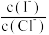 为:
为:(3)已知反应2HI(g) =H2(g) + I2(g)的ΔH= +11kJ·mol-1,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为
(4)Bodensteins研究了下列反应:2HI(g)⇌H2(g) + I2(g)
在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为:
②上述反应中,正反应速率为v正= k正·x2(HI),逆反应速率为v逆=k逆·x(H2)·x(I2),其中k正、k逆为速率常数,则k逆为
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为

您最近一年使用:0次
2019-01-30更新
|
7110次组卷
|
9卷引用:四川省南充市阆中中学2018-2019学年高二6月月考理科综合化学试题
9 . [化学-选修2:化学与技术]
双氧水是一种重要的氧化剂、漂白剂和消毒剂。生产双氧水常采用蒽醌法,其反应原理和生产流程如图所示:

A.氢化釜 B.过滤器 C.氧化塔 D.萃取塔 E.净化塔 F.工作液再生装置 G.工作液配制装置
生产过程中,把乙基蒽醌溶于有机溶剂配制成工作液,在一定的温度、压力和催化剂作用下进行氢化,再经氧化、萃取、净化等工艺得到双氧水。回答下列问题:
(1)蒽醌法制备双氧水理论上消耗的原料是_______ ,循环使用的|原料是______ ,配制工作液时采用有机溶剂而不采用水的原因是______ 。
(2)氢化釜A中反应的化学方程式为_______ ,进入氧化塔C的反应混合液中的主要溶质为_______ 。
(3)萃取塔D中的萃取剂是____ ,选择其作萃取剂的原因是______ 。
(4)工作液再生装置F中要除净残留的H2O2,原因是______ 。
(5)双氧水浓度可在酸性条件下用KMnO4溶液测定,该反应的离子方程式为_______ 。一种双氧水的质量分数为27.5%,(密度为1.10g·cm3),其浓度为______ mol/L。
双氧水是一种重要的氧化剂、漂白剂和消毒剂。生产双氧水常采用蒽醌法,其反应原理和生产流程如图所示:

A.氢化釜 B.过滤器 C.氧化塔 D.萃取塔 E.净化塔 F.工作液再生装置 G.工作液配制装置
生产过程中,把乙基蒽醌溶于有机溶剂配制成工作液,在一定的温度、压力和催化剂作用下进行氢化,再经氧化、萃取、净化等工艺得到双氧水。回答下列问题:
(1)蒽醌法制备双氧水理论上消耗的原料是
(2)氢化釜A中反应的化学方程式为
(3)萃取塔D中的萃取剂是
(4)工作液再生装置F中要除净残留的H2O2,原因是
(5)双氧水浓度可在酸性条件下用KMnO4溶液测定,该反应的离子方程式为
您最近一年使用:0次
2019-01-30更新
|
2868次组卷
|
5卷引用:2017届云南省玉溪一中高三上学期第二次月考化学试卷
2013·河北石家庄·二模
10 . 世界环保联盟建议全面禁止使用氯气用于饮用水的消毒,而建议采用高效“绿色” 消毒剂二氧化氯。二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或加热。实验室以电解法制备C1O2的流程如下:
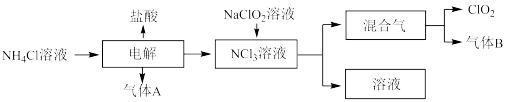
(1)C1O2中所有原子______(填“是”或“不是”)都满足8电子结构。上图所示电解法制得的产物中杂质气体B能使石蕊试液显蓝色,除去杂质气体可选用______
(2)稳定性二氧化氯是为推广二氧化氯而开发的新型产品,下列说法正确的是______(填选项字母)。
(3)欧洲国家主要采用氯酸钠氧化浓盐酸制备,化学方程式为______ 。此法缺点主要是产率低、产品难以分离,还可能污染环境。
(4)我国广泛采用经干燥空气稀释的氯气与固体亚氯酸钠(NaClO2)反应制备,化学方程式为______ 此法相比欧洲方法的优点是______ 。
(5)科学家又研究出了一种新的制备方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸钠,化学方程式为______ 。此法提高了生产及储存、运输的安全性,原因是______

(1)C1O2中所有原子______(填“是”或“不是”)都满足8电子结构。上图所示电解法制得的产物中杂质气体B能使石蕊试液显蓝色,除去杂质气体可选用______
| A.饱和食盐水B.碱石灰 C.浓硫酸D.蒸馏水 |
| A.二氧化氯可广泛用于工业和饮用水处理 |
| B.二氧化氯应用在食品工业中能有效地延长食品贮藏期 |
| C.稳定性二氧化氯的出现大大增加了二氧化氯的使用范围 |
| D.在工作区和成品储藏室内,要有通风装置和检测及警报装置 |
(4)我国广泛采用经干燥空气稀释的氯气与固体亚氯酸钠(NaClO2)反应制备,化学方程式为
(5)科学家又研究出了一种新的制备方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸钠,化学方程式为
您最近一年使用:0次
2019-01-30更新
|
1052次组卷
|
6卷引用:2016届黑龙江省哈尔滨三中高三上第三次检测理综化学试卷
2016届黑龙江省哈尔滨三中高三上第三次检测理综化学试卷2016届河南省三门峡市陕州中学高三下学期尖子生专题训练五化学试卷(已下线)2013届河北省石家庄市高中毕业班第二次模拟考试理综化学试卷(已下线)2014届湖北省孝感市高三第二次统考理综化学试卷(已下线)2014届江西省金溪一中高三理科综合训练题(三)化学试卷(已下线)2013届江西省临川一中高三最后一次模拟考试理科综合试卷



