2013·上海·零模
解题方法
1 . 无机非金属材料、金属材料和有机高分子材料并称为三大材料,是发展高新技术的基石,在未来科技发展中发挥着重要的作用。新型材料α-Fe粉具有超强的磁性能,用作高密度磁记录的介质以及高效催化剂等。将5.60 g α-Fe粉与一定量水蒸气在高温下反应一定时间后冷却,其质量变为6.88 g。
(1)产生的氢气的体积为_________ mL(标准状况下)。
(2)将冷却后的固体物质放入足量FeCl3溶液中充分反应(已知Fe3O4不溶于FeCl3溶液),计算最多消耗FeCl3的物质的量。____________
(3)Nierite是一种高熔点高硬度的陶瓷材料。Nierite的摩尔质量为140 g/mol,其中硅元素的质量分数为60%。已知1 mol NH3与足量的化合物T充分反应后可得到35 g Nierite与3 mol HCl气体。Nierite的化学式为___________ 。T的化学式为____________ 。
(4)K金是常见的贵金属材料,除黄金外,还含有银、铜中的一种或两种金属。为测定某18K金样品的组成,将2.832 g样品粉碎后投入足量的浓硝酸中,充分溶解后,收集到NO2和N2O4的混合气体224 mL(折算至标准状况,下同),将该混合气体与84 mL O2混合后缓缓通入水中,恰好被完全吸收。
①混合气体的平均摩尔质量为______________ 。
②填写该18K金的成分表(精确至0.01%,若不含该金属则填0)。
(5)有机高分子材料聚酯纤维可由二酸与二醇通过缩聚形成。如100个乙二酸分子与100个乙二醇分子发生缩聚,当形成一条聚酯链时,其(平均)式量达到最大(如图所示,其式量为11618)。
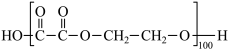
为降低聚酯链的长度与平均式量,可调整乙二酸与乙二醇的相对用量,使形成的聚酯链两端均为相同基团,从而无法再连接增长。现有100个乙二酸分子与105个乙二醇分子恰好完全反应,且聚酯链无法再增长。
①共形成_____ 条聚酯链。
②计算所得聚酯的平均式量。_______________
(1)产生的氢气的体积为
(2)将冷却后的固体物质放入足量FeCl3溶液中充分反应(已知Fe3O4不溶于FeCl3溶液),计算最多消耗FeCl3的物质的量。
(3)Nierite是一种高熔点高硬度的陶瓷材料。Nierite的摩尔质量为140 g/mol,其中硅元素的质量分数为60%。已知1 mol NH3与足量的化合物T充分反应后可得到35 g Nierite与3 mol HCl气体。Nierite的化学式为
(4)K金是常见的贵金属材料,除黄金外,还含有银、铜中的一种或两种金属。为测定某18K金样品的组成,将2.832 g样品粉碎后投入足量的浓硝酸中,充分溶解后,收集到NO2和N2O4的混合气体224 mL(折算至标准状况,下同),将该混合气体与84 mL O2混合后缓缓通入水中,恰好被完全吸收。
①混合气体的平均摩尔质量为
②填写该18K金的成分表(精确至0.01%,若不含该金属则填0)。
| 18K金成分 | Au | Ag | Cu |
| 含量(质量分数) | 75.00% |
(5)有机高分子材料聚酯纤维可由二酸与二醇通过缩聚形成。如100个乙二酸分子与100个乙二醇分子发生缩聚,当形成一条聚酯链时,其(平均)式量达到最大(如图所示,其式量为11618)。
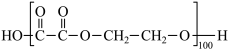
为降低聚酯链的长度与平均式量,可调整乙二酸与乙二醇的相对用量,使形成的聚酯链两端均为相同基团,从而无法再连接增长。现有100个乙二酸分子与105个乙二醇分子恰好完全反应,且聚酯链无法再增长。
①共形成
②计算所得聚酯的平均式量。
您最近一年使用:0次
2014·上海杨浦·三模
2 . 氯、磷的化合物广泛用于农药、医药、染料等领域。
(1)PCl3与氯气、水反应,得到HCl气体和一种无色透明有刺激性臭味的液体X,实验测定,1mol的H2O完全反应会生成2mol的HCl,则X的组成元素是___ ;已知X的相对分子质量为153.5,则X的化学式为___ 。
(2)X在高温与O2发生反应,形成P4O10(固态)和Cl2。将3.07gX与448mLO2(已折算至标准状况,下同)在高温下充分反应后,生成Cl2___ mol,气体的体积将变为___ mL。
(3)白磷在氯气中燃烧,一般得到PCl3和PCl5的混合物。2.480g白磷(P4),与一定量的氯气恰好完全反应,产物的总质量为14.550g,计算产物中PCl3的质量分数___ (保留4位有效数字)。
(4)PCl3和PCl5能发生如下水解反应:PCl3+3H2O→H3PO3+3HCl;PCl5+4H2O→H3PO4+5HCl
现将一定量的PCl3和PCl5混合物溶于足量水中,在加热条件下缓缓通入0.020molO2,恰好将H3PO3氧化为H3PO4。往反应后的溶液中加入15.725gCa(OH)2,充分反应后磷元素全部转化为Ca3(PO4)2沉淀,过滤后得到2.5L滤液,测得pH为12。计算:
①Ca3(PO4)2(已知式量310)沉淀的质量___ ;
②滤液中溶质的物质的量浓度___ 。
(1)PCl3与氯气、水反应,得到HCl气体和一种无色透明有刺激性臭味的液体X,实验测定,1mol的H2O完全反应会生成2mol的HCl,则X的组成元素是
(2)X在高温与O2发生反应,形成P4O10(固态)和Cl2。将3.07gX与448mLO2(已折算至标准状况,下同)在高温下充分反应后,生成Cl2
(3)白磷在氯气中燃烧,一般得到PCl3和PCl5的混合物。2.480g白磷(P4),与一定量的氯气恰好完全反应,产物的总质量为14.550g,计算产物中PCl3的质量分数
(4)PCl3和PCl5能发生如下水解反应:PCl3+3H2O→H3PO3+3HCl;PCl5+4H2O→H3PO4+5HCl
现将一定量的PCl3和PCl5混合物溶于足量水中,在加热条件下缓缓通入0.020molO2,恰好将H3PO3氧化为H3PO4。往反应后的溶液中加入15.725gCa(OH)2,充分反应后磷元素全部转化为Ca3(PO4)2沉淀,过滤后得到2.5L滤液,测得pH为12。计算:
①Ca3(PO4)2(已知式量310)沉淀的质量
②滤液中溶质的物质的量浓度
您最近一年使用:0次
解题方法
3 . 铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料,已知Pb的化合价只有0、+2、+4。回答下列问题:
(1)PbO2和PbO的混合物中,Pb和O的物质的量之比为8:11,则混合物中,PbO2和PbO的物质的量之比为___ 。
(2)用足量的CO还原13.7g某铅氧化物,把生成的CO2全部通入到过量的澄清石灰水中,得到的沉淀干燥后质量为8.0g,则此铅氧化物的化学式可表示为___ 。
(3)PbO2具有强氧化性,能氧化浓HCl生成Cl2,+4价的Pb被还原成+2价的Pb,+2价的Pb不具备该性质,据下列信息回答问题:①将amolPbO2加热分解一段时间,生成PbO和O2;②将①所得固体加入足量的浓盐酸,收集产生的Cl2;已知在①加热一段时间后剩余的固体中,+2价的Pb占铅元素质量分数为x;则反应过程中生成的氧气和氯气物质的量总和是多少___ ?
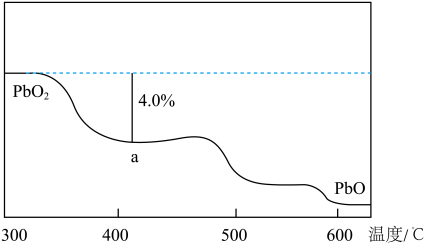
(4)PbO2在加热过程发生分解的失重曲线如图所示,已知失重曲线上的a点为样品失重4.0%【(即样品起始质量—a点固体质量)/样品起始质量×100%】的残留固体。若a点固体组成表示为PbOx或mPbO2·nPbO,列式计算x值和m:n值___ 、___ 。
(1)PbO2和PbO的混合物中,Pb和O的物质的量之比为8:11,则混合物中,PbO2和PbO的物质的量之比为
(2)用足量的CO还原13.7g某铅氧化物,把生成的CO2全部通入到过量的澄清石灰水中,得到的沉淀干燥后质量为8.0g,则此铅氧化物的化学式可表示为
(3)PbO2具有强氧化性,能氧化浓HCl生成Cl2,+4价的Pb被还原成+2价的Pb,+2价的Pb不具备该性质,据下列信息回答问题:①将amolPbO2加热分解一段时间,生成PbO和O2;②将①所得固体加入足量的浓盐酸,收集产生的Cl2;已知在①加热一段时间后剩余的固体中,+2价的Pb占铅元素质量分数为x;则反应过程中生成的氧气和氯气物质的量总和是多少
(4)PbO2在加热过程发生分解的失重曲线如图所示,已知失重曲线上的a点为样品失重4.0%【(即样品起始质量—a点固体质量)/样品起始质量×100%】的残留固体。若a点固体组成表示为PbOx或mPbO2·nPbO,列式计算x值和m:n值

您最近一年使用:0次
2010·河南郑州·二模
名校
解题方法
4 . amolFeS与bmolFe3O4投入到VL cmol/L的硝酸溶液中恰好完全反应,假设只产生NO气体。所得澄清溶液的成分是Fe(NO3)3和H2SO4的混合液,则反应中未被 还原的硝酸为
A. |
| B.(a+3b)mol |
C. |
| D.(cV-3a-9b)mol |
您最近一年使用:0次
2020-03-21更新
|
1035次组卷
|
9卷引用:2010年河南省郑州外国语学校全真模拟(二)(理科综合)化学部分
(已下线)2010年河南省郑州外国语学校全真模拟(二)(理科综合)化学部分(已下线)2010年河南省郑州外国语学校高三上学期9月月考化学试题(已下线)2014高考化学二轮专题突破 专题四氧化还原反应练习卷(已下线)2014高考名师推荐化学氧化还原规律(已下线)2015届云南省玉溪一中高三上学期第一次月考化学试卷(已下线)2015届湖南省衡阳八中高三上学期第四次月考化学试卷上海市嘉定区2016届高三第一次质量调研化学试题江西省临川一中暨临川一中实验学校2021-2022学年高二下学期第二次月考化学试题新疆维吾尔自治区和田地区和田县2022-2023学年高三上学期11月期中考试化学试题
名校
解题方法
5 . 某溶液中有S2-、SO32-、Br-、I-四种阴离子各0.1mol。现通入Cl2,则通入Cl2的体积(标准状况)和溶液中相关离子的物质的量的关系图正确的是
A. | B.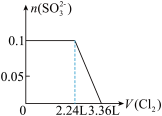 |
C.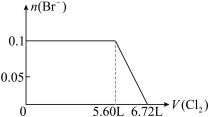 | D.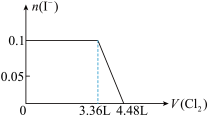 |
您最近一年使用:0次
2020-03-21更新
|
2521次组卷
|
5卷引用:上海市普陀区2016届高三下学期质量调研化学试题
上海市普陀区2016届高三下学期质量调研化学试题(已下线)小题必刷05 离子检验与推断——2021年高考化学一轮复习小题必刷(通用版)重庆市第二十九中学2021届高三上学期10月月考化学试题(已下线)练习6 常见物质的检验-2020-2021学年【补习教材·寒假作业】高一化学(苏教版)河北省昌黎第一中学2023届高三上学期第二次调研考试化学试题
名校
6 . 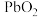 是褐色固体,受热分解为Pb的
是褐色固体,受热分解为Pb的 和
和 价的混合氧化物,
价的混合氧化物, 价的Pb能氧化浓盐酸生成
价的Pb能氧化浓盐酸生成 ,
, 价的Pb还原成
价的Pb还原成 价的Pb;现将
价的Pb;现将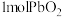 加热分解得到
加热分解得到 ,向剩余固体中加入足量的浓盐酸得到
,向剩余固体中加入足量的浓盐酸得到 ,
, 和
和 的物质的量之比为
的物质的量之比为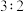 ,则剩余固体的组成及物质的量比是
,则剩余固体的组成及物质的量比是
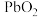 是褐色固体,受热分解为Pb的
是褐色固体,受热分解为Pb的 和
和 价的混合氧化物,
价的混合氧化物, 价的Pb能氧化浓盐酸生成
价的Pb能氧化浓盐酸生成 ,
, 价的Pb还原成
价的Pb还原成 价的Pb;现将
价的Pb;现将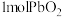 加热分解得到
加热分解得到 ,向剩余固体中加入足量的浓盐酸得到
,向剩余固体中加入足量的浓盐酸得到 ,
, 和
和 的物质的量之比为
的物质的量之比为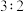 ,则剩余固体的组成及物质的量比是
,则剩余固体的组成及物质的量比是A. 混合的 混合的 、 、 | B.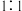 混合的 混合的 、PbO 、PbO |
C.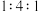 混合的 混合的 、 、 、PbO 、PbO | D.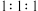 混合的 混合的 、 、 、PbO 、PbO |
您最近一年使用:0次
2020-02-06更新
|
1474次组卷
|
5卷引用:2016-2017学年黑龙江大庆实验中学高一12月月考化学卷
解题方法
7 . 向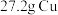 和
和 的混合物中加入某浓度的稀硝酸
的混合物中加入某浓度的稀硝酸 ,固体物质完全反应,得到标准状况下
,固体物质完全反应,得到标准状况下 和
和 的混合气体及
的混合气体及 。在所得溶液中加入
。在所得溶液中加入 的NaOH溶液
的NaOH溶液 ,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为
,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为 。下列有关说法正确的是
。下列有关说法正确的是
①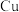 与
与 的物质的量之比为
的物质的量之比为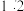
②硝酸的物质的量浓度为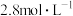
③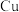 、
、 与硝酸反应后剩余
与硝酸反应后剩余 为
为
④产生的 的体积为
的体积为
⑤原混合物中Cu的质量分数为
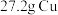 和
和 的混合物中加入某浓度的稀硝酸
的混合物中加入某浓度的稀硝酸 ,固体物质完全反应,得到标准状况下
,固体物质完全反应,得到标准状况下 和
和 的混合气体及
的混合气体及 。在所得溶液中加入
。在所得溶液中加入 的NaOH溶液
的NaOH溶液 ,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为
,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为 。下列有关说法正确的是
。下列有关说法正确的是①
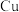 与
与 的物质的量之比为
的物质的量之比为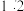
②硝酸的物质的量浓度为
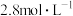
③
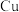 、
、 与硝酸反应后剩余
与硝酸反应后剩余 为
为
④产生的
 的体积为
的体积为
⑤原混合物中Cu的质量分数为

| A.①⑤ | B.②④ | C.①④ | D.②③ |
您最近一年使用:0次
2020-01-26更新
|
3131次组卷
|
2卷引用:2020届高三化学二轮冲刺新题专练——硝酸的性质及应用(强化练)
解题方法
8 . 已知草酸为二元中强酸,具有较强还原性,且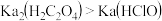 ,下列说法正确的是
,下列说法正确的是
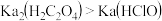 ,下列说法正确的是
,下列说法正确的是
A.草酸与氢氧化钠溶液混合呈中性时,溶液中存在: |
B.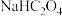 与NaClO溶液混合,反应的离子方程式为: 与NaClO溶液混合,反应的离子方程式为: |
C.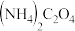 溶液中: 溶液中:  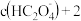  |
D.草酸使酸性 溶液褪色,离子方程式为: 溶液褪色,离子方程式为: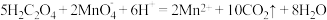 |
您最近一年使用:0次
9 . 某固体粉末甲中可能含有K2CO3、KNO3、NaNO2、K2SO3、Na2SO4、Fe、FeO、Fe2O3中的若干种。某同学为确定该固体粉末的成分,取甲进行连续实验。实验过程及现象如下:
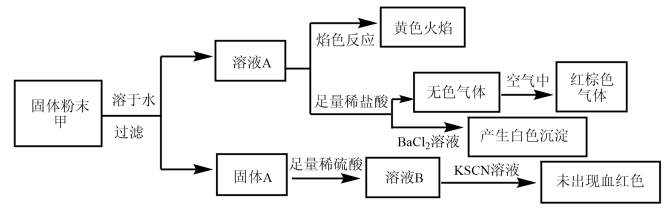
该同学得出的结论正确的是

该同学得出的结论正确的是
| A.固体粉末中含有钠元素,但不含钾元素 |
| B.固体粉末中至少含有Na2SO4、K2SO3中的一种 |
| C.固体粉末中至少含有KNO3、NaNO2中的一种 |
| D.固体粉末中可能含有K2CO3、不含Fe2O3 |
您最近一年使用:0次
名校
10 . 碲(Te)具有两性特征,铜阳极泥是提取碲的主要原料,碲在铜阳极泥中主要以MezTeCMe表 示金属Cu、Pb、Au、Ag等)的形式存在。
(1)利用“氯化浸出-还原法”制备Te的工艺流程如下所示。
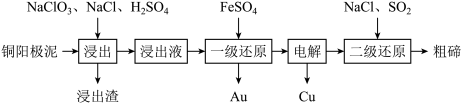
①浸出液的主要成分为CuSO4、HAuCu、H2TeO3,则浸出渣的主要成分 为____ (填化学式);“浸出”过程中有少量污染性气体生成,该气体是_______ (填物质名称)
②已知HAuCU是一种强酸,则“一级还原”过程中发生反应的离子方程式为_________ 。
③欲得到64g碲,则“二级还原”过程中至少需通入____ mol SO2。 “氧化碱浸-电解法”指的是在氧化剂的作用下,Cu2Te与NaOH溶液反应生成Na2TeO3和Cu(OH)2,经电解即可获得Te。
①以空气为氧化剂进行“氧化碱浸”的化学方程式为______ 。
②电解过程中,阴极的电极反应式为______ 。
③与“氯化浸出-还原法”相比“氧化碱浸-电解法”的优点是____ (任写一点)
(1)利用“氯化浸出-还原法”制备Te的工艺流程如下所示。

①浸出液的主要成分为CuSO4、HAuCu、H2TeO3,则浸出渣的主要成分 为
②已知HAuCU是一种强酸,则“一级还原”过程中发生反应的离子方程式为
③欲得到64g碲,则“二级还原”过程中至少需通入
①以空气为氧化剂进行“氧化碱浸”的化学方程式为
②电解过程中,阴极的电极反应式为
③与“氯化浸出-还原法”相比“氧化碱浸-电解法”的优点是
您最近一年使用:0次



