名校
1 . A2、B2、C23种单质和它们离子间能发生下列反应2A- + C2 = 2C- + A2、2C- + B2 = 2B- + C2。若X-能与C2发生反应2X- + C2 = 2C- + X2有关说法中不正确的是( )
| A.氧化性B2>C2>A2 | B.还原性X->C->B- |
| C.X2与B-能发生反应 | D.B2与X-能发生反应 |
您最近一年使用:0次
2017-11-16更新
|
146次组卷
|
4卷引用:北京市昌平临川育人学校2017-2018学年高一上学期期中考试化学试题
名校
解题方法
2 . 铬铁矿的主要成分可表示为FeO·Cr2O3,还含有SiO2、A12O3等杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的过程如图所示。
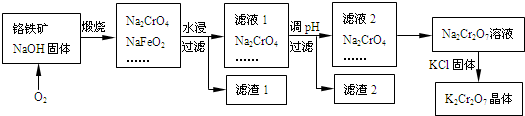
已知:①NaFeO2遇水强烈水解.②Cr2O72-+H2O 2CrO42-+2H+。
2CrO42-+2H+。
请回答:
(1)K2Cr2O7中K元素的原子结构示意图为____________ ,化合价是_______________ 。
(2)往铬铁矿里通入氧气的主要目的是__________________ 。滤液1的成分除Na2CrO4外,还含有_____ (填化学式)。
(3)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式
是________________________ 。
(4)由滤液2转化为Na2Cr2O7溶液应采取的措施是____________________ 。
(5)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、__________ 、过滤、洗涤、干燥。
(6)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是_______________________ 。

已知:①NaFeO2遇水强烈水解.②Cr2O72-+H2O
 2CrO42-+2H+。
2CrO42-+2H+。请回答:
(1)K2Cr2O7中K元素的原子结构示意图为
(2)往铬铁矿里通入氧气的主要目的是
(3)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式
是
(4)由滤液2转化为Na2Cr2O7溶液应采取的措施是
(5)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、
(6)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是
您最近一年使用:0次
名校
3 . 足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与33.6LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
| A.2.5L | B.1.2L | C.1.5L | D.3 L |
您最近一年使用:0次
2017-11-14更新
|
1806次组卷
|
4卷引用:云南省曲靖市第一中学2018届高三上学期第三次月考化学试题
名校
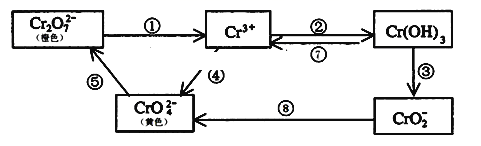
4 . 铬是人体必需元素,如含量不足会影响糖类和脂类的代谢,过高则会引起急性中毒。工业上往往采取下列循环工艺防止铬的污染:
完成下列填空:
(1)溶液配制:称取一定量纯净的K2Cr2O7晶体配制100ml标准溶液,用蒸馏水完全溶解后,全部转移至_____ 中,加蒸馏水离刻度线1---2厘米处,改用__________ 加水至刻度线。
(2)含Cr2O72-离子的废水在酸性条件下用Fe3O4处理,反应的离子方程式如下,配平该离子反应方程式:
___ Cr2O72-+___ Fe3O4 +__ H+ →__ Cr3+ +__ Fe3+ +__ H2O
(3)工业上处理含Cr2O72-的废水时,一般将剧毒的Cr2O72-转化为Cr3+,以碳为阴极,铁作阳极,电解处理含NaCl、Cr2O72-的酸性废水。写出电极反应:阳极___________ ,阴极_______________________ ;用铁做阳极的目的是:_____________________ 。
(4)反应⑤是可逆反应,在Na2CrO4溶液中加入稀硫酸,溶液由黄色逐渐变成橙色,写出该反应的离子方程式:____________ 。
(5)向上述反应后的溶液中加入碱溶液,让废水的pH升至8~10,控制适当的温度,使产物中的金属阳离子全部转变为沉淀。回收所得的Cr(OH)3,经处理后又可转变成K2Cr2O7。纯净的K2Cr2O7常用于准确测定Na2S2O3溶液的物质的量浓度,方法如下:① Cr2O72- +6I- + 14H+ →3I2 + 2Cr3+ + 7H2O ② 2S2O32- + I2→S4O62- + 2I- ,准确称取纯净的K2Cr2O7 0.294g ,配成溶液,加足量KI,用Na2S2O3溶液滴定,消耗Na2S2O3溶液25.00mL。则Na2S2O3溶液的物质的量浓度为_____________________ (保留四位有效数字)。
完成下列填空:
(1)溶液配制:称取一定量纯净的K2Cr2O7晶体配制100ml标准溶液,用蒸馏水完全溶解后,全部转移至
(2)含Cr2O72-离子的废水在酸性条件下用Fe3O4处理,反应的离子方程式如下,配平该离子反应方程式:
(3)工业上处理含Cr2O72-的废水时,一般将剧毒的Cr2O72-转化为Cr3+,以碳为阴极,铁作阳极,电解处理含NaCl、Cr2O72-的酸性废水。写出电极反应:阳极
(4)反应⑤是可逆反应,在Na2CrO4溶液中加入稀硫酸,溶液由黄色逐渐变成橙色,写出该反应的离子方程式:
(5)向上述反应后的溶液中加入碱溶液,让废水的pH升至8~10,控制适当的温度,使产物中的金属阳离子全部转变为沉淀。回收所得的Cr(OH)3,经处理后又可转变成K2Cr2O7。纯净的K2Cr2O7常用于准确测定Na2S2O3溶液的物质的量浓度,方法如下:① Cr2O72- +6I- + 14H+ →3I2 + 2Cr3+ + 7H2O ② 2S2O32- + I2→S4O62- + 2I- ,准确称取纯净的K2Cr2O7 0.294g ,配成溶液,加足量KI,用Na2S2O3溶液滴定,消耗Na2S2O3溶液25.00mL。则Na2S2O3溶液的物质的量浓度为
您最近一年使用:0次
2017-11-02更新
|
640次组卷
|
3卷引用:四川省绵阳市2018届高三一诊模拟(四)化学试题
5 . 现取m克铝镁合金与一定浓度的稀硝酸恰好完全溶解(假定硝酸的还原产物只有NO),向反应后的混合溶液中滴加b mol/L NaOH溶液,当滴加到V mL时,得到沉淀质量恰好为最大值n克,则下列有关该实验的说法中正确的有
①沉淀中氢氧根的质量为(n-m)g
②恰好溶解后溶液中的NO3-的物质的量为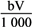 mol
mol
③反应过程中转移的电子的物质的量为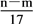 mol
mol
④生成NO气体的体积在标准状况下为 L
L
⑤与合金反应的硝酸的物质的量为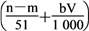 mol
mol
①沉淀中氢氧根的质量为(n-m)g
②恰好溶解后溶液中的NO3-的物质的量为
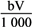 mol
mol③反应过程中转移的电子的物质的量为
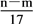 mol
mol④生成NO气体的体积在标准状况下为
 L
L⑤与合金反应的硝酸的物质的量为
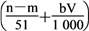 mol
mol| A.5项 | B.4项 | C.3项 | D.2项 |
您最近一年使用:0次
名校
6 . NH3和NO2在催化剂作用下反应:8NH3+6NO2=7N2+12H2O。若还原产物比氧化产物少0.1 mol,则下列判断正确的是( )
| A.转移电子3.6NA | B.生成气体的体积32.56 L(标准状况) |
| C.还原剂比氧化剂多0.2 mol | D.被还原的氮原子是11.2 g |
您最近一年使用:0次
2017-10-17更新
|
1385次组卷
|
7卷引用:福建省德化一中、永安一中、漳平一中2018届高三上学期三校联考化学试题
名校
7 . 5.76 g部分氧化的Fe、Cu合金样品(氧化产物为Fe2O3、CuO),经如下处理,下列说法正确的是
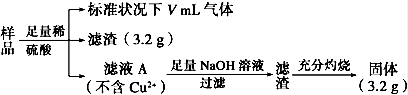

| A.V=224 |
| B.样品中Fe的质量为2.14 g |
| C.未氧化前Fe元素的质量分数约为41.2% |
| D.样品中CuO的质量为3.52 g |
您最近一年使用:0次
名校
8 . 向含a mol NaClO的溶液通入b mol SO2充分反应(不考虑二氧化硫与水之间的反应以及次氯酸的分解)。下列说法不正确的是
A.当0<b<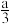 时:SO2+H2O+3ClO-= 时:SO2+H2O+3ClO-= +2HClO+Cl- +2HClO+Cl- |
B.当b=a时:SO2+H2O+ClO-= +2H++Cl- +2H++Cl- |
C.当 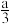 <b<a时;反应后溶液中H+的物质的量:0<n(H+)<2bmol <b<a时;反应后溶液中H+的物质的量:0<n(H+)<2bmol |
D.当0<b<a时;反应后溶液中Cl-、ClO-和 物质的量之比为:(a-b):b:b 物质的量之比为:(a-b):b:b |
您最近一年使用:0次
2017-05-27更新
|
700次组卷
|
4卷引用:辽宁省沈阳市2017届高三第三次模拟考试理综化学试题
名校
9 . 黑火药是我国的四大发明之一,深受世人称赞,其反应原理为:S+3C+2KNO3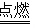 N2↑+3CO2↑+K2S请回答下列相关问题:
N2↑+3CO2↑+K2S请回答下列相关问题:
(1)当产生0.1molN2时,反应中共转移电子数为___________ ,还原剂的物质的量为___________ mol.
(2)若生成标准状况下33.6LCO2,则被S氧化的C的物质的量是___________ mol.
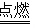 N2↑+3CO2↑+K2S请回答下列相关问题:
N2↑+3CO2↑+K2S请回答下列相关问题:(1)当产生0.1molN2时,反应中共转移电子数为
(2)若生成标准状况下33.6LCO2,则被S氧化的C的物质的量是
您最近一年使用:0次
2017-02-28更新
|
937次组卷
|
2卷引用:2016-2017学年安徽省宿州市高一上学期期末教学质量检测(a卷)化学试卷
名校
10 . F2和Xe在一定条件下生成氧化性极强且极易与水反应的XeF2、XeF4和XeF6三种化合物。其中XeF4与水可发生如下反应:6XeF4+12H2O═2XeO3+4Xe↑+24HF+3O2↑.下列判断中正确的是
| A.上述反应中氧化剂和还原剂的物质的量之比为1∶2 |
| B.XeF4按以上方式与水反应,每生成3molO2,转移12mol电子 |
| C.XeF2加入水中,在水分子的作用下,将重新生成Xe和F2 |
| D.XeF2、XeF4和XeF6在空气中都能长期存放 |
您最近一年使用:0次
2017-02-28更新
|
1337次组卷
|
2卷引用:2017届湖南省衡阳市高三下学期第一次联考理综化学试卷



