1 . 亚硝酸钠是一种工业盐,用途广泛;外观与食盐非常相似,但毒性较强。某化学兴趣小组对食盐与亚硝酸钠进行了如下探究:
㈠鉴别NaCl和NaNO2
(1)测定溶液pH
用pH试纸分别测定0.1mol•L-1两种盐溶液的pH,测得NaNO2溶液呈碱性.NaNO2溶液呈碱性的原因是__________ (用离子方程式解释),NaNO2溶液中c(HNO2)=__________ (用溶液中其它离子的浓度关系式表示)。
(2)沉淀法
取2mL0.1mol•L-1两种盐溶液于试管中,分别滴加几滴稀硝酸银溶液,两支试管均产生白色沉淀,分别滴加几滴稀硝酸并振荡,盛NaNO2溶液的试管中沉淀溶解。该温度下Ksp(AgNO2)=2×10-8 (mol•L-1)2; Ksp(AgCl)=1.8×10-10(mol•L-1)2,则反应AgNO2(s)+Cl-(aq)═AgCl(s)+NO2-(aq)的化学平衡常数K=__________ (计算结果写成分数)。
(二)实验室可用如下装置(略去部分夹持仪器)备亚硝酸钠。
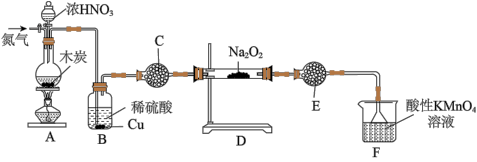
已知:①2NO+Na2O2=2NaNO2;②酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+;Na2O2能使酸性高锰酸钾溶液褪色.
(3)加热装置A前,先通一段时间N2,目的是__________ 。
(4)装置A中发生反应的化学方程式为__________ ,装置B的作用是__________ 。
(5)仪器C的名称为__________ ,其中盛放的药品为__________ (填名称)。
㈠鉴别NaCl和NaNO2
(1)测定溶液pH
用pH试纸分别测定0.1mol•L-1两种盐溶液的pH,测得NaNO2溶液呈碱性.NaNO2溶液呈碱性的原因是
(2)沉淀法
取2mL0.1mol•L-1两种盐溶液于试管中,分别滴加几滴稀硝酸银溶液,两支试管均产生白色沉淀,分别滴加几滴稀硝酸并振荡,盛NaNO2溶液的试管中沉淀溶解。该温度下Ksp(AgNO2)=2×10-8 (mol•L-1)2; Ksp(AgCl)=1.8×10-10(mol•L-1)2,则反应AgNO2(s)+Cl-(aq)═AgCl(s)+NO2-(aq)的化学平衡常数K=
(二)实验室可用如下装置(略去部分夹持仪器)备亚硝酸钠。

已知:①2NO+Na2O2=2NaNO2;②酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+;Na2O2能使酸性高锰酸钾溶液褪色.
(3)加热装置A前,先通一段时间N2,目的是
(4)装置A中发生反应的化学方程式为
(5)仪器C的名称为
您最近一年使用:0次
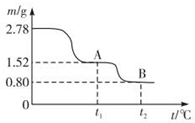
2 . 在中国古代,炼丹家以绿矾(FeSO4•7H2O为原料,放在炼丹炉中煅烧可制得绿矾油.绿矾油是一种无色粘稠液体,可用于除掉兵器上的铁锈.如图是2.78g绿矾隔绝空气受热分解时,所得固体产物的质量随温度变化的曲线.将加热产生的所有气体通入足量的BaCl2溶液.得自色沉淀1.16g.
(1)绿矾油主要成份的化学式为_________ .t1~t2.发生反应的化学方程式为_________________ .
(2)若将2.88g草酸亚铁(FeC2O4)隔绝空气加热至100℃,得到1.44g黑色细粉,则可推知该黑色细粉为_________ .
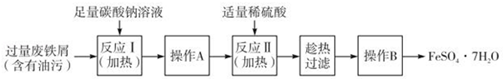
(3)以下是FeSO4•7H2O的实验室制备流理图.
根据题意完成下列填空:
①反应II需要100mL1. 5mol•L﹣1的稀H2SO4溶解洁净的铁屑,用质量分数为98%、密度为1.84g•cm﹣3的浓H2SO4配制.所用的仪器有量筒、烧杯、玻璃捧、胶头滴管及____________ .
②操作A的名称为_____________ .
③测定FeSO4•7H2O产品中Fe2+含量的常用方法是KMnO4溶液滴定法.已知称取6.0g FeSO4•7H2O产品,配制成溶液,用硫酸酸化的0.2000mol•L﹣1KMnO4溶液滴定,消耗KMnO4溶液的体积为20.00mL.发生反应的离子方程式为_______________ ,计算上述样品中FeSO4•7H2O的质量分数为_________ (保留两位有效数字).
(1)绿矾油主要成份的化学式为
(2)若将2.88g草酸亚铁(FeC2O4)隔绝空气加热至100℃,得到1.44g黑色细粉,则可推知该黑色细粉为
(3)以下是FeSO4•7H2O的实验室制备流理图.

根据题意完成下列填空:

①反应II需要100mL1. 5mol•L﹣1的稀H2SO4溶解洁净的铁屑,用质量分数为98%、密度为1.84g•cm﹣3的浓H2SO4配制.所用的仪器有量筒、烧杯、玻璃捧、胶头滴管及
②操作A的名称为
③测定FeSO4•7H2O产品中Fe2+含量的常用方法是KMnO4溶液滴定法.已知称取6.0g FeSO4•7H2O产品,配制成溶液,用硫酸酸化的0.2000mol•L﹣1KMnO4溶液滴定,消耗KMnO4溶液的体积为20.00mL.发生反应的离子方程式为
您最近一年使用:0次
解题方法
3 . 天津港“8.12”特别重大爆炸事故教训深刻。氰化钠(N元素显﹣3价)属于剧毒化学品,处理氰化物的方法主要有两种:
(1)碱性氯化法是在碱性条件下通入氯气,氯气将CN﹣氧化成无污染的气体。请补充并配平该反应的离子方程式:CN﹣+OH﹣+Cl2═CO2+ + +H2O。处理35吨NaCN,理论上需要液氯 吨。
(2)过氧化氢氧化法:NaCN+H2O2+H2O═NaHCO3+NH3↑。检测水坑里氰化钠的浓度,取水样1mL,加入11mL1mol•L﹣1H2O2溶液,充分反应后,加入过量的KI固体,充分反应后调节pH至7左右,用0.2500mol•L﹣1Na2S2O3溶液8.00mL(已知:实验中涉及的部分离子方程式为: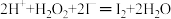 、
、 )。请计算水坑里氰化钠的浓度。
)。请计算水坑里氰化钠的浓度。
(1)碱性氯化法是在碱性条件下通入氯气,氯气将CN﹣氧化成无污染的气体。请补充并配平该反应的离子方程式:CN﹣+OH﹣+Cl2═CO2+ + +H2O。处理35吨NaCN,理论上需要液氯 吨。
(2)过氧化氢氧化法:NaCN+H2O2+H2O═NaHCO3+NH3↑。检测水坑里氰化钠的浓度,取水样1mL,加入11mL1mol•L﹣1H2O2溶液,充分反应后,加入过量的KI固体,充分反应后调节pH至7左右,用0.2500mol•L﹣1Na2S2O3溶液8.00mL(已知:实验中涉及的部分离子方程式为:
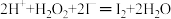 、
、 )。请计算水坑里氰化钠的浓度。
)。请计算水坑里氰化钠的浓度。
您最近一年使用:0次
解题方法
4 . 某废水中含有 和
和 等离子,需经污水处理达标后才能排放,污水处理拟采用下列流程进行处理:
等离子,需经污水处理达标后才能排放,污水处理拟采用下列流程进行处理:

回答下列问题:
(1)步骤②中, 被
被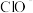 氧化为
氧化为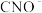 的离子方程式为
的离子方程式为________________ 。
(2)步骤③的反应的离子方程式为 (未配平),每消耗0.4mol
(未配平),每消耗0.4mol  时,反应中
时,反应中 失去
失去_________ mol电子。
(3)含Cr3+废水可以加入熟石灰进一步处理,目的是________________ 。
(4)在25℃下,将amol·L-1的NaCN溶液与0.01mol·L-1的盐酸等体积混合,反应后测得溶液pH=7,用含a的代数式表示 的水解常数Kh=
的水解常数Kh=_______ mol·L-1。若25℃时将浓度均为0.1mol·L-1的NaCN、HCN溶液等体积混合后,溶液呈碱性,则关于该溶液的说法不正确的是_______ (填代号)。
a.此溶液一定有c(Na+)+c(H+)=c(OH-)+c(CN-)
b.此溶液一定有c(Na+)=c(HCN)+c(CN-)
c.混合溶液中水的电离程度一定大于该温度下纯水的电离程度
d.此溶液加入少量氢氧化钠或盐酸,溶液的pH变化不大
(5)利用 测定某SnCl2的纯度(杂质不参与反应,溶液中Sn4+较为稳定):将
测定某SnCl2的纯度(杂质不参与反应,溶液中Sn4+较为稳定):将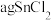 样品制成溶液的操作为
样品制成溶液的操作为________________ ,向得到的SnCl2溶液中加入过量的FeCl3溶液,用bmol·L-l 滴定生成的Fe2+(已知酸性环境下,
滴定生成的Fe2+(已知酸性环境下, 可被还原为Cr3+),共用去
可被还原为Cr3+),共用去 溶液xmL.则样品中SnCl2的的质量分数是
溶液xmL.则样品中SnCl2的的质量分数是_________ 。(SnCl2的摩尔质量为M g·mol-1,用含a、b、x、M的代数式表示)
 和
和 等离子,需经污水处理达标后才能排放,污水处理拟采用下列流程进行处理:
等离子,需经污水处理达标后才能排放,污水处理拟采用下列流程进行处理:
回答下列问题:
(1)步骤②中,
 被
被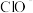 氧化为
氧化为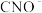 的离子方程式为
的离子方程式为(2)步骤③的反应的离子方程式为
 (未配平),每消耗0.4mol
(未配平),每消耗0.4mol  时,反应中
时,反应中 失去
失去(3)含Cr3+废水可以加入熟石灰进一步处理,目的是
(4)在25℃下,将amol·L-1的NaCN溶液与0.01mol·L-1的盐酸等体积混合,反应后测得溶液pH=7,用含a的代数式表示
 的水解常数Kh=
的水解常数Kh=a.此溶液一定有c(Na+)+c(H+)=c(OH-)+c(CN-)
b.此溶液一定有c(Na+)=c(HCN)+c(CN-)
c.混合溶液中水的电离程度一定大于该温度下纯水的电离程度
d.此溶液加入少量氢氧化钠或盐酸,溶液的pH变化不大
(5)利用
 测定某SnCl2的纯度(杂质不参与反应,溶液中Sn4+较为稳定):将
测定某SnCl2的纯度(杂质不参与反应,溶液中Sn4+较为稳定):将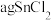 样品制成溶液的操作为
样品制成溶液的操作为 滴定生成的Fe2+(已知酸性环境下,
滴定生成的Fe2+(已知酸性环境下, 可被还原为Cr3+),共用去
可被还原为Cr3+),共用去 溶液xmL.则样品中SnCl2的的质量分数是
溶液xmL.则样品中SnCl2的的质量分数是
您最近一年使用:0次
解题方法
5 . 工业上冶炼冰铜(mCu2O·nFeS)可得到粗铜,在空气中煅烧冰铜时,产生一种有刺激性气味的气体A,该气体排放到空气中,是导致酸雨的形成的主要原因。

完成下列填空:
(1)为了降低污染气体A的排放,可选用下列试剂中的________ (填序号)吸收。
a. 浓H2SO4 b. 浓HNO3 c. NaOH溶液 d.石灰乳
(2)已知铝在高温下能将某些金属从其氧化物中置换出来。将铝与泡铜发生反应从而得到粗铜。泡铜冶炼粗铜的化学方程式是___________________ 。每当有1mol铝参加反应,则转移电子个数为____________
(3)SO2气体与氢氧化钠反应时,得到的盐为Na2SO3或 NaHSO3。通过计算回答:将0.3 mol SO2通入100mL含0.4 molNaOH溶液中,充分反应后得到的盐物质的量分别是多少?(写出计算过程)___________________

完成下列填空:
(1)为了降低污染气体A的排放,可选用下列试剂中的
a. 浓H2SO4 b. 浓HNO3 c. NaOH溶液 d.石灰乳
(2)已知铝在高温下能将某些金属从其氧化物中置换出来。将铝与泡铜发生反应从而得到粗铜。泡铜冶炼粗铜的化学方程式是
(3)SO2气体与氢氧化钠反应时,得到的盐为Na2SO3或 NaHSO3。通过计算回答:将0.3 mol SO2通入100mL含0.4 molNaOH溶液中,充分反应后得到的盐物质的量分别是多少?(写出计算过程)
您最近一年使用:0次
名校
6 . 将一定量的Cl2通入体积为40mL、浓度为7.5mol/L的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),测得反应后溶液中有三种含氯元素的离子,其中ClO-物质的量为0.06mol和ClO3-物质的量0.03mol,下列说法不正确的是
| A.该反应的离子方程式为:5Cl2+10OH-=7Cl-+2ClO-+ClO3—+5H2O |
| B.该反应中,氧化剂与还原剂物质的量之比为5:3 |
| C.上述苛性钾溶液中含有0.3mol的KOH |
| D.反应后生成的ClO-和ClO3-两种离子在一定条件下均有氧化性 |
您最近一年使用:0次
2016-12-09更新
|
2583次组卷
|
5卷引用:2015-2016学年江苏省南通中学高一上学期期末化学试卷
名校
解题方法
7 . 现有两种金属组成的混合物,把5.6g 该混合物加入到100g一定溶质质量分数的稀硫酸中,恰好完全反应,产生氢气物质的量为w。则下列说法中正确的是
| A.若混合物为Zn、Al,w不可能是0.1 mol |
| B.若混合物为Zn、Fe,w可能大于0.1 mol |
| C.若混合物为Fe、Mg,则加入的稀硫酸中溶质质量分数等于9.8% |
| D.若混合物为Cu、Fe,w是0.05mol,则混合物中Fe与Cu的质量比为1:1 |
您最近一年使用:0次
2016-12-09更新
|
722次组卷
|
3卷引用:2015-2016学年四川省南充高级中学高一上期末化学试卷
解题方法
8 . 铁及其化合物在日常生活、生产中应用广泛。
(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,工业上利用NaClO 和NaOH的混合溶液将2Fe(OH)3氧化性制备高铁酸钠,反应的化学方程式为______________________ ;高铁酸钠能用作新型净水剂的原理是____________________________ ;
(2)氧化铁红颜料跟某些油料混合,可以制成防锈油漆。以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:
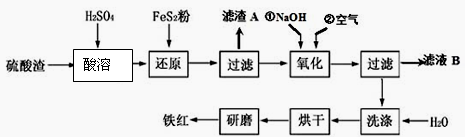
①酸溶过程中发生反应的化学方程式为___________ ,_____________ ,___________ ;“滤渣A”主要成分的化学式为_____________________ 。
②还原过程中加入FeS2的目的是将溶液中的Fe3 +还原为Fe2 +,而本身被氧化为H2SO4,请写出该反应的离子方程式_______________________________ ;
③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为_____________ 。
④为了确保铁红的质量和纯度,氧化过程需要调节溶液的pH的范围是____________ ,
如果pH过大,可能引起的后果是_____________________ 。
(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,工业上利用NaClO 和NaOH的混合溶液将2Fe(OH)3氧化性制备高铁酸钠,反应的化学方程式为
(2)氧化铁红颜料跟某些油料混合,可以制成防锈油漆。以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:

①酸溶过程中发生反应的化学方程式为
②还原过程中加入FeS2的目的是将溶液中的Fe3 +还原为Fe2 +,而本身被氧化为H2SO4,请写出该反应的离子方程式
③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为
④为了确保铁红的质量和纯度,氧化过程需要调节溶液的pH的范围是
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
如果pH过大,可能引起的后果是
您最近一年使用:0次
2016-12-09更新
|
992次组卷
|
2卷引用:2016届宁夏回族自治区银川一中高三上第三次月考化学试卷
9 . 现取m克铝镁合金与一定浓度的稀硝酸恰好完全溶解(假定硝酸的还原产物只有NO),向反应后的混合溶液中滴加bmol/LNaOH溶液,当滴加到VmL时,得到沉淀质量恰好为最大值n克,则下列有关该实验的说法中正确的有
①沉淀中氢氧根的质量为(n-m)克
②恰好溶解后溶液中的NO3-离子的物质的量为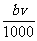 mol
mol
③反应过程中转移的电子数为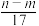 mol
mol
④生成标准状况下NO气体的体积为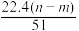 L
L
⑤与合金反应反应的硝酸的物质的量为(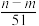 +
+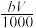 )mol
)mol
①沉淀中氢氧根的质量为(n-m)克
②恰好溶解后溶液中的NO3-离子的物质的量为
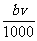 mol
mol③反应过程中转移的电子数为
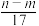 mol
mol ④生成标准状况下NO气体的体积为
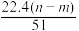 L
L⑤与合金反应反应的硝酸的物质的量为(
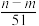 +
+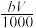 )mol
)mol| A.2项 | B.3项 | C.4项 | D.5项 |
您最近一年使用:0次
名校
10 . 将一定量的镁和铜组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物只有NO)。向反应后的溶液中加入3 mol·L−1NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1 g。下列叙述不正确 的是
| A.当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4mol |
| B.参加反应的金属的总质量3.6g<m<9.6g |
| C.当生成的沉淀量达到最大时,消耗NaOH溶液的体积一定为V=100mL |
| D.当金属全部溶解时收集到NO气体的体积在标准状况下为2.24L |
您最近一年使用:0次
2016-12-09更新
|
2468次组卷
|
11卷引用:2016届陕西省西藏民族学院附属中学高三上期末化学试卷
2016届陕西省西藏民族学院附属中学高三上期末化学试卷2017届湖南省长株潭岳益五市十校高三12月联考化学卷2017届福建省漳州市八校高三上学期期末联考化学试卷(已下线)2019年1月24日《每日一题》二轮复习—— 氮的氧化物、硝酸的性质及应用(已下线)2019年4月17日 《每日一题》三轮复习-其他金属及其化合物【全国百强校】云南省曲靖市第一中学2018-2019学年高一下学期期中考试化学试题安徽省安庆市怀宁县怀宁中学2021届高三年级第一次质量检测化学试题江西省南昌市莲塘一中2021届高三上学期11月月考化学试题辽宁省部分中学2019-2020高一下学期期末考试化学试题江西省上高二中2022届高三第二次月考化学试卷河北省张家口市宣化第一中学2021-2022学年高三上学期12月月考化学试题



