1 . 利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部分物质类别的对应关系。
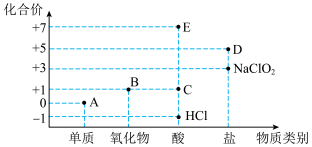
(1)物质E的化学式为___________
(2)A、B、C、D(钾盐)四种物质中,属于电解质的是___________ (填化学式)
(3)A与水反应的离子方程式为___________
(4)B为酸性氧化物,则B与氢氧化钠溶液反应的化学方程式为___________
(5)已知A与氢氧化钠溶液反应生成 和
和 的混合物,若
的混合物,若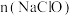 与
与 之比为2:3,则氧化剂与还原剂的物质的量之比为
之比为2:3,则氧化剂与还原剂的物质的量之比为___________
(6)已知二氧化氯( )为高效无毒的消毒剂,实际消毒效果比物质A要好。在室温及标准大气压的条件下,等物质的量的
)为高效无毒的消毒剂,实际消毒效果比物质A要好。在室温及标准大气压的条件下,等物质的量的 和物质A比较,所含的原子总数之比为
和物质A比较,所含的原子总数之比为___________ ,电子数目之比为___________ 。
(7)氯碱工业指的是工业上用电解饱和食盐水的方法,制取氯气和烧碱等主要产品,在国民经济和国防建设中占有重要地位。请写出氯化钠溶液在通电条件下,发生反应的离子方程式___________ 。

(1)物质E的化学式为
(2)A、B、C、D(钾盐)四种物质中,属于电解质的是
(3)A与水反应的离子方程式为
(4)B为酸性氧化物,则B与氢氧化钠溶液反应的化学方程式为
(5)已知A与氢氧化钠溶液反应生成
 和
和 的混合物,若
的混合物,若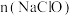 与
与 之比为2:3,则氧化剂与还原剂的物质的量之比为
之比为2:3,则氧化剂与还原剂的物质的量之比为(6)已知二氧化氯(
 )为高效无毒的消毒剂,实际消毒效果比物质A要好。在室温及标准大气压的条件下,等物质的量的
)为高效无毒的消毒剂,实际消毒效果比物质A要好。在室温及标准大气压的条件下,等物质的量的 和物质A比较,所含的原子总数之比为
和物质A比较,所含的原子总数之比为(7)氯碱工业指的是工业上用电解饱和食盐水的方法,制取氯气和烧碱等主要产品,在国民经济和国防建设中占有重要地位。请写出氯化钠溶液在通电条件下,发生反应的离子方程式
您最近一年使用:0次
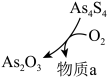
2 . 硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图。图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。
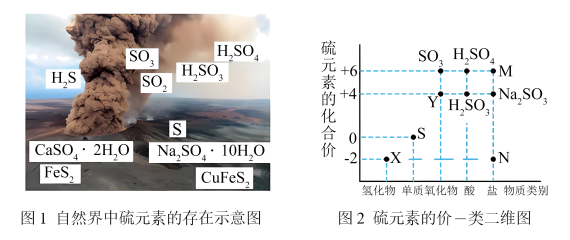
(1)图1中与图2中M、N对应的物质分别是
(2)X与Y反应中氧化剂与还原剂的物质的量之比为
(3)
 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是(4)已知
 能被酸性
能被酸性 氧化为
氧化为 ,则
,则 的
的 溶液与
溶液与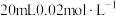 的
的 溶液恰好反应时,发生的离子方程式为:
溶液恰好反应时,发生的离子方程式为:(5)过二硫酸钠
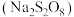 有强氧化性,在碱性条件下
有强氧化性,在碱性条件下 溶液能将
溶液能将 氧化成
氧化成 ,且反应后的溶液滴入
,且反应后的溶液滴入 溶液生成不溶于稀盐酸的白色沉淀,该反应的离子方程式为
溶液生成不溶于稀盐酸的白色沉淀,该反应的离子方程式为(6)雌黄
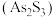 和雄黄
和雄黄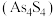 在自然界中共生且可以相互转化(两者的硫元素价态均为-2价)。
在自然界中共生且可以相互转化(两者的硫元素价态均为-2价)。① 和
和 在盐酸中恰好完全反应转化为
在盐酸中恰好完全反应转化为 和
和 并放出
并放出 气体。则参加反应的
气体。则参加反应的 和
和 的物质的量之比为
的物质的量之比为
② 和
和 可以相互转化,转化过程中存在如图所示的步骤。若
可以相互转化,转化过程中存在如图所示的步骤。若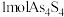 参加反应时,转移
参加反应时,转移 电子,则物质
电子,则物质 为
为
您最近一年使用:0次
名校
解题方法
3 . I.元素的“价—类”二维图体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如下图所示。回答下列问题:

(1)实验室用两种固体制备R的化学方程式________ 。
(2)下列有关图中所示含N、S物质的叙述,正确的是________ (填标号)。
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与NaOH溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠(Na2S2O5),从氧化还原反应的角度分析,可选择B和D反应
II.已知:①联氨(N2H4)性质与NH3相似,溶于水可生成一种二元弱碱。
②N2H4以还原性为主,氧化产物一般是N2,通常总是把联氨用作强还原剂。
(3)用次氯酸钠和氨气常温制备联氨,化学方程式为:________ 。
(4)根据以上信息,推断下列关于N2H4的说法不正确的是______。
(5)在标准状况下将1.92g铜粉投入一定量浓HNO3中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到只由NO2和NO组成的混合气体1.12L,则混合气体中NO的体积为_____。

(1)实验室用两种固体制备R的化学方程式
(2)下列有关图中所示含N、S物质的叙述,正确的是
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与NaOH溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠(Na2S2O5),从氧化还原反应的角度分析,可选择B和D反应
II.已知:①联氨(N2H4)性质与NH3相似,溶于水可生成一种二元弱碱。
②N2H4以还原性为主,氧化产物一般是N2,通常总是把联氨用作强还原剂。
(3)用次氯酸钠和氨气常温制备联氨,化学方程式为:
(4)根据以上信息,推断下列关于N2H4的说法不正确的是______。
| A.它与E形成的酸式盐可以表示为N2H5HSO5 |
| B.它溶于水所得的溶液中共有4种离子 |
C.它溶于水发生电离的第一步可表示为: |
| D.若已知联氨和四氧化二氮可以做火箭推进剂,两者反应产物可以是氮气和水 |
(5)在标准状况下将1.92g铜粉投入一定量浓HNO3中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到只由NO2和NO组成的混合气体1.12L,则混合气体中NO的体积为_____。
| A.56mL | B.112mL | C.224mL | D.448mL |
您最近一年使用:0次
名校
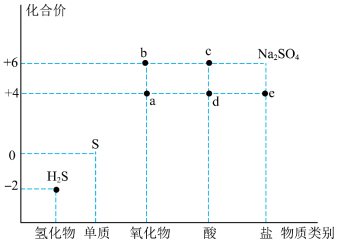
4 . 利用物质类别及核心元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:_____ 。
(2)c的浓溶液能与 反应的化学方程为
反应的化学方程为_____
(3)将足量的a通入 溶液中,下列说法正确的是
溶液中,下列说法正确的是_____ (填标号)。
A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入 或
或 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀
(4)实验室洗涤试管壁上附着的硫单质可用热的 溶液洗涤,该反应原理为
溶液洗涤,该反应原理为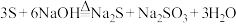
①在该反应中,氧化剂和还原剂的物质的量之比为_____ 。
②向上述反应的溶液中再加入适量的稀 ,会产生淡黄色沉淀,写出该反应的离子方程式:
,会产生淡黄色沉淀,写出该反应的离子方程式:_____ 。
(5)已知e为正盐,能被酸性 氧化为
氧化为 被还原为
被还原为 ,写出此反应的离子方程式:
,写出此反应的离子方程式:_____ 。
(6)下列反应过程中的能量变化可用图表示的是_____ 。(填序号)
⑤食物因氧化而腐败;⑥ 与
与 反应;⑦氧化钙与水反应
反应;⑦氧化钙与水反应
(2)c的浓溶液能与
 反应的化学方程为
反应的化学方程为(3)将足量的a通入
 溶液中,下列说法正确的是
溶液中,下列说法正确的是A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入
 或
或 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀(4)实验室洗涤试管壁上附着的硫单质可用热的
 溶液洗涤,该反应原理为
溶液洗涤,该反应原理为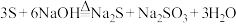
①在该反应中,氧化剂和还原剂的物质的量之比为
②向上述反应的溶液中再加入适量的稀
 ,会产生淡黄色沉淀,写出该反应的离子方程式:
,会产生淡黄色沉淀,写出该反应的离子方程式:(5)已知e为正盐,能被酸性
 氧化为
氧化为 被还原为
被还原为 ,写出此反应的离子方程式:
,写出此反应的离子方程式:(6)下列反应过程中的能量变化可用图表示的是
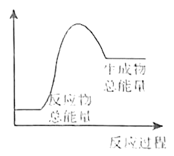
⑤食物因氧化而腐败;⑥
 与
与 反应;⑦氧化钙与水反应
反应;⑦氧化钙与水反应
您最近一年使用:0次
名校
解题方法
5 . 如图是氮元素的几种价态与物质类别的对应关系。请回答下列问题:

(1)上述物质间的转化,属于固氮反应的有________ (填序号),A是否属于酸性氧化物_______ (填“是”或“否”)。
(2)HNO3与图中的物质C常用于检验Cl-的存在,则C的化学式为________ 。
(3)工业上以B、空气、水为原料生产硝酸分为三步:其中第三步:NO2→HNO3,该反应中氧化剂与还原剂的物质的量之比为________ 。
(4)写出浓硝酸与木炭在加热条件下反应的化学方程式,并用单线桥表示其电子转移的情况_______ 。
(5)如图装置可用于探究氯气与氨气的反应,实验时先通过三颈瓶瓶口1通入氨气,然后关闭b活塞,再通过瓶口2通入氯气。实验中三颈瓶内出现白烟并在内壁凝结成固体,发生反应的化学方程式为_______ ,请设计一个实验方案鉴定该固体中的阳离子_______ 。

(6)有一瓶稀硫酸和稀硝酸的混合溶液,其中c(H2SO4)=2.0mol/L,c(HNO3)=1.0mol/L。取100mL该混合溶液与12.8g铜粉反应,标准状况下生成A的体积为_______ L。

(1)上述物质间的转化,属于固氮反应的有
(2)HNO3与图中的物质C常用于检验Cl-的存在,则C的化学式为
(3)工业上以B、空气、水为原料生产硝酸分为三步:其中第三步:NO2→HNO3,该反应中氧化剂与还原剂的物质的量之比为
(4)写出浓硝酸与木炭在加热条件下反应的化学方程式,并用单线桥表示其电子转移的情况
(5)如图装置可用于探究氯气与氨气的反应,实验时先通过三颈瓶瓶口1通入氨气,然后关闭b活塞,再通过瓶口2通入氯气。实验中三颈瓶内出现白烟并在内壁凝结成固体,发生反应的化学方程式为

(6)有一瓶稀硫酸和稀硝酸的混合溶液,其中c(H2SO4)=2.0mol/L,c(HNO3)=1.0mol/L。取100mL该混合溶液与12.8g铜粉反应,标准状况下生成A的体积为
您最近一年使用:0次
6 . 硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图。图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。
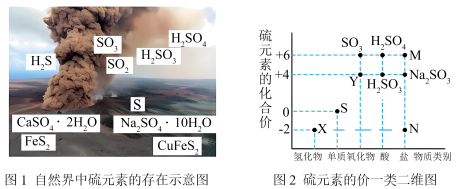
(1)图1中与图2中M、N对应的物质分别是___________ 、___________ 。
(2) 与
与 反应中氧化剂与还原剂的物质的量之比为
反应中氧化剂与还原剂的物质的量之比为___________ 。
(3) 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是___________ 。
(4)已知 能被酸性
能被酸性 氧化为
氧化为 ,则
,则 的
的 溶液与
溶液与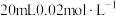 的
的 溶液恰好反应时,发生的离子方程式为:
溶液恰好反应时,发生的离子方程式为:___________ 。
(5) 的排放是造成酸雨的主要因素。形成酸雨的原理之一可简单表示如下:
的排放是造成酸雨的主要因素。形成酸雨的原理之一可简单表示如下:

请回答下列问题:
①反应b的化学方程式为:___________ 。
②在一段时间内连续不断测定溶液 的
的 ,发现
,发现 变小,表示该变化的化学方程式是:
变小,表示该变化的化学方程式是:___________ 。
③若用足量的氢氧化钠溶液吸收含二氧化硫的工业废气,写出该反应的离子方程式:___________ 。
(6)过二硫酸钠( )有强氧化性,在碱性条件下
)有强氧化性,在碱性条件下 溶液能将
溶液能将 氧化成
氧化成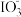 ,且反应后的溶液滴入
,且反应后的溶液滴入 溶液生成不溶于稀盐酸的白色沉淀,该反应的离子方程式为
溶液生成不溶于稀盐酸的白色沉淀,该反应的离子方程式为___________ 。
(7)雌黄( )和雄黄(
)和雄黄( )在自然界中共生且可以相互转化(两者的硫元素价态均为
)在自然界中共生且可以相互转化(两者的硫元素价态均为 价)。
价)。
① 和
和 在盐酸中恰好完全反应转化为
在盐酸中恰好完全反应转化为 和
和 并放出
并放出 气体。则参加反应的
气体。则参加反应的 和
和 的物质的量之比为
的物质的量之比为___________ 。
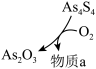
② 和
和 可以相互转化,转化过程中存在如图所示的步骤。若1molAs4S4参加反应时,转移
可以相互转化,转化过程中存在如图所示的步骤。若1molAs4S4参加反应时,转移 电子,则物质
电子,则物质 为
为___________ ,消耗氧气___________  。
。

(1)图1中与图2中M、N对应的物质分别是
(2)
 与
与 反应中氧化剂与还原剂的物质的量之比为
反应中氧化剂与还原剂的物质的量之比为(3)
 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是(4)已知
 能被酸性
能被酸性 氧化为
氧化为 ,则
,则 的
的 溶液与
溶液与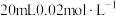 的
的 溶液恰好反应时,发生的离子方程式为:
溶液恰好反应时,发生的离子方程式为:(5)
 的排放是造成酸雨的主要因素。形成酸雨的原理之一可简单表示如下:
的排放是造成酸雨的主要因素。形成酸雨的原理之一可简单表示如下:
请回答下列问题:
①反应b的化学方程式为:
②在一段时间内连续不断测定溶液
 的
的 ,发现
,发现 变小,表示该变化的化学方程式是:
变小,表示该变化的化学方程式是:③若用足量的氢氧化钠溶液吸收含二氧化硫的工业废气,写出该反应的离子方程式:
(6)过二硫酸钠(
 )有强氧化性,在碱性条件下
)有强氧化性,在碱性条件下 溶液能将
溶液能将 氧化成
氧化成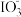 ,且反应后的溶液滴入
,且反应后的溶液滴入 溶液生成不溶于稀盐酸的白色沉淀,该反应的离子方程式为
溶液生成不溶于稀盐酸的白色沉淀,该反应的离子方程式为(7)雌黄(
 )和雄黄(
)和雄黄( )在自然界中共生且可以相互转化(两者的硫元素价态均为
)在自然界中共生且可以相互转化(两者的硫元素价态均为 价)。
价)。①
 和
和 在盐酸中恰好完全反应转化为
在盐酸中恰好完全反应转化为 和
和 并放出
并放出 气体。则参加反应的
气体。则参加反应的 和
和 的物质的量之比为
的物质的量之比为②
 和
和 可以相互转化,转化过程中存在如图所示的步骤。若1molAs4S4参加反应时,转移
可以相互转化,转化过程中存在如图所示的步骤。若1molAs4S4参加反应时,转移 电子,则物质
电子,则物质 为
为 。
。
您最近一年使用:0次
名校
解题方法
7 . 利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部分物质类别的对应关系。
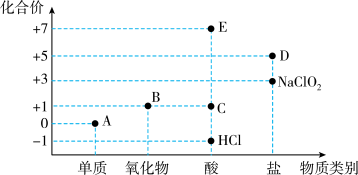
回答下列问题:
(1)已知D可用于实验室制O2,其焰色试验为紫色,D中含有的化学键有_______ ;A、B、C、D四种物质中,属于电解质的是_______ (填化学式)。
(2)B为酸性氧化物,则B与氢氧化钠溶液反应的化学方程式为_______ 。
(3)将E滴入碳酸氢钠溶液中,有大量气泡产生,该反应的离子方程式为_______ 。
(4)已知A与氢氧化钠溶液反应生成NaCl、NaClO和NaClO3的混合物,若n(NaClO)与n(NaClO3)之比为3∶1,则氧化剂与还原剂的物质的量之比为______ 。
(5)NaClO2、二氧化氯(ClO2)均为高效无毒的消毒剂。
①NaClO2的消毒效率是A的_______ 倍(还原产物都是Cl-,消毒效率以单位物质的量的物质得到的电子数表示)。
②ClO2在杀菌消毒过程中会产生亚氯酸盐( ),需将其转化为Cl-除去,下列试剂可将
),需将其转化为Cl-除去,下列试剂可将 转化为Cl-的是
转化为Cl-的是_________ (填标号)。
A.FeSO4 B.O3 C.KMnO4 D.Na2SO3

回答下列问题:
(1)已知D可用于实验室制O2,其焰色试验为紫色,D中含有的化学键有
(2)B为酸性氧化物,则B与氢氧化钠溶液反应的化学方程式为
(3)将E滴入碳酸氢钠溶液中,有大量气泡产生,该反应的离子方程式为
(4)已知A与氢氧化钠溶液反应生成NaCl、NaClO和NaClO3的混合物,若n(NaClO)与n(NaClO3)之比为3∶1,则氧化剂与还原剂的物质的量之比为
(5)NaClO2、二氧化氯(ClO2)均为高效无毒的消毒剂。
①NaClO2的消毒效率是A的
②ClO2在杀菌消毒过程中会产生亚氯酸盐(
 ),需将其转化为Cl-除去,下列试剂可将
),需将其转化为Cl-除去,下列试剂可将 转化为Cl-的是
转化为Cl-的是A.FeSO4 B.O3 C.KMnO4 D.Na2SO3
您最近一年使用:0次
2023-06-08更新
|
233次组卷
|
5卷引用:山东省临沂市2021-2022学年高一上学期期末统考化学试题
8 . 回答下列问题
(Ⅰ)自然界中硫元素的存在如图1,硫元素的常见化合价与部分物质类别的对应关系如图2,回答下列问题:

(1)图2中的N对应图1中物质的化学式为_______ 。
(2)X与Z反应中氧化剂与还原剂的物质的量之比为_______ 。
(3) 溶液易被氧化,检验
溶液易被氧化,检验 溶液变质的试剂为
溶液变质的试剂为_______ 。
(4)铜和M的浓溶液反应生成Z的化学方程式为_______ ;若要证明该反应产物有 ,需要采取的操作是
,需要采取的操作是_______ 。
(Ⅱ)氮氧化物( )是大气污染物之一,处理
)是大气污染物之一,处理 对于环境保护具有重要的意义。
对于环境保护具有重要的意义。
方案l:
(5)汽车排气管上装有催化转化器,可减少尾气对环境的污染,有害气体CO和NO反应可转化为无害气体排放,写出反应的化学方程式_______ 。
方案2:
在一定条件下 可将
可将 还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
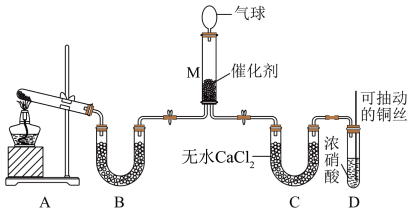
(6)用装置A制备 ,反应的化学方程式为
,反应的化学方程式为_______ ;装置B内的试剂是_______ 。
(7)装置D中发生反应的离子方程式是_______ ;可抽动铜丝的优点是_______ 。
(8)在装置M中 和
和 充分反应,生成两种对环境友好的物质,该反应中
充分反应,生成两种对环境友好的物质,该反应中 和
和 的物质的量之比为
的物质的量之比为_______ 。
方案3:
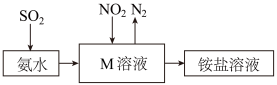
(9)工业生产中利用氨水吸收少量 和
和 ,原理如图所示。
,原理如图所示。 被吸收过程的离子方程式是
被吸收过程的离子方程式是_______ 。
(Ⅰ)自然界中硫元素的存在如图1,硫元素的常见化合价与部分物质类别的对应关系如图2,回答下列问题:

(1)图2中的N对应图1中物质的化学式为
(2)X与Z反应中氧化剂与还原剂的物质的量之比为
(3)
 溶液易被氧化,检验
溶液易被氧化,检验 溶液变质的试剂为
溶液变质的试剂为(4)铜和M的浓溶液反应生成Z的化学方程式为
 ,需要采取的操作是
,需要采取的操作是(Ⅱ)氮氧化物(
 )是大气污染物之一,处理
)是大气污染物之一,处理 对于环境保护具有重要的意义。
对于环境保护具有重要的意义。方案l:
(5)汽车排气管上装有催化转化器,可减少尾气对环境的污染,有害气体CO和NO反应可转化为无害气体排放,写出反应的化学方程式
方案2:
在一定条件下
 可将
可将 还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
(6)用装置A制备
 ,反应的化学方程式为
,反应的化学方程式为(7)装置D中发生反应的离子方程式是
(8)在装置M中
 和
和 充分反应,生成两种对环境友好的物质,该反应中
充分反应,生成两种对环境友好的物质,该反应中 和
和 的物质的量之比为
的物质的量之比为方案3:
(9)工业生产中利用氨水吸收少量
 和
和 ,原理如图所示。
,原理如图所示。 被吸收过程的离子方程式是
被吸收过程的离子方程式是
您最近一年使用:0次
解题方法
9 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:
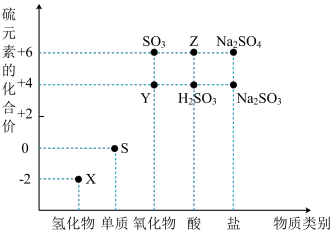
(1)S在周期表中的位置是_______ ;非金属性S_______ Cl(填“>”或“<”),S与Cl的最高价氧化物对应的水化物相比,酸性更强的是_______ (填化学式)。
(2)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有_______ (填化学式)。
(3)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是_______ (填字母)。
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(4)已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则24 mL 0.05 mol·L-1的Na2SO3溶液与20 mL 0.02 mol·L-1的K2Cr2O7溶液恰好反应时,Cr元素在还原产物中的化合价为_______ 。

(1)S在周期表中的位置是
(2)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
(3)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(4)已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则24 mL 0.05 mol·L-1的Na2SO3溶液与20 mL 0.02 mol·L-1的K2Cr2O7溶液恰好反应时,Cr元素在还原产物中的化合价为
您最近一年使用:0次
名校
10 . 如图是硫元素的常见化合价与部分物质类别的对应关系。请回答下列问题。
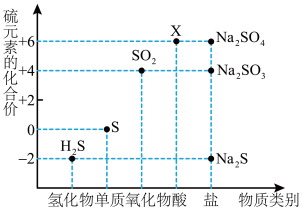
(1)X 的浓溶液与碳在一定条件下可以发生反应,体现了 X 的_______ 性。
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有_______ (填化学式)。
(3)将 H2S 与 SO2混合可生成淡黄色沉淀。该反应中氧化产物与还原产物的物质的量之比为_______ 。
(4)配平下列反应,并用单线桥法标出电子转移的方向和数目______ 。
Na2S+_______Na2SO3+_______H2SO4=_______Na2SO4+_______S↓+_______H2O
(5)下列关于硫及其化合物的叙述正确的是
(6)设 NA为阿伏加德罗常数的值。下列说法正确的是
为了证明铁和硫反应产物中铁的化合价,下面是某同学设计的实验过程的一部分:
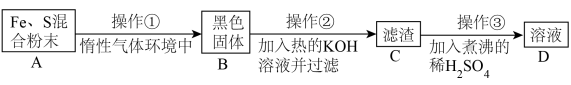
请回答以下问题:
(7)操作②的作用是_______ ,也可改用_______ 。
(8)混合粉末 A 中硫粉过量的原因是_______ 。
(9)下列溶液中通入SO2一定不会产生沉淀的是
(10)区别浓H2SO4和稀H2SO4,既简单又可靠的方法是

(1)X 的浓溶液与碳在一定条件下可以发生反应,体现了 X 的
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有
(3)将 H2S 与 SO2混合可生成淡黄色沉淀。该反应中氧化产物与还原产物的物质的量之比为
(4)配平下列反应,并用单线桥法标出电子转移的方向和数目
Na2S+_______Na2SO3+_______H2SO4=_______Na2SO4+_______S↓+_______H2O
(5)下列关于硫及其化合物的叙述正确的是
| A.试管内壁残留的硫可用酒精洗涤 | B.SO2的水溶液长期放置,酸性会增强 |
| C.SO2有毒,不可以做食品添加剂 | D.浓硫酸在空气中敞口放置,质量会减小 |
| A.1mol 铁单质与足量的硫单质充分反应,转移电子的数目为3NA |
| B.常温下,22.4LSO2与足量的O2反应,生成的SO3分子数为NA |
| C.常温下,将5.6g铁片投入足量的浓硫酸中,铁失去的电子数为0.3NA |
| D.1 molNa2O2与足量H2O反应,转移的电子数为NA |
为了证明铁和硫反应产物中铁的化合价,下面是某同学设计的实验过程的一部分:

请回答以下问题:
(7)操作②的作用是
(8)混合粉末 A 中硫粉过量的原因是
(9)下列溶液中通入SO2一定不会产生沉淀的是
| A.Ba(OH)2 | B.澄清石灰水 | C.Na2S | D.BaCl2 |
| A.各取少许溶液分别放入铜片 | B.分别与石蕊试液作用 |
| C.用玻璃棒各蘸少许液涂在纸上 | D.观察溶液的颜色 |
您最近一年使用:0次



