名校
1 . V(钒)能形成多种不同颜色的离子,其转化关系如图所示(注:图中所加试剂均足量),下列说法正确的是
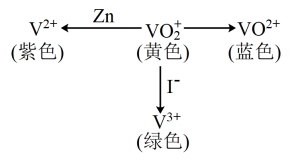

| A.图中转化关系只有部分存在电子转移 |
| B.由图中转化可知,I-比Zn还原性强 |
C.可加入氧化剂实现 溶液由黄色转化为蓝色 溶液由黄色转化为蓝色 |
D.V(钒)有 、 、 、 、 、 、 等多种化合价 等多种化合价 |
您最近一年使用:0次
2022-09-02更新
|
536次组卷
|
5卷引用:辽宁省鞍山市普通高中2021-2022学年高一上学期期末质量监测化学试题
2 . 氮、磷都是第ⅤA族元素,一些含氮、磷的化合物在生产生活中均有重要应用。
(1)磷化铝、磷化锌、磷化钙是我国目前最常见的熏蒸杀虫剂,都能与水或酸反应产生有毒气体膦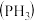 ,写出磷化铝与水反应的化学方程式:
,写出磷化铝与水反应的化学方程式:___________ 。
(2)羟基磷灰石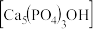 是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
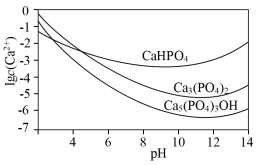
①图中所示3种钙盐,其中在人体中最稳定的存在形式是___________ (填化学式)。
②实验室制备羟基磷灰石时,应将___________ (填“磷酸”或“氢氧化钙悬浊液”,下同)滴加到___________ 中。
(3)氮的氧化物对大气污染比较严重,一定条件下可用 消除污染,请写出
消除污染,请写出 与
与 反应的化学方程式:
反应的化学方程式:___________ ,该反应中,被氧化的氮原子和被还原的氮原子的物质的量之比为___________ ,每消耗1mol ,同时转移
,同时转移___________ mol电子。
(1)磷化铝、磷化锌、磷化钙是我国目前最常见的熏蒸杀虫剂,都能与水或酸反应产生有毒气体膦
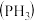 ,写出磷化铝与水反应的化学方程式:
,写出磷化铝与水反应的化学方程式:(2)羟基磷灰石
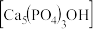 是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
①图中所示3种钙盐,其中在人体中最稳定的存在形式是
②实验室制备羟基磷灰石时,应将
(3)氮的氧化物对大气污染比较严重,一定条件下可用
 消除污染,请写出
消除污染,请写出 与
与 反应的化学方程式:
反应的化学方程式: ,同时转移
,同时转移
您最近一年使用:0次
12-13高三上·浙江宁波·期中
名校
3 . NaNO2是一种食品添加剂,它能致癌。酸性KMnO4溶液与NaNO2反应的化学方程式是:  +
+ +____→Mn2++
+____→Mn2++ +H2O。下列叙述中正确的是
+H2O。下列叙述中正确的是
 +
+ +____→Mn2++
+____→Mn2++ +H2O。下列叙述中正确的是
+H2O。下列叙述中正确的是A.该反应中 被还原 被还原 |
| B.反应过程中溶液的pH减小 |
| C.生成1molNaNO3需消耗0.4molKMnO4 |
| D.横线中的粒子是OH- |
您最近一年使用:0次
2022-07-26更新
|
555次组卷
|
45卷引用:辽宁省盘锦市高级中学2017-2018学年高二下学期期末考试化学试题
辽宁省盘锦市高级中学2017-2018学年高二下学期期末考试化学试题(已下线)2014届福建省南侨中学等五校高中毕业班期末摸底考试化学试卷(已下线)2013届浙江省宁波市效实中学高三上学期期中考试化学试卷(已下线)2014高考化学名师知识点精编 专题4氧化还原反应练习卷2016届湖南省益阳市箴言中学高三上学期第二次模拟测试化学试卷2017届新疆兵团农二师华山中学高三上学前考试化学试卷2016-2017学年河南省南阳一中高一上月考二化学卷2016-2017学年河南省南阳一中高一月考二化学卷天津市和平区2017-2018学年高一上学期期中质量调查化学试题2018-2019学年人教版高中化学必修一模块综合测评题(A)2018-2019学年苏教版高中化学必修一 模块综合测评(A)河南省安阳市第三十六中学2018-2019学年高二6月月考化学试题(已下线)专题2.3 氧化还原反应(练)-《2020年高考一轮复习讲练测》黑龙江省牡丹江市第一高级中学2019-2020学年高二上学期开学检测化学试题云南省漾濞二中2020届高三上学期开学考试化学试题江西省赣州市寻乌中学2020届高三上学期第一阶段考试化学试题(已下线)专题四 氧化还原反应(提分特训)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训(已下线)衔接点09 氧化还原反应的表示-2020年【衔接教材·暑假作业】初高中衔接化学(已下线)第09讲 氧化还原反应的计算及方程式的配平(精练)——2021年高考化学一轮复习讲练测高一必修第一册(鲁科2019)考试帮 模块综合测评B卷人教版(2019)高一必修第一册 模块综合测评-B卷贵州省铜仁市思南中学2021届高三上学期第二次月考化学试题江西省上饶市万年中学2020-2021学年高一上学期期中考试化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练湖南省武冈市第二中学2020-2021学年高一上学期第一次月考化学试题(已下线)衔接点09 氧化还原反应的表示-2021年初升高化学无忧衔接西藏拉萨市拉萨中学2022届高三上学期第一次月考理综化学试题黑龙江省哈尔滨市第六中学2021-2022学年高三上学期期中考试化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)4.2.2 氧化还原反应方程式的配平(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)黑龙江省哈尔滨市第九中学2021-2022学年高一上学期期中学业阶段性评价考试化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)考点05 氧化还原反应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题01 物质及其变化-2023年高考化学一轮复习小题多维练(全国通用)黑龙江省佳木斯市第八中学2022-2023学年高三上学期第一次调研(开学考试)化学试题黑龙江省哈尔滨市香坊区第九中学校2021-2022学年高一上学期期中考试化学试题西藏林芝市第二高级中学2022-2023学年高三上学期第二次月考化学试题(已下线)第一章 化学物质及其变化 第5练 氧化还原反应的计算与方程式的配平(已下线)考点05 氧化还原反应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)山东省枣庄市第三中学2022-2023学年高一上学期12月期中考试化学试题宁夏银川市第二中学2023-2024学年高三上学期统练二化学试题黑龙江省龙西北名校联合体2023-2024学年高三上学期期中考试化学试题黑龙江省齐齐哈尔市龙西北高中名校联盟2023-2024学年高三上学期10月联考化学试题江西省南昌市第十九中学2022-2023学年高一上学期12月第二次月考化学试卷
解题方法
4 . 中国“奋斗者”号深潜器研制及海试的成功,标志着我国在钛合金材料制备方面实现了重大突破。工业上用钛矿石(主要成分: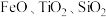 等)为原料制取钛并得到副产物绿矾(
等)为原料制取钛并得到副产物绿矾( ),工艺流程如下:
),工艺流程如下:
② 易水解,只能存在于强酸性溶液中
易水解,只能存在于强酸性溶液中
请回答以下问题:
(1)钛矿石在加入浓硫酸酸溶前要先粉碎,其目的是_______ 。
(2)加入适量铁粉的目的是_______ 。操作1名称为_______ 。
(3)固体2的主要成分是_______ 。
(4)在高温下, 和焦炭的混合物中通入
和焦炭的混合物中通入 得到
得到 和一种可燃性气体,请写出反应的化学方程式
和一种可燃性气体,请写出反应的化学方程式_______ 。
(5)用过量的钠在高温条件下与 反应可制得钛,写出此反应的化学方程式
反应可制得钛,写出此反应的化学方程式_______ 。该反应必须在高温下进行,你认为还应该控制的反应条件是_______ 。
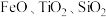 等)为原料制取钛并得到副产物绿矾(
等)为原料制取钛并得到副产物绿矾( ),工艺流程如下:
),工艺流程如下: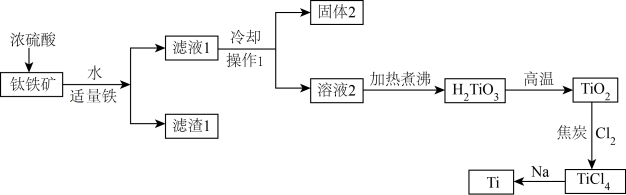

②
 易水解,只能存在于强酸性溶液中
易水解,只能存在于强酸性溶液中请回答以下问题:
(1)钛矿石在加入浓硫酸酸溶前要先粉碎,其目的是
(2)加入适量铁粉的目的是
(3)固体2的主要成分是
(4)在高温下,
 和焦炭的混合物中通入
和焦炭的混合物中通入 得到
得到 和一种可燃性气体,请写出反应的化学方程式
和一种可燃性气体,请写出反应的化学方程式(5)用过量的钠在高温条件下与
 反应可制得钛,写出此反应的化学方程式
反应可制得钛,写出此反应的化学方程式
您最近一年使用:0次
2022-07-20更新
|
466次组卷
|
4卷引用:辽宁省大连市2021-2022学年高一下学期期末考试化学试题
辽宁省大连市2021-2022学年高一下学期期末考试化学试题(已下线)综合突破02 期末压轴80题之非选择题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)河南省开封市杞县新世纪中学2022—2023学年高二上学期开学联考化学试题四川省青神中学校2022-2023学年高二下学期3月月考化学试题
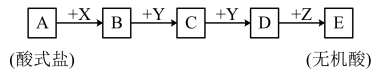
5 . Ⅰ.已知下列物质均由短周期元素组成,X无论是盐酸还是氢氧化钠,转化均能进行,又已知C的相对分子质量比D少16,A、B、C、D、E中均含有同一元素。_______ 。
(2)当X是氢氧化钠溶液时,C的化学式_______ 。
(3)写出A和足量氢氧化钠在加热条件下反应的化学方程式_______ 。
Ⅱ.金属及其化合物用途广泛,研究金属的提取、冶炼意义重大。
(4)下列各组金属,冶炼方法一定不同的是_______ (填字母)。
a.Hg、Ag b.Na、Mg c.Al、Fe d.Na、Ca
(5)以铬铁矿(主要成分为FeO和 ,含有少量
,含有少量 、
、 等杂质)为主要原料生产化工原料重铬酸钠
等杂质)为主要原料生产化工原料重铬酸钠 并制取铬,其主要工艺流程如下:
并制取铬,其主要工艺流程如下: 氧化为
氧化为 。
。
①“操作②”是_______ 。
②工业上可用固体A制取粗硅,写出反应的化学方程式:_______ 。
③写出溶液D转化为溶液E过程中反应的离子方程式:_______ 。
(2)当X是氢氧化钠溶液时,C的化学式
(3)写出A和足量氢氧化钠在加热条件下反应的化学方程式
Ⅱ.金属及其化合物用途广泛,研究金属的提取、冶炼意义重大。
(4)下列各组金属,冶炼方法一定不同的是
a.Hg、Ag b.Na、Mg c.Al、Fe d.Na、Ca
(5)以铬铁矿(主要成分为FeO和
 ,含有少量
,含有少量 、
、 等杂质)为主要原料生产化工原料重铬酸钠
等杂质)为主要原料生产化工原料重铬酸钠 并制取铬,其主要工艺流程如下:
并制取铬,其主要工艺流程如下: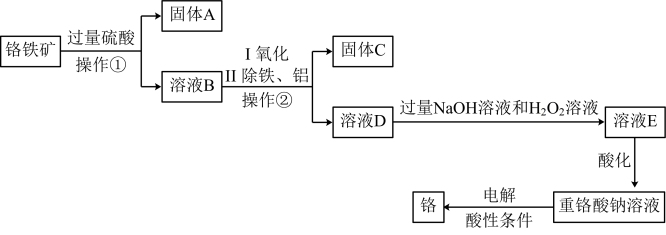
 氧化为
氧化为 。
。①“操作②”是
②工业上可用固体A制取粗硅,写出反应的化学方程式:
③写出溶液D转化为溶液E过程中反应的离子方程式:
您最近一年使用:0次
2022-07-19更新
|
392次组卷
|
3卷引用:辽宁省协作校2021-2022学年高一下学期期末考试化学试题
辽宁省协作校2021-2022学年高一下学期期末考试化学试题(已下线)专题06 化学与可持续发展-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)河南省开封市杞县新世纪中学2022—2023学年高二上学期开学联考化学试题
解题方法
6 . 海洋资源的综合利用是21世纪海祥开发利用的重点发展领域之一、从海水中可以制取氯、溴、镁等多种化工产品。在元素周期表中,溴(Br)位于第四周期,与Cl同主族。氯气可用于海水提溴,其工艺流程如下:
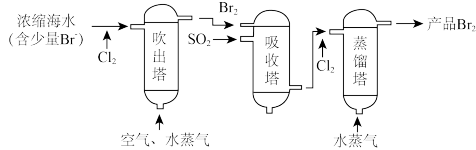
(1)进入吹出塔前海水中的 与
与 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(2)已知: 具有较强的氧化性,可氧化
具有较强的氧化性,可氧化 ,从吸收塔流出的溶液主要含
,从吸收塔流出的溶液主要含____ (写离子符号)。
(3)两次通入 的目的是富集浓缩溴,最终每获得
的目的是富集浓缩溴,最终每获得 ,理论上需消耗
,理论上需消耗_______ 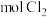 。
。
(4)某同学利用如图所示装置模拟吹出塔、吸收塔的实验,请回答下列问题:
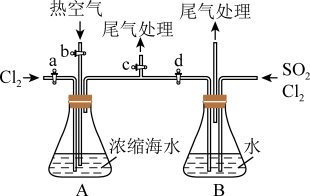
①进行吹出塔中实验时,应关闭活塞_______ ,打开活塞_______ 。
②可根据_______ (填现象),简单判断热空气的流速,通入热空气能吹出 的原因是
的原因是_______ 。
③装置B中要先通入 ,反应完全后再通入
,反应完全后再通入 ,简单判断通入的
,简单判断通入的 ,已反应完全的依据:
,已反应完全的依据:_______ 。

(1)进入吹出塔前海水中的
 与
与 发生反应的离子方程式为
发生反应的离子方程式为(2)已知:
 具有较强的氧化性,可氧化
具有较强的氧化性,可氧化 ,从吸收塔流出的溶液主要含
,从吸收塔流出的溶液主要含(3)两次通入
 的目的是富集浓缩溴,最终每获得
的目的是富集浓缩溴,最终每获得 ,理论上需消耗
,理论上需消耗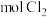 。
。(4)某同学利用如图所示装置模拟吹出塔、吸收塔的实验,请回答下列问题:

①进行吹出塔中实验时,应关闭活塞
②可根据
 的原因是
的原因是③装置B中要先通入
 ,反应完全后再通入
,反应完全后再通入 ,简单判断通入的
,简单判断通入的 ,已反应完全的依据:
,已反应完全的依据:
您最近一年使用:0次
2022-07-15更新
|
272次组卷
|
3卷引用:辽宁省辽阳市2021-2022学年高一下学期期末考试化学试题
解题方法
7 . 某校化学实验小组学生为了验证非金属元素氯的非金属性强于硫和氮,设计了一套实验装置如图(已知氯气能把氨气氧化生成氮气和氯化氢)。
(1)配平A中反应的化学方程式:_______ _______HCl(浓)+_______KMnO4=_______MnCl2+_______KCl+_______Cl2↑+_______ H2O。该反应中氧化剂与还原剂物质的量之比为_______ 。
(2)B中浸有NaOH溶液的棉花团的作用为_______ ;B中的现象为_______ ,由该现象得非金属性:Cl>>S。
(3)E中反应化学方程式为_______ 。
(4)D中出现白烟,涉及的反应化学方程式为_______ 、_______ 。
(5)有同学认为D中的现象并不能说明氯的非金属性大于氮,需要在C之前加装洗气装置,请指出洗气装置盛装试剂为_______ (填名称)。
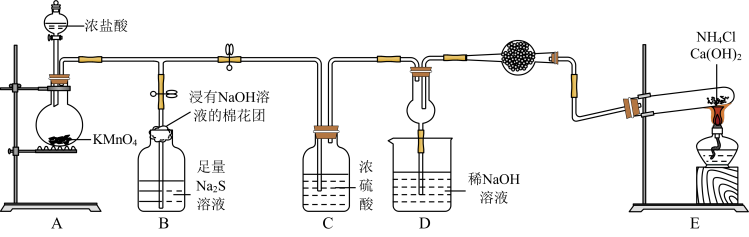
(1)配平A中反应的化学方程式:
(2)B中浸有NaOH溶液的棉花团的作用为
(3)E中反应化学方程式为
(4)D中出现白烟,涉及的反应化学方程式为
(5)有同学认为D中的现象并不能说明氯的非金属性大于氮,需要在C之前加装洗气装置,请指出洗气装置盛装试剂为
您最近一年使用:0次
2022-07-14更新
|
277次组卷
|
3卷引用:辽宁省朝阳市建平县2021-2022学年高一下学期期末考试化学试题
辽宁省朝阳市建平县2021-2022学年高一下学期期末考试化学试题黑龙江省齐齐哈尔市八校联考2022-2023学年高一下学期期末考试化学试题(已下线)专题01 硫、氮、硅及其化合物-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)
解题方法
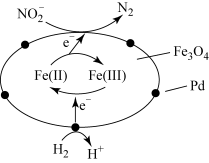
8 . 在催化剂作用下,H2可处理废水中的NO ,反应原理如图所示。下列说法错误的是
,反应原理如图所示。下列说法错误的是
 ,反应原理如图所示。下列说法错误的是
,反应原理如图所示。下列说法错误的是
| A.Fe3O4具有传递电子的作用 |
| B.Pd和Fe3O4均是该过程的催化剂 |
| C.处理后的废水中酸性增强 |
D.每消耗67.2L(标准状况下)H2,可还原2molNO |
您最近一年使用:0次
名校
解题方法
9 . 科学、安全、有效和合理地开发自然资源,对生产、生活有重要价值。请回答下列问题:
(1)活性炭吸附法是工业提取碘的方法之一,其流程如下:
II.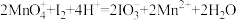
①氧化过程的离子方程式为_______ 。
②根据I2的特性,分离操作X应为_______ 、冷却结晶。
③酸性KMnO4是常用的强氧化剂,但该方法中却选择了价格较高的NaNO2,原因是_______ 。
(2)以金红石(主要成分为TiO2)为原料,制取Ti的工艺流程如图所示:_______ 。
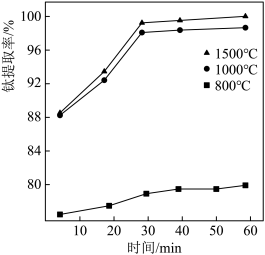
②II中钛的提取率在不同温度下随时间变化的曲线如图所示,则反应适宜的温度为_______ ℃。_______ 。
④海绵钛除杂时得到的MgCl2可以循环使用,在上述工艺流程中可循环使用的物质还有_______ (填化学式)。
(1)活性炭吸附法是工业提取碘的方法之一,其流程如下:
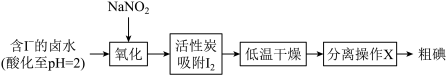
II.
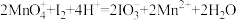
①氧化过程的离子方程式为
②根据I2的特性,分离操作X应为
③酸性KMnO4是常用的强氧化剂,但该方法中却选择了价格较高的NaNO2,原因是
(2)以金红石(主要成分为TiO2)为原料,制取Ti的工艺流程如图所示:
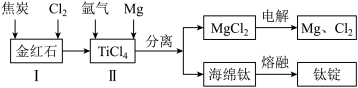
②II中钛的提取率在不同温度下随时间变化的曲线如图所示,则反应适宜的温度为
④海绵钛除杂时得到的MgCl2可以循环使用,在上述工艺流程中可循环使用的物质还有
您最近一年使用:0次
2022-07-12更新
|
652次组卷
|
6卷引用:辽宁省锦州市2021-2022学年高一下学期期末考试化学试卷
辽宁省锦州市2021-2022学年高一下学期期末考试化学试卷辽宁省沈阳市新民市第一高级中学2021-2022学年高一下学期期末考试化学试题黑龙江省齐齐哈尔市八校联考2022-2023学年高一下学期期末考试化学试题安徽省六安第一中学2022-2023学年高一下学期期末考试化学试题(已下线)猜想03 气体的制取、无机实验探究、无机综合应用(考题猜想)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)名校期末好题汇编-化学与可持续发展(非选择题)
名校
10 . 在酸性条件下,黄铁矿( )催化氧化的反应方程式为
)催化氧化的反应方程式为 。实现该反应的物质间转化如图所示。下列分析错误的是
。实现该反应的物质间转化如图所示。下列分析错误的是
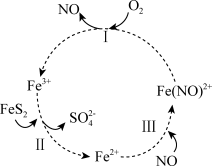
 )催化氧化的反应方程式为
)催化氧化的反应方程式为 。实现该反应的物质间转化如图所示。下列分析错误的是
。实现该反应的物质间转化如图所示。下列分析错误的是
A.反应Ⅰ的离子方程式为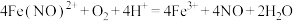 |
B.反应Ⅱ的氧化剂是 |
C.反应Ⅲ的离子方程式为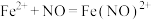 ,该反应是氧化还原反应 ,该反应是氧化还原反应 |
| D.在酸性条件下,黄铁矿催化氧化中NO作催化剂 |
您最近一年使用:0次
2022-05-28更新
|
2165次组卷
|
11卷引用:辽宁省葫芦岛市普通高中2022-2023学年高一上学期学业质量监测(期末)考试化学试题
辽宁省葫芦岛市普通高中2022-2023学年高一上学期学业质量监测(期末)考试化学试题江苏省徐州市沛县2021-2022学年高一下学期第二次学情调研化学试题(已下线)第一章《物质及其变化》能力提升单元检测-【帮课堂】2022-2023学年高一化学必修第一册精品讲义(人教版2019)(已下线)1.3.3 氧化还原反应方程式配平(好题帮)-备战2023年高考化学一轮复习考点帮(新教材新高考)安徽省舒城中学2022-2023学年高一上学期第二次月考化学试题湖北省襄阳市第一中学2022-2023学年高一上学期10月月考化学试题山西省晋城市第一中学(丹河校区)2022-2023学年高一上学期第二次调研考试化学试题山西省实验中学2022-2023学年高一上学期第一次月考化学试题江西省万载中学创新班2022-2023学年高一下学期期中考试化学试题四川省成都市成华区某校2023-2024学年高一上学期12月月考化学试题宁夏石嘴山市第三中学2023-2024学年高三上学期第二次月考 化学试题



