名校
1 . 现有部分元素的性质与原子或分子结构的相关信息如表所示:
(1)T、X、Y、Z形成的简单离子半径由大到小的顺序是_______ 。(用离子符号表示)
(2)元素Y与元素Z相比,金属性较强的是_______ (用元素符号表示),下列表述中能证明这一事实的是_______ 填字母序号。
A.Y单质的熔点比Z单质的低
B.Y的化合价比Z的低
C.常温下Y单质与水反应很剧烈,而Z单质与水很难反应
D.Y最高价氧化物对应的水化物的碱性比Z的强
(3)T与Y两种元素能形成既含离子键又含非极性共价键的常见化合物,写出该化合物的电子式_______ 。Y与和T同主族短周期元素M也能形成类似结构的化合物,请写出该化合物与硫酸反应的化学方程式_______ 。
(4)元素X与氢元素以原子个数共1∶2化合时,形成可用于火箭燃料的化合物W(W的相对分子质量为32)。元素T和氢元素以原子个数比1∶1化合形成化合物Q。Q与W发生氧化还原反应生成X的单质和的T另一种氢化物,请写出Q与W反应的化学方程式_______ 。
| 元素编号 | 元素性质与原子(或分子)结构的相关信息 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质分子为双原子分子,分子中含有3对共用电子对 |
| Y | M层比K层少1个电子 |
| Z | 其离子是第三周期金属元素的离子中半径最小的 |
(2)元素Y与元素Z相比,金属性较强的是
A.Y单质的熔点比Z单质的低
B.Y的化合价比Z的低
C.常温下Y单质与水反应很剧烈,而Z单质与水很难反应
D.Y最高价氧化物对应的水化物的碱性比Z的强
(3)T与Y两种元素能形成既含离子键又含非极性共价键的常见化合物,写出该化合物的电子式
(4)元素X与氢元素以原子个数共1∶2化合时,形成可用于火箭燃料的化合物W(W的相对分子质量为32)。元素T和氢元素以原子个数比1∶1化合形成化合物Q。Q与W发生氧化还原反应生成X的单质和的T另一种氢化物,请写出Q与W反应的化学方程式
您最近一年使用:0次
2024-03-24更新
|
216次组卷
|
2卷引用:浙江省余姚中学2023-2024学年高一下学期3月质量检测化学(选考)试题
名校
2 . 物质类别和元素化合价是研究物质性质的两个重要角度。
Ⅰ.硫在不同价态之间的转化: 溶液
溶液 溶液
溶液
(1)反应①的转化说明
 的类别属于
的类别属于 溶液,从化合价的角度分析,反应②合理的是
溶液,从化合价的角度分析,反应②合理的是a. b.
b. c.
c.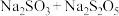
Ⅱ.某兴趣小组模拟工业制取 的装置(夹持和加热装置略)如图所示。
的装置(夹持和加热装置略)如图所示。
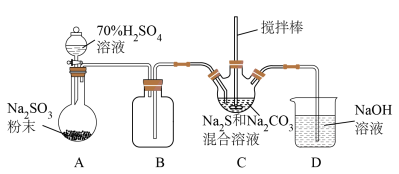
(2)装置A中发生反应的化学方程式为
(3)装置C发生的反应有①
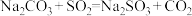 ;②……;③
;②……;③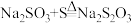 ,反应②的离子方程式为
,反应②的离子方程式为 ,应使三颈烧瓶中
,应使三颈烧瓶中 和
和 恰好完全反应,则三颈烧瓶中
恰好完全反应,则三颈烧瓶中 和
和 物质的量之比应为
物质的量之比应为(4)工业上常用
 溶液吸收尾气中的
溶液吸收尾气中的 ,氧化产物为
,氧化产物为 ,发生反应的离子方程式为
,发生反应的离子方程式为 可用于氰化物解毒,解毒原理为
可用于氰化物解毒,解毒原理为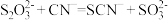 。体外模拟该解毒实验,检验该转化有
。体外模拟该解毒实验,检验该转化有 生成的实验操作是
生成的实验操作是
您最近一年使用:0次
名校
解题方法
3 . 硫酸铁是水处理行业用作净水的混凝剂和污泥的处理剂,广泛用于水的处理。一种以黄铁矿烧渣(主要成分为 、FeO、
、FeO、 等)为原料制取硫酸铁晶体的工艺流程如下:(已知:
等)为原料制取硫酸铁晶体的工艺流程如下:(已知: 不溶于水,不和硫酸反应。)
不溶于水,不和硫酸反应。)
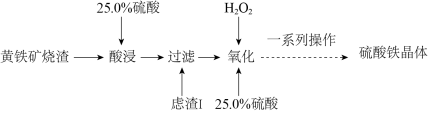
(1)“酸浸”前将黄铁矿烧渣粉碎的目的是
(2)已知:25.0%硫酸的密度
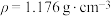 ,则25.0%硫酸的物质的量浓度为
,则25.0%硫酸的物质的量浓度为 的浓硫酸配制500mL 25.0%硫酸,则需用量筒量18
的浓硫酸配制500mL 25.0%硫酸,则需用量筒量18 的浓硫酸的体积为
的浓硫酸的体积为(3)“酸浸”后过滤所得滤液中所含的阳离子有
(4)“氧化”过程发生反应的离子方程式为
 ,优点是原料成本低,缺点是
,优点是原料成本低,缺点是(5)从“氧化”后的溶液中获得硫酸铁晶体,需经“一系列操作”,则“一系列操作”为
您最近一年使用:0次
名校
4 . 硫化氢的转化是资源利用和环境保护的重要研究课题。将 和空气的混合气体通入
和空气的混合气体通入 和
和 的混合溶液中回收S,反应历程如图。下列说法正确的是
的混合溶液中回收S,反应历程如图。下列说法正确的是
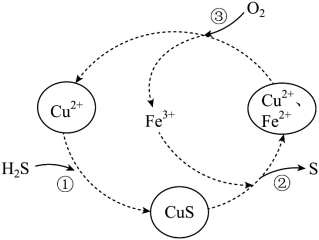
A.①反应的离子方程式为: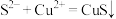 |
B.反应中, 、 、 可以循环利用 可以循环利用 |
C.由反应②③可知氧化性的强弱顺序: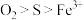 |
D.回收S的总反应为: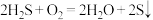 |
您最近一年使用:0次
解题方法
5 . 过氧化氢(H2O2,俗名为双氧水)、过氧化银(Ag2O2)广泛应用于抗菌消毒和化学能源等领域。


(1)根据下列三个反应回答问题:
反应Ⅰ.Ag2O+H2O2=2Ag+O2↑+H2O
反应Ⅱ.2H2O2=2H2O+O2↑
反应Ⅲ.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
①从氧化还原反应角度分析,反应Ⅰ中H2O2表现的性质为_____ 。
②上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序为_____ 。
③某强酸反应体系中发生一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、Mn 、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2.写出该反应的离子方程式:
、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2.写出该反应的离子方程式:_____ 。
(2)过氧化银(Ag2O2)为活性物质,可用作新型电池材料。用NaClO-NaOH溶液氧化AgNO3,能制得高纯度的纳米级Ag2O2.
①NaClO中Cl的化合价为_____ ,Ag2O2中O的化合价为_____ 。
②写出上述反应的化学方程式:_____ 。


(1)根据下列三个反应回答问题:
反应Ⅰ.Ag2O+H2O2=2Ag+O2↑+H2O
反应Ⅱ.2H2O2=2H2O+O2↑
反应Ⅲ.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
①从氧化还原反应角度分析,反应Ⅰ中H2O2表现的性质为
②上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序为
③某强酸反应体系中发生一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、Mn
 、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2.写出该反应的离子方程式:
、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2.写出该反应的离子方程式:(2)过氧化银(Ag2O2)为活性物质,可用作新型电池材料。用NaClO-NaOH溶液氧化AgNO3,能制得高纯度的纳米级Ag2O2.
①NaClO中Cl的化合价为
②写出上述反应的化学方程式:
您最近一年使用:0次
2024-03-23更新
|
55次组卷
|
2卷引用:湖南省衡阳市衡阳县第四中学2023-2024学年高一上学期10月月考化学试卷
解题方法
6 . 无水氯化镨( )是制取稀土金属镨及镨合金的主要原料,采用如图工艺流程可由孪生矿(主要含ZnS、FeS、
)是制取稀土金属镨及镨合金的主要原料,采用如图工艺流程可由孪生矿(主要含ZnS、FeS、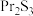 、
、 等)制备氯化镨晶体(
等)制备氯化镨晶体(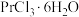 )。
)。

已知:① ;
;
② ;
;
③该条件下,溶液中部分金属离子生成氢氧化物开始沉淀和沉淀完全时的pH如表所示:
④沉淀时加入氨水逐步调节溶液的pH至6.5,此时滤渣Ⅱ中不含Pr的化合物。
回答下列问题:
(1)为了提高镨元素的浸出率,可采取的措施有_______ (填一种即可)。
(2)滤渣I的主要成分为 和S:
和S:
①写出 的一种用途:
的一种用途:_______ 。
②S可用来处理体温计破碎时渗出的液态Hg,还可用来制黑火药(由硫黄粉、硝酸钾和木炭混合而成,爆炸时的生成物为硫化钾、氮气和二氧化碳),写出黑火药爆炸时发生反应的化学方程式:_______ 。
(3)加入 的目的是
的目的是_______ ,其发生反应的离子方程式为_______
(4)滤渣Ⅱ的主要成分为_______ (填化学式)。
(5)利用表中的数据求出
_______ 。
 )是制取稀土金属镨及镨合金的主要原料,采用如图工艺流程可由孪生矿(主要含ZnS、FeS、
)是制取稀土金属镨及镨合金的主要原料,采用如图工艺流程可由孪生矿(主要含ZnS、FeS、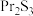 、
、 等)制备氯化镨晶体(
等)制备氯化镨晶体(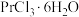 )。
)。
已知:①
 ;
;②
 ;
;③该条件下,溶液中部分金属离子生成氢氧化物开始沉淀和沉淀完全时的pH如表所示:
| 金属离子 |  |  |  |
| 开始沉淀的pH | 5.4 | 2.2 | 7.5 |
沉淀完全( )时的pH )时的pH | 6.4 | 3.2 | 9.0 |
回答下列问题:
(1)为了提高镨元素的浸出率,可采取的措施有
(2)滤渣I的主要成分为
 和S:
和S:①写出
 的一种用途:
的一种用途:②S可用来处理体温计破碎时渗出的液态Hg,还可用来制黑火药(由硫黄粉、硝酸钾和木炭混合而成,爆炸时的生成物为硫化钾、氮气和二氧化碳),写出黑火药爆炸时发生反应的化学方程式:
(3)加入
 的目的是
的目的是(4)滤渣Ⅱ的主要成分为
(5)利用表中的数据求出

您最近一年使用:0次
名校
7 . 汽车剧烈碰撞时,安全气囊中发生反应:NaN3+KNO3→K2O+Na2O+N2↑(未配平)。对上述反应的描述错误的是
| A.NaN3是还原剂,KNO3是氧化剂 |
| B.该反应中只有1种元素的化合价发生变化 |
| C.配平后物质的化学计量数依次为10、2、1、5、16 |
| D.生成N2的个数与转移电子个数之比为4:5 |
您最近一年使用:0次
2024-03-22更新
|
121次组卷
|
2卷引用:云南省腾冲市第八中学2023-2024学年高一上学期第四次月考化学试卷
8 . 氧化还原反应对我们的生产和生活同时具有正负两方面的影响,如果我们能够掌握化学变化的规律,就有可能做到趋利避害,使之更好地为社会发展服务。下面我们逐一分析:
(1)黑火药是我国古代的四大发明之一,黑火药着火时,发生如下氧化还原反应: 。在此反应中,还原剂为
。在此反应中,还原剂为_______ (填化学式),还原产物是_______ (填化学式),当该反应转移2.4mol电子时,产生气体的体积为_______ L(标况下)。
(2)湿法制备高铁酸钾 是在碱性环境中进行,反应体系中有六种反应微粒:
是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:_______ 。
(3)汽车剧烈碰撞时,安全气囊中发生反应: 。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为
。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为_______ 。
(4)在第一次世界大战期间,德军在比利时的伊普雷战役中使用了氯气制造的毒气弹。现代工业常用氯气制备漂白粉、消毒液等物质。写出制备漂白粉的化学反应方程式_______ 。
(1)黑火药是我国古代的四大发明之一,黑火药着火时,发生如下氧化还原反应:
 。在此反应中,还原剂为
。在此反应中,还原剂为(2)湿法制备高铁酸钾
 是在碱性环境中进行,反应体系中有六种反应微粒:
是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:(3)汽车剧烈碰撞时,安全气囊中发生反应:
 。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为
。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为(4)在第一次世界大战期间,德军在比利时的伊普雷战役中使用了氯气制造的毒气弹。现代工业常用氯气制备漂白粉、消毒液等物质。写出制备漂白粉的化学反应方程式
您最近一年使用:0次
解题方法
9 . 某研究小组以工厂废渣( 、
、 )为原料制取
)为原料制取 工艺流程如图。回答下列问题:
工艺流程如图。回答下列问题:
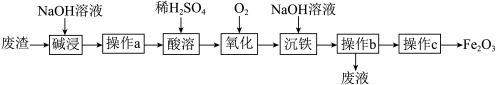
(1)“碱浸”时将固体磨碎的目的是_______ ,发生反应的离子方程式为_______ 。
(2)“操作a”需要的玻璃仪器有_______ 、_______ 、_______ 。
(3)“氧化”过程的离子方程式是_______ 。
(4)操作c的名称是_______ ;从分类的角度, 属于
属于_______ 。
(5)向 、Cu的混合物中加入盐酸,反应后的溶液中检验不出
、Cu的混合物中加入盐酸,反应后的溶液中检验不出 。检验
。检验 试剂名称是
试剂名称是_______ ,反应后溶液中没有 的原因是
的原因是_______ (用离子方程式表示)。
 、
、 )为原料制取
)为原料制取 工艺流程如图。回答下列问题:
工艺流程如图。回答下列问题:
(1)“碱浸”时将固体磨碎的目的是
(2)“操作a”需要的玻璃仪器有
(3)“氧化”过程的离子方程式是
(4)操作c的名称是
 属于
属于(5)向
 、Cu的混合物中加入盐酸,反应后的溶液中检验不出
、Cu的混合物中加入盐酸,反应后的溶液中检验不出 。检验
。检验 试剂名称是
试剂名称是 的原因是
的原因是
您最近一年使用:0次
10 . 草酸(H2C2O4)是一种二元弱酸。实验室配制了0.0100mol•L﹣1Na2C2O4标准溶液,现对25℃时该溶液的性质进行探究,下列所得结论正确的是
A.测得0.0100mol•L﹣1Na2C2O4溶液pH为8.6,此时溶液中存在:c(Na+)>c( )>c( )>c( )>c(OH-) )>c(OH-) |
B.向该溶液中滴加稀盐酸至溶液pH=7,此时溶液中存在:c(Na+)=c( )+2c( )+2c( ) ) |
C.向该溶液中加入足量稀硫酸酸化后,再滴加KMnO4溶液,发生反应的离子方程式为 +4 +4 +14H+=2CO2↑+4Mn2++7H2O +14H+=2CO2↑+4Mn2++7H2O |
D.已知CaC2O4难溶于水,存在溶解平衡,25℃时饱和CaC2O4溶液的浓度为5×10﹣5mol•L﹣1,向该溶液中加入等体积0.0200mol•L﹣1CaCl2溶液,所得上层清液中c( )<5.00×10﹣5mol•L﹣1 )<5.00×10﹣5mol•L﹣1 |
您最近一年使用:0次



