1 . 请按照要求填写:
(1)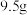 某二价金属氯化物
某二价金属氯化物 中含有
中含有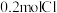 ,则
,则 的摩尔质量是
的摩尔质量是___________ 。
(2)除去镁粉中的铝粉,所选试剂为___________ ,相关的离子反应方程式为___________ 。
(3)配平离子方程式:___________ 。
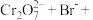 ___________=___________
___________=___________ ___________
___________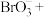 ___________
___________
(4)2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂 的一种制备方法如下。
的一种制备方法如下。___________ ;
② 的结构式是
的结构式是___________ ;
③反应Ⅰ的离子方程式是___________ 。
(1)
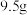 某二价金属氯化物
某二价金属氯化物 中含有
中含有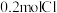 ,则
,则 的摩尔质量是
的摩尔质量是(2)除去镁粉中的铝粉,所选试剂为
(3)配平离子方程式:
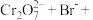 ___________=___________
___________=___________ ___________
___________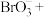 ___________
___________
(4)2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂
 的一种制备方法如下。
的一种制备方法如下。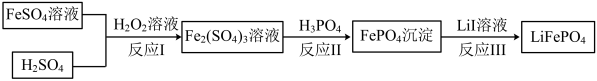
②
 的结构式是
的结构式是③反应Ⅰ的离子方程式是
您最近一年使用:0次
名校
解题方法
2 . 铈(Ce)是一种典型的稀土元素,属于国家战略资源。以某废料(主要含 ,还含少量
,还含少量 、
、 、
、 及微量MnO)为原料可制备无水氯化铈
及微量MnO)为原料可制备无水氯化铈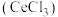 ,主要步骤如下:
,主要步骤如下:
(1)酸浸:用稀硫酸和双氧水的混合溶液浸取废料粉末,浸取液中含有 、
、 、
、 、
、 等金属阳离子。已知
等金属阳离子。已知 不溶于水,写出其发生反应的离子方程式:
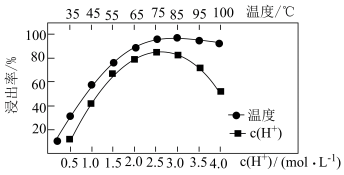
不溶于水,写出其发生反应的离子方程式:________ 。Ce的浸出率与 、温度的关系如图所示。生产中应选择的适宜条件为
、温度的关系如图所示。生产中应选择的适宜条件为________ 。
(2)除杂:向浸出液中加入NaOH溶液调节pH除去 、
、 。注:当
。注:当 时,
时, 沉淀开始溶解。有关沉淀数据(25℃)如下表(“完全沉淀”时金属离子浓度
沉淀开始溶解。有关沉淀数据(25℃)如下表(“完全沉淀”时金属离子浓度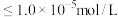 )。
)。
则 的
的
________ ,若浸取液中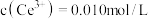 ,则须调节溶液pH的范围是
,则须调节溶液pH的范围是________ (加入NaOH溶液过程忽略体积变化)。
(3)萃取与反萃取:向除杂后的溶液中,加入有机物HT,发生反应: (水层)+3HT(有机层)
(水层)+3HT(有机层)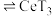 (有机层)
(有机层)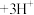 (水层)。向分离所得有机层中加入
(水层)。向分离所得有机层中加入_______ 能获得较纯的 溶液。
溶液。
结晶析出:将 溶液蒸发浓缩、冷却结晶,过滤,得到
溶液蒸发浓缩、冷却结晶,过滤,得到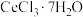 晶体。
晶体。
(4)加热脱水:将 固体和
固体和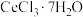 混合,在真空中加热可得无水
混合,在真空中加热可得无水 。加入
。加入 固体的作用是
固体的作用是________ 。
(5)对 样品纯度进行测定的方法:准确称取样品62.50g,配成1000mL溶液,取50.00mL上述溶液置于锥形瓶中,加入稍过量的过二硫酸铵
样品纯度进行测定的方法:准确称取样品62.50g,配成1000mL溶液,取50.00mL上述溶液置于锥形瓶中,加入稍过量的过二硫酸铵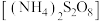 溶液使
溶液使 被氧化为
被氧化为 ,萃取剂萃取
,萃取剂萃取 ,再用
,再用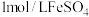 标准溶液滴定至终点,重复2~3次,平均消耗标准液10.00mL,则
标准溶液滴定至终点,重复2~3次,平均消耗标准液10.00mL,则 样品的纯度为
样品的纯度为________ %(保留小数点后两位)。
 ,还含少量
,还含少量 、
、 、
、 及微量MnO)为原料可制备无水氯化铈
及微量MnO)为原料可制备无水氯化铈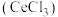 ,主要步骤如下:
,主要步骤如下:(1)酸浸:用稀硫酸和双氧水的混合溶液浸取废料粉末,浸取液中含有
 、
、 、
、 、
、 等金属阳离子。已知
等金属阳离子。已知 不溶于水,写出其发生反应的离子方程式:
不溶于水,写出其发生反应的离子方程式: 、温度的关系如图所示。生产中应选择的适宜条件为
、温度的关系如图所示。生产中应选择的适宜条件为
(2)除杂:向浸出液中加入NaOH溶液调节pH除去
 、
、 。注:当
。注:当 时,
时, 沉淀开始溶解。有关沉淀数据(25℃)如下表(“完全沉淀”时金属离子浓度
沉淀开始溶解。有关沉淀数据(25℃)如下表(“完全沉淀”时金属离子浓度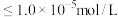 )。
)。沉淀 |
|
|
|
|
恰好完全沉淀时pH | 5.2 | 2.8 | 9.0 | 10.1 |
 的
的
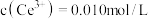 ,则须调节溶液pH的范围是
,则须调节溶液pH的范围是(3)萃取与反萃取:向除杂后的溶液中,加入有机物HT,发生反应:
 (水层)+3HT(有机层)
(水层)+3HT(有机层)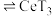 (有机层)
(有机层)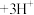 (水层)。向分离所得有机层中加入
(水层)。向分离所得有机层中加入 溶液。
溶液。结晶析出:将
 溶液蒸发浓缩、冷却结晶,过滤,得到
溶液蒸发浓缩、冷却结晶,过滤,得到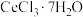 晶体。
晶体。(4)加热脱水:将
 固体和
固体和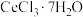 混合,在真空中加热可得无水
混合,在真空中加热可得无水 。加入
。加入 固体的作用是
固体的作用是(5)对
 样品纯度进行测定的方法:准确称取样品62.50g,配成1000mL溶液,取50.00mL上述溶液置于锥形瓶中,加入稍过量的过二硫酸铵
样品纯度进行测定的方法:准确称取样品62.50g,配成1000mL溶液,取50.00mL上述溶液置于锥形瓶中,加入稍过量的过二硫酸铵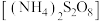 溶液使
溶液使 被氧化为
被氧化为 ,萃取剂萃取
,萃取剂萃取 ,再用
,再用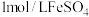 标准溶液滴定至终点,重复2~3次,平均消耗标准液10.00mL,则
标准溶液滴定至终点,重复2~3次,平均消耗标准液10.00mL,则 样品的纯度为
样品的纯度为
您最近一年使用:0次
2023-08-08更新
|
432次组卷
|
2卷引用:辽宁省丹东市等2地大石桥市第三高级中学等2校2022-2023学年高三上学期1月期末考试化学试题
3 . 往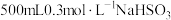 溶液中逐滴加入KIO3溶液,加入的KIO3和生成的I2的物质的量的关系曲线如图所示(不考虑物质与水发生的反应及弱电解质的电离)。
溶液中逐滴加入KIO3溶液,加入的KIO3和生成的I2的物质的量的关系曲线如图所示(不考虑物质与水发生的反应及弱电解质的电离)。
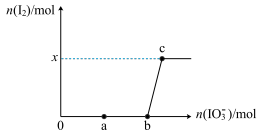
回答下列问题:
(1)NaHSO3在水中的电离方程式为___________ 。
(2)a点溶液的pH___________ (填“>”、“<”或“=”)7,判断的理由为___________ (用离子方程式表示)。
(3)b点溶液中所含的阳离子有___________ (填离子符号)。
(4)b→c的离子方程式为___________ 。
(5)往c点溶液中加入淀粉溶液,可以观察到的现象为___________ 。
(6)x=___________ 。
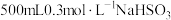 溶液中逐滴加入KIO3溶液,加入的KIO3和生成的I2的物质的量的关系曲线如图所示(不考虑物质与水发生的反应及弱电解质的电离)。
溶液中逐滴加入KIO3溶液,加入的KIO3和生成的I2的物质的量的关系曲线如图所示(不考虑物质与水发生的反应及弱电解质的电离)。
回答下列问题:
(1)NaHSO3在水中的电离方程式为
(2)a点溶液的pH
(3)b点溶液中所含的阳离子有
(4)b→c的离子方程式为
(5)往c点溶液中加入淀粉溶液,可以观察到的现象为
(6)x=
您最近一年使用:0次
4 . 近几年来关于氮污染的治理倍受关注。
(1)三效催化剂是最为常见的汽车尾气催化剂,能同时实现汽车尾气中的CO、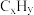 、
、 三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。

在图示的转化中,被还原的元素是___________ ,X的化学式为___________ 。
(2)SCR技术可使 与
与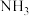 直接反应,实现无害转化。假设
直接反应,实现无害转化。假设 是NO时,发生反应的化学方程式是
是NO时,发生反应的化学方程式是_______ 。
(3)利用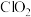 氧化氮氧化物反应过程如下:
氧化氮氧化物反应过程如下: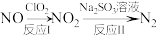 。反应I的化学方程式是
。反应I的化学方程式是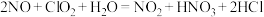 ,反应II的离子方程式是
,反应II的离子方程式是___________ 。
(4)加入过量次氯酸钠可使废水中 完全转化为
完全转化为 ,而本身被还原为NaCl。
,而本身被还原为NaCl。
①检验废水中是否存在 的方法是
的方法是___________ 。
②若处理废水产生了0.448L (标准状况),则需消耗浓度为2mol/L的次氯酸钠的体积为
(标准状况),则需消耗浓度为2mol/L的次氯酸钠的体积为___________ mL。
(1)三效催化剂是最为常见的汽车尾气催化剂,能同时实现汽车尾气中的CO、
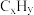 、
、 三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
在图示的转化中,被还原的元素是
(2)SCR技术可使
 与
与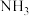 直接反应,实现无害转化。假设
直接反应,实现无害转化。假设 是NO时,发生反应的化学方程式是
是NO时,发生反应的化学方程式是(3)利用
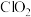 氧化氮氧化物反应过程如下:
氧化氮氧化物反应过程如下: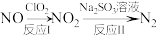 。反应I的化学方程式是
。反应I的化学方程式是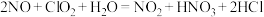 ,反应II的离子方程式是
,反应II的离子方程式是(4)加入过量次氯酸钠可使废水中
 完全转化为
完全转化为 ,而本身被还原为NaCl。
,而本身被还原为NaCl。①检验废水中是否存在
 的方法是
的方法是②若处理废水产生了0.448L
 (标准状况),则需消耗浓度为2mol/L的次氯酸钠的体积为
(标准状况),则需消耗浓度为2mol/L的次氯酸钠的体积为
您最近一年使用:0次
5 . 化学是一门实用性很强的科学,请根据题意填空:
(1)铝制餐具不宜长时间存放酸性、碱性食物,但常温下铝制容器可以盛装___________ (填“浓硫酸”或“浓盐酸”)。
(2)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是___________ (填化学式)。
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质,请完成一定条件下该反应的化学方程式:2NO+2CO 2CO2+
2CO2+__________ 。
(4)“厉害了,我的国”,2017年4月:“天舟一号”成功对接,12月:大型客机C919(如下图)第二次在上海浦东机场试飞成功,实现了我国航空领域的新突破。
请回答下列问题:

①铝合金和碳纤维复合材料是飞机、火箭的常用材料,这主要利用了它们具有的共同性能是___________ (填字母序号)。
A.密度小 强度好 B.密度大 硬度大 C.熔点低 硬度小
②铝的金属活动性比铁的___________ (填“强”或“弱”),空气中,铝比铁具有更好的抗腐蚀性,原因是___________ (用化学反应方程式解释)。
③高温结构陶瓷可用于制造汽车发动机,通常所用的材料是氮化硅(Si3N4),该化合物中硅元素的化合价为___________ 。
(1)铝制餐具不宜长时间存放酸性、碱性食物,但常温下铝制容器可以盛装
(2)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质,请完成一定条件下该反应的化学方程式:2NO+2CO
 2CO2+
2CO2+(4)“厉害了,我的国”,2017年4月:“天舟一号”成功对接,12月:大型客机C919(如下图)第二次在上海浦东机场试飞成功,实现了我国航空领域的新突破。
请回答下列问题:

①铝合金和碳纤维复合材料是飞机、火箭的常用材料,这主要利用了它们具有的共同性能是
A.密度小 强度好 B.密度大 硬度大 C.熔点低 硬度小
②铝的金属活动性比铁的
③高温结构陶瓷可用于制造汽车发动机,通常所用的材料是氮化硅(Si3N4),该化合物中硅元素的化合价为
您最近一年使用:0次
解题方法
6 . 氯元素的单质及其化合物在生产、生活中均有重要用途。请结合相关知识回答下列问题:
(1)84消毒液能有效杀灭新冠病毒,其主要成分为NaClO,在常温下,将氯气通入烧碱中可以得到NaClO,写出该反应的离子方程式___________ ,使用说明中特别提醒84消毒液不可与洁厕灵(主要成分盐酸)混合使用,否则会产生 ,请用离子方程式表示其原因
,请用离子方程式表示其原因___________ 。
(2)世界卫生组织(WHO)和中国卫健委公认二氧化氯( )为新时代绿色消毒剂。工业上可采用
)为新时代绿色消毒剂。工业上可采用 与氯酸钠在硫酸存在的条件下反应制取
与氯酸钠在硫酸存在的条件下反应制取 ,并生成
,并生成 ,写出工业上制取
,写出工业上制取 反应的化学方程式
反应的化学方程式___________ ,该反应中氧化剂与还原剂物质的量之比为___________ 。
(3)现测定二氧化氯漂白液的浓度。步骤如下:量取5mL二氧化氯漂白液于锥形瓶中,加蒸馏水稀释到25mL,再加入硫酸和10%碘化钾10mL,此时溶液出现棕色(发生反应: ,然后再逐滴滴入0.12
,然后再逐滴滴入0.12 硫代硫酸钠溶液15mL,恰好完全反应(发生反应:
硫代硫酸钠溶液15mL,恰好完全反应(发生反应: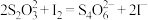 ,计算该漂白液中二氧化氯的物质的量浓度:
,计算该漂白液中二氧化氯的物质的量浓度:___________ 。
(4)实验室要配制1L 0.2 的NaClO溶液。配制过程如下:
的NaClO溶液。配制过程如下:
①将已恢复至室温的溶液沿玻璃棒注入1L容量瓶中。
②盖好容量瓶瓶塞,反复上下颠倒,摇匀。
③用天平准确称取14.9g的NaClO固体并放入烧杯中,加入约30mL的蒸馏水充分搅拌、溶解。
④用30mL蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将每次洗涤的溶液转入容量瓶中,振荡。
⑤定容。
⑥将配置好的溶液倒入试剂瓶中,贴好标签。
实验操作顺序依次为___________ (填序号),定容的具体操作是___________ 。
(1)84消毒液能有效杀灭新冠病毒,其主要成分为NaClO,在常温下,将氯气通入烧碱中可以得到NaClO,写出该反应的离子方程式
 ,请用离子方程式表示其原因
,请用离子方程式表示其原因(2)世界卫生组织(WHO)和中国卫健委公认二氧化氯(
 )为新时代绿色消毒剂。工业上可采用
)为新时代绿色消毒剂。工业上可采用 与氯酸钠在硫酸存在的条件下反应制取
与氯酸钠在硫酸存在的条件下反应制取 ,并生成
,并生成 ,写出工业上制取
,写出工业上制取 反应的化学方程式
反应的化学方程式(3)现测定二氧化氯漂白液的浓度。步骤如下:量取5mL二氧化氯漂白液于锥形瓶中,加蒸馏水稀释到25mL,再加入硫酸和10%碘化钾10mL,此时溶液出现棕色(发生反应:
 ,然后再逐滴滴入0.12
,然后再逐滴滴入0.12 硫代硫酸钠溶液15mL,恰好完全反应(发生反应:
硫代硫酸钠溶液15mL,恰好完全反应(发生反应: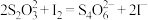 ,计算该漂白液中二氧化氯的物质的量浓度:
,计算该漂白液中二氧化氯的物质的量浓度:(4)实验室要配制1L 0.2
 的NaClO溶液。配制过程如下:
的NaClO溶液。配制过程如下:①将已恢复至室温的溶液沿玻璃棒注入1L容量瓶中。
②盖好容量瓶瓶塞,反复上下颠倒,摇匀。
③用天平准确称取14.9g的NaClO固体并放入烧杯中,加入约30mL的蒸馏水充分搅拌、溶解。
④用30mL蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将每次洗涤的溶液转入容量瓶中,振荡。
⑤定容。
⑥将配置好的溶液倒入试剂瓶中,贴好标签。
实验操作顺序依次为
您最近一年使用:0次
7 . 氯元素形成的单质或化合物用途广泛。
(1)氯元素在周期表中的位置_____ 。
(2)工业上可用钢瓶储运液氯,在加注液氯前要对钢瓶进行充分干燥的原因是_____ (填合适的化学方程式)。
如图是氯的价类二维图:

其中C是一种新型净水剂,其合成路线如图:
(3)C为______ (填化学式)。
(4)在氧化还原反应中,可将其拆成氧化半反应和还原半反应,比如:Zn+Cu2+=Zn2++Cu的氧化半反应可以表示为:Zn-2e-=Zn2+,电解时生成d的氧化半反应式为______ 。
(5)“a的合成塔”中发生反应的化学方程式为______ 。
(6)“c的发生器”中发生反应的离子方程式为_____ (写出正确的离子方程式并用单线桥法分析电子转移的情况)。
(7)实验测得等物质的量的f、O3、H2O2具有相同的漂白能力,原因是_____ 。
(1)氯元素在周期表中的位置
(2)工业上可用钢瓶储运液氯,在加注液氯前要对钢瓶进行充分干燥的原因是
如图是氯的价类二维图:

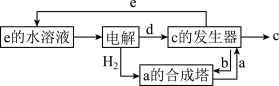
其中C是一种新型净水剂,其合成路线如图:

(3)C为
(4)在氧化还原反应中,可将其拆成氧化半反应和还原半反应,比如:Zn+Cu2+=Zn2++Cu的氧化半反应可以表示为:Zn-2e-=Zn2+,电解时生成d的氧化半反应式为
(5)“a的合成塔”中发生反应的化学方程式为
(6)“c的发生器”中发生反应的离子方程式为
(7)实验测得等物质的量的f、O3、H2O2具有相同的漂白能力,原因是
您最近一年使用:0次
名校
解题方法
8 . 生活离不开化学.家庭厨卫中有许多中学化学常见的物质,括号内为厨卫商品的主要成分。
①食盐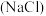 ②料酒(乙醇) ③食醋(乙酸) ④碱面
②料酒(乙醇) ③食醋(乙酸) ④碱面
⑤发酵粉( 和明矾) ⑥84消毒液
和明矾) ⑥84消毒液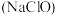 ⑦洁厕灵
⑦洁厕灵
回答下列问题:
(1)当食盐不慎洒落在天然气的火焰上,观察到的现象是______________ 。
(2)②③的主要成分可以归为一类物质,其分类的依据是______________(填正确答案标号)。
(3)明矾可做净水剂的理由是(用离子方程式表示)_________________ 。
(4)除去 固体中混有的少量
固体中混有的少量 杂质,应采取的最佳方法是
杂质,应采取的最佳方法是______________ 。
(5)相同条件下,等质量的 与
与 分别与足量的盐酸反应产生气体的体积比为
分别与足量的盐酸反应产生气体的体积比为____________ 。
(6)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:__________________ 。
①食盐
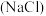 ②料酒(乙醇) ③食醋(乙酸) ④碱面
②料酒(乙醇) ③食醋(乙酸) ④碱面
⑤发酵粉(
 和明矾) ⑥84消毒液
和明矾) ⑥84消毒液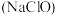 ⑦洁厕灵
⑦洁厕灵
回答下列问题:
(1)当食盐不慎洒落在天然气的火焰上,观察到的现象是
(2)②③的主要成分可以归为一类物质,其分类的依据是______________(填正确答案标号)。
| A.两种物质都是非电解质 | B.两种物质都是电解质 |
| C.两种物质都是含碳化合物 | D.两种物质都是氧化物 |
(4)除去
 固体中混有的少量
固体中混有的少量 杂质,应采取的最佳方法是
杂质,应采取的最佳方法是(5)相同条件下,等质量的
 与
与 分别与足量的盐酸反应产生气体的体积比为
分别与足量的盐酸反应产生气体的体积比为(6)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:
您最近一年使用:0次
2023-02-19更新
|
102次组卷
|
2卷引用:辽宁省葫芦岛市普通高中2022-2023学年高一上学期学业质量监测(期末)考试化学试题
名校
9 . 从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。氯及其化合物有重要用途,下图为氯元素的“价类二维图”的部分信息。请回答下列问题:
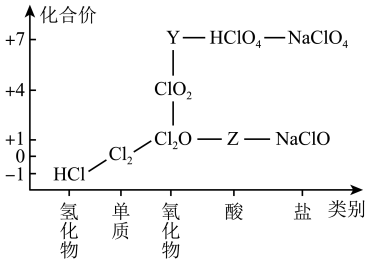
(1)根据图中信息写出Y、Z的化学式_______ 、_______ 。(每空1分)
(2)84消毒液能有效杀灭新冠病毒。某品牌84消毒液瓶体的部分标签如图所示。

①某使用说明中特别提醒84消毒液不可与洁厕灵(主要成分盐酸)混合使用,否则会产生 ,请用离子方程式表示其原因
,请用离子方程式表示其原因_______ 。
②如图所示,该品牌84消毒液的物质的量浓度为_______ ,84消毒液使用时需要稀释,某化学实验小组用上述84消毒液配制500mL 的稀溶液,需要用量筒量取该84消毒液
的稀溶液,需要用量筒量取该84消毒液_______ mL。
③配制过程中,下列操作会造成新配制的稀溶液浓度偏低的是_______ 。
A.量取浓84消毒液的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
B.容量瓶使用时未干燥
C.定容时俯视刻度线
D.定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线

(1)根据图中信息写出Y、Z的化学式
(2)84消毒液能有效杀灭新冠病毒。某品牌84消毒液瓶体的部分标签如图所示。

①某使用说明中特别提醒84消毒液不可与洁厕灵(主要成分盐酸)混合使用,否则会产生
 ,请用离子方程式表示其原因
,请用离子方程式表示其原因②如图所示,该品牌84消毒液的物质的量浓度为
 的稀溶液,需要用量筒量取该84消毒液
的稀溶液,需要用量筒量取该84消毒液③配制过程中,下列操作会造成新配制的稀溶液浓度偏低的是
A.量取浓84消毒液的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
B.容量瓶使用时未干燥
C.定容时俯视刻度线
D.定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
您最近一年使用:0次
10 . 氮、磷都是第ⅤA族元素,一些含氮、磷的化合物在生产生活中均有重要应用。
(1)磷化铝、磷化锌、磷化钙是我国目前最常见的熏蒸杀虫剂,都能与水或酸反应产生有毒气体膦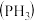 ,写出磷化铝与水反应的化学方程式:
,写出磷化铝与水反应的化学方程式:___________ 。
(2)羟基磷灰石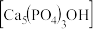 是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
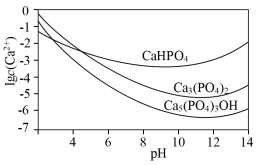
①图中所示3种钙盐,其中在人体中最稳定的存在形式是___________ (填化学式)。
②实验室制备羟基磷灰石时,应将___________ (填“磷酸”或“氢氧化钙悬浊液”,下同)滴加到___________ 中。
(3)氮的氧化物对大气污染比较严重,一定条件下可用 消除污染,请写出
消除污染,请写出 与
与 反应的化学方程式:
反应的化学方程式:___________ ,该反应中,被氧化的氮原子和被还原的氮原子的物质的量之比为___________ ,每消耗1mol ,同时转移
,同时转移___________ mol电子。
(1)磷化铝、磷化锌、磷化钙是我国目前最常见的熏蒸杀虫剂,都能与水或酸反应产生有毒气体膦
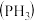 ,写出磷化铝与水反应的化学方程式:
,写出磷化铝与水反应的化学方程式:(2)羟基磷灰石
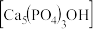 是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
①图中所示3种钙盐,其中在人体中最稳定的存在形式是
②实验室制备羟基磷灰石时,应将
(3)氮的氧化物对大气污染比较严重,一定条件下可用
 消除污染,请写出
消除污染,请写出 与
与 反应的化学方程式:
反应的化学方程式: ,同时转移
,同时转移
您最近一年使用:0次





