解题方法
1 . 填空
(1)在钢铁厂的生产中,炽热的铁水或者钢水注入模具之前,模具必须进行充分的干燥处理,不得留有水,原因是________ (用化学方程式表示)。
(2)由于Na2O2已与CO2、H2O发生反应放出氧气,因此可在呼吸面具或潜水艇中作为氧气的来源,写出Na2O2与H2O反应的化学方程式_________ 。
(3)将Cl2通入冷的石灰乳中,即制得以Ca(ClO)2为有效成分的漂白粉,写出对应的化学方程式________ 。
(4)配平化学方程式:Fe2++ +H+=Fe3++NO↑+H2O。
+H+=Fe3++NO↑+H2O。_______
(5)向一个铝制易拉罐中充满CO2,然后往罐中注入足量的浓NaOH溶液,立即用胶布封严罐口。一会儿听到罐内发出“咔、咔”的响声,且易拉罐变瘪,再过一会易拉罐又鼓起来恢复原样,写出变瘪的离子方程式___________ 。
(1)在钢铁厂的生产中,炽热的铁水或者钢水注入模具之前,模具必须进行充分的干燥处理,不得留有水,原因是
(2)由于Na2O2已与CO2、H2O发生反应放出氧气,因此可在呼吸面具或潜水艇中作为氧气的来源,写出Na2O2与H2O反应的化学方程式
(3)将Cl2通入冷的石灰乳中,即制得以Ca(ClO)2为有效成分的漂白粉,写出对应的化学方程式
(4)配平化学方程式:Fe2++
 +H+=Fe3++NO↑+H2O。
+H+=Fe3++NO↑+H2O。(5)向一个铝制易拉罐中充满CO2,然后往罐中注入足量的浓NaOH溶液,立即用胶布封严罐口。一会儿听到罐内发出“咔、咔”的响声,且易拉罐变瘪,再过一会易拉罐又鼓起来恢复原样,写出变瘪的离子方程式
您最近一年使用:0次
解题方法
2 . 钛是一种性能非常优越的金属,有着广泛的应用,有人说“21世纪将是钛的世纪”。以金红石矿(主要成分为TiO2,含有少量Al2O3、SiO2、FeO、Fe2O3等杂质)为主要原料,首先反应生成TiCl4,然后再用镁还原得到金属钛,其工艺流程如下:

已知:常温下Fe(OH)3和Fe(OH)2溶度积(Ksp)分别为4.0×10-38和8.0×10-16
请回答下列问题:
(1)加入浓NaOH溶液的目的是_________ 。
(2)镁和氯气主要来源于流程中的某种物质通过电解方法获得,该物质是_________ 。工业生产中需要适当补充该物质,该物质可来源于海水,制备过程如下:向海水中加入石灰乳后,向分离得到的固体中加入过量的盐酸,目的是_________ ,将得到的溶液通过_________ 、冷却结晶操作后得到晶体,在HCl气流中加热晶体即可得到该物质。
(3)高温下,滤渣Y、焦炭和氯气发生反应生成可燃性气体的化学方程式为:_________ 。
(4)工艺流程中稀有气体Ar的作用是_________ 。
(5)为提高原料的利用率,常温下某研究小组向⑤过滤后的滤液中,先加适量的H2O2,再加适量的碱调节溶液的pH至4,过滤后将滤渣加热灼烧,得到了常用的涂料。调节溶液的pH至4时,溶液中金属离子的浓度为_________ mol/L。
(6)TiN具有重要的用途,可在高温下由TiO2与NH3反应制得,同时生成一种可用作保护气的单质气体和一种无色无味的液体。该反应的化学方程式为_________ 。

已知:常温下Fe(OH)3和Fe(OH)2溶度积(Ksp)分别为4.0×10-38和8.0×10-16
请回答下列问题:
(1)加入浓NaOH溶液的目的是
(2)镁和氯气主要来源于流程中的某种物质通过电解方法获得,该物质是
(3)高温下,滤渣Y、焦炭和氯气发生反应生成可燃性气体的化学方程式为:
(4)工艺流程中稀有气体Ar的作用是
(5)为提高原料的利用率,常温下某研究小组向⑤过滤后的滤液中,先加适量的H2O2,再加适量的碱调节溶液的pH至4,过滤后将滤渣加热灼烧,得到了常用的涂料。调节溶液的pH至4时,溶液中金属离子的浓度为
(6)TiN具有重要的用途,可在高温下由TiO2与NH3反应制得,同时生成一种可用作保护气的单质气体和一种无色无味的液体。该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
3 . 黄色固体X是由四种元素组成的化合物,用作颜料和食品的抗结剂,为测定其组成,进行如下实验。已知气体D能使澄清石灰水变浑浊,溶液F中只含有一种溶质。回答下列问题:
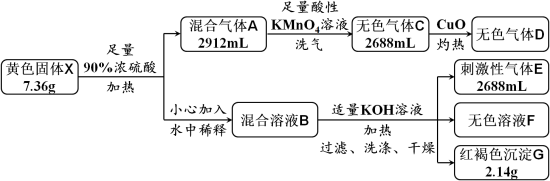
(1)固体X的组成元素是_______ 。
(2)混合气体A中所含物质的化学式为_______ 。
(3)实验中溶液B由X转化而来的溶质与KOH反应的总离子方程式为_______ 。
(4)证明沉淀G中的金属元素已完全沉淀的方法是_______ 。
(5)X与酸性KMnO4溶液反应,可生成一种与X组成元素相同,但式量比其小39的化合物,该反应的化学方程式为_______ 。

(1)固体X的组成元素是
(2)混合气体A中所含物质的化学式为
(3)实验中溶液B由X转化而来的溶质与KOH反应的总离子方程式为
(4)证明沉淀G中的金属元素已完全沉淀的方法是
(5)X与酸性KMnO4溶液反应,可生成一种与X组成元素相同,但式量比其小39的化合物,该反应的化学方程式为
您最近一年使用:0次
2022-12-09更新
|
426次组卷
|
4卷引用:浙江省诸暨海亮高级中学2021-2022学年高三12月份选考模拟化学试题
浙江省诸暨海亮高级中学2021-2022学年高三12月份选考模拟化学试题浙江省舟山中学2022-2023学年高三上学期首考模拟卷(三)化学试题(已下线)浙江省温州市普通高中2023届高三下学期第二次适应性考试化学试题变式题(无机推断题)甘肃省两县高中联考2023-2024学年高三上学期12月月考化学试题
4 . 细菌与矿物表面接触,通过酶的作用将金属硫化物氧化为酸溶性的二价金属离子和硫化物的原子团,使矿物溶解。细菌-硫化矿作用机理表述如下:

下列有关说法错误的是

下列有关说法错误的是
A.若MS为 ,1 mol ,1 mol  发生反应转移16 mol e- 发生反应转移16 mol e- |
B.若MS为 ,发生反应: ,发生反应: |
| C.温度越高,反应速率越快,浸出率一定得到提高 |
| D.若MS为CuS,发生反应中消耗的氧化剂与还原剂的物质的量比为2∶1 |
您最近一年使用:0次
2022-12-07更新
|
212次组卷
|
2卷引用:河北省衡水市冀州区第一中学2020-2021学年高三上学期期末考试化学试题
5 . 除去烟气中的NO,能促进生态文明建设。
(1)含 和
和 的酸性吸收液可以处理烟气中NO,原理是:
的酸性吸收液可以处理烟气中NO,原理是: 催化
催化 产生
产生 ,后者将NO最终氧化成
,后者将NO最终氧化成 。
。
①写出 将NO氧化成
将NO氧化成 的离子方程式为:
的离子方程式为:_______ 。
②吸收液的初始pH和温度对 氧化NO的效果分别如图1和图2所示。
氧化NO的效果分别如图1和图2所示。

当吸收液的初始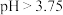 时,NO氧化率明显降低,原因可能是:
时,NO氧化率明显降低,原因可能是:
(i)pH较大时, 容易发生歧化反应,导致
容易发生歧化反应,导致 浓度降低,氧化能力减弱:
浓度降低,氧化能力减弱:
(ii)_______ 。
③当超过60℃时,NO的氧化率明显降低,原因可能是:_______ 。
(2) 可在
可在 催化下还原烟气中NO,温度对该反应的影响如图3所示。
催化下还原烟气中NO,温度对该反应的影响如图3所示。
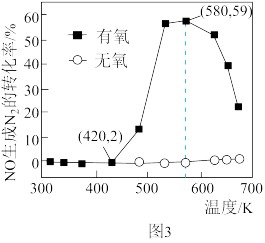
①在420~580K之间,有氧条件下NO生成 的转化率明显高于无氧条件,原因可能是
的转化率明显高于无氧条件,原因可能是_______ 。
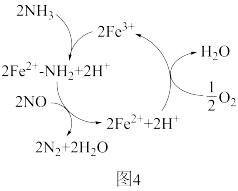
②进一步研究发现,以 为催化利时,
为催化利时, 在有氧条件下还原NO的机理如图4所示。该反应的总化学方程式为:
在有氧条件下还原NO的机理如图4所示。该反应的总化学方程式为:_______ 。
(1)含
 和
和 的酸性吸收液可以处理烟气中NO,原理是:
的酸性吸收液可以处理烟气中NO,原理是: 催化
催化 产生
产生 ,后者将NO最终氧化成
,后者将NO最终氧化成 。
。①写出
 将NO氧化成
将NO氧化成 的离子方程式为:
的离子方程式为:②吸收液的初始pH和温度对
 氧化NO的效果分别如图1和图2所示。
氧化NO的效果分别如图1和图2所示。
当吸收液的初始
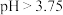 时,NO氧化率明显降低,原因可能是:
时,NO氧化率明显降低,原因可能是:(i)pH较大时,
 容易发生歧化反应,导致
容易发生歧化反应,导致 浓度降低,氧化能力减弱:
浓度降低,氧化能力减弱:(ii)
③当超过60℃时,NO的氧化率明显降低,原因可能是:
(2)
 可在
可在 催化下还原烟气中NO,温度对该反应的影响如图3所示。
催化下还原烟气中NO,温度对该反应的影响如图3所示。
①在420~580K之间,有氧条件下NO生成
 的转化率明显高于无氧条件,原因可能是
的转化率明显高于无氧条件,原因可能是②进一步研究发现,以
 为催化利时,
为催化利时, 在有氧条件下还原NO的机理如图4所示。该反应的总化学方程式为:
在有氧条件下还原NO的机理如图4所示。该反应的总化学方程式为:
您最近一年使用:0次
解题方法
6 . 以红土镍矿(主要成分为NiS,还反应少量CaS和 )为原料制备
)为原料制备 的流程如下 :
的流程如下 :
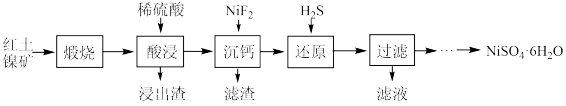
已知:①“煅烧”得到 、CaO和
、CaO和 ;②“酸浸”时,有
;②“酸浸”时,有 和
和 产生。
产生。
下列关于说法错误的是
 )为原料制备
)为原料制备 的流程如下 :
的流程如下 :
已知:①“煅烧”得到
 、CaO和
、CaO和 ;②“酸浸”时,有
;②“酸浸”时,有 和
和 产生。
产生。下列关于说法错误的是
| A.“煅烧”时,为加快反应速率,可以将红土镍矿粉碎 |
B.“沉钙”后所得滤液中,主要存在的离子有: 、 、 、 、 |
C.“还原”时,反应的离子方程式为: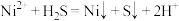 |
D.该流程中, 是可以循环使用的物质 是可以循环使用的物质 |
您最近一年使用:0次
解题方法
7 . 走进“化学村”。“化学村”的布局如下:
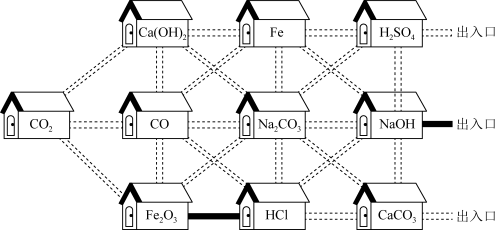
(1)10户“居民”中,俗称熟石灰的是___________ ,属于氧化物的有___________ 。
(2)“居民”CO与Fe2O3反应的化学方程式为___________ ,该反应是为___________ 。(填氧化还原反应或非氧化还原反应)

(1)10户“居民”中,俗称熟石灰的是
(2)“居民”CO与Fe2O3反应的化学方程式为
您最近一年使用:0次
解题方法
8 . 回答下列问题:
(1)在分析化学中,可以采用酸性高锰酸钾与Fe2+反应来检测Fe2+的含量:Fe2+与酸性高锰酸钾发生如下反应:Fe2++MnO +H+=Mn2++Fe3++H2O。
+H+=Mn2++Fe3++H2O。
①配平上述离子方程式并用单线桥法描述电子转移的方向及数目:_____ 。
____Fe2++____MnO +_____H+=_____Mn2++_____Fe3++_____H2O
+_____H+=_____Mn2++_____Fe3++_____H2O
②若有0.5molKMnO4参与反应,则有____ 个电子发生转移。
③其中,_____ 是氧化剂,____ 元素被氧化。
(2)以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3•6H2O)的工艺流程如图:
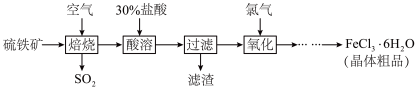
完成下列填空:
①硫铁矿焙烧后的烧渣中含有Fe2O3、Fe3O4等。酸溶后溶液中主要存在的阳离子有____ ,不能用硫酸代替盐酸的原因是____ 。
②通入氯气时,主要反应的离子方程式为____ 。从氧化后的溶液中得到氯化铁晶体的实验步骤为____ 、____ 、过滤洗涤。
(1)在分析化学中,可以采用酸性高锰酸钾与Fe2+反应来检测Fe2+的含量:Fe2+与酸性高锰酸钾发生如下反应:Fe2++MnO
 +H+=Mn2++Fe3++H2O。
+H+=Mn2++Fe3++H2O。①配平上述离子方程式并用单线桥法描述电子转移的方向及数目:
____Fe2++____MnO
 +_____H+=_____Mn2++_____Fe3++_____H2O
+_____H+=_____Mn2++_____Fe3++_____H2O②若有0.5molKMnO4参与反应,则有
③其中,
(2)以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3•6H2O)的工艺流程如图:

完成下列填空:
①硫铁矿焙烧后的烧渣中含有Fe2O3、Fe3O4等。酸溶后溶液中主要存在的阳离子有
②通入氯气时,主要反应的离子方程式为
您最近一年使用:0次
9 . 某种煤气的主要成分是CO、 。
。
(1)分别写出该煤气和天然气在空气中燃烧的化学方程式_______ 。
(2)把一套以煤气为燃料的灶具改为以天然气为燃料的灶具时,应对空气和燃气的进气量做怎样的调整_______ ?
 。
。(1)分别写出该煤气和天然气在空气中燃烧的化学方程式
(2)把一套以煤气为燃料的灶具改为以天然气为燃料的灶具时,应对空气和燃气的进气量做怎样的调整
您最近一年使用:0次
解题方法
10 . 向氯化铁溶液中通入硫化氢气体(硫化氢的水溶液称作氢硫酸,是一种弱酸),发现溶液变浑浊。试写出发生反应的离子方程式_______ 。
您最近一年使用:0次



