解题方法
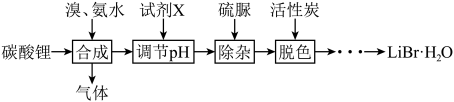
1 . 溴化锂是一种高效水汽吸收剂和空气湿度调节剂。工业上以碳酸锂为原料制备LiBr·H2O的流程如下:
已知:①Br2+H2O HBr+HBrO,Br2+3H2O
HBr+HBrO,Br2+3H2O 5HBr+HBrO3;②NH3有还原性,HBrO、HBrO3均具有强氧化性。
5HBr+HBrO3;②NH3有还原性,HBrO、HBrO3均具有强氧化性。
(1)合成时,除生成LiBr外,还产生了2种参与大气循环的气体,写出该化学方程式:___________ 。
(2)合成时,向碳酸锂中滴加溴和氨水的顺序是___________ (填字母),可能的理由是______________ 。
a.先加氨水再滴溴 b.先滴溴再加氨水 c.边滴溴边加氨水
(3)合成所得的溶液中存在过量的溴会导致溶液pH<3,可用试剂X将溶液pH调节至8~9以除去过量的溴,则X的化学式为___________ 。
(4)加入硫脲[CS(NH2)2]的作用是除去 ,反应中硫脲表现
,反应中硫脲表现___________ (填“氧化性”或“还原性”)。
(5)已知脱色后的混合液中还含有少量的 。溴化锂溶液的溶解度随温度变化曲线如图所示,请补充完整脱色后得到的溶液制备LiBr·H2O的实验方案:加入活性炭脱色后,
。溴化锂溶液的溶解度随温度变化曲线如图所示,请补充完整脱色后得到的溶液制备LiBr·H2O的实验方案:加入活性炭脱色后,___________ 。(实验中可供选择的试剂:盐酸、氢溴酸、乙醇、蒸馏水)。


已知:①Br2+H2O
 HBr+HBrO,Br2+3H2O
HBr+HBrO,Br2+3H2O 5HBr+HBrO3;②NH3有还原性,HBrO、HBrO3均具有强氧化性。
5HBr+HBrO3;②NH3有还原性,HBrO、HBrO3均具有强氧化性。(1)合成时,除生成LiBr外,还产生了2种参与大气循环的气体,写出该化学方程式:
(2)合成时,向碳酸锂中滴加溴和氨水的顺序是
a.先加氨水再滴溴 b.先滴溴再加氨水 c.边滴溴边加氨水
(3)合成所得的溶液中存在过量的溴会导致溶液pH<3,可用试剂X将溶液pH调节至8~9以除去过量的溴,则X的化学式为
(4)加入硫脲[CS(NH2)2]的作用是除去
 ,反应中硫脲表现
,反应中硫脲表现(5)已知脱色后的混合液中还含有少量的
 。溴化锂溶液的溶解度随温度变化曲线如图所示,请补充完整脱色后得到的溶液制备LiBr·H2O的实验方案:加入活性炭脱色后,
。溴化锂溶液的溶解度随温度变化曲线如图所示,请补充完整脱色后得到的溶液制备LiBr·H2O的实验方案:加入活性炭脱色后,
您最近一年使用:0次
名校
2 . 回答下列氧化还原反应相关问题
(1)完成下列反应方程式的配平:
①____ 
②____ 
③____ 
(2)一个完整的氧化还原反应方程式可以拆开,写成两个“半反应”,如
 可拆写为氧化反应:
可拆写为氧化反应:
 还原反应:
还原反应: ,据此,请将反应
,据此,请将反应 ,拆写成两个半反应。氧化反应:
,拆写成两个半反应。氧化反应:___________ ;还原反应:___________ 。
(3)PH3作为一种熏蒸剂,在贮粮中用于防治害虫,一种制备PH3的流程如图所示:

①白磷与浓 NaOH 溶液反应的化学方程式为___________ ;
②次磷酸的化学式为___________ , 属于
属于___________ (选填“正盐”或“酸式盐”);
③理论上,1mol白磷可生产___________ mol PH3。
(1)完成下列反应方程式的配平:
①

②

③

(2)一个完整的氧化还原反应方程式可以拆开,写成两个“半反应”,如

 可拆写为氧化反应:
可拆写为氧化反应:
 还原反应:
还原反应: ,据此,请将反应
,据此,请将反应 ,拆写成两个半反应。氧化反应:
,拆写成两个半反应。氧化反应:(3)PH3作为一种熏蒸剂,在贮粮中用于防治害虫,一种制备PH3的流程如图所示:

①白磷与浓 NaOH 溶液反应的化学方程式为
②次磷酸的化学式为
 属于
属于③理论上,1mol白磷可生产
您最近一年使用:0次
3 . 黄铁矿(主要含 ,其中Fe的化合价为+2)是一种常见的含硫矿物,酸性条件下,黄铁矿中的
,其中Fe的化合价为+2)是一种常见的含硫矿物,酸性条件下,黄铁矿中的 可与空气中的
可与空气中的 发生反应。已知
发生反应。已知 与
与 反应的化学计量数之比为2∶7,且化合价发生变化的元素只有S和O,则
反应的化学计量数之比为2∶7,且化合价发生变化的元素只有S和O,则 中的S元素可能完全转化为
中的S元素可能完全转化为
 ,其中Fe的化合价为+2)是一种常见的含硫矿物,酸性条件下,黄铁矿中的
,其中Fe的化合价为+2)是一种常见的含硫矿物,酸性条件下,黄铁矿中的 可与空气中的
可与空气中的 发生反应。已知
发生反应。已知 与
与 反应的化学计量数之比为2∶7,且化合价发生变化的元素只有S和O,则
反应的化学计量数之比为2∶7,且化合价发生变化的元素只有S和O,则 中的S元素可能完全转化为
中的S元素可能完全转化为A. | B.S | C. | D. |
您最近一年使用:0次
名校
解题方法
4 . 根据信息书写反应方程式:
(1)以 溶液为原料可以制取磁性氧化铁(
溶液为原料可以制取磁性氧化铁( ),制取流程如下:
),制取流程如下:
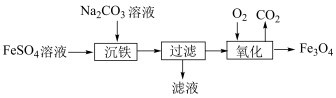
①写出沉铁时反应的离子方程式:____________ 。
②“氧化”的条件为高温。写出该反应的化学方程式:____________ 。
③ 可以溶于盐酸;写出该反应的离子方程式:
可以溶于盐酸;写出该反应的离子方程式:____________ 。
(2)漂白粉中的 在潮湿的空气中与
在潮湿的空气中与 和
和 会发生变质,变质时发生复分解反应,产物之一为
会发生变质,变质时发生复分解反应,产物之一为 。写出该反应的化学方程式:
。写出该反应的化学方程式:__________________ 。
(3)某氧化还原反应包含 、
、 、NaCl、NaClO、NaOH、
、NaCl、NaClO、NaOH、 六种物质,
六种物质, 是产物之一,写出该反应的化学方程式:
是产物之一,写出该反应的化学方程式:____________ 。
(1)以
 溶液为原料可以制取磁性氧化铁(
溶液为原料可以制取磁性氧化铁( ),制取流程如下:
),制取流程如下:
①写出沉铁时反应的离子方程式:
②“氧化”的条件为高温。写出该反应的化学方程式:
③
 可以溶于盐酸;写出该反应的离子方程式:
可以溶于盐酸;写出该反应的离子方程式:(2)漂白粉中的
 在潮湿的空气中与
在潮湿的空气中与 和
和 会发生变质,变质时发生复分解反应,产物之一为
会发生变质,变质时发生复分解反应,产物之一为 。写出该反应的化学方程式:
。写出该反应的化学方程式:(3)某氧化还原反应包含
 、
、 、NaCl、NaClO、NaOH、
、NaCl、NaClO、NaOH、 六种物质,
六种物质, 是产物之一,写出该反应的化学方程式:
是产物之一,写出该反应的化学方程式:
您最近一年使用:0次
名校
5 . 下图为氯气及氯的化合物的“价—类”二维图,下列叙述不 正确的是


| A.b、d、f的水溶液均具有漂白性 | B.理论上a溶液和e混合可制得b |
| C.c和f均可用于环境杀菌消毒 | D.工业上常将b通入NaOH溶液中制备漂白粉 |
您最近一年使用:0次
名校
解题方法
6 . 高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,Na2FeO4只能在强碱性条件下稳定存在,主要用于饮用水处理,制备高铁酸钠有多种方法,其中一种方法的实验流程如下:
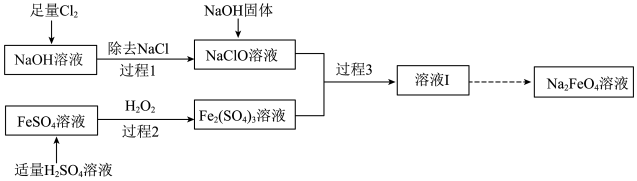
请回答下列问题。
(1)流程中需要使用Cl2。下图装置可用于制备较干燥、纯净的Cl2。
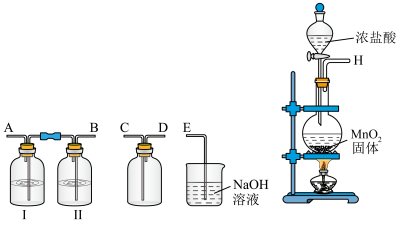
①广口瓶Ⅱ中盛放的溶液为_________ (填字母)。
A.氢氧化钠溶液 B.饱和食盐水 C.浓硫酸 D.硝酸银溶液
②请按正确的顺序连接装置:H→_____、_____→____、____→E,_________ 。
③MnO2与浓盐酸反应的化学方程式为___________ ;反应中,体现还原性和酸性的HC1之比
_________ 。
(2)过程1所得NaClO溶液中需要加入NaOH固体,其目的是___________ 。
(3)过程2中所发生反应的离子方程式为___________ 。
(4)过程3中所发生反应的离子方程式如下:

①请将上述离子方程式配平,并用双线桥表示电子的转移__________ 。
②一个完整的氧化还原反应往往可以拆成两个半反应,一个为“氧化半反应”,另一个为“还原半反应”,两个半反应可以通过叠加得到总反应。如Zn+Cu2+=Zn2++Cu的氧化半反应为Zn-2e- =Zn2+,还原半反应为Cu2++2e- =Cu。则上述离子方程式对应的氧化半反应为___________ (请将化学计量数化到最简整数比)。

请回答下列问题。
(1)流程中需要使用Cl2。下图装置可用于制备较干燥、纯净的Cl2。

①广口瓶Ⅱ中盛放的溶液为
A.氢氧化钠溶液 B.饱和食盐水 C.浓硫酸 D.硝酸银溶液
②请按正确的顺序连接装置:H→_____、_____→____、____→E,
③MnO2与浓盐酸反应的化学方程式为

(2)过程1所得NaClO溶液中需要加入NaOH固体,其目的是
(3)过程2中所发生反应的离子方程式为
(4)过程3中所发生反应的离子方程式如下:

①请将上述离子方程式配平,并用双线桥表示电子的转移
②一个完整的氧化还原反应往往可以拆成两个半反应,一个为“氧化半反应”,另一个为“还原半反应”,两个半反应可以通过叠加得到总反应。如Zn+Cu2+=Zn2++Cu的氧化半反应为Zn-2e- =Zn2+,还原半反应为Cu2++2e- =Cu。则上述离子方程式对应的氧化半反应为
您最近一年使用:0次
名校
解题方法
7 . 下列离子方程式正确的是
| A.铜片插入硝酸银溶液: Cu +Ag+= Cu2++Ag |
| B.盐酸跟氢氧化镁反应: H++OH-= H2O |
| C.向FeI2溶液中通入Cl2:2Fe2++Cl2= 2Fe3++2Cl- |
D.向明矾溶液中滴入Ba(OH)2溶液至 完全沉淀:Al3++2 完全沉淀:Al3++2 +2Ba2++4OH-=2BaSO4↓+ +2Ba2++4OH-=2BaSO4↓+ |
您最近一年使用:0次
8 . 氯的化合物在生活中有着广泛的用途。
(1)二氧化氯(ClO2)的熔点-59℃,沸点11℃,易溶于水,是一种常用的饮用水消毒剂,消毒时会产生 和少量的
和少量的 ,可利用酸性FeSO4溶液将
,可利用酸性FeSO4溶液将 转化为
转化为 除去。
除去。
①关于二氧化氯的说法不正确 的是______ 。
A.易液化 B.实验室可用排水法收集
C.氯的化合价为+4 D.消毒时利用其强还原性
②FeSO4除去 的离子方程式为
的离子方程式为______ 。
(2)亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,某种制备亚氯酸钠的反应为: (未配平)。
(未配平)。
①ClO2的氧化性______ H2O2的氧化性(填“大于”或“小于”)。
②当消耗标准状况下2.24 L ClO2时,生成O2的质量为___________ 。
(3)“84”消毒液是一种常用家庭消毒液,其有效成分为NaClO。一种碱性NaClO溶液吸收SO2的过程如下图。

①该过程的总反应的离子方程式是___________ 。
②整个吸收SO2过程中作氧化剂的微粒有___________ 。
(1)二氧化氯(ClO2)的熔点-59℃,沸点11℃,易溶于水,是一种常用的饮用水消毒剂,消毒时会产生
 和少量的
和少量的 ,可利用酸性FeSO4溶液将
,可利用酸性FeSO4溶液将 转化为
转化为 除去。
除去。①关于二氧化氯的说法
A.易液化 B.实验室可用排水法收集
C.氯的化合价为+4 D.消毒时利用其强还原性
②FeSO4除去
 的离子方程式为
的离子方程式为(2)亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,某种制备亚氯酸钠的反应为:
 (未配平)。
(未配平)。①ClO2的氧化性
②当消耗标准状况下2.24 L ClO2时,生成O2的质量为
(3)“84”消毒液是一种常用家庭消毒液,其有效成分为NaClO。一种碱性NaClO溶液吸收SO2的过程如下图。

①该过程的总反应的离子方程式是
②整个吸收SO2过程中作氧化剂的微粒有
您最近一年使用:0次
9 .  与浓盐酸的反应是实验室制备氯气的方法之一:
与浓盐酸的反应是实验室制备氯气的方法之一: ,下列说法不正确的是
,下列说法不正确的是
 与浓盐酸的反应是实验室制备氯气的方法之一:
与浓盐酸的反应是实验室制备氯气的方法之一: ,下列说法不正确的是
,下列说法不正确的是A.氧化性: |
| B.HCl在反应中表现出还原性和酸性 |
| C.被氧化的氯原子与被还原的氯原子的个数之比为5∶1 |
D.用双线桥法表示电子得失情况: |
您最近一年使用:0次
10 . 草酸 又叫乙二酸,广泛存在于植物源食品中,
又叫乙二酸,广泛存在于植物源食品中, 时,其电离常数
时,其电离常数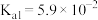 ,
,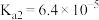 。下列与草酸有关的说法错误的是
。下列与草酸有关的说法错误的是
 又叫乙二酸,广泛存在于植物源食品中,
又叫乙二酸,广泛存在于植物源食品中, 时,其电离常数
时,其电离常数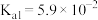 ,
,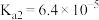 。下列与草酸有关的说法错误的是
。下列与草酸有关的说法错误的是A.  ,升温有利于提高草酸的电离程度 ,升温有利于提高草酸的电离程度 |
B.同浓度同体积 和 和 混合溶液: 混合溶液: |
C. 时, 时, 溶液呈弱酸性,有时用于清洗金属表面的锈迹 溶液呈弱酸性,有时用于清洗金属表面的锈迹 |
D.草酸中的碳为 价,具有较强的还原性,可使酸性高锰酸钾溶液褪色 价,具有较强的还原性,可使酸性高锰酸钾溶液褪色 |
您最近一年使用:0次



