1 . 如图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条,F中为红色的铜网,其右端出气管口放有脱脂棉。
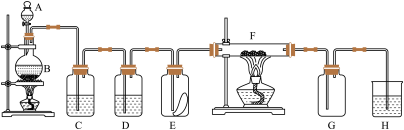
(1)写出实验室制取氯气的化学方程式:___________ 。
(2)装置C中盛装的溶液是___________ ,作用是___________ 。D中盛装的试剂是___________ ,作用是___________ 。
(3)E中红色布条是否褪色?___________ ,F中的反应产物为___________ 。
(4)若H中选用NaOH溶液进行尾气处理,则发生的反应是___________ (用离子方程式表示)。

(1)写出实验室制取氯气的化学方程式:
(2)装置C中盛装的溶液是
(3)E中红色布条是否褪色?
(4)若H中选用NaOH溶液进行尾气处理,则发生的反应是
您最近一年使用:0次
2023-07-16更新
|
64次组卷
|
2卷引用:四川省宜宾市兴文第二中学校2023-2024学年高一上学期12月月考化学试题
名校
解题方法
2 . 下列化学表达式正确,且与所给事实相符的是
A.氯化铜溶液中通入硫化氢: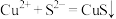 |
B.用过量NaOH溶液脱除烟气中的SO2:SO2+OH-= |
C.稀硝酸中加入过量铁粉:3Fe+8H++2 =3Fe2++2NO↑+4H2O =3Fe2++2NO↑+4H2O |
D.湿润的淀粉碘化钾试纸遇氯气变蓝:3Cl2+I-+3H2O=6Cl-+ +6H+ +6H+ |
您最近一年使用:0次
3 . 高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂。某化学实验小组模拟工业生产路线,在实验室中制备高铁酸钾,其实验装置如图:
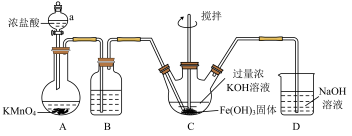
已知:K2FeO4易溶于水,水溶液为紫色,微溶于浓KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在0℃~5℃、强碱性溶液中较稳定。
(1)仪器a的名称是_________ 。
(2)装置A中发生反应的离子方程式为_________ 。
(3)装置B中试剂为________ 。
(4)装置C中观察到溶液的颜色变化为________ ,制备K2FeO4的化学方程式为______ ,加入过量浓KOH溶液的原因是_______ 。
(5)有同学提出,装置C在制备K2FeO4时存在一定缺陷,改进的措施是_______ 。
(6)装置D的作用是________ 。
(7)取C中洗涤并干燥后样品10g,加入稀硫酸,收集到0.672L气体(标准状况下)。则样品中高铁酸钾的质量分数约为________ 。

已知:K2FeO4易溶于水,水溶液为紫色,微溶于浓KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在0℃~5℃、强碱性溶液中较稳定。
(1)仪器a的名称是
(2)装置A中发生反应的离子方程式为
(3)装置B中试剂为
(4)装置C中观察到溶液的颜色变化为
(5)有同学提出,装置C在制备K2FeO4时存在一定缺陷,改进的措施是
(6)装置D的作用是
(7)取C中洗涤并干燥后样品10g,加入稀硫酸,收集到0.672L气体(标准状况下)。则样品中高铁酸钾的质量分数约为
您最近一年使用:0次
名校
解题方法
4 . 硫代硫酸钠Na2S2O3(又名大苏打),化学性质不稳定,在酸性溶液中会分解成 和S;还具有较强的还原性,可做脱氯剂等。实验室用
和S;还具有较强的还原性,可做脱氯剂等。实验室用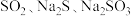 ,为原料通过如下装置(略去部分夹持仪器)生产硫代硫酸钠。
,为原料通过如下装置(略去部分夹持仪器)生产硫代硫酸钠。
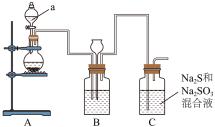
回答下列问题:
(1)仪器a的名称是___________ 。
(2)利用 固体和较浓的硫酸溶液在装置A中制取
固体和较浓的硫酸溶液在装置A中制取 气体,该反应的化学方程式为
气体,该反应的化学方程式为___________ 。
(3)装置B盛装的液体最好为___________ 。
①饱和 溶液②饱和
溶液②饱和 溶液③饱和
溶液③饱和 溶液④浓硫酸
溶液④浓硫酸
(4)该实验装置有不完善的地方,以下装置中能完善该实验的是___________。(下列装置中试剂均为 溶液)
溶液)
(5)停止反应后,烧瓶C中的溶液经___________ (填写操作名称)、洗涤、干燥可得到Na2S2O3·5H2O晶体;产品中可能含有Na2SO3、Na2SO4等杂质,为检验产品中是否含有Na2SO4,下列试剂及添加顺序正确的时___________ 。(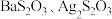 均为白色沉淀)
均为白色沉淀)
A.先加入稀硝酸再加入 溶液 B.先加入稀盐酸再加入
溶液 B.先加入稀盐酸再加入 溶液
溶液
C.先加入 溶液,再加入硫酸溶液 D.先加入稀盐酸再加入
溶液,再加入硫酸溶液 D.先加入稀盐酸再加入 溶液
溶液
(6) 做脱氯剂可除去自来水中残留的
做脱氯剂可除去自来水中残留的 ,从而消除
,从而消除 对环境的污染,写出该原理的离子反应方程式
对环境的污染,写出该原理的离子反应方程式___________ 。
 和S;还具有较强的还原性,可做脱氯剂等。实验室用
和S;还具有较强的还原性,可做脱氯剂等。实验室用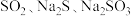 ,为原料通过如下装置(略去部分夹持仪器)生产硫代硫酸钠。
,为原料通过如下装置(略去部分夹持仪器)生产硫代硫酸钠。
回答下列问题:
(1)仪器a的名称是
(2)利用
 固体和较浓的硫酸溶液在装置A中制取
固体和较浓的硫酸溶液在装置A中制取 气体,该反应的化学方程式为
气体,该反应的化学方程式为(3)装置B盛装的液体最好为
①饱和
 溶液②饱和
溶液②饱和 溶液③饱和
溶液③饱和 溶液④浓硫酸
溶液④浓硫酸(4)该实验装置有不完善的地方,以下装置中能完善该实验的是___________。(下列装置中试剂均为
 溶液)
溶液)A. | B.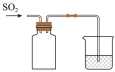 | C.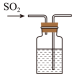 | D.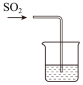 |
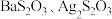 均为白色沉淀)
均为白色沉淀)A.先加入稀硝酸再加入
 溶液 B.先加入稀盐酸再加入
溶液 B.先加入稀盐酸再加入 溶液
溶液C.先加入
 溶液,再加入硫酸溶液 D.先加入稀盐酸再加入
溶液,再加入硫酸溶液 D.先加入稀盐酸再加入 溶液
溶液(6)
 做脱氯剂可除去自来水中残留的
做脱氯剂可除去自来水中残留的 ,从而消除
,从而消除 对环境的污染,写出该原理的离子反应方程式
对环境的污染,写出该原理的离子反应方程式
您最近一年使用:0次
名校
解题方法
5 . 设 是阿伏加德罗常数的值。下列说法错误的是
是阿伏加德罗常数的值。下列说法错误的是
 是阿伏加德罗常数的值。下列说法错误的是
是阿伏加德罗常数的值。下列说法错误的是A.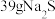 和 和 组成的混合物中,含有阴离子的数目为0.5NA 组成的混合物中,含有阴离子的数目为0.5NA |
| B.密闭容器中,1mol N2(g)与3mol H2(g)充分反应制备氨气,形成N−H键少于6NA |
C.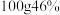 的乙醇溶液中,含 的乙醇溶液中,含 键的数目为 键的数目为 |
D.在标况下将 溶于足量 溶于足量 溶液中,转移电子数目为 溶液中,转移电子数目为 |
您最近一年使用:0次
2023-06-19更新
|
98次组卷
|
2卷引用:四川省仁寿第一中学校南校区2023-2024学年高二上学期10月月考化学试题
名校
6 . 下列指定反应的离子方程式正确的是
A. 通入水中制氯水: 通入水中制氯水: |
B. 通入水中制硝酸: 通入水中制硝酸: |
C. 溶液中通入少量 溶液中通入少量 : : |
D.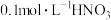 溶液中加入过量 溶液中加入过量 : :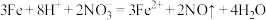 |
您最近一年使用:0次
名校
解题方法
7 . 以工业废渣[主要成分为 ,杂质为
,杂质为 ]为原料制备
]为原料制备 的流程如图:
的流程如图:

氯化时控制温度在75℃左右进行,充分反应后过滤所得滤液为 、
、 的混合溶液。下列有关说法正确的是
的混合溶液。下列有关说法正确的是
 ,杂质为
,杂质为 ]为原料制备
]为原料制备 的流程如图:
的流程如图:
氯化时控制温度在75℃左右进行,充分反应后过滤所得滤液为
 、
、 的混合溶液。下列有关说法正确的是
的混合溶液。下列有关说法正确的是A.氯化过程中通入 的速率越快越好 的速率越快越好 |
B.氯化后过滤,测定滤液中 与 与 的个数之比为2:3 的个数之比为2:3 |
C.滤渣的主要成分为 |
D.转化过程可能发生反应的化学方程式为 |
您最近一年使用:0次
2023-05-14更新
|
157次组卷
|
2卷引用:四川省成都市双流中学2023-2024学年高一上学期10月月考化学试题
名校
解题方法
8 . 化学与生活息息相关,以下说法正确的是
| A.漂白粉、漂白液和漂粉精可用于游泳池等场所的消毒剂 |
| B.Cl2具有漂白性,所以可以漂白有色布条 |
| C.铁生锈过程中未涉及到氧化还原反应 |
| D.铝表面容易生成一层致密的氧化膜,所以铝制品可以长期存放酸性或碱性食物。 |
您最近一年使用:0次
名校
9 . 下列离子方程式书写正确的是
A.将覆铜板放到 溶液中制作图案: 溶液中制作图案: |
B.氯气与水的反应原理: |
C.碳酸氢钠溶液与 溶液反应: 溶液反应: |
D.向 溶液中通入少量 溶液中通入少量 : :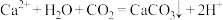 |
您最近一年使用:0次
2023-04-03更新
|
163次组卷
|
2卷引用:四川省华蓥中学2022-2023学年高一下学期2月月考化学试题
解题方法
10 . 化学小组同学为研究氯气制备进行了如图实验。如图是实验室制取纯净、干燥氯气装置图。
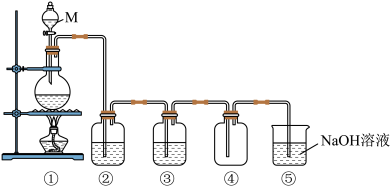
(1)M仪器的名称是_______ ,①中反应的反应的化学方程式是_______
(2)③中存放的试剂是_______
(3)⑤中反应的离子方程式是_______

(1)M仪器的名称是
(2)③中存放的试剂是
(3)⑤中反应的离子方程式是
您最近一年使用:0次



