名校
1 . X、Y、Z、W为四种短周期元素,其中Y元素最外层电子数是其电子层数的3倍,它们在周期表中的相对位置如图所示:请回答下列问题:
(1)W位于周期表中第____ 周期第____ 族,画出该元素阴离子的结构示意图____ 。
(2)X可形成双原子分子,其分子式是____ (填化学式,下同);X和Y形成的简单氢化物中,稳定性较弱的是____ ;Z和W的最高价氧化物的水化物中,酸性较强的是____ 。
(3)工业上将W的单质通入石灰浆中可制得漂白粉,该反应的化学方程式是:____ 。
| X | Y | |
| Z | W |
(2)X可形成双原子分子,其分子式是
(3)工业上将W的单质通入石灰浆中可制得漂白粉,该反应的化学方程式是:
您最近一年使用:0次
2 . 利用下列装置进行实验,不能达到相应实验目的的是


| A.利用装置①证明Cl2易被NaOH溶液吸收 |
| B.利用装置②检查装置的气密性 |
| C.利用装置③比较碳酸钠与碳酸氢钠的热稳定性 |
| D.利用装置④制取并收集干燥、纯净的NH3 |
您最近一年使用:0次
2022-04-06更新
|
117次组卷
|
2卷引用:四川省宜宾市叙州区第二中学校2022-2023学年高一上学期第三次月考试化学试题
名校
3 . 下列除去杂质(括号中的物质为杂质)的方法中,正确的是
| A.Cu(Fe):加足量FeCl3溶液 | B.CO2(HCl):通过Na2CO3溶液 |
| C.FeCl3溶液(FeCl2):通入适量Cl2 | D.Cl2(O2):通过灼热的铜丝网 |
您最近一年使用:0次
2022-04-05更新
|
667次组卷
|
7卷引用:四川省内江市第六中学2022-2023学年高一上学期第一次月考(创新班)化学试题
名校
4 . 下列“类推”合理的是
| A.Na与H2O反应生成NaOH和H2,则Fe与H2O反应生成Fe(OH)3和H2 |
| B.CO2可与水反应生成H2CO3,则SiO2可与水反应生成H2SiO3 |
| C.已知Ca(OH)2为强碱,则Sr(OH)2也为强碱 |
| D.Cl2与H2O反应生成HCl和HClO,则F2与H2O反应生成HF和HFO |
您最近一年使用:0次
名校
5 . 硫酸亚铁是一种重要的工业原料,同时也可以用于制造补血药物,但其具有毒性,故严禁在食品中滥用硫酸亚铁,请回答下列问题:
I.
(1)下列说法中正确的是___________(填字母)。
II.某同学为探究富含硫酸亚铁且保存时间较长的糕点情况,设计了如下实验方案:

(2)试剂1的名称是___________ ,FeSO4固体应___________ 保存。
(3)加入新制氯水后,溶液红色加深的原因是___________ (用离子方程式表示)。
(4)该同学实验中加入过量新制氯水,放置一段时间后,深红色褪去,现对褪色原因进行探究(已知SCN-有还原性)。
①【提出假设】假设1:溶液中的+3价铁被氧化为更高的价态。
假设2:___________ 。
②【设计方案】为了对假设2进行验证,简述你的设计方案:___________ 。
(5)将铜片放入0.1mol/LFeCl3溶液中浸泡,一段时间,溶液中c(Fe3+):c(Fe2+)=2:3,则此时Cu2+与Fe3+的物质的量之比为_______ 。再过一段时间,取出铜片称量铜片减轻了3.2g,在浸泡液中加入足量的铁粉使之充分反应,过滤并干燥固体,固体质量比加入的铁粉质量减少了2.4g,参与反应的铁粉的质量是_______ g。
I.
(1)下列说法中正确的是___________(填字母)。
| A.可以使用纯碱作糕点膨化剂 |
| B.大量服用FeSO4导致人体中毒可能与其还原性有关 |
| C.向FeSO4溶液中加入铜粉可析出铁单质 |
| D.向FeSO4溶液中加入少许铁粉,其目的是防止Fe2+被还原 |
II.某同学为探究富含硫酸亚铁且保存时间较长的糕点情况,设计了如下实验方案:

(2)试剂1的名称是
(3)加入新制氯水后,溶液红色加深的原因是
(4)该同学实验中加入过量新制氯水,放置一段时间后,深红色褪去,现对褪色原因进行探究(已知SCN-有还原性)。
①【提出假设】假设1:溶液中的+3价铁被氧化为更高的价态。
假设2:
②【设计方案】为了对假设2进行验证,简述你的设计方案:
(5)将铜片放入0.1mol/LFeCl3溶液中浸泡,一段时间,溶液中c(Fe3+):c(Fe2+)=2:3,则此时Cu2+与Fe3+的物质的量之比为
您最近一年使用:0次
名校
6 . 在学习元素周期表后,某化学兴趣小组在老师的指导下,设计实验以探究元素性质的递变规律。为了验证卤族部分元素性质递变规律,设计如图所示装置(夹持装置已略去)进行实验。( 易溶于
易溶于 ,液体呈紫红色)。
,液体呈紫红色)。
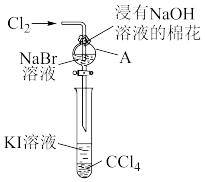
(1)指出溴元素在周期表中的位置:_______ 。
(2)A中发生反应的离子方程式是_______ 。
(3)向A中通入 充分反应后,将A中液体滴入试管内,取下试管,充分振荡,静置,可观察到的现象是
充分反应后,将A中液体滴入试管内,取下试管,充分振荡,静置,可观察到的现象是_______ 。
(4)根据上述实验操作步骤,为确保“非金属性:氯元素>溴元素>碘元素”的实验结论可靠,你认为做好本实验最关键因素是_______ 。
(5)下列性质的递变规律正确,且能作为卤族元素非金属性递变规律判断依据的是_______ (填序号)。
a. 的熔点逐渐升高 b.HCl、HBr、HI的稳定性逐渐减弱
的熔点逐渐升高 b.HCl、HBr、HI的稳定性逐渐减弱
c.HCl、HBr、HI的酸性逐渐减弱 d.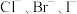 的还原性逐渐增强
的还原性逐渐增强
 易溶于
易溶于 ,液体呈紫红色)。
,液体呈紫红色)。
(1)指出溴元素在周期表中的位置:
(2)A中发生反应的离子方程式是
(3)向A中通入
 充分反应后,将A中液体滴入试管内,取下试管,充分振荡,静置,可观察到的现象是
充分反应后,将A中液体滴入试管内,取下试管,充分振荡,静置,可观察到的现象是(4)根据上述实验操作步骤,为确保“非金属性:氯元素>溴元素>碘元素”的实验结论可靠,你认为做好本实验最关键因素是
(5)下列性质的递变规律正确,且能作为卤族元素非金属性递变规律判断依据的是
a.
 的熔点逐渐升高 b.HCl、HBr、HI的稳定性逐渐减弱
的熔点逐渐升高 b.HCl、HBr、HI的稳定性逐渐减弱c.HCl、HBr、HI的酸性逐渐减弱 d.
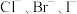 的还原性逐渐增强
的还原性逐渐增强
您最近一年使用:0次
7 . 某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置,按要求回答问题。(说明:①部分夹持装置省略 ② Cl2在水中溶解度不大,而易溶于有机溶剂;HCl溶解性与Cl2相反。)
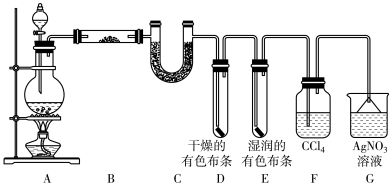
(1)若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积(标准状况下)小于1.12 L的原因是_______ 。
(2)①装置B中盛放的试剂名称为_______ ,作用是_______ 。装置C中盛放的试剂名称为_______ ,作用是_______ 。
② 装置D和E中出现的不同现象说明的问题是_______ 。
③ 装置F的作用是_______ 。
④写出装置G中发生反应的离子方程式_______ 。

(1)若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积(标准状况下)小于1.12 L的原因是
(2)①装置B中盛放的试剂名称为
② 装置D和E中出现的不同现象说明的问题是
③ 装置F的作用是
④写出装置G中发生反应的离子方程式
您最近一年使用:0次
8 . 如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。
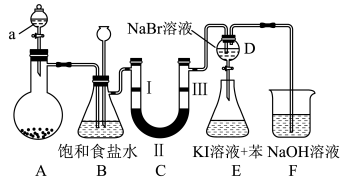
(1)仪器a的名称___________ 。
(2)制备氯气选用的药品为二氧化锰和浓盐酸,则相关的化学反应方程式为___________ 。
(3)装置B中饱和食盐水的作用是___________ ;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象___________ 。
(4)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入___________ 。
(5)装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入少量氯气时,反应的离子方程式为___________ ,打开活塞,将装置D中少量溶液加入装置E中,振荡、静置,观察到的现象为溶液分层,上层溶液为紫红色,下层几乎无色,根据实验得出氯、溴、碘单质的氧化性强弱为___________ 。
(6)装置F中用足量的 溶液吸收多余的氯气,试写出相应的离子方程式
溶液吸收多余的氯气,试写出相应的离子方程式___________ 。

(1)仪器a的名称
(2)制备氯气选用的药品为二氧化锰和浓盐酸,则相关的化学反应方程式为
(3)装置B中饱和食盐水的作用是
(4)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入
| 选项 | a | b | c | d |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 浓硫酸 | 硅胶 | 无水氯化钙 | 碱石灰 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(6)装置F中用足量的
 溶液吸收多余的氯气,试写出相应的离子方程式
溶液吸收多余的氯气,试写出相应的离子方程式
您最近一年使用:0次
2022-01-27更新
|
549次组卷
|
6卷引用:四川省合江县马街中学校2023-2024学年高一上学期12月月考化学试题
四川省合江县马街中学校2023-2024学年高一上学期12月月考化学试题贵州省铜仁市2021-2022学年高一上学期期末考试化学试题(已下线)2.2.3 氯气的实验室制法 氯离子的检验-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)广东省广州市育才中学2022-2023学年高一上学期期中考试化学试题广东省广州市育才中学2022-2023学年高一上学期期中考试化学试题(已下线)【知识图鉴】单元讲练测必修第一册第二单元03巩固练
解题方法
9 . 实验室利用下图装置制备 ,并探究其性质。据图回答下列问题:
,并探究其性质。据图回答下列问题:
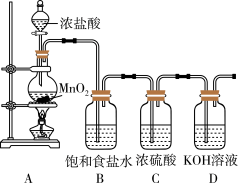
(1)组装该装置的一般原则是___________ ,气密性检查应在盛装药品___________ (填“前”或“后”)。
(2)B为洗气装置,制作它需要玻璃导管、双孔塞,还有___________ (填写所需仪器的名称)。
(3)A中发生反应的化学方程式为___________ 。
(4)制备 的反应是放热反应,反应温度升高时有副反应发生,改进该实验装置以减少副反应发生的方法是
的反应是放热反应,反应温度升高时有副反应发生,改进该实验装置以减少副反应发生的方法是___________ 。除上述不足外,是否存在“设计错误”___________ (填是或否)。
(5)在一支试管中依次加入氢氧化铁和氢氧化钾溶液,再加入 溶液,有紫红色的高铁酸钾(
溶液,有紫红色的高铁酸钾( )生成,由此可知
)生成,由此可知 具有
具有___________ 性(填“氧化”或“还原”),根据提示完成并配平该反应的化学方程式:___________ 。
提示: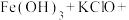 _______
_______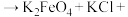 _______(未配平)
_______(未配平)
 ,并探究其性质。据图回答下列问题:
,并探究其性质。据图回答下列问题:
(1)组装该装置的一般原则是
(2)B为洗气装置,制作它需要玻璃导管、双孔塞,还有
(3)A中发生反应的化学方程式为
(4)制备
 的反应是放热反应,反应温度升高时有副反应发生,改进该实验装置以减少副反应发生的方法是
的反应是放热反应,反应温度升高时有副反应发生,改进该实验装置以减少副反应发生的方法是(5)在一支试管中依次加入氢氧化铁和氢氧化钾溶液,再加入
 溶液,有紫红色的高铁酸钾(
溶液,有紫红色的高铁酸钾( )生成,由此可知
)生成,由此可知 具有
具有提示:
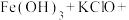 _______
_______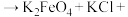 _______(未配平)
_______(未配平)
您最近一年使用:0次
2022-01-24更新
|
81次组卷
|
2卷引用:四川省宜宾市叙州区第二中学校2022-2023学年高一上学期第三次月考试化学试题
10 . 实验室里可用如下图所示的装置制取氯酸钾、次氯酸钠,并验证氯水的性质。

图中a为氯气发生装置,c的试管中盛有15mL30%的 溶液,并置于热水浴中,d的试管中盛有15mL 8%的
溶液,并置于热水浴中,d的试管中盛有15mL 8%的 溶液,并置于冰水浴中,f为
溶液,并置于冰水浴中,f为 的发生装置。
的发生装置。
(1)制取氯气时,在烧瓶中先加入一定量的 固体,再通过
固体,再通过___________ (填写仪器名称)向烧瓶中加入适量的浓盐酸。
(2)装置b的作用是___________ 。
(3)f装置中反应的化学方程式为___________ 。
(4)比较制取氯酸钾和次氯酸钠的条件,两者的差异是___________ 。
(5)反应完毕经冷却后,c装置的试管中有大量晶体析出,图中符合该晶体溶解度随温度变化规律的曲线是___________ (选填字母);从c装置的试管中分离该晶体的操作是___________ (填写实验操作名称)。

(6)将d中余气与f中产生的气体通入e中,产生的现象为___________ 。
(7)该实验有一处明显的缺点是___________ 。

图中a为氯气发生装置,c的试管中盛有15mL30%的
 溶液,并置于热水浴中,d的试管中盛有15mL 8%的
溶液,并置于热水浴中,d的试管中盛有15mL 8%的 溶液,并置于冰水浴中,f为
溶液,并置于冰水浴中,f为 的发生装置。
的发生装置。(1)制取氯气时,在烧瓶中先加入一定量的
 固体,再通过
固体,再通过(2)装置b的作用是
(3)f装置中反应的化学方程式为
(4)比较制取氯酸钾和次氯酸钠的条件,两者的差异是
(5)反应完毕经冷却后,c装置的试管中有大量晶体析出,图中符合该晶体溶解度随温度变化规律的曲线是

(6)将d中余气与f中产生的气体通入e中,产生的现象为
(7)该实验有一处明显的缺点是
您最近一年使用:0次
2022-01-23更新
|
202次组卷
|
2卷引用:四川省泸县第四中学2022-2023学年高一上学期第三次月考化学试题



