名校
1 . 用下列装置不能达到实验目的的是
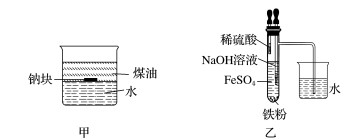
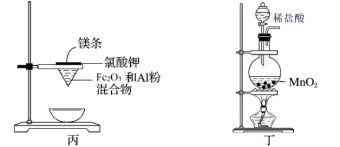


| A.用甲图装置可证明ρ(煤油)<ρ(钠)<ρ(水) | B.用乙图装置制备Fe(OH)2 |
| C.用丙图装置制取金属铁 | D.用丁图装置制取氯气 |
您最近一年使用:0次
名校
解题方法
2 . 图为一些物质之间的转化关系,其中部分反应中反应物或生成物未列全。已知A、H、I、K均为家庭厨房中的常见物质,其中A是食品调味剂,H是消毒剂的有效成分,I、K可用作食品发泡剂。B是一种有机酸盐,E、F、G均为氧化物,L是红褐色沉淀。
根据以上信息,回答下列问题:

(1)B的组成元素为________________ 。
(2)实验室制取C的离子方程式为_________________________________________ 。
(3)鉴别等物质的量浓度的I、K稀溶液的实验方法为_________________________________ 。
(4)G→J的离子方程式为_________________________________________ 。
(5)M是含氧酸盐,反应①中H、L、D的物质的量之比为3: 2: 4,则M的化学式为___________ 。
(6)某化学学习小组探究FeSO4与“84”消毒液的反应过程,向酸化的FeSO4溶液中逐滴滴入“84”消毒液,780s时停止滴入;滴加过程中bc、cd段产生相同的刺激性气味的气体。采用pH传感器测得溶液的pH随时间t(s)的变化曲线如图所示。

①bc段发生反应的离子方程式:______________________ 。
②cd段产生刺激性气味气体反应的离子方程式:____________________ 。
③de段pH减小的原因是(请用必要的文字和化学方程式表达)_______________ 。
根据以上信息,回答下列问题:

(1)B的组成元素为
(2)实验室制取C的离子方程式为
(3)鉴别等物质的量浓度的I、K稀溶液的实验方法为
(4)G→J的离子方程式为
(5)M是含氧酸盐,反应①中H、L、D的物质的量之比为3: 2: 4,则M的化学式为
(6)某化学学习小组探究FeSO4与“84”消毒液的反应过程,向酸化的FeSO4溶液中逐滴滴入“84”消毒液,780s时停止滴入;滴加过程中bc、cd段产生相同的刺激性气味的气体。采用pH传感器测得溶液的pH随时间t(s)的变化曲线如图所示。

①bc段发生反应的离子方程式:
②cd段产生刺激性气味气体反应的离子方程式:
③de段pH减小的原因是(请用必要的文字和化学方程式表达)
您最近一年使用:0次
名校
解题方法
3 . 实验室制备氯气的装置如下,以下装置中最多有几处错误

稀盐酸

| A.4 | B.5 | C.7 | D.9 |
您最近一年使用:0次
4 . Ⅰ.现用溶质质量分数为98%、密度为1.84 g·cm-3的浓硫酸来配制480 mL、0.2 mol·L-1的稀硫酸。
现有仪器:①玻璃棒;②烧瓶;③烧杯;④胶头滴管;⑤量筒。
请完成下列问题:
(1)在配制过程中用到的仪器除现有仪器外,还需_______ 。
(2)经计算,需浓硫酸的体积为_______ mL。
(3)在配制过程中,其他操作都准确,能引起误差偏高的有_______ (填代号)。
①洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中;
②定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线;
③定容时,俯视标线;
④定容时,加蒸馏水超过标线,又用胶头滴管吸出;
⑤转移前,容量瓶中含有少量蒸馏水;
⑥浓硫酸溶解后,立即转移至容量瓶。
Ⅱ.无水FeCl3在空气中易潮解,遇水水解,加热易升华。实验室可用下列装置制备。
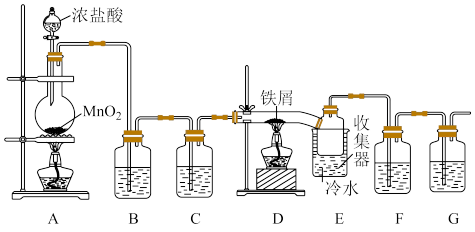
(4)A中反应的化学方程式为:_______ 。
(5)装置B、F中所盛的试剂分别是_______ ,_______ 。
(6)何时开始点燃D处的酒精灯?_______ 。
(7)写出G中反应的离子方程式:_______
现有仪器:①玻璃棒;②烧瓶;③烧杯;④胶头滴管;⑤量筒。
请完成下列问题:
(1)在配制过程中用到的仪器除现有仪器外,还需
(2)经计算,需浓硫酸的体积为
(3)在配制过程中,其他操作都准确,能引起误差偏高的有
①洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中;
②定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线;
③定容时,俯视标线;
④定容时,加蒸馏水超过标线,又用胶头滴管吸出;
⑤转移前,容量瓶中含有少量蒸馏水;
⑥浓硫酸溶解后,立即转移至容量瓶。
Ⅱ.无水FeCl3在空气中易潮解,遇水水解,加热易升华。实验室可用下列装置制备。

(4)A中反应的化学方程式为:
(5)装置B、F中所盛的试剂分别是
(6)何时开始点燃D处的酒精灯?
(7)写出G中反应的离子方程式:
您最近一年使用:0次
解题方法
5 . 下列实验对应的结论正确的是
| A | B | C | D | |
装置 | 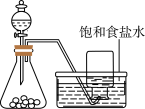 | 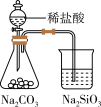 | 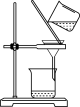 | 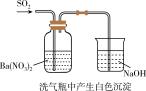 |
| 结论 | 用浓盐酸与高锰酸钾制氯气 | 能证明非金属性 Cl > C > Si | 分离出Cl2与KI溶液反应生成的碘 | 白色沉淀是BaSO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 下图为制取无水氯化铁粉末的装置,已知无水氯化铁粉末很容易吸水生成结晶水合物FeCl3+6H2O=FeCl3·6H2O。

(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序):①接___________,___________接___________;___________接___________。___________
(2)装置A烧瓶中发生的反应,氧化剂是___________ (填物质名称),装置B中反应的化学方程式是___________ 。
(3)装置C的作用是___________ 。
(4)装置A、B中的酒精灯应先点燃___________ 处(填“A”或“B”)的酒精灯。
(5)某同学认为这套实验装置不完整,还须补充___________ 装置。
(6)反应结束后,将B装置中的固体溶于一定量的水中,固体完全溶解,向其中滴加KSCN溶液,发现溶液没有变成红色。则B装置中所制得无水氯化铁产品中FeCl3的质量分数为___________ 。(计算结果保留3位有效数字)

(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序):①接___________,___________接___________;___________接___________。
(2)装置A烧瓶中发生的反应,氧化剂是
(3)装置C的作用是
(4)装置A、B中的酒精灯应先点燃
(5)某同学认为这套实验装置不完整,还须补充
(6)反应结束后,将B装置中的固体溶于一定量的水中,固体完全溶解,向其中滴加KSCN溶液,发现溶液没有变成红色。则B装置中所制得无水氯化铁产品中FeCl3的质量分数为
您最近一年使用:0次
解题方法
7 . 一氧化二氯(Cl2O)是一种氯化剂和氧化剂,黄棕色具有强烈刺激性气味,有毒,高温下易分解,它易溶于水(1体积:100体积),是一种酸性氧化物,遇有机物易燃烧或爆炸。利用如图装置可制备少量Cl2O。

已知Cl2O的部分性质如表:
回答下列问题:
(1)装置甲中仪器B的名称是___________ 。
(2)装置丙的集气瓶中盛有的试剂是___________ 。
(3)装置甲的作用是为该制备反应提供Cl2,写出该装置中制备Cl2的离子方程式:_______ 。
(4)装置丁中通入的空气要提前干燥的原因是(用化学方程式表示)___________ 。
(5)装置戊中采用18℃~20℃水浴而不采用更高温度的原因是___________ 。
(6)氨的沸点为-33.4℃,熔点为-77.7℃,则装置己中收集到的产物为___________ (填“固体”“液体”或“气体”)物质。若实验开始前称量装置戊中的玻璃丝与HgO的混合物的质量为ag,实验结束后玻璃丝及其附着物的质量为bg,则制备的Cl2O为___________ mol。
(7)尾气中的有毒气体成分是___________ ,可用___________ 吸收除去(均填写化学式)

已知Cl2O的部分性质如表:
| 熔点 | 沸点 | 制备方法 |
| -120.6℃ | 2.0℃ | 2HgO+2Cl2=Cl2O+HgCl2·HgO |
(1)装置甲中仪器B的名称是
(2)装置丙的集气瓶中盛有的试剂是
(3)装置甲的作用是为该制备反应提供Cl2,写出该装置中制备Cl2的离子方程式:
(4)装置丁中通入的空气要提前干燥的原因是(用化学方程式表示)
(5)装置戊中采用18℃~20℃水浴而不采用更高温度的原因是
(6)氨的沸点为-33.4℃,熔点为-77.7℃,则装置己中收集到的产物为
(7)尾气中的有毒气体成分是
您最近一年使用:0次
8 . 三氯乙醛常用于制造敌百虫等杀虫剂、三氯乙醛脲除草剂。已知部分信息如下:
制备原理:CH3CH2OH+4Cl2→CCl3CHO+5HCl;
副反应:CH3CH2OH+HCl→CH3CH2Cl+H2O。
制备三氯乙醛的流程:乙醇 三氯乙醛的混合液
三氯乙醛的混合液 三氯乙醛粗产品
三氯乙醛粗产品
(一)制备三氯乙醛的混合液,装置如图(部分夹持及加热装置省略)。
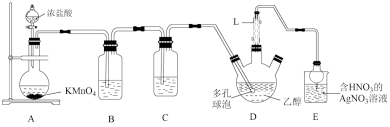
(1)L仪器的名称是_______ 。
(2)多孔球泡的作用是_______ 。
(3)装置A中发生反应的离子方程式为_______ 。
(4)为了证明装置D中产生HCl,需要在装置D和装置E之间增加下列装置_______ (填字母)。
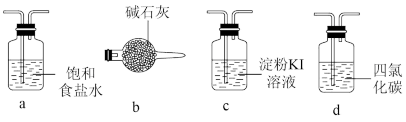
(二)制备三氯乙醛粗产品,装置如图。
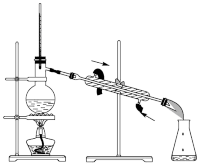
(5)烧瓶中加入几块碎瓷片,其作用是_______ 。
(6)粗产品中可能含有机物杂质CH3CH2OCH2CH3,写出其产生的化学方程式_______ 。
(7)鉴定产物中的官能团,一般用什么仪器:_______ 。
制备原理:CH3CH2OH+4Cl2→CCl3CHO+5HCl;
副反应:CH3CH2OH+HCl→CH3CH2Cl+H2O。
制备三氯乙醛的流程:乙醇
 三氯乙醛的混合液
三氯乙醛的混合液 三氯乙醛粗产品
三氯乙醛粗产品(一)制备三氯乙醛的混合液,装置如图(部分夹持及加热装置省略)。

(1)L仪器的名称是
(2)多孔球泡的作用是
(3)装置A中发生反应的离子方程式为
(4)为了证明装置D中产生HCl,需要在装置D和装置E之间增加下列装置

(二)制备三氯乙醛粗产品,装置如图。

(5)烧瓶中加入几块碎瓷片,其作用是
(6)粗产品中可能含有机物杂质CH3CH2OCH2CH3,写出其产生的化学方程式
(7)鉴定产物中的官能团,一般用什么仪器:
您最近一年使用:0次
9 . 在给定条件下物质间转化均能实现的是
A.MnO2 Cl2 Cl2 漂白粉 漂白粉 |
B.Fe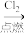 FeCl2 FeCl2 FeCl3 FeCl3 Fe(OH)3 Fe(OH)3 |
C.N2 NH3 NH3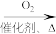 NO NO NO2 NO2 HNO3 HNO3 |
D.S(s)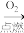 SO3(g) SO3(g)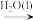 H2SO4(aq) H2SO4(aq) |
您最近一年使用:0次
10 . 图中为实验室制取氯气及性质验证的装置图:

参考装置图回答下列问题:
(1)请指出仪器a的名称___________ ,写出装置A中反应的离子方程式___________ 。
(2)在装置D中可观察到的现象是___________ ,装置F中可观察到的现象是___________ 。
(3)装置B的作用为___________ ,装置C的作用为___________ 。
(4)装置H的作用为___________ ,写出装置H中的离子方程式___________ 。

参考装置图回答下列问题:
(1)请指出仪器a的名称
(2)在装置D中可观察到的现象是
(3)装置B的作用为
(4)装置H的作用为
您最近一年使用:0次



