1 . 锡箔纸常用于食品包装和食品加工。制作锡箔纸的主要金属元素锡(Sn)位于周期表的第ⅣA族,它的常见价态有+2、 +4价,其单质沸点为2260℃,四氯化锡( SnCl4)是无色液体,熔点-33℃,沸点114℃,极易水解,在潮湿的空气中发烟。实验室中可用氯气与过量金属锡通过下图装置制备SnCl4(夹持装置已略去)。

(1)装置乙的作用是_______ ,装置丙中的试剂是_______ 。实验过程中应先点燃_______ 处酒精灯(填“甲”或“丁”)。
(2)装置甲中生成标况下44.8L Cl2时,被氧化的HCl数目为_______ 。
(3)氯气与锡的反应类似与铁的反应,但该实验中对装置丁要持续加热,其原因是_______ 。
(4)你认为该实验装置最大的缺点是:_______ 。
(5)用滴定法测定所用金属锡样品的纯度(杂质不参加反应)。
①将一定量锡粉完全溶于过量稀盐酸中,并用所得溶液去还原过量的FeCl3稀溶液。写出第二步反应的离子方程式:_______ 。
②取①所得溶液用K2Cr2O7溶液滴定,发生如下反应:6FeCl2+ K2Cr2O7+14HCl=6FeCl3+2KCl+2CrCl3+7H2O。K2Cr2O7溶液应注入到_______ 式填“酸”或“碱”) 式滴定管中。滴定完后发现滴定尖嘴处有气泡,则滴定结果_______ 。(填“偏高”、“偏低”或者“不变”)

(1)装置乙的作用是
(2)装置甲中生成标况下44.8L Cl2时,被氧化的HCl数目为
(3)氯气与锡的反应类似与铁的反应,但该实验中对装置丁要持续加热,其原因是
(4)你认为该实验装置最大的缺点是:
(5)用滴定法测定所用金属锡样品的纯度(杂质不参加反应)。
①将一定量锡粉完全溶于过量稀盐酸中,并用所得溶液去还原过量的FeCl3稀溶液。写出第二步反应的离子方程式:
②取①所得溶液用K2Cr2O7溶液滴定,发生如下反应:6FeCl2+ K2Cr2O7+14HCl=6FeCl3+2KCl+2CrCl3+7H2O。K2Cr2O7溶液应注入到
您最近一年使用:0次
名校
解题方法
2 . 如图为某学习小组制取并验证Cl2性质的实验装置,下列叙述不正确 的是
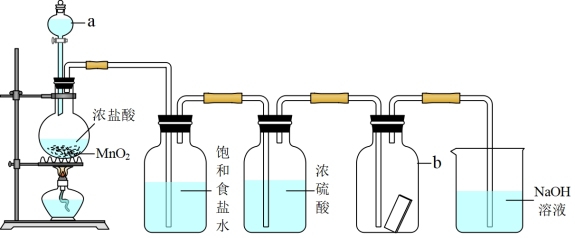

| A.仪器a的名称为分液漏斗 |
| B.浓硫酸的作用是除去Cl2中混有的HCl气体 |
| C.b中湿润的有色布条褪色 |
| D.NaOH溶液的主要作用是吸收Cl2,防止污染环境 |
您最近一年使用:0次
2022-04-20更新
|
436次组卷
|
6卷引用:贵州省2021-2022学年高二上学期12月普通高中学业水平考试化学试题
贵州省2021-2022学年高二上学期12月普通高中学业水平考试化学试题浙江省舟山中学2021-2022学年高一下学期6月月考化学试题(已下线)第05练 氯及其化合物-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第05练 氯及其化合物-2023年高考化学一轮复习小题多维练(全国通用)内蒙古乌兰察布市化德县第一中学2022-2023学年高一上学期期末考试化学试题河南省周口市太康县2022-2023学年高一上学期11月期中考试化学试题
3 . 在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图所示。
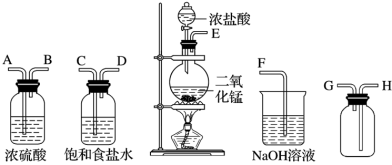
(1)连接上述仪器的正确顺序(填各接口处的字母):_______ 。盛放浓盐酸的仪器名称为:_______ 。
(2)装置中,饱和食盐水的作用是_______ 。
(3)化学实验中常用湿润的KI-淀粉试纸检验是否有Cl2产生。如果有Cl2产生,可观察到_______ ,反应的化学方程式为_______ 。
(4)写出下列反应的化学方程式:
①气体发生装置中进行的反应:_______ 。
②NaOH溶液中发生的反应:_______ 。
(5)将8.7gMnO2与含HCl14.6g的浓盐酸共热制Cl2,甲同学认为可制得Cl27.1g,乙同学认为制得Cl2的质量小于7.1g,你认为_______ (填“甲”或“乙”)同学正确,原因是_______ 。

(1)连接上述仪器的正确顺序(填各接口处的字母):
(2)装置中,饱和食盐水的作用是
(3)化学实验中常用湿润的KI-淀粉试纸检验是否有Cl2产生。如果有Cl2产生,可观察到
(4)写出下列反应的化学方程式:
①气体发生装置中进行的反应:
②NaOH溶液中发生的反应:
(5)将8.7gMnO2与含HCl14.6g的浓盐酸共热制Cl2,甲同学认为可制得Cl27.1g,乙同学认为制得Cl2的质量小于7.1g,你认为
您最近一年使用:0次
名校
4 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
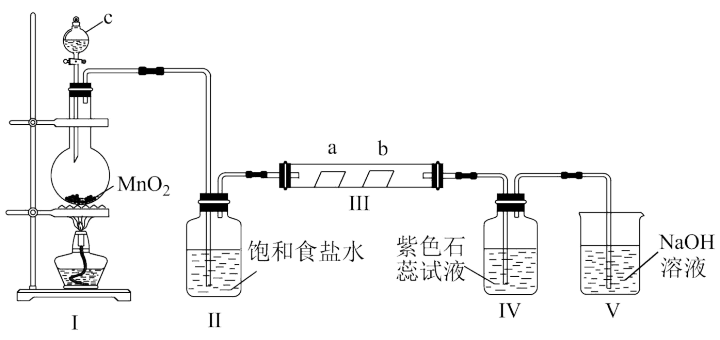
(1)装置Ⅰ中仪器c的名称是___________ ,实验室以二氧化锰和浓盐酸制备氯气的化学方程式为___________ 。
(2)装置Ⅱ的作用是___________ 。
(3)若产生的Cl2足量,实验过程中装置Ⅳ中的实验现象是___________ 。
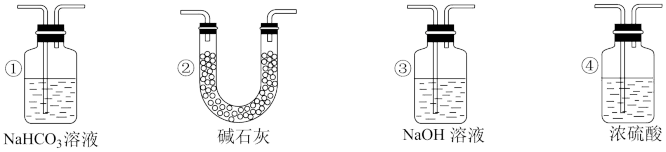
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。
(5)除了Cl2能够对自来水杀菌消毒外,工业中还常用高铁酸钾(K2FeO4)作为高效、多功能的自来水处理剂,高铁酸钾与水反应时,能生成Fe(OH)3胶体吸附杂质净水,同时还产生一种气体,写出该原理的离子方程式___________ ,每生成1mol该气体,K2FeO4转移的电子数目为___________ NA。

(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生的Cl2足量,实验过程中装置Ⅳ中的实验现象是
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(5)除了Cl2能够对自来水杀菌消毒外,工业中还常用高铁酸钾(K2FeO4)作为高效、多功能的自来水处理剂,高铁酸钾与水反应时,能生成Fe(OH)3胶体吸附杂质净水,同时还产生一种气体,写出该原理的离子方程式
您最近一年使用:0次
2021-12-18更新
|
293次组卷
|
2卷引用:贵州省黔南州都匀市都匀第一中学2021-2022学年高一上学期期中化学试题
5 . 实验室用Cl2氧化K2MnO4来制备KMnO4,装置如图1所示:
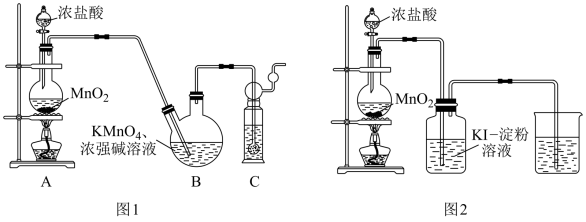
已知:K2MnO4在浓强碱溶液中可稳定存在,碱性减弱时易发生反应3MnO + 2H2O=2
+ 2H2O=2 +MnO2↓+4OH-。
+MnO2↓+4OH-。
请回答下列问题:。
(1)K2 MnO4中锰元素的化合价为___________ 价。
(2)装置B中生成KMnO4的离子方程式为___________
(3)进入装置B的Cl2中含有杂质HCl,HCl___________ (填“ 需要”或“不需要”)除去,理由是___________ 。
(4)甲同学设计如图2所示的实验来研究二氧化锰与盐酸的反应情况,各组实验参数如表所示:
根据第一组、第二组的实验可得出的结论是___________ ,根据第 三组实验可得出的结论是___________ 。
(5)为测定某NaHSO3固体的纯度,现用0. 1000 mol·L-1的酸性KMnO4溶液进行滴定。(已知: 2 +5
+5 +H+=2Mn2+ +5
+H+=2Mn2+ +5 +3H2O)
+3H2O)
①称取W g NaHSO3固体溶于水配成100 mL溶液,下列仪器在该过程中肯定不需要用到的是___________ (填仪器名称)。
a. b.
b.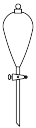 c.
c.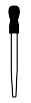 d.
d.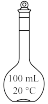
②取25.00mLNaHSO3溶液置于锥形瓶中,用酸性KMnO4溶液滴定至终点,消耗KMnO4溶液VmL。滴定终点的现象为。___________ ,NaHSO3固体的纯度为___________ (用含V 和W的代数式表示)。

已知:K2MnO4在浓强碱溶液中可稳定存在,碱性减弱时易发生反应3MnO
 + 2H2O=2
+ 2H2O=2 +MnO2↓+4OH-。
+MnO2↓+4OH-。请回答下列问题:。
(1)K2 MnO4中锰元素的化合价为
(2)装置B中生成KMnO4的离子方程式为
(3)进入装置B的Cl2中含有杂质HCl,HCl
(4)甲同学设计如图2所示的实验来研究二氧化锰与盐酸的反应情况,各组实验参数如表所示:
| 组别 | 反应条件 | 盐酸浓度 | 淀粉—KI溶液的颜色变化 |
| 第一组 | 微热 | 10mol/L | 变蓝色 |
| 第二组 | 常温 | 10mol/L | 不变色 |
| 第三组 | 微热 | 5mol/L | 不变色 |
(5)为测定某NaHSO3固体的纯度,现用0. 1000 mol·L-1的酸性KMnO4溶液进行滴定。(已知: 2
 +5
+5 +H+=2Mn2+ +5
+H+=2Mn2+ +5 +3H2O)
+3H2O)①称取W g NaHSO3固体溶于水配成100 mL溶液,下列仪器在该过程中肯定不需要用到的是
a.
 b.
b.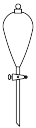 c.
c.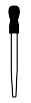 d.
d.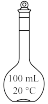
②取25.00mLNaHSO3溶液置于锥形瓶中,用酸性KMnO4溶液滴定至终点,消耗KMnO4溶液VmL。滴定终点的现象为。
您最近一年使用:0次
6 . 某学校兴趣小组采用如图装置制取 及无水
及无水 固体(容易潮解,在100℃左右升华)。
固体(容易潮解,在100℃左右升华)。
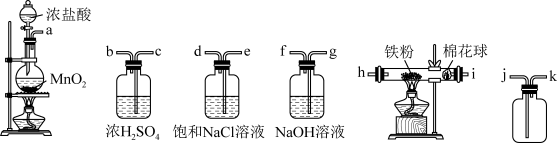
回答下列问题:
(1)上述装置从左至右的连接顺序为___________ →cbgf(填字母,必要的装置可重复使用)。
(2)饱和NaCl溶液的作用为___________ ;棉花球的作用为___________ ; 与Fe粉反应的化学方程式为
与Fe粉反应的化学方程式为___________ 。
(3)NaOH溶液的作用是___________ 。
(4)将干燥的 依次通过干燥的有色布条、湿润的有色布条,可观察到的现象是
依次通过干燥的有色布条、湿润的有色布条,可观察到的现象是___________ ,得出的结论是___________ 。
(5)实验结束后,从盛有NaOH溶液的广口瓶中取少量溶液于烧杯中,加入足量浓盐酸后,会产生一种黄绿色气体,写出生成该气体的离子方程式___________ 。
 及无水
及无水 固体(容易潮解,在100℃左右升华)。
固体(容易潮解,在100℃左右升华)。
回答下列问题:
(1)上述装置从左至右的连接顺序为
(2)饱和NaCl溶液的作用为
 与Fe粉反应的化学方程式为
与Fe粉反应的化学方程式为(3)NaOH溶液的作用是
(4)将干燥的
 依次通过干燥的有色布条、湿润的有色布条,可观察到的现象是
依次通过干燥的有色布条、湿润的有色布条,可观察到的现象是(5)实验结束后,从盛有NaOH溶液的广口瓶中取少量溶液于烧杯中,加入足量浓盐酸后,会产生一种黄绿色气体,写出生成该气体的离子方程式
您最近一年使用:0次
2021-11-15更新
|
59次组卷
|
2卷引用:贵州省遵义市2021-2022学年高一上学期期中联合考试化学试题
7 . 下列实验装置不能达到实验目的的是
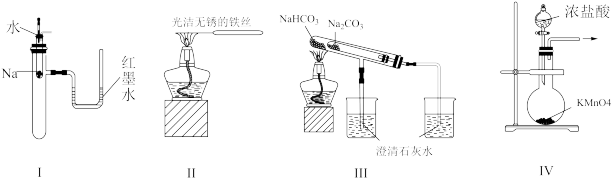

| A.图I:验证Na和水反应是否为放热反应 | B.图II:观察纯碱的焰色试验 |
| C.图III:比较Na2CO3、NaHCO3的稳定性 | D.图IV:制取Cl2 |
您最近一年使用:0次
2021-11-15更新
|
228次组卷
|
2卷引用:贵州省六盘水红桥学校2021-2022学年高一上学期11月月考化学试题
名校
8 . 铝土矿是生产金属铝的最佳原料,也是最主要的应用领域,其用量占世界铝土矿总产量的90%以上。以铝土矿(主要成分为Al2O3,含有Fe2O3和SiO2)等杂质)为原料,制备有机合成中的重要还原剂铝氢化钠(NaAlH4) 的一种工业流程如图:

已知: AlCl3、 NaH、NaAlH4遇水都能迅速发生反应。
(1)写出碱溶时发生反应的离子方程式:_______ 、_______ 。
(2)滤渣I中的主要成分为_______ (写物质名称)。
(3)写出反应I中主要反应的化学方程式:_______ 。
(4)甲同学设计了如图实验装置在实验室模拟制备无水氯化铝,应用该装置制备无水氯化铝,B、C中的试剂分别为_______ 和_______ 。

(5)A中发生反应的化学方程式为_______ ;该反应中氧化剂和还原剂的物质的量之比为_______ 。
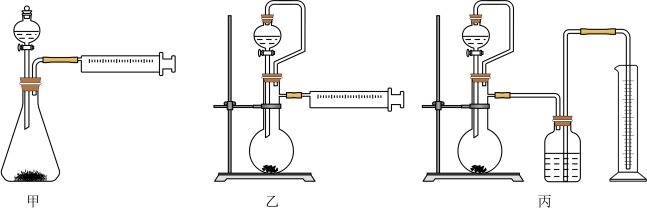
(6)乙同学设计了以下三种装置测定工业制取的铝氢化钠样品的纯度,从易操作、准确性角度考虑宜选择的装置是_______ (填“甲”“乙”或“丙”)

已知: AlCl3、 NaH、NaAlH4遇水都能迅速发生反应。
(1)写出碱溶时发生反应的离子方程式:
(2)滤渣I中的主要成分为
(3)写出反应I中主要反应的化学方程式:
(4)甲同学设计了如图实验装置在实验室模拟制备无水氯化铝,应用该装置制备无水氯化铝,B、C中的试剂分别为

(5)A中发生反应的化学方程式为
(6)乙同学设计了以下三种装置测定工业制取的铝氢化钠样品的纯度,从易操作、准确性角度考虑宜选择的装置是

您最近一年使用:0次
名校
解题方法
9 . Cl2与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐。某兴趣小组利用如图装置以Cl2分别与KOH溶液和NaOH溶液反应为原理,制备KClO3和NaClO,并探究KClO3和NaClO的部分性质。

回答下列问题:
(1)盛放浓盐酸的仪器名称是_______ ,b装置的作用为_______ 。
(2)a装置中发生反应的离子方程式为_______ 。
(3)c装置中采用的加热方式的名称为_______ ;d装置采用冰水浴冷却的目的是_______ ;e装置的作用是_______ 。
(4)取少量c、d装置中生成的KClO3和NaClO溶液(两溶液均调至碱性),分别置于1号和2号试管中,向两试管中分别滴加等量且适量的KI溶液。1号试管溶液颜色不变;2号试管溶液颜色变为棕色,加入CCl4,振荡、静置后CCl4层显_______ 色。由此可推知,在碱性条件下,KClO3的氧化能力_______ (填“>”或“<”)NaClO的氧化能力。
(5)该兴趣小组在40℃条件下,将一定量的Cl2通入600 mL 1.00 mol·L-1 NaOH溶液中,NaOH恰好反应完全,得到的产物中含有NaCl、NaClO和NaClO3,则参加反应的Cl2的物质的量为_______ mol。

回答下列问题:
(1)盛放浓盐酸的仪器名称是
(2)a装置中发生反应的离子方程式为
(3)c装置中采用的加热方式的名称为
(4)取少量c、d装置中生成的KClO3和NaClO溶液(两溶液均调至碱性),分别置于1号和2号试管中,向两试管中分别滴加等量且适量的KI溶液。1号试管溶液颜色不变;2号试管溶液颜色变为棕色,加入CCl4,振荡、静置后CCl4层显
(5)该兴趣小组在40℃条件下,将一定量的Cl2通入600 mL 1.00 mol·L-1 NaOH溶液中,NaOH恰好反应完全,得到的产物中含有NaCl、NaClO和NaClO3,则参加反应的Cl2的物质的量为
您最近一年使用:0次
2021-09-17更新
|
214次组卷
|
3卷引用:贵州省部分重点中学2021-2022学年高三上学期8月联考化学试题
贵州省部分重点中学2021-2022学年高三上学期8月联考化学试题云南省峨山彝族自治县第一中学2021-2022学年高二上学期9月月考化学试题(已下线)专题39 氯的氧化物、含氧酸及含氧酸盐-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
10 .  溶液常用作氧化还原反应滴定的标准液,利用
溶液常用作氧化还原反应滴定的标准液,利用 氧化
氧化 制备
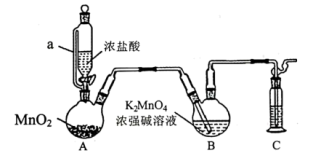
制备 的装置如图所示(加热、夹持装置略):
的装置如图所示(加热、夹持装置略):
已知: 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
在浓强碱溶液中可稳定存在,碱性减弱时易发生反应: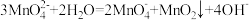
回答下列问题:
(1) 的化学名称为
的化学名称为_______ 。
(2)装置A中所发生反应的化学方程式为_______ ;其中a的作用是_______ 。
(3)装置C中盛装的试剂是_______ 。
(4)分析发现该装置有不足之处,改进的方法是_______ 。
(5)为测定某 固体的纯度,现用
固体的纯度,现用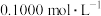 的酸性
的酸性 溶液进行滴定。(已知:
溶液进行滴定。(已知: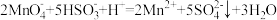 )
)
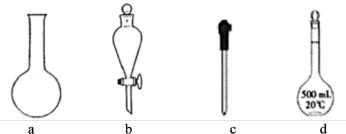
①确称取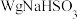 固体溶于水配成
固体溶于水配成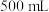 溶液,下列仪器中肯定需要的是
溶液,下列仪器中肯定需要的是_______ (填仪器名称)。
②取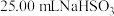 溶液置于锥形瓶中,用
溶液置于锥形瓶中,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液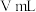 。滴定终点的现象为
。滴定终点的现象为_______ , 固体的纯度为
固体的纯度为_______ 。
 溶液常用作氧化还原反应滴定的标准液,利用
溶液常用作氧化还原反应滴定的标准液,利用 氧化
氧化 制备
制备 的装置如图所示(加热、夹持装置略):
的装置如图所示(加热、夹持装置略):
已知:
 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
在浓强碱溶液中可稳定存在,碱性减弱时易发生反应: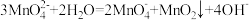
回答下列问题:
(1)
 的化学名称为
的化学名称为(2)装置A中所发生反应的化学方程式为
(3)装置C中盛装的试剂是
(4)分析发现该装置有不足之处,改进的方法是
(5)为测定某
 固体的纯度,现用
固体的纯度,现用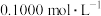 的酸性
的酸性 溶液进行滴定。(已知:
溶液进行滴定。(已知: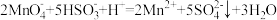 )
)①确称取
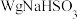 固体溶于水配成
固体溶于水配成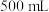 溶液,下列仪器中肯定需要的是
溶液,下列仪器中肯定需要的是
②取
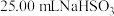 溶液置于锥形瓶中,用
溶液置于锥形瓶中,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液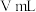 。滴定终点的现象为
。滴定终点的现象为 固体的纯度为
固体的纯度为
您最近一年使用:0次
2021-08-22更新
|
318次组卷
|
4卷引用:贵州省贵阳市2022届高三上学期8月摸底考试(开学考试)化学试题



