名校
解题方法
1 . 下列装置适用于实验室制氨气并验证氨气的某化学性质,其中能达到实验目的的是
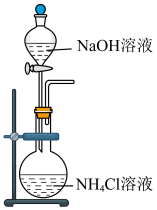 | 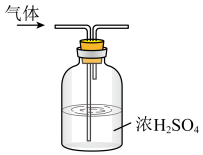 | 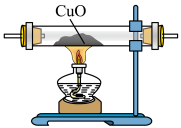 | 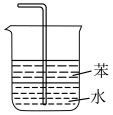 |
| A.用装置制取氨 | B.用装置除去氨中的水蒸气 | C.用装置验证氨具有还原性 | D.用装置吸收尾气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-20更新
|
222次组卷
|
53卷引用:黑龙江省哈尔滨师范大学附属中学2020-2021学年高一下学期期末考试化学(理)试题
黑龙江省哈尔滨师范大学附属中学2020-2021学年高一下学期期末考试化学(理)试题2016-2017学年黑龙江省大庆实验中学高一下学期第一次月考(4月)化学试卷山东省济南市2020-2021学年高一上学期学情诊断考试化学试题(已下线)5.2.2 氨与铵盐(练好题)(能力提升)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)(已下线)【浙江新东方】双师169高一下(已下线)【浙江新东方】双师173高一下上海市南洋模范中学2020-2021学年高一下学期期中考试化学试题江苏省仪征中学2020-2021学年高一下学期4月学情检测化学试题江苏省2020-2021学年高一下学期5月百校联考化学试题河北省沧州市第一中学2020-2021学年高一下学期第二次检测化学试题云南省梁河县第一中学2021-2022学年高二上学期开学考试化学试题安徽省合肥市第一中学2021-2022学年高三上学期10月月考化学试题黑龙江省哈尔滨师范大学附属中学2021-2022学年高一下学期期末考试化学试题黑龙江省牡丹江市第三高级中学2022-2023学年高一下学期期末考试化学试题2015届江苏省南通市高三三模化学试卷2016届山东省烟台市高三上学期期中测试化学试卷2016届宁夏六盘山高级中学高三上第二次月考理综化学试卷2015-2016学年江苏省扬州中学高一下3月月考化学试卷2016-2017学年云南省临沧一中高二上起点考试化学卷2017届江苏省丹阳高级中学高三上期初考试化学试卷2017届河北省定州中学高三高补班12月月考化学卷2017届江苏省南通市高三高考全真模拟(五)化学 试卷江苏省常熟市2018届高三上学期期中考试化学试题(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第4讲 氮及其化合物【押题专练】【全国百强校】甘肃省天水一中2018-2019学年高一下学期第一阶段考试化学试题(已下线)2019年8月25日 《每日一题》2020年高考一轮复习—— 每周一测2020届高三化学二轮冲刺新题专练——气体制取流程的规范操作(提升练)2020届高三化学一轮复习 化学基础实验(选择题和大题训练)湖北省荆州市2019-2020学年高一上学期期末考试化学试题湖北省武汉市黄陂区第六中学2019-2020学年高一3月月考化学试卷(已下线)3.3.2 氨的转化与生成练习(1)——《高中新教材同步备课》(鲁科版 必修第一册)鲁科版(2019)高一必修第一册第3章 物质的性质与转化 第3节 氮的循环 课时2 氨的转化与生成高一必修第二册(人教2019版)第五章 第二节 氮及其化合物 课时2 氨与铵盐(已下线)练习11 氮的循环-2020-2021学年【补习教材·寒假作业】高一化学(鲁科版2019)云南省宣威市第三中学2021-2022学年高一下学期4月考试化学试题浙江省台州市三门启超中学等两校2021-2022学年高一下学期期中联考化学试题上海市七宝中学2021-2022学年高一下学期线上检测4月月考化学试题广西三新教学质量测评2021-2022学年高一4月段考化学试题贵州省六盘水市六枝特区2021-2022学年高一下学期期中教学质量检测化学试题(已下线)第14讲 氮及其化合物(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第13练 氮及其化合物-2023年高考化学一轮复习小题多维练(全国通用)云南省石屏县第一中学2021-2022学年高一下学期3月份考试化学试题湖北省罗田县第一中学2021-2022学年高一下学期3月月考化学试题江苏省新高考基地学校2022-2023学年高三上学期第三次大联考化学试题(已下线)5.2.2 氨和铵盐——同步学习必备知识(已下线)第四章 非金属及其化合物 第24练 常见气体的实验室制备、净化和收集江苏省南京市第五高级中学2022-2023学年高一下学期3月月考化学试题(已下线)专题04 常见气体的实验室制取(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)安徽省六安第一中学2022-2023学年高一下学期第一次阶段检测化学试题江苏省扬州市邗江区2022-2023学年高一下学期期中调研测试化学试题北京市第五十中学2022-2023学年高一下学期期中考试化学试题上海市民办南模中学2022-2023学年高一下学期期中考试化学试题第2课时 氨与铵态氮肥
解题方法
2 . 如图为实验室制取纯净、干燥的Cl2,并验证Cl2性质的装置。其中E瓶放有干燥红色布条,F中为红色的铜网,其右端出气管口放有脱脂棉。

(1)写出实验室制取氯气的化学方程式:_______ 。
(2)装置C中盛装的溶液是_______ ,D中试剂的作用是_______ 。
(3)E中红色布条是否褪色?_______ ,F中的反应产物为_______ 。
(4)向新制氯水中滴加紫色石蕊,能观察到紫色石蕊先变红后褪色,由此可判断新制氯水的成分中含有_______ 和_______ 。
(5)若H中选用NaOH溶液进行尾气处理,则发生反应的离子方程式表示_______ 。

(1)写出实验室制取氯气的化学方程式:
(2)装置C中盛装的溶液是
(3)E中红色布条是否褪色?
(4)向新制氯水中滴加紫色石蕊,能观察到紫色石蕊先变红后褪色,由此可判断新制氯水的成分中含有
(5)若H中选用NaOH溶液进行尾气处理,则发生反应的离子方程式表示
您最近一年使用:0次
3 . 如图是一套制取并验证氯气部分化学性质的实验装置。已知: 。
。

回答下列问题:
(1)装置A中,仪器a的名称叫_______ ,该仪器中盛放的试剂为_______ ,写出A装置发生反应的化学方程式:_______ 。
(2)装置B的作用是_______ 。
(3)当有少量 通过后,观察到装置C中溶液变成
通过后,观察到装置C中溶液变成_______ 色。
(4)当 持续通过时,装置D中干燥的有色布条能否褪色?为什么?
持续通过时,装置D中干燥的有色布条能否褪色?为什么?_______ ,_______ 。
(5)若要证明 无漂白性,则必须在装置D之前加一个
无漂白性,则必须在装置D之前加一个_______ 。
(6)装置E的作用是_______ ,该反应的离子方程式为_______ 。
(7)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下。
消毒液与洁厕灵不能同时使用,原因是(用离子方程式表示)_______ 。
 。
。
回答下列问题:
(1)装置A中,仪器a的名称叫
(2)装置B的作用是
(3)当有少量
 通过后,观察到装置C中溶液变成
通过后,观察到装置C中溶液变成(4)当
 持续通过时,装置D中干燥的有色布条能否褪色?为什么?
持续通过时,装置D中干燥的有色布条能否褪色?为什么?(5)若要证明
 无漂白性,则必须在装置D之前加一个
无漂白性,则必须在装置D之前加一个(6)装置E的作用是
(7)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下。
| 注意事项: 1.本品对棉制品有漂白脱白作用,对金属制品有腐蚀作用。 2.密封保存,请勿与洁厕灵同时使用。 3.保质期为一年 |
您最近一年使用:0次
2022-12-20更新
|
106次组卷
|
2卷引用:黑龙江省鹤岗市绥滨县第一中学2021-2022年度高一上学期期中考试化学试题
解题方法
4 . 肼(N2H4)作为火箭发动机的燃料,可通过反应NaClO+2NH3=N2H4+NaCl+H2O制取。某化学兴趣小组尝试在实验室制取N2H4,设计了如图实验:
(1)制备NaClO溶液,装置如图所示。(已知:3Cl2+6NaOH 5NaCl+NaClO3+3H2O)
5NaCl+NaClO3+3H2O)
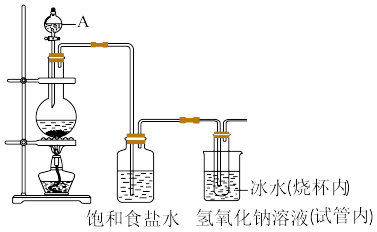
①仪器A的名称是_____ 。
②连接好装置,装药品之前,必须进行的一项操作是_____ 。
③圆底烧瓶内发生反应的化学方程式为_____ ;当生成71g氯气时,被氧化的HCl为_____ mol,试管内发生反应的离子方程式为______ 。
④饱和食盐水的作用是_____ ,冰水的作用是_____ 。
(2)将NaClO溶液倒入烧杯中,持续通入NH3制取N2H4。通常情况下,1体积水能溶解700体积的氨气,则图装置中漏斗的作用是_____ 。

(3)火箭发射时用N2H4作燃料,用N2O4助燃,燃烧生成两种可参与大气循环的物质,写出该反应的化学方程式_____ 。
(1)制备NaClO溶液,装置如图所示。(已知:3Cl2+6NaOH
 5NaCl+NaClO3+3H2O)
5NaCl+NaClO3+3H2O)
①仪器A的名称是
②连接好装置,装药品之前,必须进行的一项操作是
③圆底烧瓶内发生反应的化学方程式为
④饱和食盐水的作用是
(2)将NaClO溶液倒入烧杯中,持续通入NH3制取N2H4。通常情况下,1体积水能溶解700体积的氨气,则图装置中漏斗的作用是

(3)火箭发射时用N2H4作燃料,用N2O4助燃,燃烧生成两种可参与大气循环的物质,写出该反应的化学方程式
您最近一年使用:0次
解题方法
5 . 由于“新冠”病毒的输入,“84”消毒液已成为必需品。“84”消毒液一般是用氯气和氢氧化钠制备。某同学设计了如图所示的实验装置,按要求回答下列问题:

(1)装置A中反应的离子方程式为_______ 。
(2)装置B中装入的药品为_______ 。
(3)装置C、D中的实验现象有何不同:_______ ;A中挥发出的HCl对C、D中的实验现象是否有影响,请判断并说明理由:_______ 。
(4)E中反应的离子方程式为_______ 。
(5)“84”清毒液在空气中久置后,NaClO会转化为HClO,HClO分解失效,HClO分解的化学方程式为_______ ;所以买回来的“84”消毒液应_______ 保存。

(1)装置A中反应的离子方程式为
(2)装置B中装入的药品为
(3)装置C、D中的实验现象有何不同:
(4)E中反应的离子方程式为
(5)“84”清毒液在空气中久置后,NaClO会转化为HClO,HClO分解失效,HClO分解的化学方程式为
您最近一年使用:0次
6 . 实验室制备并收集一定量 时,下图所示方法肯定不能用的是
时,下图所示方法肯定不能用的是
 时,下图所示方法肯定不能用的是
时,下图所示方法肯定不能用的是A. | B. | C. | D. |
您最近一年使用:0次
7 . 无水AlCl3可用作有机合成的催化剂,食品膨松剂等。已知AlCl3、FeCl3分别在183℃、315℃时升华,无水AlCl3遇潮湿空气即产生大量白雾。工业上由铝土矿(主要成分是Al2O3和Fe2O3)和石油焦(主要成分是碳单质)制备无水AlCl3的流程如下:

(1)氯化炉中Al2O3、Cl2和C在高温下发生反应的化学方程式为_______ ;炉气中含有大量CO和少量Cl2,可用Na2SO3溶液除去Cl2,其离子方程式为_______ 。
(2)精制无水AlCl3的合格品中,AlCl3的质量分数不得低于96%。现称取16.25g精制后的无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,其残留固体质量为0.16g。该样品中AlCl3的质量分数为_______ 。
(3)实验室可用下列装置制备无水AlCl3,装置B、C中应盛放的试剂名称分别为_______ 、_______ ,F中所盛放试剂的作用是_______ 。


(1)氯化炉中Al2O3、Cl2和C在高温下发生反应的化学方程式为
(2)精制无水AlCl3的合格品中,AlCl3的质量分数不得低于96%。现称取16.25g精制后的无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,其残留固体质量为0.16g。该样品中AlCl3的质量分数为
(3)实验室可用下列装置制备无水AlCl3,装置B、C中应盛放的试剂名称分别为

您最近一年使用:0次
解题方法
8 . 实验室要制取一瓶纯净干燥的氯气。现有如图所示仪器和药品可供使用:

(1)实验室制取氯气的原理:
其中HCl所表现的性质是
(2)接上述仪器的正确顺序是 。
| A.ABCEFGHD | B.ABCFEGHD | C.AFEBCGHD | D.AFEBCHGD |
A.除去氯气中的水蒸气 B.除去氯气中的氯化氢
C.尾气吸收 D.收集氯气
您最近一年使用:0次
2022-12-07更新
|
330次组卷
|
2卷引用:黑龙江省海林林业局第一中学2021-2022学年高一上学期第二次月考化学试题
名校
解题方法
9 . 化学工业为新冠疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。实验室中利用如图装置(部分装置省略)制备制备KClO3和NaClO,探究其氧化还原性质。
回答下列问题:
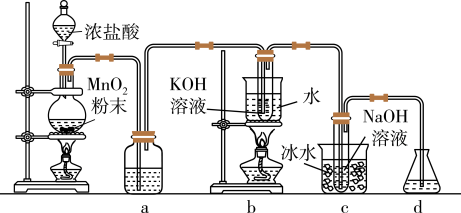
(1)加浓盐酸的仪器名称是___________ ,b中化学反应的离子方程式是 ___________ 。
(2)c中采用冰水浴冷却的目的是___________ 。
(3)反应结束后取出c中试管,取其中少量溶液加入稀H2SO4产生黄绿色气体,原因是___________ (用离子方程式表示)。
(4)氯的化合物ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1.6molClO2消耗NaClO2的物质的量为___________ mol;产生“气泡”的化学方程式为 ___________ 。
回答下列问题:

(1)加浓盐酸的仪器名称是
(2)c中采用冰水浴冷却的目的是
(3)反应结束后取出c中试管,取其中少量溶液加入稀H2SO4产生黄绿色气体,原因是
(4)氯的化合物ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1.6molClO2消耗NaClO2的物质的量为
您最近一年使用:0次
名校
解题方法
10 . 工业上,向500~600℃的铁屑中通入氯气生产无水氯化铁。资料显示:氯化铁极易潮解。
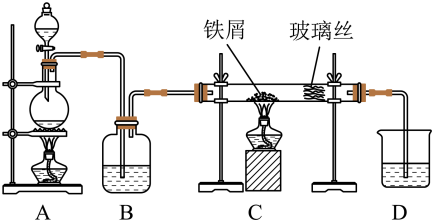
回答下列问题:
(1)A中反应的离子方程式为___________ ,装置B中加入的试剂是 ___________ 。
(2)某同学认为实验装置存在不足,提出用装有足量碱石灰的干燥管替换装置D,装有足量碱石灰的干燥管的作用是___________ ,___________ 。

回答下列问题:
(1)A中反应的离子方程式为
(2)某同学认为实验装置存在不足,提出用装有足量碱石灰的干燥管替换装置D,装有足量碱石灰的干燥管的作用是
您最近一年使用:0次



