名校
1 . 回答下列问题
(1)过氧化钠与二氧化碳反应的化学方程式_____________ ,并用单线桥标出电子转移的方向和数目__________________ 。
(2)漂白粉的有效成分是______ (填化学式),制取漂白粉的化学方程式__________________ 。
(3)漂白粉长时间暴露在空气中就会失去效用,失效原因是(写出2个化学方程式)__________________ ;__________________ 。
(4)实验室用 制氯气的离子方程式
制氯气的离子方程式_______________ 。
(5)将钠投入到 溶液中,写出化学方程式
溶液中,写出化学方程式______________ 。
(6)除去碳酸钠中混有的碳酸氢钠应加入______ (填化学式)溶液,涉及到的反应的离子方程式为__________________ 。
(7)厨房里常用小苏打做糕点的发泡剂,写出其受热分解的化学方程式_________________ 。
(1)过氧化钠与二氧化碳反应的化学方程式
(2)漂白粉的有效成分是
(3)漂白粉长时间暴露在空气中就会失去效用,失效原因是(写出2个化学方程式)
(4)实验室用
 制氯气的离子方程式
制氯气的离子方程式(5)将钠投入到
 溶液中,写出化学方程式
溶液中,写出化学方程式(6)除去碳酸钠中混有的碳酸氢钠应加入
(7)厨房里常用小苏打做糕点的发泡剂,写出其受热分解的化学方程式
您最近一年使用:0次
名校
2 . 某同学用 与浓盐酸反应制备纯净的
与浓盐酸反应制备纯净的 的装置如图所示。回答下列问题:
的装置如图所示。回答下列问题:
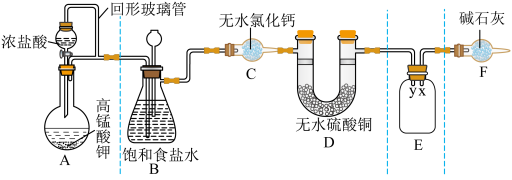
已知: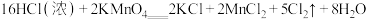
(1)装置A中盛放浓盐酸的仪器名称是
(2)E装置中导管(填“x”或“y”)
(3)装置F的作用有两个:一是
请写出氯气与碱石灰反应的化学方程式
(4)
 、HClO和
、HClO和 三种微粒的物质的量分数随pH(即
三种微粒的物质的量分数随pH(即 )变化的关系如图所示。
)变化的关系如图所示。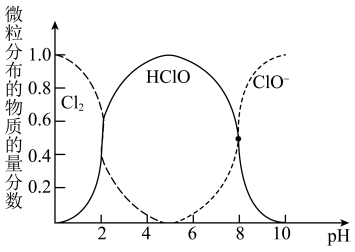
回答问题:①使用84消毒液时为增强消毒效果常调节4<pH<6,原因是
②通常购买的84消毒液pH在12左右,为增强消毒效果可向其中滴加
A.可口可乐 B.稀 C.食醋 D.浓盐酸
C.食醋 D.浓盐酸
(5)实验室将
 通入质量分数40%的NaOH溶液中来制备84消毒液。当NaOH消耗一半时转移电子数为
通入质量分数40%的NaOH溶液中来制备84消毒液。当NaOH消耗一半时转移电子数为 ,计算此时所得溶液中NaClO的质量分数为
,计算此时所得溶液中NaClO的质量分数为
您最近一年使用:0次
名校
3 . 某同学利用Cl2氧化K2MnO4制备KMnO4的装置如图所示(夹持装置略):
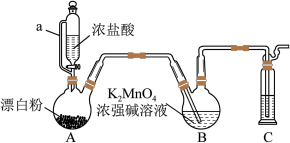
已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3MnO +2H2O═2MnO
+2H2O═2MnO +MnO2↓+4OH-
+MnO2↓+4OH-
回答下列问题:
(1)装置A中a的作用是_________ 装置C中的试剂为_________ ;装置A中制备Cl2的化学方程式为_________ 。
(2)上述装置存在一处缺陷,会导致KMnO4产率降低,改进的方法是_________ 。
(3)高锰酸钾还可以用电解法制备:
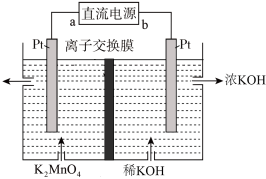
①电解时阳极的电极反应式是_________ 。
②该装置中的离子交换膜是_________ 离子交换膜(填“阴”或“阳”)。
(4)某化学学习小组测定某草酸溶液的浓度,并用所测草酸溶液测定某样品中高锰酸钾的纯度(已知:杂质不参与反应;KMnO4的摩尔质量为158g/mol),进行了如下实验:
步骤i.配制0.1000mol/L的标准氢氧化钠溶液;
步骤ii.取草酸溶液10.00mL,用0.1000mol/L的标准氢氧化钠溶液滴定,结果用去氢氧化钠溶液20.00mL;
步骤iii.取1.0g样品溶于水,滴入几滴稀硫酸酸化,用测定的草酸溶液进行滴定,达到滴定终点消耗草酸溶液50.00mL。
①步骤ii中应选择_________ 作指示剂。
②样品中高锰酸钾的纯度为_________ 。
③本实验中,若第一次滴定时盛装氢氧化钠溶液的滴定管未润洗,会测得高锰酸钾纯度_________ (填“偏大”、“偏小”或“无影响”)。

已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3MnO
 +2H2O═2MnO
+2H2O═2MnO +MnO2↓+4OH-
+MnO2↓+4OH-回答下列问题:
(1)装置A中a的作用是
(2)上述装置存在一处缺陷,会导致KMnO4产率降低,改进的方法是
(3)高锰酸钾还可以用电解法制备:

①电解时阳极的电极反应式是
②该装置中的离子交换膜是
(4)某化学学习小组测定某草酸溶液的浓度,并用所测草酸溶液测定某样品中高锰酸钾的纯度(已知:杂质不参与反应;KMnO4的摩尔质量为158g/mol),进行了如下实验:
步骤i.配制0.1000mol/L的标准氢氧化钠溶液;
步骤ii.取草酸溶液10.00mL,用0.1000mol/L的标准氢氧化钠溶液滴定,结果用去氢氧化钠溶液20.00mL;
步骤iii.取1.0g样品溶于水,滴入几滴稀硫酸酸化,用测定的草酸溶液进行滴定,达到滴定终点消耗草酸溶液50.00mL。
①步骤ii中应选择
②样品中高锰酸钾的纯度为
③本实验中,若第一次滴定时盛装氢氧化钠溶液的滴定管未润洗,会测得高锰酸钾纯度
您最近一年使用:0次
4 . 下图中A~H均为中学化学中常见的物质,A、B、H是气体,A是有刺激性气味的气体,B、H是无色无味气体,它们之间有如下转化关系。(反应中生成的水已略去)
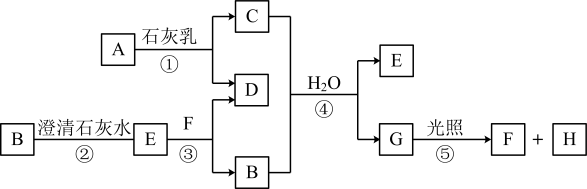
请回答以下问题:
(1)C是___________ ,E是___________ ,G是___________ 。(填化学式)。
(2)C物质在日常生活中可作___________ 剂。
(3)写出反应①的化学方程式:___________ 。写出反应②的化学方程式:___________ 。
(4)写出实验室制取A气体的化学反应方程式:___________

请回答以下问题:
(1)C是
(2)C物质在日常生活中可作
(3)写出反应①的化学方程式:
(4)写出实验室制取A气体的化学反应方程式:
您最近一年使用:0次
解题方法
5 . Ⅰ.某兴趣小组利用所给仪器在实验室制备纯净干燥的氯气并探究其性质。请回答下列问题:
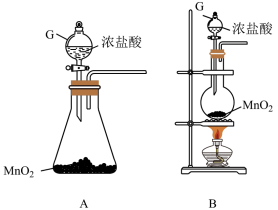

(1)装置G的名称为___________ ;
(2)装置F的作用为___________ ;
(3)从上图中选择合适装置制备并收集纯净干燥的氯气(仪器不重复使用),仪器连接顺序为___________ (用仪器下方字母表示,例如A→B→C)
(4)制备氯气的反应中体现了浓盐酸的___________ 性和___________ 性。
Ⅱ.甲同学设计如图所示装置研究氯气能否与水发生反应,气体a是含有少量空气和水蒸气的氯气。请回答下列问题:

(5)浓硫酸的作用是___________ ;
(6)证明氯气和水反应的实验现象为___________
(7)漂白粉溶于水后,遇到空气中的CO2,即产生漂白、杀菌作用,反应的化学方程式是___________ 。


(1)装置G的名称为
(2)装置F的作用为
(3)从上图中选择合适装置制备并收集纯净干燥的氯气(仪器不重复使用),仪器连接顺序为
(4)制备氯气的反应中体现了浓盐酸的
Ⅱ.甲同学设计如图所示装置研究氯气能否与水发生反应,气体a是含有少量空气和水蒸气的氯气。请回答下列问题:

(5)浓硫酸的作用是
(6)证明氯气和水反应的实验现象为
(7)漂白粉溶于水后,遇到空气中的CO2,即产生漂白、杀菌作用,反应的化学方程式是
您最近一年使用:0次
解题方法
6 . 为验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:

(1)装置B中盛放的试剂是_______ (填选项),实验现象为_______ 。
a.Na2S溶液 b.Na2SO3溶液 c.Na2SO4溶液
(2)装置C中盛放烧碱稀溶液,目的是_______ 。
(3)能证明氯元素比硫元素非金属性强的依据为_______ 。 (填序号)
①氯原子比硫原子更容易获得电子形成离子;
②次氯酸的氧化性比稀硫酸强;
③S2-比Cl-还原性强;
④HCl比H2S稳定。
(4)若B瓶中盛放KI溶液和CCl4试剂,实验后,振荡、静置,会出现的实验现象_______ ,写出反应的离子方程式_______ 。
(5)写出装置A反应的离子方程式_______ 。

(1)装置B中盛放的试剂是
a.Na2S溶液 b.Na2SO3溶液 c.Na2SO4溶液
(2)装置C中盛放烧碱稀溶液,目的是
(3)能证明氯元素比硫元素非金属性强的依据为
①氯原子比硫原子更容易获得电子形成离子;
②次氯酸的氧化性比稀硫酸强;
③S2-比Cl-还原性强;
④HCl比H2S稳定。
(4)若B瓶中盛放KI溶液和CCl4试剂,实验后,振荡、静置,会出现的实验现象
(5)写出装置A反应的离子方程式
您最近一年使用:0次
解题方法
7 . 新冠疫情的发生,消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一,而氯气是制取消毒液的重要原料之一。
请回答下列问题:
(1)请写出舍勒发现氯气的化学反应方程式___________________________________ ,若收集到标准状况下3.36LCl2,则被氧化的HCl的物质的量为_____________ mol。
(2)84消毒液(主要成分是NaClO)是常用的消毒剂,工业上将氯气通入烧碱溶液中制取84消毒液,写出此反应的离子方程式_______________________________________ ,若要制取1.5L 2 mol/L的84消毒液,则需要标准状况下___________ L 氯气。
(3)新冠疫情下,人们对杀菌消毒特别重视,曾有报道某居民将84消毒液与洁厕灵(主要成分是浓盐酸)混合使用而中毒,请解释原因__________________________________ (用化学方程式表示), 该反应中氧化剂是______________ 。
请回答下列问题:
(1)请写出舍勒发现氯气的化学反应方程式
(2)84消毒液(主要成分是NaClO)是常用的消毒剂,工业上将氯气通入烧碱溶液中制取84消毒液,写出此反应的离子方程式
(3)新冠疫情下,人们对杀菌消毒特别重视,曾有报道某居民将84消毒液与洁厕灵(主要成分是浓盐酸)混合使用而中毒,请解释原因
您最近一年使用:0次
解题方法
8 . 某化学兴趣小组在加热条件下利用二氧化锰与浓盐酸反应来制取并收集氯气。
(1)写出该反应的化学方程式_______ ,可选择的气体发生装置是_______ (填序号)。

(2)若有同学不慎将MnO2和KCl粉末混合,分离该混合物的方法和步骤如下,请补充完整:
①先在盛有混合粉末的烧杯中加入适量水溶解;
②将所得混合液进行过滤,该操作所用的玻璃仪器有_______ ;
③洗涤、干燥沉淀得到MnO2;将②所得液体蒸发结晶得到KCl固体。
(3)将制得的氯气与一定体积的甲烷混合,在光照条件下发生_______ (填反应类型),生成物质的量最多的物质是_______ (填化学式)。
(4)若要制取干燥纯净的氯气,应先将气体依次通过装有_______ 和_______ 的洗气瓶。
(1)写出该反应的化学方程式

(2)若有同学不慎将MnO2和KCl粉末混合,分离该混合物的方法和步骤如下,请补充完整:
①先在盛有混合粉末的烧杯中加入适量水溶解;
②将所得混合液进行过滤,该操作所用的玻璃仪器有
③洗涤、干燥沉淀得到MnO2;将②所得液体蒸发结晶得到KCl固体。
(3)将制得的氯气与一定体积的甲烷混合,在光照条件下发生
(4)若要制取干燥纯净的氯气,应先将气体依次通过装有
您最近一年使用:0次
9 . 图中为实验室制取氯气及性质验证的装置图,参考装置图回答下列问题:

(1)请指出仪器的名称:a:_______ b:_______ ,
(2)写出装置A中反应的化学方程式:_______ 。
(3)在装置D中可观察到的现象是_______ ,装置E中可观察到的现象是_______ 。
(4)装置B的作用为_______ ,装置C的作用为_______ ,小明同学认为该套装置应该添加装置F,其作用是_______ 。

(1)请指出仪器的名称:a:
(2)写出装置A中反应的化学方程式:
(3)在装置D中可观察到的现象是
(4)装置B的作用为
您最近一年使用:0次
解题方法
10 . 实验室制取氯气通常采用MnO2与浓盐酸反应制取,下列说法中错误的是
| A.该反应是一个氧化还原反应,其中二氧化锰是氧化剂 |
| B.瑞典化学家舍勒最先发现 |
C.该反应的离子方程式为MnO2+4H++4Cl- MnCl2+2H2O+Cl2↑ MnCl2+2H2O+Cl2↑ |
| D.HCl表现还原性和酸性 |
您最近一年使用:0次



