1 . 拟用如图装置设计实验来探究纯净、干燥的氯气与氨气的反应。___________ 。
(2)如图中的装置连接顺序为A→___________ (用大写字母表示)。若按照正确顺序连接实验装置后,整套实验装置存在的主要缺点___________ 。
(3)写出F装置中的反应的一种工业用途:___________ 。
(4)在工业上利用反应N2+3H2 2NH3制备氨气。现在实验室模拟该反应探究影响反应速率的因素,在四个相同的容器中,在不同的温度下(其他条件相同)进行合成氨的反应,根据下列在相同时间内测得的结果判断,该反应所处的温度最高的是
2NH3制备氨气。现在实验室模拟该反应探究影响反应速率的因素,在四个相同的容器中,在不同的温度下(其他条件相同)进行合成氨的反应,根据下列在相同时间内测得的结果判断,该反应所处的温度最高的是___________ (填字母)。
A.v(NH3)=0.1mol/(L·min) B.v(H2)=0.6mol/(L·min) C.v(N2)=0.3mol/(L·min)

(2)如图中的装置连接顺序为A→
(3)写出F装置中的反应的一种工业用途:
(4)在工业上利用反应N2+3H2
 2NH3制备氨气。现在实验室模拟该反应探究影响反应速率的因素,在四个相同的容器中,在不同的温度下(其他条件相同)进行合成氨的反应,根据下列在相同时间内测得的结果判断,该反应所处的温度最高的是
2NH3制备氨气。现在实验室模拟该反应探究影响反应速率的因素,在四个相同的容器中,在不同的温度下(其他条件相同)进行合成氨的反应,根据下列在相同时间内测得的结果判断,该反应所处的温度最高的是A.v(NH3)=0.1mol/(L·min) B.v(H2)=0.6mol/(L·min) C.v(N2)=0.3mol/(L·min)
您最近一年使用:0次
名校
2 . 氯化铁(FeCl3)是一种棕色结晶,易升华,有强烈的吸水性。实验室制备无水氯化铁并探究氯化铁性质的相关实验如下。
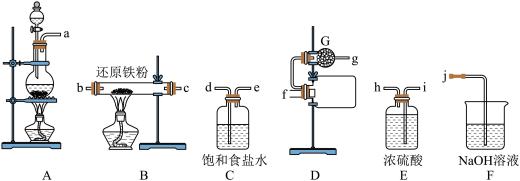
(1)装置A中发生反应的离子方程式是_______ 。
(2)实验装置接口的连接顺序是a→_______ →j, G中盛装的物质是_______ 。
(3)当观察到出现_______ 现象时,再点燃B处的酒精灯。
(4)若没有使用C装置,则可能导致的不良后果是_______ 。
Ⅱ.探究D中固态产物的相关性质
(5)取适量D中收集到的固态物质进行相关实验,完成下列实验,回答问题。

(1)装置A中发生反应的离子方程式是
(2)实验装置接口的连接顺序是a→
(3)当观察到出现
(4)若没有使用C装置,则可能导致的不良后果是
Ⅱ.探究D中固态产物的相关性质
(5)取适量D中收集到的固态物质进行相关实验,完成下列实验,回答问题。
| 序号 | 实验操作 | 实验现象 | 问题或结论 |
① | 取少量固态物质置于烧杯中,加入适量蒸馏水,搅拌,溶解 | 溶液浑浊,滴加某试剂,振荡,得到棕黄色澄清溶液 | 该试剂是 |
② | 取少量①中的澄清溶液于试管 中,滴加一滴 | 无明显现象 | 证明原固体中不含 FeCl2 |
③ | 将①中的澄清溶液滴入刚做完 银镜反应实验的试管中,振荡 | 管壁上的银镜溶解,溶液浑 浊 | 相关离子方程式是 |
您最近一年使用:0次
名校
3 . 工业利用反应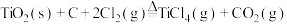 ,在无水无氧条件下制取
,在无水无氧条件下制取 ,实验装置如图所示。(
,实验装置如图所示。( 的熔点为25℃,沸点为136℃,
的熔点为25℃,沸点为136℃, 遇水发生水解生成
遇水发生水解生成 )
)

回答下列问题:
(1)该实验设计中存在一个明显的错误:_____ ,会导致无法制得 ;装置F中的试剂为
;装置F中的试剂为_____ 。
(2)装置A中发生反应的离子方程式为_____ 。
(3)当观察到装置E中_____ (现象)时才开始点燃D处酒精灯,装置E中冰水的作用是_____ 。
(4)若上述装置中缺少装置C,则D处硬质试管中发生的主要副反应化学方程式为:_____ 。
(5)利用如图所示的装置测定 的纯度,取
的纯度,取 产品,向安全漏斗中加入适当的蒸馏水,待
产品,向安全漏斗中加入适当的蒸馏水,待 充分反应后,将烧瓶和漏斗中的液体并转移至锥形瓶中,加入
充分反应后,将烧瓶和漏斗中的液体并转移至锥形瓶中,加入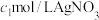 溶液
溶液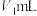 ,使氯离子完全沉淀,以高铁铵钒为指示剂,用
,使氯离子完全沉淀,以高铁铵钒为指示剂,用 溶液滴定过量的
溶液滴定过量的 生成
生成 沉淀,滴定终点时,消耗滴定液
沉淀,滴定终点时,消耗滴定液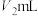 。
。

①安全漏斗在实验中的作用除加水外,还有_____ 。
②根据上述数据计算该样品的纯度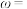
_____ (用含m、 、
、 、
、 、
、 的代数式表示)。
的代数式表示)。
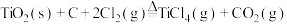 ,在无水无氧条件下制取
,在无水无氧条件下制取 ,实验装置如图所示。(
,实验装置如图所示。( 的熔点为25℃,沸点为136℃,
的熔点为25℃,沸点为136℃, 遇水发生水解生成
遇水发生水解生成 )
)
回答下列问题:
(1)该实验设计中存在一个明显的错误:
 ;装置F中的试剂为
;装置F中的试剂为(2)装置A中发生反应的离子方程式为
(3)当观察到装置E中
(4)若上述装置中缺少装置C,则D处硬质试管中发生的主要副反应化学方程式为:
(5)利用如图所示的装置测定
 的纯度,取
的纯度,取 产品,向安全漏斗中加入适当的蒸馏水,待
产品,向安全漏斗中加入适当的蒸馏水,待 充分反应后,将烧瓶和漏斗中的液体并转移至锥形瓶中,加入
充分反应后,将烧瓶和漏斗中的液体并转移至锥形瓶中,加入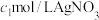 溶液
溶液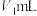 ,使氯离子完全沉淀,以高铁铵钒为指示剂,用
,使氯离子完全沉淀,以高铁铵钒为指示剂,用 溶液滴定过量的
溶液滴定过量的 生成
生成 沉淀,滴定终点时,消耗滴定液
沉淀,滴定终点时,消耗滴定液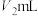 。
。
①安全漏斗在实验中的作用除加水外,还有
②根据上述数据计算该样品的纯度
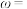
 、
、 、
、 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
4 . 下列化学教材的实验操作中,主要不是从安全因素考虑的是
| A.实验室制备氯气,需要在通风橱中进行 |
| B.海带提碘实验的萃取操作中,振荡后需要放气 |
| C.制取氢氧化铁胶体时,滴加饱和氯化铁溶液5-6滴后继续加热至出现红褐色即停止加热 |
| D.浓硫酸与铜反应的实验后,将冷却后的反应液缓慢倒入装有水的另一支试管中以观察溶液颜色 |
您最近一年使用:0次
5 . 无水四氯化锡(SnCl4)常用作有机合成的氯化催化剂。实验室可用熔融的锡(熔点为232℃)与Cl2反应制备SnCl4,装置如图所示。

已知:①SnCl4在潮湿空气中极易水解生成SnO2·xH2O
②各物质熔沸点:
请回答下列问题:
(1)仪器a的名称为_______ ,重铬酸钾(K2Cr2O7)与浓盐酸反应时,还原产物是CrCl3,装置A中发生反应的离子方程式为_______ 。
(2)F装置中试剂b为_______ ,其作用是_______ 。
(3)锡屑中含铜杂质导致D中产生CuCl2,但不影响E中产品的纯度,原因是_______ 。
(4)E所得产品SnCl4中常溶有少量SnCl2杂质,可用蒸馏法提纯(装置如下图)
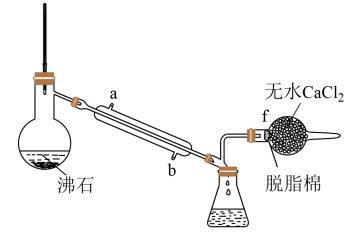
冷凝管的进水口是_______ (填“a”或“b”),当温度计显示温度在_______ 时锥形瓶中收集的馏分为SnCl4。
A.114℃ B.114℃-246℃之间 C.114℃-652℃之间

已知:①SnCl4在潮湿空气中极易水解生成SnO2·xH2O
②各物质熔沸点:
| 物质 | 熔点/℃ | 沸点/℃ |
| SnCl2 | 246 | 652 |
| SnCl4 | -33 | 114 |
| CuCl2 | 620 | 993 |
(1)仪器a的名称为
(2)F装置中试剂b为
(3)锡屑中含铜杂质导致D中产生CuCl2,但不影响E中产品的纯度,原因是
(4)E所得产品SnCl4中常溶有少量SnCl2杂质,可用蒸馏法提纯(装置如下图)

冷凝管的进水口是
A.114℃ B.114℃-246℃之间 C.114℃-652℃之间
您最近一年使用:0次
6 .  和
和 用途广泛,某同学为探究
用途广泛,某同学为探究 、
、 的性质,设计如下装置进行实验。
的性质,设计如下装置进行实验。
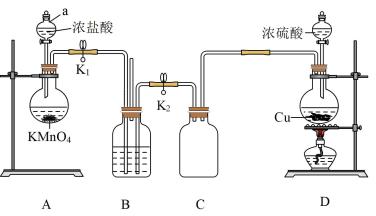
(1)图中仪器a的名称_______ ,E中发生反应的化学方程式为_______ 。
(2)若B中加入淀粉碘化钾溶液,关闭 ,打开
,打开 ,使A产生的气体进入B,则B中实验现象为
,使A产生的气体进入B,则B中实验现象为_______ 。
(3)若要实现硫元素由 价转化为0价,需关闭
价转化为0价,需关闭 ,打开
,打开 ,在B中加入
,在B中加入_______ 溶液,此过程体现了 的
的_______ 性。
(4)若B中是水,打开 、
、 ,使A、E产生的气体同时进入B中,一段时间后关闭活塞。待反应完全后,小组同学又继续如下实验。
,使A、E产生的气体同时进入B中,一段时间后关闭活塞。待反应完全后,小组同学又继续如下实验。
①甲同学取适量B中溶液于试管中,向其中滴加少量 溶液,有白色沉淀生成。甲同学由此认为
溶液,有白色沉淀生成。甲同学由此认为 和
和 发生了反应,理由是该反应中生成了
发生了反应,理由是该反应中生成了_______ (填离子符号)。
②乙同学认为甲同学的结论不合理,认为A中生成的 中混有
中混有_______ 杂质,应该把装置改进,然后再按甲同学的方法即可得到正确结论。乙同学应如何改进上述装置_______ 。
③丙同学则认为甲、乙两位同学的结论均不合理。丙同学取适量B中溶液于试管中,向其中滴加少量溶液X,有白色沉淀生成,则可得出结论,即 与
与 同时通入水中,可以发生反应。溶液X是
同时通入水中,可以发生反应。溶液X是_______ (填选项序号)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.品红溶液
溶液 D.品红溶液
 与
与 同时通入水中反应的化学方程式是
同时通入水中反应的化学方程式是_______ 。
(5)该同学设计的装置有一处明显的缺陷是_______ 。
 和
和 用途广泛,某同学为探究
用途广泛,某同学为探究 、
、 的性质,设计如下装置进行实验。
的性质,设计如下装置进行实验。
(1)图中仪器a的名称
(2)若B中加入淀粉碘化钾溶液,关闭
 ,打开
,打开 ,使A产生的气体进入B,则B中实验现象为
,使A产生的气体进入B,则B中实验现象为(3)若要实现硫元素由
 价转化为0价,需关闭
价转化为0价,需关闭 ,打开
,打开 ,在B中加入
,在B中加入 的
的(4)若B中是水,打开
 、
、 ,使A、E产生的气体同时进入B中,一段时间后关闭活塞。待反应完全后,小组同学又继续如下实验。
,使A、E产生的气体同时进入B中,一段时间后关闭活塞。待反应完全后,小组同学又继续如下实验。①甲同学取适量B中溶液于试管中,向其中滴加少量
 溶液,有白色沉淀生成。甲同学由此认为
溶液,有白色沉淀生成。甲同学由此认为 和
和 发生了反应,理由是该反应中生成了
发生了反应,理由是该反应中生成了②乙同学认为甲同学的结论不合理,认为A中生成的
 中混有
中混有③丙同学则认为甲、乙两位同学的结论均不合理。丙同学取适量B中溶液于试管中,向其中滴加少量溶液X,有白色沉淀生成,则可得出结论,即
 与
与 同时通入水中,可以发生反应。溶液X是
同时通入水中,可以发生反应。溶液X是A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.品红溶液
溶液 D.品红溶液 与
与 同时通入水中反应的化学方程式是
同时通入水中反应的化学方程式是(5)该同学设计的装置有一处明显的缺陷是
您最近一年使用:0次
名校
解题方法
7 . 某研究性学习小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略)。已知:Cl2易溶于CCl4而HCl不溶于CCl4

按要求回答问题:
(1)装置A中仪器H的名称是_______ ,写出装置A制取Cl2的化学方程式_______ 。
(2)装置B中的试剂是_______ ,现象是_______ 。装置D和E中出现的不同现象说明氯气没有漂白性,氯水有漂白性。
(3)装置F的作用是_______ 。
(4)有一种“地康法”制取氯气的反应原理如图所示:
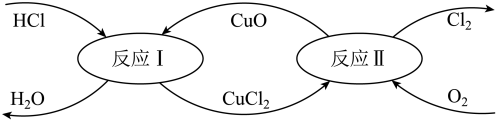
①反应I属于_______ 反应。(填四种基本反应类型之一)
②在450℃条件下,反应II的化学方程式为_______ 。
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:_______ 。

按要求回答问题:
(1)装置A中仪器H的名称是
(2)装置B中的试剂是
(3)装置F的作用是
(4)有一种“地康法”制取氯气的反应原理如图所示:

①反应I属于
②在450℃条件下,反应II的化学方程式为
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:
您最近一年使用:0次
8 . 下列实验装置设计正确且能达到目的的是
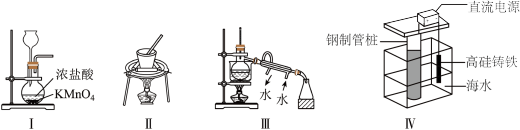

| A.实验Ⅰ:制取氯气 |
| B.实验Ⅱ:瓷坩埚加热熔融NaOH固体 |
| C.实验Ⅲ:分离乙酸乙酯和乙醚的混合物 |
| D.实验Ⅳ:防止钢制管桩被腐蚀 |
您最近一年使用:0次
解题方法
9 . 某研究性学习小组利用以下装置探究氯气和氨气之间的反应情况。其中A、F分别为氨气和氯气的制取发生装置,C为纯净干燥的氯气与干燥的氨气发生反应的装置。请回答下列问题:
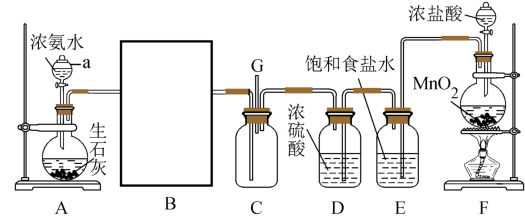
(1)仪器a的名称是_______ 。
(2)检查装置A气密性的方法是:塞紧橡皮塞,关闭分液漏斗的活塞,将导管末端伸入盛水的烧杯中,微热烧瓶,导管口有__________________ ,说明装置A气密性良好。
(3)用装置A制取氨气的化学方程式为_______ 。
(4)请为B处框内选择合适的装置及相应的试剂_______(选填字母)。
(5)装置E的作用是___________ ,装置D和E的位置_______ (选填“能”或“不能”)调换。
(6)实验中可观察到装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,请写出此反应的化学方程式:_______ 。若有1mol 被氧化,则转移的电子数目为
被氧化,则转移的电子数目为_______ 。

(1)仪器a的名称是
(2)检查装置A气密性的方法是:塞紧橡皮塞,关闭分液漏斗的活塞,将导管末端伸入盛水的烧杯中,微热烧瓶,导管口有
(3)用装置A制取氨气的化学方程式为
(4)请为B处框内选择合适的装置及相应的试剂_______(选填字母)。
| A.球形干燥管装碱石灰 |
| B.洗气瓶装浓硫酸 |
| C.球形干燥管装氧化钙 |
D.球形干燥管装 |
(6)实验中可观察到装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,请写出此反应的化学方程式:
 被氧化,则转移的电子数目为
被氧化,则转移的电子数目为
您最近一年使用:0次
10 . 请分析下列氧化还原反应,该反应为实验室用MnO2和浓盐酸(注意不是稀盐酸)反应制备Cl2:MnO2 + 4 HCl(浓)  MnCl2 + Cl2↑ + 2H2O
MnCl2 + Cl2↑ + 2H2O
(1)用双线桥法表示出电子转移方向和数量____________________
(2)该反应的氧化剂是___________ ,被氧化的元素是___________ 元素。
(3)HCl在该反应中体现的化学性质有___________ 、___________
(4)实验测定,当MnO2足量时,无论如何控制条件,用含146g HCl的浓盐酸参与反应,得到的氯气始终小于71g,产生该现象的原因可能是___________
 MnCl2 + Cl2↑ + 2H2O
MnCl2 + Cl2↑ + 2H2O(1)用双线桥法表示出电子转移方向和数量
(2)该反应的氧化剂是
(3)HCl在该反应中体现的化学性质有
(4)实验测定,当MnO2足量时,无论如何控制条件,用含146g HCl的浓盐酸参与反应,得到的氯气始终小于71g,产生该现象的原因可能是
您最近一年使用:0次



