名校
1 . 某化学兴趣小组同学利用以下装置制取Cl2并探究红色纸条褪色的原因(Ⅳ中夹持装置已略去,a为干燥的红色纸条,b为湿润的红色纸条)。

(1)装置Ⅰ可用于制取Cl2,写出该反应的化学方程式_________________ 。
(2)装置Ⅱ的作用是___________ 。
(3)装置Ⅳ中a处红色纸条无明显变化,b处红色纸条褪色,同学猜测使b处红色纸条褪色的物质是_____________ 。
(4)该小组同学查阅资料,发现:
①NaClO溶液具有氧化性,能使红色纸条褪色
②溶液的pH会影响NaClO溶液的漂白效果
该小组同学利用市售“84”消毒液(主要成分:NaClO)探究不同pH下红色纸条褪色的情况,实验如下:
已知:溶液中HClO、ClO-物质的量分数(a)随溶液pH变化的关系如下图所示:

①由实验现象可知:溶液的pH在4~10范围内,pH越大,红纸褪色____________ 。
②结合图像分析pH=7和pH=4的溶液,现象差异的原因____________________ 。
③结合实验现象和图像可知,氧化性:HClO____ NaClO(填“>”或“<”)。“84”消毒液主要成分是NaClO而不是HClO,因为HClO不稳定,不易保存。
写出HClO见光分解的化学方程式____________________ 。
综上所述,HClO能使红色纸条褪色,“84”消毒液在酸性环境下漂白效果更佳。

(1)装置Ⅰ可用于制取Cl2,写出该反应的化学方程式
(2)装置Ⅱ的作用是
(3)装置Ⅳ中a处红色纸条无明显变化,b处红色纸条褪色,同学猜测使b处红色纸条褪色的物质是
(4)该小组同学查阅资料,发现:
①NaClO溶液具有氧化性,能使红色纸条褪色
②溶液的pH会影响NaClO溶液的漂白效果
该小组同学利用市售“84”消毒液(主要成分:NaClO)探究不同pH下红色纸条褪色的情况,实验如下:
| 实验方案 | 实验现象 | |
| 1.将市售“84”消毒液稀释至溶液的pH=12。 2.取20mL pH=12的稀释液各3份,分别用H2SO4溶液将pH调至10、7和4(溶液体积变化忽略不计)。 3.分别放入大小相同的红色纸条。 | pH=10 | 10min后,红色纸条基本不褪色;4h后红色褪去。 |
| pH=7 | 10min后,红色纸条颜色变浅;4h后红色褪去。 | |
| pH=4 | 10min后,红色纸条颜色变得更浅;4h后红色褪去。 | |

①由实验现象可知:溶液的pH在4~10范围内,pH越大,红纸褪色
②结合图像分析pH=7和pH=4的溶液,现象差异的原因
③结合实验现象和图像可知,氧化性:HClO
写出HClO见光分解的化学方程式
综上所述,HClO能使红色纸条褪色,“84”消毒液在酸性环境下漂白效果更佳。
您最近一年使用:0次
2 . 自来水是自然界中的淡水经过絮凝、沉淀、过滤、消毒等工艺处理后得到的。常用二氧化氯(ClO2)给自来水消毒。某研究小组用下图装置制备少量ClO2(夹持装置已略去)。
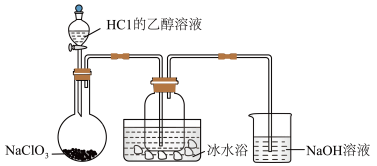
资料:ClO2常温下为易溶于水而不与水反应的气体,水溶液呈深黄绿色,11℃时液化成红棕色液体。以NaClO3和HCl的乙醇溶液为原料制备ClO2的反应为2NaClO3+4HCl =2ClO2↑+Cl2↑+2NaCl+2H2O。
(1)冰水浴的作用是_____________________ 。
(2)NaOH溶液中发生主要反应的离子方程式______________________ 。
(3)ClO2中氯元素的化合价为______ ,ClO2因其具有_______ 用于纸浆漂白、杀菌消毒。
(4)ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO ),需将其转化为Cl-除去,下列试剂中,可将ClO
),需将其转化为Cl-除去,下列试剂中,可将ClO 转化为Cl-的是
转化为Cl-的是_________ (填字母序号)。
a.Fe b.O2 c.KMnO4 d.KI

资料:ClO2常温下为易溶于水而不与水反应的气体,水溶液呈深黄绿色,11℃时液化成红棕色液体。以NaClO3和HCl的乙醇溶液为原料制备ClO2的反应为2NaClO3+4HCl =2ClO2↑+Cl2↑+2NaCl+2H2O。
(1)冰水浴的作用是
(2)NaOH溶液中发生主要反应的离子方程式
(3)ClO2中氯元素的化合价为
(4)ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO
 ),需将其转化为Cl-除去,下列试剂中,可将ClO
),需将其转化为Cl-除去,下列试剂中,可将ClO 转化为Cl-的是
转化为Cl-的是a.Fe b.O2 c.KMnO4 d.KI
您最近一年使用:0次
名校
3 . 漂白液广泛用于杀菌消毒。使用软锰矿(主要成分为 ,含少量CaO、
,含少量CaO、 等)为原料精制
等)为原料精制 ,进而制备含氯消毒液、漂白粉的工艺流程如下:
,进而制备含氯消毒液、漂白粉的工艺流程如下:

(1)步骤②中发生反应的离子方程式 :_______ ;
(2)写出步骤③纯化后制备漂白粉的化学方程式:_______ ;
(3)漂白粉的有效成分是_______ (填化学式),长期露置于空气中会失效,向失效的漂白粉中加稀盐酸,产生的气体是_______ (填字母);
A. B.
B. C.
C. D.HClO
D.HClO
(4)若软锰矿1kg在生产中与足量浓HCl反应后得到224L的 (标准状况),则软锰矿中
(标准状况),则软锰矿中 的质量分数为
的质量分数为_______ 。
 ,含少量CaO、
,含少量CaO、 等)为原料精制
等)为原料精制 ,进而制备含氯消毒液、漂白粉的工艺流程如下:
,进而制备含氯消毒液、漂白粉的工艺流程如下:
(1)步骤②中发生反应的
(2)写出步骤③纯化后制备漂白粉的化学方程式:
(3)漂白粉的有效成分是
A.
 B.
B. C.
C. D.HClO
D.HClO(4)若软锰矿1kg在生产中与足量浓HCl反应后得到224L的
 (标准状况),则软锰矿中
(标准状况),则软锰矿中 的质量分数为
的质量分数为
您最近一年使用:0次
2022-12-29更新
|
248次组卷
|
2卷引用:北京市通州区2021-2022学年高一上学期期末测试化学试题
名校
解题方法
4 . 实验室用下图装置制备并收集干燥纯净 的 。
。
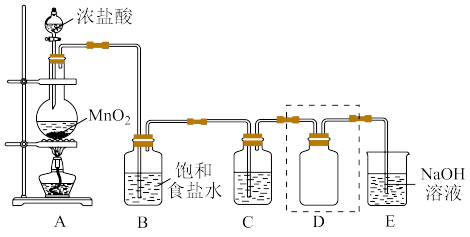
(1)装置A中反应的化学方程式是_______ 。
(2)装置B的作用是_______ 。
(3)装置C中盛放的物质是_______ 。
(4)装置D用于收集 ,请将图中装置D的导气管补充完整。
,请将图中装置D的导气管补充完整。_____
(5)装置E用于吸收尾气,E中反应的离子方程式是_______ 。
 。
。
(1)装置A中反应的化学方程式是
(2)装置B的作用是
(3)装置C中盛放的物质是
(4)装置D用于收集
 ,请将图中装置D的导气管补充完整。
,请将图中装置D的导气管补充完整。(5)装置E用于吸收尾气,E中反应的离子方程式是
您最近一年使用:0次
2022-12-02更新
|
149次组卷
|
7卷引用:北京市第四十三中学2021-2022学年高一上学期12月月考化学试题
名校
5 . 某研究小组制备氯气并对产生氯气的反应原理进行探究。
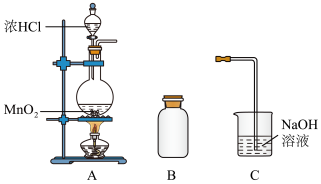
(1)装置A中用MnO2与浓盐酸反应制取Cl2,利用了浓HCl的_______ (填“氧化性”或“还原性”)。
(2)A中产生的气体不纯,含有的杂质有_______ (填化学式)。
(3)B用于排空气法收集Cl2,请完善装置B,并用箭头标明进出气体方向_______ 。
(4)该小组对产生氯气的反应原理,设计实验进行如下探究。
结合查阅资料,可知:
①Ⅰ中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,化学方程式是_______ 。
②Ⅱ中发生了分解反应,反应的化学方程式是_______ 。

(1)装置A中用MnO2与浓盐酸反应制取Cl2,利用了浓HCl的
(2)A中产生的气体不纯,含有的杂质有
(3)B用于排空气法收集Cl2,请完善装置B,并用箭头标明进出气体方向
(4)该小组对产生氯气的反应原理,设计实验进行如下探究。
| 实验 | 操作 | 现象 |
| Ⅰ | 常温下将MnO2和浓盐酸混合 | 溶液呈浅棕色,略有刺激性气味 |
| Ⅱ | 将Ⅰ中混合物过滤,加热滤液 | 生成大量黄绿色气体 |
①Ⅰ中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,化学方程式是
②Ⅱ中发生了分解反应,反应的化学方程式是
您最近一年使用:0次
6 . 回答下列问题:
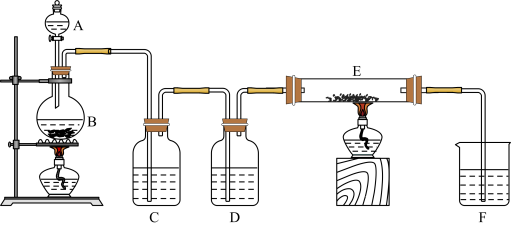
(1)如图是制取氯气并进行有关氯气性质实验的装置,装置中C、D均为洗气瓶,E中有铁粉,右端导管口处放有脱脂棉,F为尾气吸收装置。
试回答:
①B中发生反应的化学方程式为_______ ;反应中氧化剂为_______ (填化学式)。
②为使E装置中进入纯净干燥的氯气,C中盛装试剂是饱和食盐水,作用是_______ ;D装置中的试剂是_______ 。
③E中发生的化学反应方程式为_______ 。
④F是尾气处理装置,反应离子方程式为_______ 。
⑤实验室也可以用KMnO4替代MnO2与浓HCl反应制取Cl2,但反应不需要加热,写出此反应的离子方程式_______ 。(已知 被还原为Mn2+)
被还原为Mn2+)
(2)Cl2是一种重要的化工原料,下图是一些含氯产品。
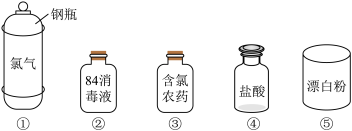
①中钢瓶上应贴的标签为_______ 。
A.腐蚀品 B.有毒品 C.易燃品
②漂白粉可用于游泳池及环境消毒剂,制漂白粉的反应原理为_______ 。
(3)2016年10月20日生活日报讯,一位温州小伙将84消毒液与洁厕灵共用来刷洗厕所时,突然瘫坐在地,无力挪步,呼吸急促。经医生诊断,小伙子为轻度氯气中毒。某大学化工系教授,该教授表示洁厕灵含有盐酸,84消毒液含有NaClO(次氯酸钠),二者不可混用,一旦混合会产生有毒的氯气,如果不慎发生事故,应立即开窗通风,用湿毛巾捂住口鼻向高处转移,事后要多喝水,并及时就医。
①请用离子方程式分析小伙子中毒的原因_______ 。
②发生事故后,要用湿毛巾捂住口鼻向高处转移,事后还要多喝水,用化学方程式表示用湿毛巾捂住口鼻,事后多喝水的原因:_______
(1)如图是制取氯气并进行有关氯气性质实验的装置,装置中C、D均为洗气瓶,E中有铁粉,右端导管口处放有脱脂棉,F为尾气吸收装置。

试回答:
①B中发生反应的化学方程式为
②为使E装置中进入纯净干燥的氯气,C中盛装试剂是饱和食盐水,作用是
③E中发生的化学反应方程式为
④F是尾气处理装置,反应离子方程式为
⑤实验室也可以用KMnO4替代MnO2与浓HCl反应制取Cl2,但反应不需要加热,写出此反应的离子方程式
 被还原为Mn2+)
被还原为Mn2+)(2)Cl2是一种重要的化工原料,下图是一些含氯产品。

①中钢瓶上应贴的标签为
A.腐蚀品 B.有毒品 C.易燃品
②漂白粉可用于游泳池及环境消毒剂,制漂白粉的反应原理为
(3)2016年10月20日生活日报讯,一位温州小伙将84消毒液与洁厕灵共用来刷洗厕所时,突然瘫坐在地,无力挪步,呼吸急促。经医生诊断,小伙子为轻度氯气中毒。某大学化工系教授,该教授表示洁厕灵含有盐酸,84消毒液含有NaClO(次氯酸钠),二者不可混用,一旦混合会产生有毒的氯气,如果不慎发生事故,应立即开窗通风,用湿毛巾捂住口鼻向高处转移,事后要多喝水,并及时就医。
①请用离子方程式分析小伙子中毒的原因
②发生事故后,要用湿毛巾捂住口鼻向高处转移,事后还要多喝水,用化学方程式表示用湿毛巾捂住口鼻,事后多喝水的原因:
您最近一年使用:0次
名校
7 . 下列实验室制取气体的方法不合理 的是
| A.锌粒与稀硫酸反应制H2 | B.二氧化锰与浓盐酸共热制Cl2 |
| C.电石与饱和食盐水制C2H2 | D.氯化铵受热分解制NH3 |
您最近一年使用:0次
8 . 一氧化二氯(Cl2O)是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸。Cl2O的熔点是-120.6℃,沸点是2.0℃。利用反应2HgO+2Cl2=Cl2O+HgCl2·HgO可制备Cl2O。

某同学利用如图装置制备Cl2O,请回答下列问题:
(1)仪器A的名称为:____ 。
(2)实验室常用MnO2固体与浓盐酸反应制取氯气,请写出化学方程式:____ 。
(3)装置乙中的试剂是___ ;装置丙的作用是____ 。
(4)反应2HgO+2Cl2=Cl2O+HgCl2·HgO中,每生成0.5molCl2O转移电子的物质的量为____ mol。

某同学利用如图装置制备Cl2O,请回答下列问题:
(1)仪器A的名称为:
(2)实验室常用MnO2固体与浓盐酸反应制取氯气,请写出化学方程式:
(3)装置乙中的试剂是
(4)反应2HgO+2Cl2=Cl2O+HgCl2·HgO中,每生成0.5molCl2O转移电子的物质的量为
您最近一年使用:0次
21-22高一上·北京西城·期中
名校
9 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和NaClO,并探究NaClO的性质。
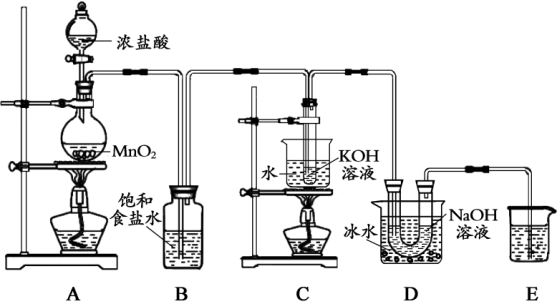
回答下列问题:
(1)A中反应的化学方程式是___________ 。
(2)C中反应的离子方程式为:□Cl2+□OH- □
□ +□_____+□______,
+□_____+□______,___________ 。
(3)D中采用冰水浴冷却的目的是___________ 。
(4)探究NaClO的性质。
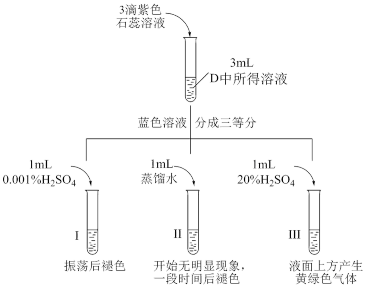
①I中溶液褪色的原因是___________ 。
②III中产生黄绿色气体的原因是___________ (写离子方程式)。
(5)通过上述实验可知,影响氧化还原反应的因素有______ 。

回答下列问题:
(1)A中反应的化学方程式是
(2)C中反应的离子方程式为:□Cl2+□OH-
 □
□ +□_____+□______,
+□_____+□______,(3)D中采用冰水浴冷却的目的是
(4)探究NaClO的性质。

①I中溶液褪色的原因是
②III中产生黄绿色气体的原因是
(5)通过上述实验可知,影响氧化还原反应的因素有
您最近一年使用:0次
21-22高一上·北京西城·期中
名校
10 . 为除去括号内的杂质,所选用的试剂或方法不正确 的是
| A.Na2CO3固体粉末(NaHCO3),加热分解 |
| B.NaHCO3溶液(Na2CO3),应通入足量的CO2气体 |
| C.Cl2(HCl),将混合气体通过足量的饱和食盐水 |
| D.Na2CO3溶液(Na2SO4),加入适量的Ba(OH)2溶液,过滤 |
您最近一年使用:0次



