名校
解题方法
1 . 如图是制取干燥纯净的 Cl2 并探究其化学性质的装置图(已知:I2 遇淀粉变蓝)。
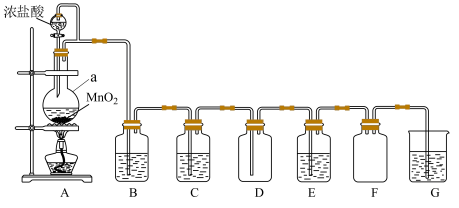
(1)仪器 a 的名称为_______ ,其中发生反应的化学方程式为_______ , 氧化剂与还原剂之比为_______ 。
(2)B 中应盛放的试剂是_______ ;C 的作用是_______ ;F 的作用是_______ 。
(3)E 中装有淀粉碘化钾溶液,观察到无色溶液变蓝,原因是_______ 。
(4)G 中发生反应的离子方程式为_______ 。

(1)仪器 a 的名称为
(2)B 中应盛放的试剂是
(3)E 中装有淀粉碘化钾溶液,观察到无色溶液变蓝,原因是
(4)G 中发生反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 . 化学让生活更美好,各类水处理剂能让水质得到提升达到饮用水的标准。生活中较常见的水处理剂有:氯气、次氯酸钠、漂白粉(主要成分为次氯酸钙)、二氧化氯、明矾、硫酸铁、高铁酸钠等等。
(1)氯气常用于自来水的消毒,请写出舍勒研究软锰矿时发现氯气的化学方程式:___________ 。
(2)氯气能用于制备易于保存、使用方便的漂白液,但若温度过高会发生副反应生成NaCl、NaClO3。请写出在加热时,当NaOH与Cl2反应生成的n(NaClO):n(NaClO3)=5:1时,NaOH与Cl2反应的化学方程式:___________ 。
(3)下列有关水资源及水质净化的说法,不正确的是___________(填序号)。
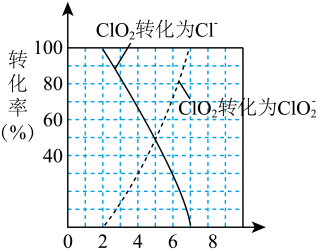
(4)近年来有科学家提出,氯气消毒时,会与水中的有机物发生反应,生成的有机氯化物可能对人体有害。因此,人们已开始研究并试用新的自来水消毒剂,如二氧化氯(ClO2)、臭氧等。ClO2被世界卫生组织(WHO)列为A级高效、安全灭菌消毒剂,将逐渐取代Cl2成为自来水的消毒剂。ClO2气体具有强氧化性,其还原产物ClO 、Cl﹣的转化率与pH关系如图所示。ClO2对污水中S2﹣、CN﹣等也有明显的去除效果,请写出pH≤2时,ClO2与S2﹣反应的离子方程式:
、Cl﹣的转化率与pH关系如图所示。ClO2对污水中S2﹣、CN﹣等也有明显的去除效果,请写出pH≤2时,ClO2与S2﹣反应的离子方程式:___________ 。某工厂污水中含CN﹣amg/L,现用ClO2将CN﹣氧化,生成了两种无毒无害的气体,处理50m3这种污水,至少需要ClO2___________ mol。
(5)高铁酸钠(Na2FeO4)在水中既能消毒杀菌,其产物Fe(OH)3胶体又能净水除去悬浮杂质,是一种理想的水处理剂。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么,Cl2、ClO2(pH≤2时)、Na2FeO4三种消毒杀菌剂的消毒效率由大到小的顺序是___________ 。
(1)氯气常用于自来水的消毒,请写出舍勒研究软锰矿时发现氯气的化学方程式:
(2)氯气能用于制备易于保存、使用方便的漂白液,但若温度过高会发生副反应生成NaCl、NaClO3。请写出在加热时,当NaOH与Cl2反应生成的n(NaClO):n(NaClO3)=5:1时,NaOH与Cl2反应的化学方程式:
(3)下列有关水资源及水质净化的说法,不正确的是___________(填序号)。
| A.将自来水煮沸烧开后再饮用更健康、因为能除去残留的Cl2及溶于其中的Cl﹣ |
| B.自来水用于洗涤后得到的含磷污水是很好的肥料,可灌溉庄稼,能直接排放到自然界水体中 |
| C.煤、石油的燃烧和汽车排放的尾气都会引起大气污染,且会出现酸雨等环境问题 |
| D.纳米铁粉可以高效地去除被污染水体中的Pb2+、Cu2+、Cd2+、Hg2+等重金属离子,其本质是纳米铁粉对重金属离子有较强的物理吸附 |
 、Cl﹣的转化率与pH关系如图所示。ClO2对污水中S2﹣、CN﹣等也有明显的去除效果,请写出pH≤2时,ClO2与S2﹣反应的离子方程式:
、Cl﹣的转化率与pH关系如图所示。ClO2对污水中S2﹣、CN﹣等也有明显的去除效果,请写出pH≤2时,ClO2与S2﹣反应的离子方程式:(5)高铁酸钠(Na2FeO4)在水中既能消毒杀菌,其产物Fe(OH)3胶体又能净水除去悬浮杂质,是一种理想的水处理剂。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么,Cl2、ClO2(pH≤2时)、Na2FeO4三种消毒杀菌剂的消毒效率由大到小的顺序是

您最近一年使用:0次
名校
3 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.100mL12mol/L盐酸与足量的MnO2共热,被氧化的HCl小于0.6NA |
| B.将含0.01molFeCl3的饱和溶液滴入到沸水,得到Fe(OH)3胶体微粒数目为0.01NA |
| C.1L、0.5mol/LNa2SO4溶液中,含有氧原子数为2NA |
| D.标准状况下,4.48LHCl溶于水形成100mL溶液,溶液中含有2NA个HCl分子 |
您最近一年使用:0次
4 . 氯气广泛应用于杀菌、消毒及化工领域,某化学小组设计如图装置制备少量干燥纯净的氯气,试回答下列问题:

(1)盛有浓盐酸仪器名称_____ ,装置的正确连接顺序为_____ 。
(2)气体发生装置中发生反应的化学方程式为____ ,该反应中体现HCl的_____ 性。
(3)题给装置中饱和食盐水的作用是____ ,检验氯气是否收集满的方法是____ 。
(4)写出尾气吸收装置中反应的离子方程式____ 。
(5)Cl2与石灰乳反应制取漂白粉的化学方程式为____ 。

(1)盛有浓盐酸仪器名称
(2)气体发生装置中发生反应的化学方程式为
(3)题给装置中饱和食盐水的作用是
(4)写出尾气吸收装置中反应的离子方程式
(5)Cl2与石灰乳反应制取漂白粉的化学方程式为
您最近一年使用:0次
解题方法
5 . 实验室制取并收集氯气的装置如图所示,请回答下列问题:

(1)气体发生装置中进行的反应化学方程式是_______ 。
(2)在装置中:①饱和食盐水的作用是_______ ,②浓硫酸的作用是_______ 。
(3)化学实验中检验是否有Cl2产生常用湿润的淀粉-KI试纸。如果有Cl2产生,可观察到的现象是_______ 。
(4)写出尾气吸收装置中进行的反应的化学方程式:_______ 。

(1)气体发生装置中进行的反应化学方程式是
(2)在装置中:①饱和食盐水的作用是
(3)化学实验中检验是否有Cl2产生常用湿润的淀粉-KI试纸。如果有Cl2产生,可观察到的现象是
(4)写出尾气吸收装置中进行的反应的化学方程式:
您最近一年使用:0次
名校
解题方法
6 . 实验室用如图装置制取氯气,并用氯气进行实验。回答下列问题:

(1)A中盛有浓盐酸,B中盛有MnO2,写出反应的离子方程式:_______ 。
(2)D中放入浓H2SO4,其目的是_______ 。
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是_______ ,对比E和F中现象的差异可得出的结论是_______ 。
(4)G处的现象是_______ 。
(5)用化学方程式写出H处尾气吸收装置中的反应原理:_______ 。
(6)家庭中常用消毒液(有效成分为NaClO)与洁厕灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上的说明如下。
注意事项:
1.本品对棉织品有漂白脱色作用,对金属制品有腐蚀作用。
2.密封保存,请勿与洁厕灵同时使用。
3.保质期为一年。
①消毒液与洁厕灵不能同时使用,原因是_______ (用离子方程式表示)。
②需“密封保存”的原因是______ 。

(1)A中盛有浓盐酸,B中盛有MnO2,写出反应的离子方程式:
(2)D中放入浓H2SO4,其目的是
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是
(4)G处的现象是
(5)用化学方程式写出H处尾气吸收装置中的反应原理:
(6)家庭中常用消毒液(有效成分为NaClO)与洁厕灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上的说明如下。
注意事项:
1.本品对棉织品有漂白脱色作用,对金属制品有腐蚀作用。
2.密封保存,请勿与洁厕灵同时使用。
3.保质期为一年。
①消毒液与洁厕灵不能同时使用,原因是
②需“密封保存”的原因是
您最近一年使用:0次
名校
解题方法
7 . 如图为实验室制取纯净、干燥的Cl2,并进行检验Cl2性质实验的装置。其中E瓶中放有干燥红色布条;F中为铜网,F右端出气管口附近放有脱脂棉。

(1)如图,实验室制备Cl2的离子方程式_______
(2)C中试剂是_______ ,其作用是_______ ;D中试剂的作用是_______ ;
(3)E中现象是_______ ; F中现象是_______ ,其反应的化学方程式为_______ ;
(4)H中试剂为_______ ;其作用是_______ ,其中涉及到的离子反应是 _______ ;
(5)整套装置中有两处用酒精灯加热,两处酒精灯先点燃的是_______ (用①或②填写);
(6)实验室制备Cl2还可以用以下方法制备,请配平:_______ 。
_______HCl(浓)+_______KMnO4 = _______MnCl2+_______KCl+_______Cl2 ↑ +_______H2O

(1)如图,实验室制备Cl2的离子方程式
(2)C中试剂是
(3)E中现象是
(4)H中试剂为
(5)整套装置中有两处用酒精灯加热,两处酒精灯先点燃的是
(6)实验室制备Cl2还可以用以下方法制备,请配平:
_______HCl(浓)+_______KMnO4 = _______MnCl2+_______KCl+_______Cl2 ↑ +_______H2O
您最近一年使用:0次
8 . 用含有Al2O3、SiO2和少量FeO∙xFe2O3的铝灰制备Al2(SO4)3∙18H2O。工艺流程如图:
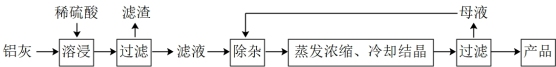
(一定条件下, 可与Mn2+反应生成MnO2)
可与Mn2+反应生成MnO2)
已知:生成氢氧化物沉淀的pH
(1)H2SO4溶解Al2O3的离子方程式是___________ ;
(2)检验滤液中还存在Fe2+的方法是___________ (注明试剂、现象)。
(3)“除杂”环节有如下几个步骤:
(Ⅰ)向滤液中加入过量KMnO4溶液,调节溶液的pH为3.2;
(Ⅱ)加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
(Ⅲ)加入MnSO4至紫红色消失,过滤。
①步骤Ⅰ的目的___________ 。
②向Ⅱ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是___________ ,写出其反应方程式___________ ;
③Ⅲ中加入MnSO4的目的是___________ 。
(4)从多次循环使用后母液中可回收的主要物质是___________ (填化学式)。

(一定条件下,
 可与Mn2+反应生成MnO2)
可与Mn2+反应生成MnO2)已知:生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 2.7 |
| 完全沉淀时 | 5.2 | 9.7 | 3.2 |
(2)检验滤液中还存在Fe2+的方法是
(3)“除杂”环节有如下几个步骤:
(Ⅰ)向滤液中加入过量KMnO4溶液,调节溶液的pH为3.2;
(Ⅱ)加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
(Ⅲ)加入MnSO4至紫红色消失,过滤。
①步骤Ⅰ的目的
②向Ⅱ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是
③Ⅲ中加入MnSO4的目的是
(4)从多次循环使用后母液中可回收的主要物质是
您最近一年使用:0次
解题方法
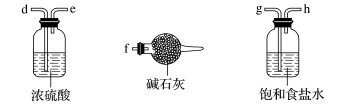
9 . 已知三氯化铁的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。某学习小组的同学对氯气与铁的反应及产物做了如下探究实验:___________ 。
(2)实验中制备氯气的离子方程式为___________
(3)饱和食盐水的作用是___________ ,碱石灰的作用是___________
(4)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,对固体混合物进行如下实验:___________ (写出离子方程式);b: Fe3+ + 3SCN- = Fe(SCN)3
(5)该小组同学对红色褪去的原因进行探究。
步骤1:取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;
第二份滴加KSCN,溶液出现红色;
第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀,该白色沉淀是___________ (填化学式)
步骤2:另取同浓度的FeCl3溶液滴加2滴KSCN,溶液变红,再通入O2,无明显变化。
得出结论:溶液红色褪去的原因是___________ 。

(2)实验中制备氯气的离子方程式为
(3)饱和食盐水的作用是
(4)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,对固体混合物进行如下实验:

(5)该小组同学对红色褪去的原因进行探究。
步骤1:取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;
第二份滴加KSCN,溶液出现红色;
第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀,该白色沉淀是
步骤2:另取同浓度的FeCl3溶液滴加2滴KSCN,溶液变红,再通入O2,无明显变化。
得出结论:溶液红色褪去的原因是
您最近一年使用:0次
2022-03-31更新
|
451次组卷
|
3卷引用:重庆市主城区六校2020-2021学年高一上学期期末联考化学试题
解题方法
10 . 苯乙酮( )广泛用于皂用香料和烟草香精中,可由苯和乙酸酐制备,其反应原理为:
)广泛用于皂用香料和烟草香精中,可由苯和乙酸酐制备,其反应原理为:
已知:
Ⅰ.催化剂无水 的制备
的制备
图中是实验室制取并收集少量无水 的相关实验装置的仪器和药品。
的相关实验装置的仪器和药品。

(1)B中发生的反应的离子方程式为___________ 。
(2)制备无水 的导管接口顺序为c→
的导管接口顺序为c→___________ (填序号,装置不可重复使用),E的作用是___________ 。
(3)在选择收集装置时,常选用图中F,而不选择下图的原因是___________ 。
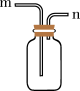
Ⅱ. 苯乙酮的制备
步骤一:向三颈烧瓶中加入28.0g苯和12.0g无水氯化铝,在搅拌下滴加20.4g乙酸酐,在70~80℃下加热45min,反应装置如图(省略部分装置)。

步骤二:冷却后将反应物倒入50.0g冰水中,有白色胶状沉淀生成,水层用苯萃取,合并苯层溶液,再依次用15mL 5%NaOH溶液和15mL水洗涤,分离出苯层。
步骤三:苯层用无水硫酸镁干燥,蒸馏回收苯,再收集产品苯乙酮。
请回答下列问题:
(4)步骤一中适宜的加热方式为___________ 。
(5)根据上述实验药品的用量,三颈烧瓶的最适宜规格为___________。
(6)图示仪器N的名称为___________ ,其作用是___________ 。
(7)步骤二中用NaOH溶液洗涤的目的是___________ 。
(8)实验中收集到18.0g苯乙酮,则苯乙酮的产率为___________ 。
 )广泛用于皂用香料和烟草香精中,可由苯和乙酸酐制备,其反应原理为:
)广泛用于皂用香料和烟草香精中,可由苯和乙酸酐制备,其反应原理为:
已知:
名称 | 相对分子质量 | 沸点/℃ | 密度(g·mL-1) | 溶解性 |
苯 | 78 | 80.1 | 0.88 | 不溶于水,易溶于有机溶剂 |
苯乙酮 | 120 | 203 | 1.03 | 微溶于水,易溶于有机溶剂 |
乙酸酐 | 102 | 139 | 1.08 | 溶于水生成乙酸,易溶于有机溶剂 |
| 133.5 | 178(升华) | 2.44 | 遇水水解,微溶于苯 |
 的制备
的制备图中是实验室制取并收集少量无水
 的相关实验装置的仪器和药品。
的相关实验装置的仪器和药品。
(1)B中发生的反应的离子方程式为
(2)制备无水
 的导管接口顺序为c→
的导管接口顺序为c→(3)在选择收集装置时,常选用图中F,而不选择下图的原因是

Ⅱ. 苯乙酮的制备
步骤一:向三颈烧瓶中加入28.0g苯和12.0g无水氯化铝,在搅拌下滴加20.4g乙酸酐,在70~80℃下加热45min,反应装置如图(省略部分装置)。

步骤二:冷却后将反应物倒入50.0g冰水中,有白色胶状沉淀生成,水层用苯萃取,合并苯层溶液,再依次用15mL 5%NaOH溶液和15mL水洗涤,分离出苯层。
步骤三:苯层用无水硫酸镁干燥,蒸馏回收苯,再收集产品苯乙酮。
请回答下列问题:
(4)步骤一中适宜的加热方式为
(5)根据上述实验药品的用量,三颈烧瓶的最适宜规格为___________。
| A.50mL | B.100mL | C.250mL | D.500mL |
(7)步骤二中用NaOH溶液洗涤的目的是
(8)实验中收集到18.0g苯乙酮,则苯乙酮的产率为
您最近一年使用:0次
2022-03-31更新
|
262次组卷
|
2卷引用:重庆市主城区六校2020-2021学年高二下学期期末联考化学试题



