1 . CuI是有机合成的一种催化剂,受热易氧化。实验室可通过向CuSO4与NaI的混合溶液中通入SO2制备CuI(2CuSO4+2NaI+SO2+2H2O 2CuI↓+2H2SO4+Na2SO4)。下列实验原理和装置不能达到实验目的的是( )
2CuI↓+2H2SO4+Na2SO4)。下列实验原理和装置不能达到实验目的的是( )
 2CuI↓+2H2SO4+Na2SO4)。下列实验原理和装置不能达到实验目的的是( )
2CuI↓+2H2SO4+Na2SO4)。下列实验原理和装置不能达到实验目的的是( )A. 制备SO2 制备SO2 |
B.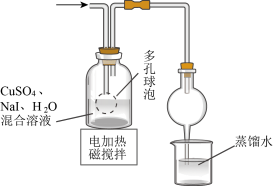 制备CuI并制备少量含SO2的溶液 制备CuI并制备少量含SO2的溶液 |
C.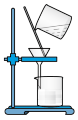 将CuI与母液分离并用装置制得的含SO2的溶液洗涤沉淀 将CuI与母液分离并用装置制得的含SO2的溶液洗涤沉淀 |
D. 加热干燥湿的CuI固体 加热干燥湿的CuI固体 |
您最近一年使用:0次
2019-05-24更新
|
810次组卷
|
6卷引用:【市级联考】江苏省盐城市2019届高三下学期第四次模拟考试化学试题
2 . 实验室拟采用如下装置制备 并研究
并研究 的相关性质:
的相关性质: 易溶于乙醇,回答下列问题:
易溶于乙醇,回答下列问题:
(1)写出浓硫酸和亚硫酸钠反应制取 的化学方程式
的化学方程式________ 。
(2)干燥管中的 的作用是
的作用是________ ,装置Ⅱ中的干燥管作用是________ 。
(3)反应开始后,观察到装置Ⅰ中品红溶液(测得pH=3)迅速褪色,查询资料可知: 通入水中存在如下反应:
通入水中存在如下反应: ;
; ,通过分析上述现象,推测使品红水溶液褪色的微粒不可能为
,通过分析上述现象,推测使品红水溶液褪色的微粒不可能为 ,原因是
,原因是________ 。
(4)造成品红水溶液褪色的微粒可能是i, ;ii.
;ii. ;iii.
;iii. 。将上述装置Ⅰ中的品红水溶液换成品红乙醇溶液,重复实验,观察到溶液红色不褪色,证明
。将上述装置Ⅰ中的品红水溶液换成品红乙醇溶液,重复实验,观察到溶液红色不褪色,证明 不可能使品红水溶液褪色,其原因是
不可能使品红水溶液褪色,其原因是________ 。
(5)继续设计实验验证 、
、 对品红的漂白性:
对品红的漂白性:
设计实验c、d的目的是________ 。结合(4)、(5)的实验现象推测: 使品红水溶液褪色时起主要作用的微粒是
使品红水溶液褪色时起主要作用的微粒是________ 。
 并研究
并研究 的相关性质:
的相关性质:
 易溶于乙醇,回答下列问题:
易溶于乙醇,回答下列问题:(1)写出浓硫酸和亚硫酸钠反应制取
 的化学方程式
的化学方程式(2)干燥管中的
 的作用是
的作用是(3)反应开始后,观察到装置Ⅰ中品红溶液(测得pH=3)迅速褪色,查询资料可知:
 通入水中存在如下反应:
通入水中存在如下反应: ;
; ,通过分析上述现象,推测使品红水溶液褪色的微粒不可能为
,通过分析上述现象,推测使品红水溶液褪色的微粒不可能为 ,原因是
,原因是(4)造成品红水溶液褪色的微粒可能是i,
 ;ii.
;ii. ;iii.
;iii. 。将上述装置Ⅰ中的品红水溶液换成品红乙醇溶液,重复实验,观察到溶液红色不褪色,证明
。将上述装置Ⅰ中的品红水溶液换成品红乙醇溶液,重复实验,观察到溶液红色不褪色,证明 不可能使品红水溶液褪色,其原因是
不可能使品红水溶液褪色,其原因是(5)继续设计实验验证
 、
、 对品红的漂白性:
对品红的漂白性:
| 试管中的液体(浓度均相同) | 现象 |
a. 溶液(pH=10) 溶液(pH=10) | 溶液立即褪色 | |
b. 溶液(pH约为5) 溶液(pH约为5) | 溶液立即变浅,约10s后完全褪色 | |
| c.NaOH溶液(pH=10) | 红色溶液不褪色 | |
d.pH=3的 溶液 溶液 | 红色溶液不褪色 |
 使品红水溶液褪色时起主要作用的微粒是
使品红水溶液褪色时起主要作用的微粒是
您最近一年使用:0次
名校
3 . 某化学课外兴趣小组用如图所示装置进行实验,制备某气体并验证其性质。请回答下列问题:
①装置A中发生反应的化学方程式为___________ 。
②实验中,取一定质量的铜片和一定体积 的浓硫酸在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
的浓硫酸在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
A.有一定量的余酸但未能使铜片完全溶解,你认为原因是___________ 。
B.下列药品中能用来证明反应结束后的烧瓶中确有余酸的是___________ (填标号)。
a.铁粉 b. 溶液 c. 银粉 d.
溶液 c. 银粉 d.  溶液
溶液
(2)若装置A中分液漏斗盛装浓硫酸,圆底烧瓶盛装木炭。
①装置A中发生反应的化学方程式为___________ 。
②设计实验证明装置C中含有 时,所需的试剂有
时,所需的试剂有___________ (填标号)。
a.NaOH溶液 b. 澄清石灰水 c. 品红溶液 d. 酸性 溶液
溶液
(3)反应(1)(2)D中品红溶液褪色,加热试管里已褪色溶液时的现象为:___________ 。
(4)装置D中试管口放置的棉花中浸了一种液体用于吸收尾气,该液体是___________ ,反应的离子方程式为___________ 。

①装置A中发生反应的化学方程式为
②实验中,取一定质量的铜片和一定体积
 的浓硫酸在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
的浓硫酸在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。A.有一定量的余酸但未能使铜片完全溶解,你认为原因是
B.下列药品中能用来证明反应结束后的烧瓶中确有余酸的是
a.铁粉 b.
 溶液 c. 银粉 d.
溶液 c. 银粉 d.  溶液
溶液(2)若装置A中分液漏斗盛装浓硫酸,圆底烧瓶盛装木炭。
①装置A中发生反应的化学方程式为
②设计实验证明装置C中含有
 时,所需的试剂有
时,所需的试剂有a.NaOH溶液 b. 澄清石灰水 c. 品红溶液 d. 酸性
 溶液
溶液(3)反应(1)(2)D中品红溶液褪色,加热试管里已褪色溶液时的现象为:
(4)装置D中试管口放置的棉花中浸了一种液体用于吸收尾气,该液体是
您最近一年使用:0次
解题方法
4 . 某化学小组为了证明二氧化硫和氯水的漂白性,设计了如图所示的实装置:
(1)用来制取氯气的装置是___________ (填字母序号)。
(2)反应开始一段时间后,B、D试管中的品红溶液均褪色。停止通气后,再将B、D两个试管分别加热,___________ (填“B”或“D”)试管中无明显现象。
(3)装置C的主要作用是______________________ 。
(4)该小组同学将两种气体混合后通入品红溶液中,发现漂白效果并不像预期的一样增强。查阅资料得知:两种气体混合,再与水反应可生成两种常见的酸,因而漂白作用减弱,该反应的化学方程式是_________________________ 。

(1)用来制取氯气的装置是
(2)反应开始一段时间后,B、D试管中的品红溶液均褪色。停止通气后,再将B、D两个试管分别加热,
(3)装置C的主要作用是
(4)该小组同学将两种气体混合后通入品红溶液中,发现漂白效果并不像预期的一样增强。查阅资料得知:两种气体混合,再与水反应可生成两种常见的酸,因而漂白作用减弱,该反应的化学方程式是
您最近一年使用:0次
5 . 研究硫及其化合物的应用价值对于社会发展意义重大。请回答以下问题。
(1)用下图装置制备纯净的SO2(同时生成一种正盐),请写出装置A中反应的离子方程式为___________ ,装置的连接顺序为: a → ___________ → e ( 按气流方向,用小写字母表示 ),C装置的仪器名称是___________ ,碱石灰的主要作用为___________ 。___________ ;
② 为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成。
上述方案中合理的是___________ (填Ⅰ、Ⅱ或Ⅲ);试管b中发生反应的离子方程式为___________ 。
(1)用下图装置制备纯净的SO2(同时生成一种正盐),请写出装置A中反应的离子方程式为
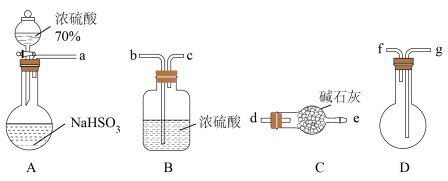
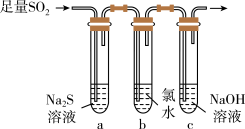
② 为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成。
上述方案中合理的是
您最近一年使用:0次
名校
6 . 黄铜矿( )是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物,冶炼铜的反应为
)是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物,冶炼铜的反应为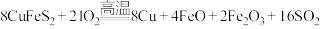 。
。
(1)若 中Fe的化合价为+2价,则反应中的氧化产物是
中Fe的化合价为+2价,则反应中的氧化产物是___________ (填化学式)。
(2)用稀硫酸浸泡上述反应制取铜后剩余的固体残渣,取少量所得溶液,检验该溶液中存在 的方法是
的方法是___________ (注明试剂、现象)。
(3)上述冶炼过程中会产生大量 ,下列处理方案中合理的是___________(填字母)。
,下列处理方案中合理的是___________(填字母)。
(4)验证黄铜矿冶炼铜的反应所得气体中含有 的方法是
的方法是___________ 。
(5)实验室制备、收集干燥的 所需装置如图所示。
所需装置如图所示。
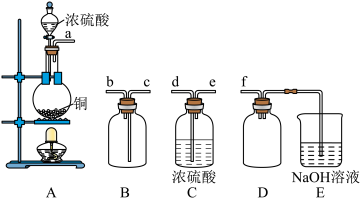
①其中装置A产生 ,反应的化学方程式为
,反应的化学方程式为___________ 。
②请按气流方向连接各仪器接口,顺序为a→___________ →f,装置D的作用是___________ ,装置E中反应的离子方程式为___________ 。
 )是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物,冶炼铜的反应为
)是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物,冶炼铜的反应为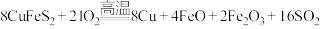 。
。(1)若
 中Fe的化合价为+2价,则反应中的氧化产物是
中Fe的化合价为+2价,则反应中的氧化产物是(2)用稀硫酸浸泡上述反应制取铜后剩余的固体残渣,取少量所得溶液,检验该溶液中存在
 的方法是
的方法是(3)上述冶炼过程中会产生大量
 ,下列处理方案中合理的是___________(填字母)。
,下列处理方案中合理的是___________(填字母)。| A.高空排放 | B.用于制备硫酸 |
C.用纯碱溶液吸收制 | D.用浓硫酸吸收 |
 的方法是
的方法是(5)实验室制备、收集干燥的
 所需装置如图所示。
所需装置如图所示。
①其中装置A产生
 ,反应的化学方程式为
,反应的化学方程式为②请按气流方向连接各仪器接口,顺序为a→
您最近一年使用:0次
7 . 人类农业生产离不开氮肥,几乎所有的氮肥都以氨为原料生产,某化学兴趣小组利用如图装置制备氨气并探究相关性质。
已知:①Cu、Cu2O均为红色固体
②Cu2O+2H+=Cu2++Cu+H2O_______ ,装置E的作用是_______ 。
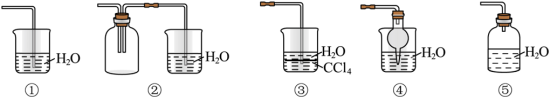
(2)氨气极易溶于水,下列能用作吸收氨气的装置是_______ (填序号)。
②实验后取C中固体加足量稀硫酸,充分反应后溶液变蓝且有红色固体剩余,则实验后C中固体一定存在的是_______ ,再加入下列试剂_______ (填选项),固体又可以继续溶解。
A.FeCl3溶液 B.FeCl2溶液 C.KCl溶液 D.KNO3溶液
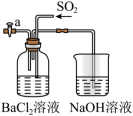
(4)若将发生装置A与a相连(如图),BaCl2溶液中产生白色沉淀,写出生成白色沉淀的离子方程式为_______ ,若向a处分别通入_______ (填选项),也会产生白色沉淀。
已知:①Cu、Cu2O均为红色固体
②Cu2O+2H+=Cu2++Cu+H2O
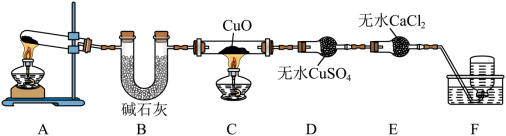
(2)氨气极易溶于水,下列能用作吸收氨气的装置是
| 序号 | 实验现象 | 实验结论 |
| I | C装置中黑色CuO固体全部变红 | / |
| II | D装置中无水CuSO4变蓝 | 反应生成了 |
| III | F装置中收集到无色无味气体,且遇到空气不变色 | 反应生成了N2 |
A.FeCl3溶液 B.FeCl2溶液 C.KCl溶液 D.KNO3溶液
(4)若将发生装置A与a相连(如图),BaCl2溶液中产生白色沉淀,写出生成白色沉淀的离子方程式为
您最近一年使用:0次
2024-03-25更新
|
424次组卷
|
3卷引用:广东省深圳市光明中学2023-2024学年高一下学期3月第一次统测化学试题
解题方法
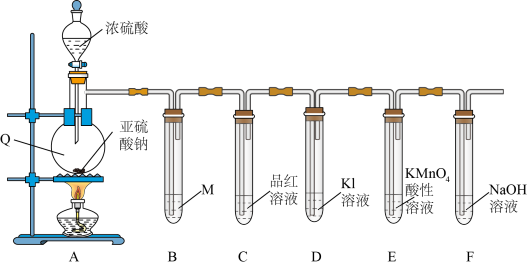
8 . 学习小组在实验室中利用下图装置制备SO2并进行相关性质的探究。
(1)仪器Q的名称为_________ 。
(2)装置B是为了观察气体的流速,则试剂M为_________(填字母)。
(3)装置C中出现的现象说明SO2具有_________ 性。
(4)装置E中__________________ (填现象)可说明SO2具有还原性,发生反应的离子方程式为__________________ 。
(5)装置F的作用是_________ 。
(1)仪器Q的名称为
(2)装置B是为了观察气体的流速,则试剂M为_________(填字母)。
| A.NaOH溶液 | B.饱和NaHSO3溶液 | C.Na2S溶液 | D.Na2SO3溶液 |
(3)装置C中出现的现象说明SO2具有
(4)装置E中
(5)装置F的作用是
您最近一年使用:0次
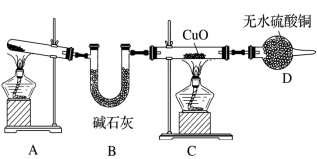
9 . 人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料生产,某化学兴趣小组利用如图装置探究氨气的相关性质。
②参阅资料:Cu、Cu2O均为红色固体,其中Cu2O能溶于氨水,生成无色溶液,在空气中立即氧化成蓝色[Cu(NH3)2]2+,而Cu不与氨水反应。
(1)装置D的作用:_______ 。
(2)甲同学认为该实验装置不严谨,应在装置D后再连接一个装有CaCl2固体的球形干燥管,其目的是_______ 。
(3)实验开始时,先点燃装置_______ (填“A”或“C”)的酒精灯,一段时间后再点燃另一装置的酒精灯。实验结束发现:C中粉末完全变红,D中无水硫酸铜变蓝,还产生一种单质气体。为进一步确定红色固体物质,乙同学提出假设:①红色固体为Cu单质;②红色固体为Cu2O;③_______ 。
设计实验操作:取反应后的红色固体物质于洁净试管中,向其中滴加足量氨水并充分振荡,观察到溶液变为蓝色,固体有剩余。丙同学为验证乙同学的假设,取CuO固体4.0 g重复上述加热实验,反应后装置C中得红色固体3.52 g。请结合上述信息,写出NH3与CuO反应的化学方程式:____ 。
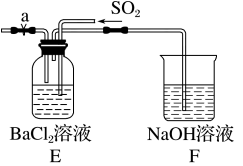
(4)已知,将SO2通入BaCl2溶液中,无明显现象。如图若将生成的NH3与SO2同时通入BaCl2溶液中,产生白色沉淀,反应的化学方程式为_______ 。若向a处通入_______ (填字母),在E中也能产生白色沉淀,其白色沉淀为_______ 。
②参阅资料:Cu、Cu2O均为红色固体,其中Cu2O能溶于氨水,生成无色溶液,在空气中立即氧化成蓝色[Cu(NH3)2]2+,而Cu不与氨水反应。
(1)装置D的作用:
(2)甲同学认为该实验装置不严谨,应在装置D后再连接一个装有CaCl2固体的球形干燥管,其目的是
(3)实验开始时,先点燃装置
设计实验操作:取反应后的红色固体物质于洁净试管中,向其中滴加足量氨水并充分振荡,观察到溶液变为蓝色,固体有剩余。丙同学为验证乙同学的假设,取CuO固体4.0 g重复上述加热实验,反应后装置C中得红色固体3.52 g。请结合上述信息,写出NH3与CuO反应的化学方程式:
(4)已知,将SO2通入BaCl2溶液中,无明显现象。如图若将生成的NH3与SO2同时通入BaCl2溶液中,产生白色沉淀,反应的化学方程式为
您最近一年使用:0次
10 . 连四硫酸钠 可延长血液凝结时间,也可用作修饰剂。某小组设计实验探究连四硫酸钠的性质,装置如图所示。回答下列问题:
可延长血液凝结时间,也可用作修饰剂。某小组设计实验探究连四硫酸钠的性质,装置如图所示。回答下列问题:
(1)仪器M的名称为___________ ,橡皮管N的作用是___________ 。
(2)工业上用双氧水和 反应制备
反应制备 ,反应的化学方程式为
,反应的化学方程式为___________ 。
(3)B中现象说明A中产生了_________ (填化学式),C中溶液变红的原因是_________ 。
(4)E中产生白色沉淀的离子方程式为___________ 。
(5)从环保角度分析,本实验应改进之处是___________ 。
(6)连四硫酸钠保存不当会变质,设计简单实验证明连四硫酸钠已变质:___________ 。
 可延长血液凝结时间,也可用作修饰剂。某小组设计实验探究连四硫酸钠的性质,装置如图所示。回答下列问题:
可延长血液凝结时间,也可用作修饰剂。某小组设计实验探究连四硫酸钠的性质,装置如图所示。回答下列问题: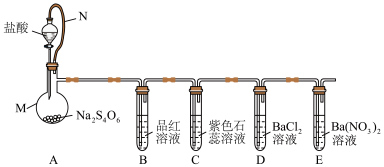
(1)仪器M的名称为
(2)工业上用双氧水和
 反应制备
反应制备 ,反应的化学方程式为
,反应的化学方程式为(3)B中现象说明A中产生了
(4)E中产生白色沉淀的离子方程式为
(5)从环保角度分析,本实验应改进之处是
(6)连四硫酸钠保存不当会变质,设计简单实验证明连四硫酸钠已变质:
您最近一年使用:0次
2024-02-25更新
|
773次组卷
|
5卷引用:2024届陕西省安康市高三下学期一模考试理科综合试题-高中化学
2024届陕西省安康市高三下学期一模考试理科综合试题-高中化学(已下线)专题09 化学实验综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)大题02 化学实验综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)2024届陕西省西安博爱国际学校高三下学期第一次模拟考试理科综合试卷-高中化学内蒙古自治区赤峰第四中学2023-2024学年高三下学期开学考试理综试题-高中化学




