名校
1 . 谢弗勒尔盐(Cu2SO3·CuSO3·2H2O)是一种不溶于水、酸和乙醇的固体,100℃时发生分解。可由CuSO4·5H2O和SO2等为原料制备,实验装置如下图所示:
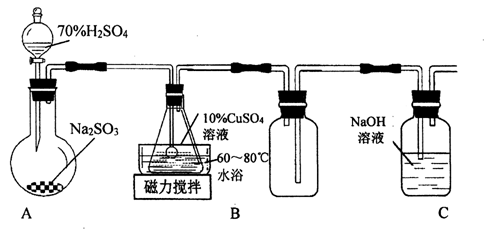
(1)装置A在常温下制取SO2时,用70%硫酸而不用稀硫酸和98%浓硫酸,其原因是________ 。
(2)装置B中发生反应的离子方程式为_________ 。
(3)装置C的作用是__________ 。
(4)从B中获得的固体需先用蒸馏水充分洗涤,再真空干燥。检验已洗涤完全的方法是________________ 。
(5)请补充完整由工业级氧化铜(含少量FeO)制备实验原料(纯净CuSO4·5H2O)的实验方案:向工业级氧化铜中边搅拌边加入稍过量的硫酸溶液,微热使其完全溶解,边搅拌边向其中滴入______ 溶液,加入适量纯净的________ 调节3.2<pH<4.2,静置,过滤,将滤液水浴加热蒸发浓缩至表面出现晶膜,冷却结晶,过滤,用95%酒精洗涤晶体2~3次,晾干,得到CuSO4·5H2O。
[已知:该溶液中氢氧化物开始沉淀与沉淀完全时的pH范围分别为:Fe(OH)2(5.8, 8.8); Cu(OH)2(4.2, 6.7); Fe(OH)3(1.1,3.2)]

(1)装置A在常温下制取SO2时,用70%硫酸而不用稀硫酸和98%浓硫酸,其原因是
(2)装置B中发生反应的离子方程式为
(3)装置C的作用是
(4)从B中获得的固体需先用蒸馏水充分洗涤,再真空干燥。检验已洗涤完全的方法是
(5)请补充完整由工业级氧化铜(含少量FeO)制备实验原料(纯净CuSO4·5H2O)的实验方案:向工业级氧化铜中边搅拌边加入稍过量的硫酸溶液,微热使其完全溶解,边搅拌边向其中滴入
[已知:该溶液中氢氧化物开始沉淀与沉淀完全时的pH范围分别为:Fe(OH)2(5.8, 8.8); Cu(OH)2(4.2, 6.7); Fe(OH)3(1.1,3.2)]
您最近半年使用:0次
2 . 某矿样中含有大量的 CuS 及少量其他不溶于酸的杂质。实验室中以该矿样为原料制备CuCl2·2H2O 晶体,流程如下:
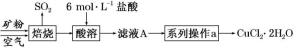
(1)在实验室中,欲用 37%(密度为 1.19 g·mL-1)的盐酸配制 500 mL 6 mol·L-1 的盐酸,需要的仪器除 量筒、烧杯、玻璃棒外,还有_____ 、_____ 。
(2)①若在实验室中完成系列操作 a。则下列实验操作中,不需要的是____________ (填字母)。
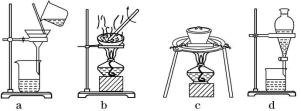
②CuCl2 溶液中存在平衡:Cu(H2O)42+(蓝色)+4Cl- CuCl42-(黄色)+4H2O。欲用实验证明滤液 A(绿色)中存在上述平衡,除滤液 A 外,下列试剂中还需要的是
CuCl42-(黄色)+4H2O。欲用实验证明滤液 A(绿色)中存在上述平衡,除滤液 A 外,下列试剂中还需要的是_____ (填字 母)。
a.FeCl3 固体 b.CuCl2 固体 c.蒸馏水
(3)某化学小组欲在实验室中研究 CuS 焙烧的反应过程,查阅资料得知在空气中焙烧 CuS 时,固体 质量变化曲线及 SO2 生成曲线如图。
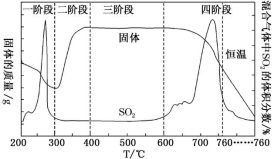
①CuS 矿样在焙烧过程中,有 Cu2S、CuO·CuSO4、CuSO4、CuO 生成,转化顺序为CuS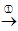 Cu2S
Cu2S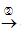 CuO·CuSO4
CuO·CuSO4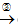 CuSO4
CuSO4 CuO第 ① 步 转 化 主 要 在 200 ~ 300 ℃ 内 进 行 , 该 步 转 化 的 化 学 方 程 式
CuO第 ① 步 转 化 主 要 在 200 ~ 300 ℃ 内 进 行 , 该 步 转 化 的 化 学 方 程 式______ 。
②300~400 ℃内,固体质量明显增加的原因是_____ ,图所示过程中,CuSO4固体能稳定存在的阶段是____________ (填字母)。
a.一阶段 b.二阶段 c.三阶段 d.四阶段
③该化学小组设计如下装置模拟 CuS 矿样在氧气中焙烧第四阶段的过程,并验证所得气体为 SO2和 O2 的混合物。
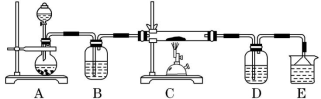
a.装置组装完成后,应立即进行的一项操作是_____ 。
b.当 D 中产生白色沉淀时,说明第四阶段所得气体为 SO2 和 O2 的混合物,你认为 D 中原来盛有________ 溶液。
c.若原 CuS 矿样的质量为 10.0 g,实验过程中,保持在 760 ℃左右持续加热,待矿样充分反应后, 石英玻璃管内所得固体的质量为 8.0 g,则原矿样中 CuS 的质量分数为_____ 。

(1)在实验室中,欲用 37%(密度为 1.19 g·mL-1)的盐酸配制 500 mL 6 mol·L-1 的盐酸,需要的仪器除 量筒、烧杯、玻璃棒外,还有
(2)①若在实验室中完成系列操作 a。则下列实验操作中,不需要的是

②CuCl2 溶液中存在平衡:Cu(H2O)42+(蓝色)+4Cl-
 CuCl42-(黄色)+4H2O。欲用实验证明滤液 A(绿色)中存在上述平衡,除滤液 A 外,下列试剂中还需要的是
CuCl42-(黄色)+4H2O。欲用实验证明滤液 A(绿色)中存在上述平衡,除滤液 A 外,下列试剂中还需要的是a.FeCl3 固体 b.CuCl2 固体 c.蒸馏水
(3)某化学小组欲在实验室中研究 CuS 焙烧的反应过程,查阅资料得知在空气中焙烧 CuS 时,固体 质量变化曲线及 SO2 生成曲线如图。

①CuS 矿样在焙烧过程中,有 Cu2S、CuO·CuSO4、CuSO4、CuO 生成,转化顺序为CuS
 Cu2S
Cu2S CuO·CuSO4
CuO·CuSO4 CuSO4
CuSO4 CuO第 ① 步 转 化 主 要 在 200 ~ 300 ℃ 内 进 行 , 该 步 转 化 的 化 学 方 程 式
CuO第 ① 步 转 化 主 要 在 200 ~ 300 ℃ 内 进 行 , 该 步 转 化 的 化 学 方 程 式②300~400 ℃内,固体质量明显增加的原因是
a.一阶段 b.二阶段 c.三阶段 d.四阶段
③该化学小组设计如下装置模拟 CuS 矿样在氧气中焙烧第四阶段的过程,并验证所得气体为 SO2和 O2 的混合物。

a.装置组装完成后,应立即进行的一项操作是
b.当 D 中产生白色沉淀时,说明第四阶段所得气体为 SO2 和 O2 的混合物,你认为 D 中原来盛有
c.若原 CuS 矿样的质量为 10.0 g,实验过程中,保持在 760 ℃左右持续加热,待矿样充分反应后, 石英玻璃管内所得固体的质量为 8.0 g,则原矿样中 CuS 的质量分数为
您最近半年使用:0次
2016-12-09更新
|
604次组卷
|
5卷引用:2014届山东省济南市高三3月模拟考试理综化学试卷
13-14高三上·宁夏银川·阶段练习
3 . 铜及其化合物在生产、生活中有广泛的应用。
(1)铜可采用如下方法制备:
火法炼铜:Cu2S+O2 2Cu+SO2
2Cu+SO2
湿法炼铜:CuSO4+Fe=FeSO4+Cu
上述两种方法中,铜元素均被_______ (填“氧化”还是“还原”)成铜单质。
(2)印刷电路板上使用的铜需要回收利用。
用FeCl3溶液浸泡印刷电路板制备CuCl2·2H2O,实验室模拟回收过程如图:
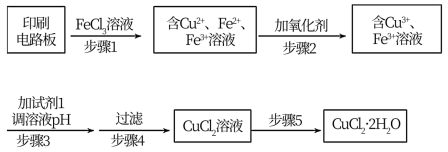
①步骤1中反应的离子方程式是_______ 。
②步骤2所加的氧化剂最适宜的是_______ 。
A.HNO3 B.H2O2 C.KMnO4
③步骤3的目的是使溶液的pH升高到5,此时Fe3+浓度为_______ [Ksp(Fe(OH)3)=4×10-38],可选用的“试剂1”是_______ (写出一种即可)。
④蒸发浓缩CuCl2溶液时,要滴加浓盐酸,目的是_______ (用化学方程式并结合简要的文字说明),再经冷却、结晶、过滤,得到CuCl2·2H2O。
(3)欲实现反应Cu+H2SO4(aq)=CuSO4+H2↑,在你认为能实现该转化的装置中的括号内,标出电极材料__ (填“Cu”或“C”)。并写出电极反应式____ 。

(1)铜可采用如下方法制备:
火法炼铜:Cu2S+O2
 2Cu+SO2
2Cu+SO2湿法炼铜:CuSO4+Fe=FeSO4+Cu
上述两种方法中,铜元素均被
(2)印刷电路板上使用的铜需要回收利用。
用FeCl3溶液浸泡印刷电路板制备CuCl2·2H2O,实验室模拟回收过程如图:

①步骤1中反应的离子方程式是
②步骤2所加的氧化剂最适宜的是
A.HNO3 B.H2O2 C.KMnO4
③步骤3的目的是使溶液的pH升高到5,此时Fe3+浓度为
④蒸发浓缩CuCl2溶液时,要滴加浓盐酸,目的是
(3)欲实现反应Cu+H2SO4(aq)=CuSO4+H2↑,在你认为能实现该转化的装置中的括号内,标出电极材料

您最近半年使用:0次
真题
4 . 现拟用图所示装置(尾气处理部分略)来制取一氧化碳,并用以测定某铜粉样品(混有CuO粉末)中金属铜的含量

(1)制备一氧化碳的化学方程式是______ ;
(2)试验中,观察到反应管中发生的现象是______ ;尾气的主要成分是______ ;
(3)反应完成后,正确的操作顺序为______ (填字母)
a.关闭漏斗开关 b.熄灭酒精1 c.熄灭酒精灯2
(4)若试验中称取铜粉样品5.0g,充分反应后,反应管中剩余固体的质量为4.8g,则原样品中单质铜的质量分数为______ ;
(5)从浓硫酸、浓硝酸、蒸馏水、双氧水中选用合适的试剂,设计一个测定样品中金属铜质量分数的方案;
①设计方案的主要步骤是(不必描述操作过程的细节)______ ;
②写出有关反应的化学方程式______ 。

(1)制备一氧化碳的化学方程式是
(2)试验中,观察到反应管中发生的现象是
(3)反应完成后,正确的操作顺序为
a.关闭漏斗开关 b.熄灭酒精1 c.熄灭酒精灯2
(4)若试验中称取铜粉样品5.0g,充分反应后,反应管中剩余固体的质量为4.8g,则原样品中单质铜的质量分数为
(5)从浓硫酸、浓硝酸、蒸馏水、双氧水中选用合适的试剂,设计一个测定样品中金属铜质量分数的方案;
①设计方案的主要步骤是(不必描述操作过程的细节)
②写出有关反应的化学方程式
您最近半年使用:0次
5 . 盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现就硫酸、硝酸与金属铜反应的情况,回答下列问题:
(1)工业上制备硫酸铜是利用废铜屑经灼烧后,在加热情况下跟稀硫酸反应,有关的化学方程式是: 。
不采用铜跟浓硫酸反应来制取硫酸铜的原因:
从环境角度来讲: 。
从原料角度来讲: 。
(2)在一定体积的10 mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9 mol。则浓硫酸的实际体积 (填“大于”、“等于”或“小于”)180 mL。
(3)若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为 。
(4)碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是
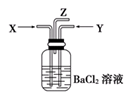
A.洗气瓶中产生的沉淀是碳酸钡
B.从Z导管出来的气体中无二氧化碳
C.洗气瓶中产生的沉淀是亚硫酸钡
D.在Z导管口有红棕色气体出现
(5)为了测定某铜银合金的成分,将30.0 g 合金溶于80 mL13.5 mol·L-1的浓HNO3中,待合金完全溶解后,收集到气体6.72 L (标准状况),并测得溶液中c(H+)=1mol·L-1。假设反应后溶液的体积仍为80 mL,试计算:
①被还原的HNO3的物质的量是____________;(只写结果)
②合金中铜的质量分数为____________。(写出计算过程)
(1)工业上制备硫酸铜是利用废铜屑经灼烧后,在加热情况下跟稀硫酸反应,有关的化学方程式是: 。
不采用铜跟浓硫酸反应来制取硫酸铜的原因:
从环境角度来讲: 。
从原料角度来讲: 。
(2)在一定体积的10 mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9 mol。则浓硫酸的实际体积 (填“大于”、“等于”或“小于”)180 mL。
(3)若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为 。
(4)碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是

A.洗气瓶中产生的沉淀是碳酸钡
B.从Z导管出来的气体中无二氧化碳
C.洗气瓶中产生的沉淀是亚硫酸钡
D.在Z导管口有红棕色气体出现
(5)为了测定某铜银合金的成分,将30.0 g 合金溶于80 mL13.5 mol·L-1的浓HNO3中,待合金完全溶解后,收集到气体6.72 L (标准状况),并测得溶液中c(H+)=1mol·L-1。假设反应后溶液的体积仍为80 mL,试计算:
①被还原的HNO3的物质的量是____________;(只写结果)
②合金中铜的质量分数为____________。(写出计算过程)
您最近半年使用:0次



