名校
1 . 以下说法中能证明无色透明液体是纯净水的是
| A.在l.0l×105Pa压强下测得沸点为373.15K |
| B.电解该液体得到氢气和氧气,且其体积比为2:1 |
| C.向其中投入金属钠,钠于液面上迅速游动,并发出丝丝声 |
| D.常温下,测得该液体pH=7 |
您最近一年使用:0次
名校
解题方法
2 . 已知反应S2O (aq)+2I-(aq)
(aq)+2I-(aq) 2SO
2SO (aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如下图所示。下列有关该反应的说法不正确的是 ( )
(aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如下图所示。下列有关该反应的说法不正确的是 ( )

①2Fe3+(aq)+2I-(aq) I2(aq)+2Fe2+(aq)
I2(aq)+2Fe2+(aq)
②2Fe2+(aq)+S2O (aq)
(aq) 2Fe3+(aq)+2SO
2Fe3+(aq)+2SO (aq)
(aq)
 (aq)+2I-(aq)
(aq)+2I-(aq) 2SO
2SO (aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如下图所示。下列有关该反应的说法不正确的是 ( )
(aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如下图所示。下列有关该反应的说法不正确的是 ( )
①2Fe3+(aq)+2I-(aq)
 I2(aq)+2Fe2+(aq)
I2(aq)+2Fe2+(aq)②2Fe2+(aq)+S2O
 (aq)
(aq) 2Fe3+(aq)+2SO
2Fe3+(aq)+2SO (aq)
(aq)| A.Fe3+是该反应的催化剂,加入Fe3+后降低了该反应的活化能 |
| B.反应①比反应②所需活化能大 |
| C.向该溶液中滴加淀粉溶液,溶液变蓝,适当升温,蓝色加深 |
| D.该反应可设计成原电池 |
您最近一年使用:0次
2020-09-25更新
|
1729次组卷
|
14卷引用:山西省大同市2021届高三上学期学情调研测试化学试题
山西省大同市2021届高三上学期学情调研测试化学试题辽宁省六校协作体2021届高三第一次联考化学试题江西省赣州市会昌县七校2021届高三联合9月月考化学试题辽宁省开原市中固镇第二中学2021届高三上学期9月月考化学试题内蒙古自治区赤峰二中2020-2021学年高二上学期第一次月考化学试题江西省红色七校(分宜中学、会昌中学、莲花中学、南城一中、任弼时中学、瑞金一中、遂川中学)2021届高三上学期第一次联考化学试题陕西省西安市长安区第一中学2021届高三上学期第三次月考化学试题江西省吉安县立中学2020-2021学年高二上学期12月月考化学(B班)试题吉林省延边第二中学2020-2021学年高二上学期第二次考试月考化学试题江苏省苏州市姑苏区苏州中学2020-2021学年高二下学期期中考试化学试题江西省景德镇一中2020-2021学年高一下学期期中考试化学(1班)试题黑龙江省双鸭山市第一中学2021-2022学年高二上学期第一次月考化学试题吉林省汪清县第六中学2021-2022学年高二12月月考化学试题吉林省乾安县第七中学2021-2022学年高二上学期第一次质量检测化学试题
名校
解题方法
3 . 开发氢能是实现社会可持续发展的需要。下图是以含H2S杂质的天然气为原料制取氢气的流程图。

回答下列问题:
(1)反应②的化学方程式为____________________________________________ 。
(2)反应④的离子方程式为____________________________________________ 。
(3)步骤③中制氢气的原理如下:
Ⅰ:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=+206.4 kJ·mol-1
CO(g)+3H2(g) ΔH=+206.4 kJ·mol-1
Ⅱ:CO(g)+H2O(g) CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
①对于反应Ⅰ,一定可以提高平衡体系中H2的百分含量,又能加快反应速率的措施是________  (填字母代号)。
(填字母代号)。
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
②利用反应Ⅱ,将CO进一步转化,可提高H2的产量。若1.00 mol CO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18 mol CO、CO2和H2的混合气体,则CO的转化率为____________ 。
③已知:反应Fe(s)+CO2(g) FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g) FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度时K1、K2的值如下表:
FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度时K1、K2的值如下表:
求:Ⅱ反应的逆反应方程式CO2(g)+H2(g) CO(g)+H2O(g)的平衡常数K=
CO(g)+H2O(g)的平衡常数K=________ (用K1和K2表示),且由表可知,反应CO2(g)+H2(g) CO(g)+H2O(g)是
CO(g)+H2O(g)是___________ 反应(填“吸热”或“放热”)。
(4)我国科研人员也提出了由CO2和CH4转化为高附加值产品和CH3COOH的催化反应历程,该历程示意图如下。下列说法不正确的是________

A.生成CH3COOH总反应的原子利用率为100%
B.CH4→CH3COOH过程中,有C—H键发生断裂
C.①→②放出能量并形成了C—C键
D.该催化剂可有效提高反应物的平衡转化率

回答下列问题:
(1)反应②的化学方程式为
(2)反应④的离子方程式为
(3)步骤③中制氢气的原理如下:
Ⅰ:CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH=+206.4 kJ·mol-1
CO(g)+3H2(g) ΔH=+206.4 kJ·mol-1Ⅱ:CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1①对于反应Ⅰ,一定可以提高平衡体系中H2的百分含量,又能加快反应速率的措施是
 (填字母代号)。
(填字母代号)。a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
②利用反应Ⅱ,将CO进一步转化,可提高H2的产量。若1.00 mol CO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18 mol CO、CO2和H2的混合气体,则CO的转化率为
③已知:反应Fe(s)+CO2(g)
 FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g) FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度时K1、K2的值如下表:
FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度时K1、K2的值如下表:| 700 ℃ | 900 ℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
求:Ⅱ反应的逆反应方程式CO2(g)+H2(g)
 CO(g)+H2O(g)的平衡常数K=
CO(g)+H2O(g)的平衡常数K= CO(g)+H2O(g)是
CO(g)+H2O(g)是(4)我国科研人员也提出了由CO2和CH4转化为高附加值产品和CH3COOH的催化反应历程,该历程示意图如下。下列说法不正确的是

A.生成CH3COOH总反应的原子利用率为100%
B.CH4→CH3COOH过程中,有C—H键发生断裂
C.①→②放出能量并形成了C—C键
D.该催化剂可有效提高反应物的平衡转化率
您最近一年使用:0次
4 . 聚乙烯醇具有亲水性和成膜性,在适宜的浓度下,能起类似人工泪液的作用,作为润滑剂预防或治疗眼部刺激症状。聚乙烯醇生产过程中会产生大量副产物乙酸甲酯,其催化醇解反应可用于制备甲醇和乙酸己酯,该反应的化学方程式为:CH3COOCH3(l)+C6H13OH(l)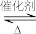 CH3COOC6H13(l)+CH3OH(l),已知v正=k正x(CH3COOCH3)·x(C6H13OH),v逆=k逆x(CH3COOC6H13)·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的物质的量分数。
CH3COOC6H13(l)+CH3OH(l),已知v正=k正x(CH3COOCH3)·x(C6H13OH),v逆=k逆x(CH3COOC6H13)·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的物质的量分数。
(1)“洗衣凝珠”是由一层薄膜包裹洗衣液制成的新型洗涤产品,该薄膜的主要化学成分是可溶于水的聚乙烯醇(简称PVA)塑料,聚乙烯醇的化学式为(C2H4O)n,试回答:聚乙烯醇属于_____ (填“金属材料”、“有机合成材料”、“硅酸盐材料”、“复合材料”之一),从物质结构的角度解释聚乙烯醇具有亲水性的原因___________________________ 。
(2)343K时,乙酸甲酯和己醇按物质的量之比1:1、1:2和2:1进行初始投料。则达到平衡后,初始投料比____ 时,乙酸甲酯转化率最大;与按1:2投料相比,按2:1投料时化学平衡常数Kx___ (填增大、减小或不变)。
(3)反应开始时,己醇和乙酸甲酯按物质的量之比1:1投料,测得348K、343K、338K三个温度下乙酸甲酯转化率(α)随时间(t)的变化关系如图所示。

该醇解反应的ΔH____ 0(填>或<)。348K时,以物质的量分数表示的化学平衡常数Kx=____ (保留2位有效数字)。A、B、C、D四点中,v逆最大的是___ ,v正最大的是____ 。
(4)该醇解反应使用离子交换树脂作催化剂,下列关于该催化剂的说法正确的是____ 。
a.参与了醇解反应,但并不改变反应历程 b.提高乙酸甲酯的平衡转化率
c.提高了醇解反应的活化能 d.使k正和k逆增大相同倍数
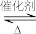 CH3COOC6H13(l)+CH3OH(l),已知v正=k正x(CH3COOCH3)·x(C6H13OH),v逆=k逆x(CH3COOC6H13)·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的物质的量分数。
CH3COOC6H13(l)+CH3OH(l),已知v正=k正x(CH3COOCH3)·x(C6H13OH),v逆=k逆x(CH3COOC6H13)·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的物质的量分数。(1)“洗衣凝珠”是由一层薄膜包裹洗衣液制成的新型洗涤产品,该薄膜的主要化学成分是可溶于水的聚乙烯醇(简称PVA)塑料,聚乙烯醇的化学式为(C2H4O)n,试回答:聚乙烯醇属于
(2)343K时,乙酸甲酯和己醇按物质的量之比1:1、1:2和2:1进行初始投料。则达到平衡后,初始投料比
(3)反应开始时,己醇和乙酸甲酯按物质的量之比1:1投料,测得348K、343K、338K三个温度下乙酸甲酯转化率(α)随时间(t)的变化关系如图所示。

该醇解反应的ΔH
(4)该醇解反应使用离子交换树脂作催化剂,下列关于该催化剂的说法正确的是
a.参与了醇解反应,但并不改变反应历程 b.提高乙酸甲酯的平衡转化率
c.提高了醇解反应的活化能 d.使k正和k逆增大相同倍数
您最近一年使用:0次
名校
5 . A和B转化为C的催化反应历程示意图如下。下列说法不正确的是


| A.催化剂在反应前后保持化学性质不变 |
| B.生成C总反应的原子利用率为100% |
| C.①→②的过程吸收能量 |
| D.C的水溶液呈弱酸性 |
您最近一年使用:0次
2019-02-14更新
|
450次组卷
|
7卷引用:【市级联考】福建省泉州市2019届高三上学期单科质量检查化学试题
【市级联考】福建省泉州市2019届高三上学期单科质量检查化学试题福建省平和县第一中学2018-2019学年高二下学期期末考试化学试题(已下线)专题6.1 化学能与热能(练)——2020年高考化学一轮复习讲练测(已下线)本册综合检测(二)——2020-2021学年高二化学选修四同步单元AB卷(人教版)(已下线)福建省霞浦第一中学2018-2019学年高二下学期第一次月考化学试题(B卷)山西省晋城市(高平一中、阳城一中、高平实验中学)2020-2021学年高二上学期期末考试化学试题河北省衡水市第十四中学2020-2021学年高二下学期摸底考试化学试题
名校
6 . 下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

下列说法不正确的是( )

下列说法不正确的是( )
A.通过计算,可知系统(Ⅰ)制备氢气的热化学方程式为:H2O(l)= H2(g)+1/2O2(g) ΔH = 286 kJ· mol-1 |
| B.通过计算,可知系统(Ⅱ)制备氢气的热化学方程式为:H2S(g)=H2(g)+S(s) ΔH =20kJ·mol-1 |
C.若反应H2(g)+1/2O2(g)=H2O(g) ΔH = -a kJ · mol-1, 则a>286  |
| D.制得等量H2所需能量较少的是热化学硫碘循环硫化氢分解法 |
您最近一年使用:0次
2019-08-11更新
|
965次组卷
|
4卷引用:山西省太原市2019-2020学年高二上学期期中测评化学试题
山西省太原市2019-2020学年高二上学期期中测评化学试题浙江省稽阳2018-2019学年高三联考化学试题江西省吉安市遂川中学2019—2020学年高二上学期第一次月考化学试题(B)(已下线)课时28 焓变与热化学方程式-2022年高考化学一轮复习小题多维练(全国通用)
真题
名校
7 . 氢气与氧气生成水的反应是氢能源应用的重要途径。下列有关说法正确的是
| A.一定温度下,反应2H2(g)+O2(g) =2H2O(g)能自发进行,该反应的ΔH<0 |
| B.氢氧燃料电池的负极反应为O2+2H2O+4e−=4OH− |
| C.常温常压下,氢氧燃料电池放电过程中消耗11.2 L H2,转移电子的数目为6.02×1023 |
| D.反应2H2(g)+O2(g) =2H2O(g)的ΔH可通过下式估算:∆H=反应中形成新共价键的键能之和-反应中断裂旧共价键的键能之和 |
您最近一年使用:0次
2019-06-10更新
|
5085次组卷
|
30卷引用:山西省祁县第二中学校2020届高三上学期期中考试化学试题
山西省祁县第二中学校2020届高三上学期期中考试化学试题2019年江苏省高考化学试题(已下线)专题07 化学反应中的能量变化——2019年高考真题和模拟题化学分项汇编陕西省渭南市临渭区尚德中学2020届高三上学期第三次月考化学试题陕西省西安中学2020届高三上学期第三次月考化学试题2019年秋高三化学复习强化练习——化学反应的方向及判断(已下线)专题九 化学能与热能(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训广西桂林市第十八中学2019-2020学年高二下学期开学考试化学试题(已下线)第六章能力提升检测卷-2021年高考化学一轮复习讲练测江苏省镇江市吕叔湘中学2019-2020学年高二下学期期中考试化学试题湖南省衡阳市第二十六中学2021届高三上学期9月月考化学试题江苏省苏州市新草桥中学2019-2020学年高二下学期6月月考化学试题(已下线)小题必刷23 焓变与热化学方程式——2021年高考化学一轮复习小题必刷(通用版)(已下线)小题必刷24 盖斯定律及反应热计算——2021年高考化学一轮复习小题必刷(通用版)湖北省荆州中学2020-2021学年高二12月月考化学试题(已下线)【镇江新东方】高二下21心湖期中安徽省淮北市树人高级中学2020-2021学年高二上学期第四阶段考试化学试题福建省厦门第一中学2020-2021学年高二上学期期中考试化学试题重庆市缙云教育联盟2020-2021学年高二上学期期末考试化学试题辽宁省沈阳市郊联体2021届高三上学期期末考试化学试题黑龙江省哈尔滨市呼兰区第一中学校等三校2020-2021学年高二上学期期末联考化学试题(已下线)专题05 化学反应与能量——备战2021年高考化学纠错笔记(已下线)【浙江新东方】高中化学20210304-003(已下线)课时29 盖斯定律及反应热计算-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点17 化学反应的热效应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)2019年高考江苏卷化学试题变式题(不定项选择题)天津市武清区城关中学2023-2024学年高三上学期第二次阶段性练习化学试题重庆十八中两江实验中学校2022-2023学年高二上学期第一次月考化学试题
名校
8 . pC类似于pH,是指极稀溶液中的溶质浓度的常用对数的负值。如某溶液中某溶质的浓度为1×10-3mol·L-1,则该溶液中该溶质的pC=-lg(1×10-3) = 3。下图为25℃时H2CO3溶液的pC-pH图(若离子浓度小于10-5 mol·L-1,可认为该离子不存在)。下列说法错误的是


| A.向Na2CO3溶液中滴加盐酸至pH等于11时,溶液中:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-)+c(Cl-) |
| B.25℃时,H2CO3的一级电离平衡常数Ka1= 10-6 |
| C.25℃时,CO2饱和溶液的浓度是0.05 mol·L-1,其中1/5的CO2转变为H2CO3,若此时溶液的pH 约为5,据此可得该温度下CO2饱和溶液中H2CO3的电离度约为1% |
| D.25℃时,0.1 mol·L-1,的Na2CO3和0.1 mol·L-1的NaHCO3混合溶液中离子浓度的大小为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
您最近一年使用:0次
2018-03-27更新
|
1064次组卷
|
7卷引用:山西省吕梁市2018届高三上学期第一次模拟考试化学试题
山西省吕梁市2018届高三上学期第一次模拟考试化学试题山东省新泰市第一中学2019届高三上学期第二次质量检测化学试题【市级联考】安徽省黄山市2018-2019学年高二上学期期末考试化学试题安徽省阜阳市第三中学2018-2019学年高一下学期期末考试化学试题夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——电解质溶液中的曲线问题(提升练习)(已下线)本册综合检测(一)——2020-2021学年高二化学选修四同步单元AB卷(人教版)(已下线)2022年湖北省高考真题变式题11-15
9 . 甲醇是重要的化工原料,利用煤化工中生产的CO和H2可制取甲醇,发生的反应为CO(g)+2H2(g)  CH3OH(g) △H=-99kJ/mol。
CH3OH(g) △H=-99kJ/mol。
(1)关于该反应的下列说法,错误的是___________ 。
A.消耗CO和消耗CH3OH的速率相等时,说明该反应达到平衡状态
B.升高温度,正反应速率减小,逆反应速率增大
C.使用催化剂,可以提高CO的转化率
D.增大压强,该反应的化学平衡常数不变
(2)在某温度时,将1.0mol CO 与2.0 mol H2充入2 L的空钢瓶中,发生上述反应,在第5 min时达到化学平衡状态,此时甲醇的物质的量分数为10%。甲醇浓度的变化状况如图所示:

①从反应开始到5 min 时,生成甲醇的平均速率为________ 。
②5 min 时达到平衡,H2的平衡转化率α=_____ %.化学平衡常数K= _______ 。
③1min 时的v正(CH3OH)______ 4min 时v逆(CH3OH ) (填“大于“小于“或“等于”)。
④若将钢瓶换成同容积的绝热钢瓶,重复上述实验,平衡时甲醇的物质的量分数_____ 0.1(填“>”“<”或“=”)
 CH3OH(g) △H=-99kJ/mol。
CH3OH(g) △H=-99kJ/mol。(1)关于该反应的下列说法,错误的是
A.消耗CO和消耗CH3OH的速率相等时,说明该反应达到平衡状态
B.升高温度,正反应速率减小,逆反应速率增大
C.使用催化剂,可以提高CO的转化率
D.增大压强,该反应的化学平衡常数不变
(2)在某温度时,将1.0mol CO 与2.0 mol H2充入2 L的空钢瓶中,发生上述反应,在第5 min时达到化学平衡状态,此时甲醇的物质的量分数为10%。甲醇浓度的变化状况如图所示:

①从反应开始到5 min 时,生成甲醇的平均速率为
②5 min 时达到平衡,H2的平衡转化率α=
③1min 时的v正(CH3OH)
④若将钢瓶换成同容积的绝热钢瓶,重复上述实验,平衡时甲醇的物质的量分数
您最近一年使用:0次
名校
10 . 下列有关说法正确的是
A.一定条件下反应N2+3H2 2NH3,达到平衡时,3v正(H2)=2v正(NH3) 2NH3,达到平衡时,3v正(H2)=2v正(NH3) |
| B.25℃时,0.1 mol/L的NaHB溶液呈酸性,说明H2B为强酸 |
| C.将pH=a+1的氨水稀释为pH=a的过程中,c(OH-)/c(NH3•H2O)变小 |
| D.10mL浓度为1mol/L的盐酸与过量的Zn粉反应,若加入适量的CH3COONa溶液,既能降低反应速率,又不影响H2的生成 |
您最近一年使用:0次
2019-01-08更新
|
392次组卷
|
2卷引用:【全国百强校】山西省长治市第二中学2018-2019学年高二上学期第二次月考(期中)化学试题



