解题方法
1 . 聚乙烯醇生产过程中会产生大量副产物乙酸甲酯,其催化醇解反应可用于制备甲醇和乙酸己酯,该反应的化学方程式为:
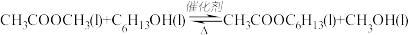
已知v正=k正χ(CH3COOCH3)·χ(C6H13OH),v逆=k逆χ(CH3COOC6H13)·χ(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,χ为备组分的物质的量分数。
(1)反应开始时,己醇和乙酸甲酯按物质的量之比1:1投料,测得348K、343K、338K三个温度下乙酸甲酯转化率(α)随时间(t)的变化关系如图所示。

该醇解反应的
_______ 0(填>或<)。348K时,以物质的量分数表示的化学平衡常数KX=________ (保留2位有效数字)。
在曲线①、②、③中,k正—k逆值最小的曲线是______________ ;A、B、C、D四点中,v正最小的是_____________ ,v逆最大的是_________________ 。
(2)343K时,乙酸甲酯和己醇按物质的量之比1:1、1:2和2:1进行初始投料。则达到甲衡后,初始投料比__________ 时,乙酸甲酯转化率最大;与按2:1投料相比,按1:2投料时化学平衡常数KX_____________ (填增大、减小或不变)。
(3)该醇解反应使用离子交换树脂作催化剂,下列关于该催化剂的说法不正确的是_______
a.参与了醇解反应,但并不改变反应历程 b.使k正和k逆增大相同倍数
c.降低了醇解反应的活化能 d.提高乙酸甲酯的平衡转化率
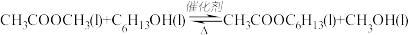
已知v正=k正χ(CH3COOCH3)·χ(C6H13OH),v逆=k逆χ(CH3COOC6H13)·χ(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,χ为备组分的物质的量分数。
(1)反应开始时,己醇和乙酸甲酯按物质的量之比1:1投料,测得348K、343K、338K三个温度下乙酸甲酯转化率(α)随时间(t)的变化关系如图所示。

该醇解反应的

在曲线①、②、③中,k正—k逆值最小的曲线是
(2)343K时,乙酸甲酯和己醇按物质的量之比1:1、1:2和2:1进行初始投料。则达到甲衡后,初始投料比
(3)该醇解反应使用离子交换树脂作催化剂,下列关于该催化剂的说法不正确的是
a.参与了醇解反应,但并不改变反应历程 b.使k正和k逆增大相同倍数
c.降低了醇解反应的活化能 d.提高乙酸甲酯的平衡转化率
您最近一年使用:0次
名校
解题方法
2 .  和
和 是两种主要的温室气体,以
是两种主要的温室气体,以 和
和 为原料制造更高价值的化学产品是用来缓解温室效应的研究方向,回答下列问题:
为原料制造更高价值的化学产品是用来缓解温室效应的研究方向,回答下列问题:
(1)工业上 催化重整是目前大规模制取合成气(CO和H2混合气称为合成气)的重要方法,其原理为:
催化重整是目前大规模制取合成气(CO和H2混合气称为合成气)的重要方法,其原理为:
反应Ⅰ: ;
;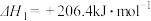
反应Ⅱ: ;
;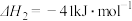
 和
和 反应生成
反应生成 和
和 的热化学方程式是
的热化学方程式是___________________ 。
(2)将1 mol 和1 mol
和1 mol  加入恒温恒压的密闭容器中(温度298K、压强100kPa),发生反应Ⅰ,不考虑反应Ⅱ的发生,该反应中,正反应速率
加入恒温恒压的密闭容器中(温度298K、压强100kPa),发生反应Ⅰ,不考虑反应Ⅱ的发生,该反应中,正反应速率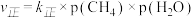 ,p为分压(分压=总压×物质的量分数),若该条件下
,p为分压(分压=总压×物质的量分数),若该条件下 ,当
,当 分解20%时,
分解20%时,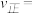
__________ kPa∙s-1。
(3)将 和
和 在一定条件下反应可制得合成气,在1 L密闭容器中通入
在一定条件下反应可制得合成气,在1 L密闭容器中通入 与
与 ,使其物质的量浓度均为
,使其物质的量浓度均为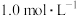 ,在一定条件下发生反应:
,在一定条件下发生反应: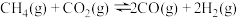 ,测得CH4的平衡转化率与温度及压强的关系如下图所示:
,测得CH4的平衡转化率与温度及压强的关系如下图所示:
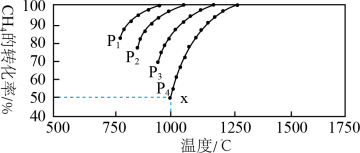
①压强 、
、 、
、 、
、 由小到大的关系为
由小到大的关系为_________ 。
②对于气相反应,用某组分(B)的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数(记作 ),如果
),如果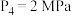 ,求x点的平衡常数
,求x点的平衡常数
________________ (用平衡分压代替平衡浓度计算)。
③下列措施中能使平衡正向移动的是___________ (填字母)。
a.升高温度
b.增大压强
c.保持温度、压强不变,充入He
d.恒温、恒容,再充入1 mol 和1 mol
和1 mol 
(4)科学家还研究了其他转化温室气体的方法,利用图所示装置可以将 转化为气体燃料CO(电解质溶液为稀硫酸),该装置工作时,M为
转化为气体燃料CO(电解质溶液为稀硫酸),该装置工作时,M为_________ 极(填“正”或“负”),导线中通过2 mol电子后,假定体积不变M极电解质溶液的pH__________ (填“增大”、“减小”或“不变”),N极电解质溶液变化的质量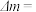
__________ g。

 和
和 是两种主要的温室气体,以
是两种主要的温室气体,以 和
和 为原料制造更高价值的化学产品是用来缓解温室效应的研究方向,回答下列问题:
为原料制造更高价值的化学产品是用来缓解温室效应的研究方向,回答下列问题:(1)工业上
 催化重整是目前大规模制取合成气(CO和H2混合气称为合成气)的重要方法,其原理为:
催化重整是目前大规模制取合成气(CO和H2混合气称为合成气)的重要方法,其原理为:反应Ⅰ:
 ;
;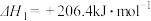
反应Ⅱ:
 ;
;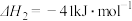
 和
和 反应生成
反应生成 和
和 的热化学方程式是
的热化学方程式是(2)将1 mol
 和1 mol
和1 mol  加入恒温恒压的密闭容器中(温度298K、压强100kPa),发生反应Ⅰ,不考虑反应Ⅱ的发生,该反应中,正反应速率
加入恒温恒压的密闭容器中(温度298K、压强100kPa),发生反应Ⅰ,不考虑反应Ⅱ的发生,该反应中,正反应速率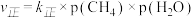 ,p为分压(分压=总压×物质的量分数),若该条件下
,p为分压(分压=总压×物质的量分数),若该条件下 ,当
,当 分解20%时,
分解20%时,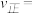
(3)将
 和
和 在一定条件下反应可制得合成气,在1 L密闭容器中通入
在一定条件下反应可制得合成气,在1 L密闭容器中通入 与
与 ,使其物质的量浓度均为
,使其物质的量浓度均为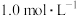 ,在一定条件下发生反应:
,在一定条件下发生反应: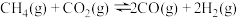 ,测得CH4的平衡转化率与温度及压强的关系如下图所示:
,测得CH4的平衡转化率与温度及压强的关系如下图所示:
①压强
 、
、 、
、 、
、 由小到大的关系为
由小到大的关系为②对于气相反应,用某组分(B)的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数(记作
 ),如果
),如果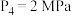 ,求x点的平衡常数
,求x点的平衡常数
③下列措施中能使平衡正向移动的是
a.升高温度
b.增大压强
c.保持温度、压强不变,充入He
d.恒温、恒容,再充入1 mol
 和1 mol
和1 mol 
(4)科学家还研究了其他转化温室气体的方法,利用图所示装置可以将
 转化为气体燃料CO(电解质溶液为稀硫酸),该装置工作时,M为
转化为气体燃料CO(电解质溶液为稀硫酸),该装置工作时,M为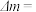

您最近一年使用:0次
2020-05-09更新
|
439次组卷
|
2卷引用:山东省枣庄市2020届高三模拟考试(二调)化学试题
3 . 氮、碳氧化物的排放会对环境造成污染。多年来化学工作者对氮、碳的氧化物做了广泛深入的研究并取得一些重要成果。
I.已知2NO(g)+O2(g) 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
第一步:2NO(g) N2O2(g) (快) ∆H1<0;
N2O2(g) (快) ∆H1<0;
v1正=k1正c2(NO) ;v1逆=k1逆c(N2O2)
第二步:N2O2(g)+O2(g) 2NO2(g) (慢) ∆H2< 0;
2NO2(g) (慢) ∆H2< 0;
v2正=k2正c(N2O2)c(O2);v2逆=k2逆c2(NO2)
①在两步的反应中,哪一步反应的活化能更大___ (填“第一步”或“第二步”)。
②一定温度下,反应2NO(g)+O2(g) 2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=
2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=____________ ;
II.(1)利用CO2和CH4重整不仅可以获得合成气(主要成分为CO、H2),还可减少温室气体的排放。已知重整过程中部分反应的热化方程式为:
① CH4(g)=C(s)+2H2(g) ΔH1>0
② CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2>0
③ CO(g)+H2(g)=C(s)+H2O(g) ΔH3<0
则反应CH4(g)+CO2(g)=2CO(g)+2H2(g)的ΔH=______________________ (用含 ΔH1 、ΔH2 、 ΔH3的代数式表示)若固定n(CO2)=n(CH4),改变反应温度,CO2和CH4的平衡转化率见图甲。


同温度下CO2的平衡转化率大于CH4的平衡转化率,原因是_________ 。
(2)在密闭容器中通入物质的量均为0.1mol的CH4和CO2,在一定条件下发生反应CO2(g) + CH4(g) 2CO(g) + 2H2(g),CH4的平衡转化率与温度及压强(单位Pa)的关系如图乙所示。y点:v(正)
2CO(g) + 2H2(g),CH4的平衡转化率与温度及压强(单位Pa)的关系如图乙所示。y点:v(正)_____ v(逆)(填 “大于”“小于”或“等于”)。已知气体分压(p 分)=气体总压(p 总)× 气体的物质的量分数。用平衡分压代替平衡浓度可以得到平衡常数Kp,求x 点对应温度下反应的平衡常数Kp=__________________ 。
III.根据2CrO42﹣+2H+ Cr2O72﹣+H2O设计如图丙装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图丙中左侧电极连接电源的
Cr2O72﹣+H2O设计如图丙装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图丙中左侧电极连接电源的_________ 极,电解制备过程的总反应化学方程式为_________ 。测定阳极液中Na和Cr的含量,若Na与Cr的物质的量之比为a:b,则此时Na2CrO4的转化率为_________ 。若选择用熔融K2CO3作介质的甲烷(CH4)燃料电池充当电源,则负极反应式为________________ 。
I.已知2NO(g)+O2(g)
 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:第一步:2NO(g)
 N2O2(g) (快) ∆H1<0;
N2O2(g) (快) ∆H1<0;v1正=k1正c2(NO) ;v1逆=k1逆c(N2O2)
第二步:N2O2(g)+O2(g)
 2NO2(g) (慢) ∆H2< 0;
2NO2(g) (慢) ∆H2< 0;v2正=k2正c(N2O2)c(O2);v2逆=k2逆c2(NO2)
①在两步的反应中,哪一步反应的活化能更大
②一定温度下,反应2NO(g)+O2(g)
 2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=
2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=II.(1)利用CO2和CH4重整不仅可以获得合成气(主要成分为CO、H2),还可减少温室气体的排放。已知重整过程中部分反应的热化方程式为:
① CH4(g)=C(s)+2H2(g) ΔH1>0
② CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2>0
③ CO(g)+H2(g)=C(s)+H2O(g) ΔH3<0
则反应CH4(g)+CO2(g)=2CO(g)+2H2(g)的ΔH=


同温度下CO2的平衡转化率大于CH4的平衡转化率,原因是
(2)在密闭容器中通入物质的量均为0.1mol的CH4和CO2,在一定条件下发生反应CO2(g) + CH4(g)
 2CO(g) + 2H2(g),CH4的平衡转化率与温度及压强(单位Pa)的关系如图乙所示。y点:v(正)
2CO(g) + 2H2(g),CH4的平衡转化率与温度及压强(单位Pa)的关系如图乙所示。y点:v(正)III.根据2CrO42﹣+2H+
 Cr2O72﹣+H2O设计如图丙装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图丙中左侧电极连接电源的
Cr2O72﹣+H2O设计如图丙装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图丙中左侧电极连接电源的
您最近一年使用:0次
名校
解题方法
4 . 硼氢化钠(NaBH4)在工业生产中应用广泛。它在催化剂作用下与水反应获取氢气的微观过程如图所示。下列说法正确的是( )
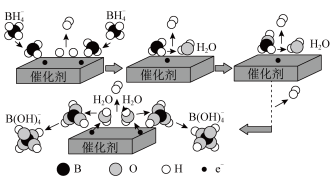

| A.水在此过程中作还原剂 |
| B.若将NaBH4中的H用D代替,反应后生成的气体中含有H2、HD和D2 |
| C.催化剂可以加快反应速率,其用量多少不影响反应速率 |
| D.NaBH4与水反应的离子方程式为:BH4-+4H2O=B(OH)4-+4H2↑ |
您最近一年使用:0次
2020-04-05更新
|
631次组卷
|
3卷引用:山东省枣庄三中、高密一中、莱西一中2020届高三下学期第一次在线联考化学试题
名校
解题方法
5 . 煤的气化和液化是现代能源工业中重点考虑的综合利用技术。最常见的气化方法是用煤作原料生产水煤气,而比较流行的液化方法是煤在催化剂等条件下生产CH3OH。
已知制备甲醇的有关化学反应如下:
①CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H1=-90.8 kJ•mol-1
②CO(g)+H2O(g)⇌CO2(g)+H2(g)△H2=-412 kJ•mol-1
③CO(g)+2H2(g)⇌CH3OH(g)△H3
I.回答下列问题:
(1)欲提高甲醇的产率,可以采取的措施有______ (填字母序号)。
A.升高温度
B.增大压强
C.降低温度
D.降低压强
(2)提高甲醇反应选择性的关键因素是______ 。
(3)保持温度和容积不变,下列描述能说明反应③达到平衡状态的是______ (填字母序号)。
A.v(CO):v(H2):v(CH3OH)=1:2:1
B.混合气体的压强不再随时间的变化而变化
C.单位时间内断裂2 mol H-H键,同时生成3mol C-H键
D.一段时间内的平均反应速率等于0
E.混合气体的平均摩尔质量保持不变
Ⅱ.在一密闭容器中投入1mol CO和2molH2发生反应③,实验测得平衡时甲醇的物质的量随温度、压强变化关系如图1所示:
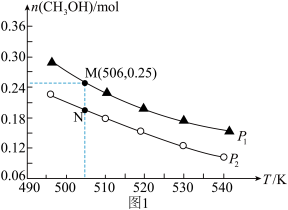
(1)压强P1______ P2(填“>”、“<“或”=”)。
(2)M、N两点的化学反应速率:vM______ vN(填“>”、“<“或“=”)
(3)对于气相反应,用某组分B的平衡压强P(B)代替物质的量浓度c(B)也可表示平衡常数(Kp),则M点时,平衡常数Kp=______ (P1=5 MPa)。
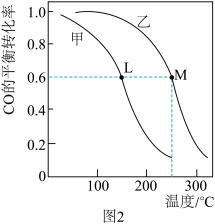
(4)甲、乙两个恒容密闭容器的体积相同,向甲中加入 1molCO和 2mol H2,向乙中加入2mol CO和4molH2,测得不同温度下CO的平衡转化率如图2所示,则L、M两点容器内压强:P(M)______ 2P(L),平衡常数:K(M)______ K(L)(填“>”、“>”或“=”)。
已知制备甲醇的有关化学反应如下:
①CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H1=-90.8 kJ•mol-1
②CO(g)+H2O(g)⇌CO2(g)+H2(g)△H2=-412 kJ•mol-1
③CO(g)+2H2(g)⇌CH3OH(g)△H3
I.回答下列问题:
(1)欲提高甲醇的产率,可以采取的措施有
A.升高温度
B.增大压强
C.降低温度
D.降低压强
(2)提高甲醇反应选择性的关键因素是
(3)保持温度和容积不变,下列描述能说明反应③达到平衡状态的是
A.v(CO):v(H2):v(CH3OH)=1:2:1
B.混合气体的压强不再随时间的变化而变化
C.单位时间内断裂2 mol H-H键,同时生成3mol C-H键
D.一段时间内的平均反应速率等于0
E.混合气体的平均摩尔质量保持不变
Ⅱ.在一密闭容器中投入1mol CO和2molH2发生反应③,实验测得平衡时甲醇的物质的量随温度、压强变化关系如图1所示:

(1)压强P1
(2)M、N两点的化学反应速率:vM
(3)对于气相反应,用某组分B的平衡压强P(B)代替物质的量浓度c(B)也可表示平衡常数(Kp),则M点时,平衡常数Kp=

(4)甲、乙两个恒容密闭容器的体积相同,向甲中加入 1molCO和 2mol H2,向乙中加入2mol CO和4molH2,测得不同温度下CO的平衡转化率如图2所示,则L、M两点容器内压强:P(M)
您最近一年使用:0次
2020-03-09更新
|
180次组卷
|
2卷引用:山东省枣庄市2020届高三上学期期末考试化学试题
名校
解题方法
6 . 钒(V)为过渡元素,可形成多价态化合物,在工业催化、新材料、新能源等领域有广泛应用。
(1)金属钒熔点很高,可由铝热反应制得。
已知25℃、101 KPa时
4A1(s)+3O2(g)═2Al2O3(s)△H1=akJ•mol-1
4V(s)+5O2(g)═2V2O5(s)△H2=bkJ•mol-1
则用铝热反应冶炼金属V(s)的热化学方程式为______ 。
(2)全钒液流电池是一种新型的绿色环保储能系统,工作原理如图所示:

查阅相关资料可知:
①该电池放电时,VO2+发生还原反应,则正极的反应式是______ 。
②当完成储能时,负极溶液的颜色为______ 。
③电池放电时,负极区溶液的pH将______ (填“增大”、“减小”或“不变”)。
④用该钒电池在铁制品上镀铜,铁制品应与电池的______ 极(填“A“或“B“)相连。若电镀开始时两电极质量相等,电镀一段时间后,两电极质量之差为128g,此时转移电子的物质的量为______ 。
(1)金属钒熔点很高,可由铝热反应制得。
已知25℃、101 KPa时
4A1(s)+3O2(g)═2Al2O3(s)△H1=akJ•mol-1
4V(s)+5O2(g)═2V2O5(s)△H2=bkJ•mol-1
则用铝热反应冶炼金属V(s)的热化学方程式为
(2)全钒液流电池是一种新型的绿色环保储能系统,工作原理如图所示:

查阅相关资料可知:
| 离子种类 | VO2+ | VO2+ | V3+ | V2+ |
| 颜色 | 黄色 | 蓝色 | 绿色 | 紫色 |
①该电池放电时,VO2+发生还原反应,则正极的反应式是
②当完成储能时,负极溶液的颜色为
③电池放电时,负极区溶液的pH将
④用该钒电池在铁制品上镀铜,铁制品应与电池的
您最近一年使用:0次
2020-03-09更新
|
129次组卷
|
2卷引用:山东省枣庄市2020届高三上学期期末考试化学试题
名校
7 . 已知X和Y能发生如下反应:X+Y=H2O+盐,下列有关物质X和Y所属种类的判断中一定不正确的是( )
| A.X为酸、Y为碱 | B.X为碱性氧化物、Y为酸 |
| C.X为盐、Y为碱 | D.X为碱性氧化物、Y为酸性氧化物 |
您最近一年使用:0次
2018-09-12更新
|
1837次组卷
|
31卷引用:【全国百强校】山东省枣庄市第八中学东校区2019届高三9月月考化学试题
【全国百强校】山东省枣庄市第八中学东校区2019届高三9月月考化学试题云南省峨山彝族自治县峨山一中2018-2019学年高二入学考试化学试题贵州省毕节市织金县第一中学2018-2019学年高一上学期12月份考试化学试题鲁科版新教材(2019)化学同步2.1.1 元素与物质的关系 物质分类与物质性质福建省莆田市第六中学2019-2020学年高一上学期第一次月考化学试题(B)备战2020高考化学二轮专项训练:多角度考查物质变化云南省福贡县第一中学2019-2020学年高一上学期期末考试化学试题人教版高一化学必修1第二章《化学物质及其变化》测试卷(已下线)专题2.1 物质的分类 胶体 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》(已下线)2.1.1 元素与物质的关系 物质分类与物质性质练习(2)——《高中新教材同步备课》(鲁科版 必修第一册)(已下线)专题01 物质的分类及转化(核心素养卷)——【新教材精创】2019-2020学年高中化学新教材知识讲学广东省深圳市第七高级中学2020-2021学年高一上学期第一学段考试化学试题(已下线)练习2 物质的转化-2020-2021学年【补习教材·寒假作业】高一化学(苏教版)(已下线)衔接点02 酸碱盐的分类和命名-2021年初升高化学无忧衔接(已下线)课时03 物质的组成、分类和性质-2022年高考化学一轮复习小题多维练(全国通用)福建省漳州市正兴学校2020-2021学年高二下学期期末考试化学试题陕西省西安市长安区第一中学2021-2022学年高二下学期期中考试化学试题(已下线)衔接点03 酸碱盐的分类和命名-2022年初升高化学无忧衔接(已下线)第01练 物质的分类及转化-2023年高考化学一轮复习小题多维练(全国通用)广东省揭阳华侨高级中学2021-2022学年高一上学期第一次阶段考试化学试题黑龙江省哈尔滨市第一中学2021-2022学年高一上学期期中考试化学试题 甘肃省兰州市西固区三校2021-2022学年高一上学期期中联考化学试题广西钦州市第四中学2021-2022学年高一上学期期中考试化学试题吉林省长春外国语学校2022-2023学年高一上学期第一次月考化学试题山东省“学情空间”区域教研共同体2022-2023学年高一上学期10月联考(人教版)化学试题甘肃省天水市第一中学2022-2023学年高一上学期第一学段检测化学试题(已下线)第二章 化学物质及其变化 第1讲 物质的变化及分类第2课时 物质的转化甘肃省部分学校2023-2024学年高一上学期10月期中考试化学试题湖北省荆州市沙市中学2023-2024学年高一上学期9月月考化学试题河北省石家庄北华中学2023-2024学年高一上学期10月月考考试化学试题
名校
8 . 下列物质间相互发生反应时:①Na+O2 ②Fe+Cl2 ③AgNO3溶液+氨水 ④KI溶液+AgNO3溶液 ⑤Na2CO3+C6H5COOH ⑥AlCl3+KOH ⑦P+Cl2 ⑧Cu+HNO3;在不同条件下得到不同产物的是( )
| A.除②④⑤ | B.除②④ | C.除④⑥ | D.除④⑤⑥ |
您最近一年使用:0次
2018-09-08更新
|
347次组卷
|
5卷引用:【全国百强校】山东省枣庄市第八中学东校区2019届高三9月月考化学试题
【全国百强校】山东省枣庄市第八中学东校区2019届高三9月月考化学试题【全国百强校】黑龙江省大庆实验中学2019届高三上学期第一次月考化学试题辽宁省大连市第二十四中学2020届高三上学期阶段联合考试化学试题(已下线)专题2.2 离子反应-巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》山东省邹城市兖矿第一中学2021届高三上学期9月份月考化学试题
名校
解题方法
9 . 铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大.回答下列问题:
(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+ CO(g)═Fe(s)+CO2(g)△H1
Fe2O3(s)+1/3CO(g)═ 2/3Fe3O4(s)+ 1/3 CO2(g)△H2
Fe3O4(s)+ CO(g)═3Fe(s)+CO2(g)△H3
Fe2O3(s)+ CO(g)═2Fe(s)+3CO2(g)△H4
则△H4 的表达式为_____ (用含△H1、△H2、△H3 的代数式表示)。
(2)上述反应在高炉中大致分为三个阶段,各阶段主要成分与温度的关系如下:
1600℃时固体物质的主要成分为_____ ,该温度下若测得固体混合物中 m(Fe):m(O)=35:2, 则 FeO 被 CO 还原为 Fe 的百分率为_________ (设其它固体杂质中不含 Fe、O 元素)。
(3)铁等金属可用作 CO 与氢气反应的催化剂.已知某种催化剂可用来催化反应 CO(g)+3H2(g) = CH4(g) +H2O(g)△H<0.在 T℃,106Pa 时将 l mol CO 和 3mol H2 加入体积可变的密闭容器 中.实验测得 CO 的体积分数 x(CO)如下表:
①能判断 CO(g)+3H2(g)⇌ CH4(g)+H2O(g)达到平衡的是_____ (填序号)。
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v 正(CO)=3v 逆(H2) d.混合气体的平均相对分子质量不再发生变化
②达到平衡时 CO 的转化率为___________ ;在 T℃106Pa 时该反应的压强平衡常数 Kp(用平衡分 压代替平衡浓度计算,分压=总压×物质的量分数)的计算式为_____ 。
③图表示该反应 CO 的平衡转化率与温度、压强的关系.图中温度 T1、T2、T3 由高到低的顺序是_____ ,理由是_____________ .

(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+ CO(g)═Fe(s)+CO2(g)△H1
Fe2O3(s)+1/3CO(g)═ 2/3Fe3O4(s)+ 1/3 CO2(g)△H2
Fe3O4(s)+ CO(g)═3Fe(s)+CO2(g)△H3
Fe2O3(s)+ CO(g)═2Fe(s)+3CO2(g)△H4
则△H4 的表达式为
(2)上述反应在高炉中大致分为三个阶段,各阶段主要成分与温度的关系如下:
| 温度 | 250℃ | 600℃ | 1000℃ | 2000℃ |
| 主要成分 | Fe2O3 | Fe3O4 | FeO | Fe |
1600℃时固体物质的主要成分为
(3)铁等金属可用作 CO 与氢气反应的催化剂.已知某种催化剂可用来催化反应 CO(g)+3H2(g) = CH4(g) +H2O(g)△H<0.在 T℃,106Pa 时将 l mol CO 和 3mol H2 加入体积可变的密闭容器 中.实验测得 CO 的体积分数 x(CO)如下表:
t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| x(CO) | 0.25 | 0.23 | 0.214 | 0.202 | 0.193 | 0.193 |
①能判断 CO(g)+3H2(g)⇌ CH4(g)+H2O(g)达到平衡的是
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v 正(CO)=3v 逆(H2) d.混合气体的平均相对分子质量不再发生变化
②达到平衡时 CO 的转化率为
③图表示该反应 CO 的平衡转化率与温度、压强的关系.图中温度 T1、T2、T3 由高到低的顺序是

您最近一年使用:0次
2016-12-09更新
|
243次组卷
|
3卷引用:【全国百强校】山东省枣庄市第三中学新城校区2019届高三上学期12月月考理科综合化学试题
10 . 铁、铜及其化合物在工农业生产中应用广泛。
(1)在潮湿空气中,钢铁发生电化学腐蚀转化为Fe(OH)2的反应方程式为_______ 。在含有等浓度硫酸溶液的下列装置中,铁腐蚀的速率由快到慢的顺序是____________ (用序号填写)。
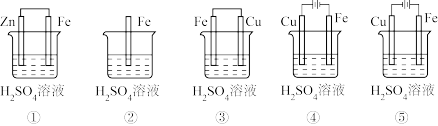
(2)已知:①3Fe(s)+2O2(g)=Fe3O4(s) H=-1118 kJ·mol-1
H=-1118 kJ·mol-1
②2Al(s)+3/2O2(g)=A12O3(s) H=-1675.7 kJ·mol-1
H=-1675.7 kJ·mol-1
则焊接钢轨时铝与Fe3O4发生反应生成铁和Al2O3的热化学方程式为______________ 。
(3)Na2FeO4具有强氧化性,其电解制法如图所示,请写出阳极的电极反应式______ 。Na2FeO4是一种既能杀菌、消毒,又能絮凝净水的水处理剂,其原理是______________ 。
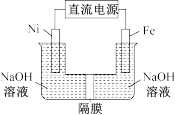
(4)工业上常用FeCl3溶液腐蚀印刷线路板,发生反应的离子方程式是____________ 。若腐蚀铜板后的溶液中,Cu2+、Fe3+和Fe2+浓度均为0.1 mol·L-1,结合下图分析,当混合溶液中通入氨气调节溶液的pH=5.6时,溶液中存在的金属阳离子为____ 。从图中数据计算Fe(OH)2的溶度积Ksp[Fe(OH)2]=______ 。
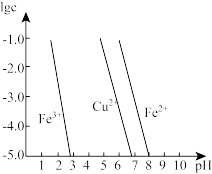
已知:横坐标为溶液的pH,纵坐标为金属离子的物质的量浓度的对数(当溶液中金属离子浓度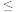 10-5mol·L-1时,可认为沉淀完全)。
10-5mol·L-1时,可认为沉淀完全)。
(1)在潮湿空气中,钢铁发生电化学腐蚀转化为Fe(OH)2的反应方程式为
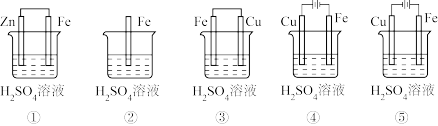
(2)已知:①3Fe(s)+2O2(g)=Fe3O4(s)
 H=-1118 kJ·mol-1
H=-1118 kJ·mol-1②2Al(s)+3/2O2(g)=A12O3(s)
 H=-1675.7 kJ·mol-1
H=-1675.7 kJ·mol-1则焊接钢轨时铝与Fe3O4发生反应生成铁和Al2O3的热化学方程式为
(3)Na2FeO4具有强氧化性,其电解制法如图所示,请写出阳极的电极反应式

(4)工业上常用FeCl3溶液腐蚀印刷线路板,发生反应的离子方程式是

已知:横坐标为溶液的pH,纵坐标为金属离子的物质的量浓度的对数(当溶液中金属离子浓度
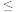 10-5mol·L-1时,可认为沉淀完全)。
10-5mol·L-1时,可认为沉淀完全)。
您最近一年使用:0次
2016-12-09更新
|
822次组卷
|
3卷引用:2015届山东省枣庄市六中高三下学期开学初检测试题理综化学试卷



