名校
解题方法
1 . 依据事实,写出下列反应的热化学方程式
(1)化合物AX3和单质X2在一定条件下反应可生成化合物AX5.回答下列问题:已知AX3的熔点和沸点分别为-93.6℃和76℃,AX5的熔点为167℃。室温时AX3与气体X2反应生成1molAX5,放出热量123.8kJ。该反应的热化学方程式为_______ 。
(2)在25℃、101kPa下,一定质量的无水乙醇完全燃烧时放出热量QkJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100gCaCO3沉淀,则乙醇燃烧的热化学方程式为_______ 。
(3)化学反应N2+3H2=2NH3的能量变化如图所示

试写出N2(g)和H2(g)反应生成NH3(l)的热化学方程式:_______ 。
(4)NaBH4(s)与H2O(l)反应生成NaBO2(s)和氢气,在25℃、101kPa下,已知每消耗3.8gNaBH4(s)放热21.6kJ,该反应的热化学方程式是_______ 。
(5)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下2gSiH4自燃放出热量89.2kJ。SiH4自燃的热化学方程式为_______ 。
(6)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式_______ 。

(1)化合物AX3和单质X2在一定条件下反应可生成化合物AX5.回答下列问题:已知AX3的熔点和沸点分别为-93.6℃和76℃,AX5的熔点为167℃。室温时AX3与气体X2反应生成1molAX5,放出热量123.8kJ。该反应的热化学方程式为
(2)在25℃、101kPa下,一定质量的无水乙醇完全燃烧时放出热量QkJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100gCaCO3沉淀,则乙醇燃烧的热化学方程式为
(3)化学反应N2+3H2=2NH3的能量变化如图所示

试写出N2(g)和H2(g)反应生成NH3(l)的热化学方程式:
(4)NaBH4(s)与H2O(l)反应生成NaBO2(s)和氢气,在25℃、101kPa下,已知每消耗3.8gNaBH4(s)放热21.6kJ,该反应的热化学方程式是
(5)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下2gSiH4自燃放出热量89.2kJ。SiH4自燃的热化学方程式为
(6)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式

您最近一年使用:0次
2 . 下列关于热化学方程式的叙述正确的是
| A.已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定 |
| B.已知2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ•mol -1,则H2燃烧热为241.8kJ•mol -1 |
| C.中和热的测定实验中,氢氧化钠分批加入,反应更充分,测定的中和热数值误差更小 |
| D.S(g)+O2(g) =SO2(g) ΔH1; S(s)+O2(g) =SO2(g) ΔH2,则ΔH1<ΔH2 |
您最近一年使用:0次
名校
3 . 已知充分燃烧a g乙烯气体时生成1 mol二氧化碳气体和液态水,并放出热量b kJ,则乙烯燃烧的热化学方程式正确的是
| A.C2H4(g)+3O2(g)=2CO2(g)+2H2O(l) ΔH=-2b kJ/mol |
| B.C2H4(g)+3O2(g)=2CO2(g)+2H2O(l) ΔH=+2b kJ/mol |
| C.2C2H4(g)+6O2(g)=4CO2(g)+4H2O(l) ΔH=-2b kJ/mol |
| D.2C2H4(g)+6O2(g)=4CO2(g)+4H2O(l) ΔH=+b kJ/mol |
您最近一年使用:0次
2021-06-23更新
|
553次组卷
|
4卷引用:甘肃省静宁县第一中学2020-2021学年高一下学期第三次月考化学(普通班)试题
甘肃省静宁县第一中学2020-2021学年高一下学期第三次月考化学(普通班)试题山东省济宁市微山县第二中学2021-2022学年高二上学期第一学段考试化学试题(已下线)1.3 燃料的合理利用-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)1.3 燃料的合理利用-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)
名校
4 . 能源是人类赖以生存和发展的重要物质基础,常规能源的合理利用和新能源的合理开发是当今社会面临的严峻课题。回答下列问题:
(1)乙醇是未来内燃机的首选环保型液体燃料。2.0 g乙醇完全燃烧生成液态水放出59.43 kJ的热量,则乙醇燃烧的热化学方程式____ 。
(2)在C3H8(g)=C3H6(g)+H2(g) ΔH=+b kJ·mol-1(b>0)的反应中,反应物具有的总能量____ (填“大于”“等于”或“小于”)生成物具有的总能量,那么在发生该反应时,反应物就需要_____ (填“放出”或“吸收”)能量才能转化为生成物。
(3)关于用水制取二次能源氢气,以下研究方向不正确的是_______ (填序号)。
A.组成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二次能源
B.设法将太阳光聚焦,产生高温,使水分解产生氢气
C.寻找高效催化剂,使水分解产生氢气,同时释放能量
D.寻找特殊催化剂,用于开发廉价能源,以分解水制取氢气
(4)二氧化碳是引起“温室效应”的主要物质,节能减排以及高效利用能源能够减少二氧化碳
的排放。有一种用CO2生产甲醇燃料的方法:
已知:①CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH=-a kJ·mol-1
②CH3OH(g)=CH3OH(l) ΔH=-b kJ·mol-1
③2H2(g)+O2(g)=2H2O(g) ΔH=-c kJ·mol-1
④H2O(g)=H2O(l) ΔH=-d kJ·mol-1
则表示CH3OH(l) 燃烧热的热化学方程式为____ 。
(5)化工发展是我国能源安全的重要保证。近年来,我国煤化工技术获得重大突破,利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇(CH3OH)是其中的一个研究项目。该研究发生的主要反应之一如下:
CO与H2反应合成甲醇:CO(g)+2H2(g)⇌CH3OH(g)
提示:甲醇的电子式: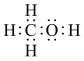 、结构式:
、结构式: 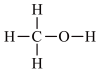
若生成1mol CH3OH放出 a kJ的能量,反应中拆开1mol化学键所需的能量(E)的相关数据如下:
根据相关数据计算拆开1molC O所需的能量E1=
O所需的能量E1=____ kJ。
(1)乙醇是未来内燃机的首选环保型液体燃料。2.0 g乙醇完全燃烧生成液态水放出59.43 kJ的热量,则乙醇燃烧的热化学方程式
(2)在C3H8(g)=C3H6(g)+H2(g) ΔH=+b kJ·mol-1(b>0)的反应中,反应物具有的总能量
(3)关于用水制取二次能源氢气,以下研究方向不正确的是
A.组成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二次能源
B.设法将太阳光聚焦,产生高温,使水分解产生氢气
C.寻找高效催化剂,使水分解产生氢气,同时释放能量
D.寻找特殊催化剂,用于开发廉价能源,以分解水制取氢气
(4)二氧化碳是引起“温室效应”的主要物质,节能减排以及高效利用能源能够减少二氧化碳
的排放。有一种用CO2生产甲醇燃料的方法:
已知:①CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH=-a kJ·mol-1
②CH3OH(g)=CH3OH(l) ΔH=-b kJ·mol-1
③2H2(g)+O2(g)=2H2O(g) ΔH=-c kJ·mol-1
④H2O(g)=H2O(l) ΔH=-d kJ·mol-1
则表示CH3OH(l) 燃烧热的热化学方程式为
(5)化工发展是我国能源安全的重要保证。近年来,我国煤化工技术获得重大突破,利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇(CH3OH)是其中的一个研究项目。该研究发生的主要反应之一如下:
CO与H2反应合成甲醇:CO(g)+2H2(g)⇌CH3OH(g)
提示:甲醇的电子式:
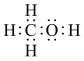 、结构式:
、结构式: 
若生成1mol CH3OH放出 a kJ的能量,反应中拆开1mol化学键所需的能量(E)的相关数据如下:
| 化学键 | H—H | C—O | CO中的 C O O | H—O | C—H |
| E(kJ) | m | n | E1 | x | y |
根据相关数据计算拆开1molC
 O所需的能量E1=
O所需的能量E1=
您最近一年使用:0次
5 . 关于化学反应中能量变化的说法正确的是( )
| A.在CO2中,Mg燃烧生成MgO和C。该反应中化学能全部转化为热能 |
| B.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同 |
| C.CO(g)的燃烧热是283.0kJ·mol-1,则2CO2(g)=2CO(g)+O2(g)反应的ΔH=+566.0kJ·mol-1 |
| D.催化剂能改变反应的焓变 |
您最近一年使用:0次
2020-11-28更新
|
198次组卷
|
5卷引用:甘肃省平凉市2022-2023学年高三上学期11月期中化学试题
名校
解题方法
6 . 下列热化学方程式中△H的绝对值能表示可燃物的燃烧热的是
| A.H2(g)+Cl2(g)=2HCl(g) △H=-184.6kJ/mol | B.C(s)+ O2(g)=CO(g) △H=-110.5kJ/mol O2(g)=CO(g) △H=-110.5kJ/mol |
| C.2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ/mol | D.CO(g)+ O2(g)=CO2(g) △H=-283kJ/mol O2(g)=CO2(g) △H=-283kJ/mol |
您最近一年使用:0次
7 . 已知反应:①2C(s)+O2(g)=2CO(g)△H=-221 kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(1) △H=-57.3kJ/mol
下列结论正确的是
②稀溶液中,H+(aq)+OH-(aq)=H2O(1) △H=-57.3kJ/mol
下列结论正确的是
| A.①的反应热为221kJ/mol |
| B.碳的燃烧热等于110.5kJ/mol |
| C.稀H2SO4和稀NaOH溶液反应的中和热为57.3kJ/mol |
| D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ/mol |
您最近一年使用:0次
2020-03-23更新
|
410次组卷
|
16卷引用:甘肃省庄浪县第一中学2020-2021学年高二上学期第二学段考试化学试题
甘肃省庄浪县第一中学2020-2021学年高二上学期第二学段考试化学试题(已下线)2012-2013学年湖南省益阳市一中高二上学期期末考试理科化学试卷(已下线)2014-2015学年北京市第六十六中学高二上第一次质量检测化学试卷(已下线)2014-2015学年山西省山大附中高二上学期期中化学试卷2015-2016学年海南省国科园实验学校高一下学期期末考试化学试卷2016-2017学年河南省郸城中学高二上第一次考试化学卷2016-2017学年贵州省贵阳六中高二上10月月考化学卷天津市杨柳青一中2017-2018第一学期高二第一次化学月考广东省肇庆市实验中学2017-2018学年高二上学期期中考试化学(理)试题云南省峨山彝族自治县第一中学2017-2018学年高二12月月考(理)化学试题河南省林州市林虑中学2019-2020学年高二3月线上考试化学试题贵州省思南中学2020-2021学年高二上学期期中考试化学试题(已下线)专题09 化学反应与能量变化-备战2022年高考化学学霸纠错(全国通用)湖北省枣阳一中2021-2022学年高二上学期10月月考化学试题广东省肇庆市实验中学2021-2022学年高二上学期期中考试化学试题河南省驻马店市新蔡县第一高级中学2021-2022学年高二下学期7月份月考化学试题
名校
解题方法
8 . 下列说法中正确的是( )
| A.同一可逆反应使用不同的催化剂时,高效催化剂可增大平衡转化率 |
| B.已知反应H2O(g) +SO2(g)= H2SO3 (l),该过程熵值增大 |
| C.同温同压下,H2(g) + Cl2(g) =2HCl(g)在光照和点燃条件下的ΔH不同 |
| D.已知2H2O(l) =2H2(g) + O2(g) ΔH = +571.6 kJ·mol-1,则氢气燃烧热为285.8 kJ·mol-1 |
您最近一年使用:0次
2020-01-28更新
|
91次组卷
|
3卷引用:甘肃省静宁县第一中学2020-2021学年高二上学期第二次月考(实验班)化学试题
名校
9 . 下列热化学方程式及有关应用的叙述中,正确的是( )
| A.甲烷的燃烧热为 890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+ 2O2(g) ═ CO2(g) + 2H2O(g) △H = -890.3kJ•mol-1 |
B.已知强酸与强碱在稀溶液里反应的中和热为 57.3kJ•mol-1,则 H2SO4(aq)+ H2SO4(aq)+  Ba(OH)2(aq)═ Ba(OH)2(aq)═ BaSO4(s)+H2O(l) △H = -57.3kJ•mol-1 BaSO4(s)+H2O(l) △H = -57.3kJ•mol-1 |
C.500℃、30MPa 下,将 0.5mol N2 和 1.5molH2 置于密闭的容器中充分反应生成 NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2(g)  2NH3(g) △H= -38.6kJ•mol-1 2NH3(g) △H= -38.6kJ•mol-1 |
| D.已知 25℃、101KPa 条件下:4Al(s) + 3O2(g) ═ 2A12O3(s) △H= -2834.9kJ•mol-1,4Al(s) + 2O3(g) ═ 2A12O3(s) △H = -3119.1kJ•mol-1,则 O2比 O3 稳定 |
您最近一年使用:0次
2019-11-20更新
|
261次组卷
|
12卷引用:甘肃省静宁县第一中学2019-2020学年高二上学期第一次月考化学试题
甘肃省静宁县第一中学2019-2020学年高二上学期第一次月考化学试题2015-2016学年山东省济宁市高二下期末化学试卷【全国百强校】广东省佛山市第一中学2018-2019学年高二上学期第一次段考化学试题湖北省荆州中学2018-2019学年高一下学期5月月考化学试题辽宁省阜新市第二高级中学2019-2020学年高二上学期第一次月考化学试题辽宁省沈阳铁路实验中学2020届高三10月月考化学试题河北省隆化县存瑞中学2020届高三上学期期中考试化学试题河南省周口中英文学校2019-2020学年高二上学期期中考试化学试题甘肃省兰州市第一中学2019-2020学年高二上学期期末考试化学试题安徽省黄山市屯溪第一中学2020-2021学年高二上学期期中考试化学试题辽宁省渤海大学附属高级中学2021-2022学年高二上学期第一次月考化学试题宁夏石嘴山市第三中学2022-2023学年高二下学期第一次月考化学(理)试题
名校
10 . 航天飞船可用肼(N2H4)作动力源。已知1 g液态肼和足量的液态过氧化氢反应生成N2和水蒸气时放出20.05 kJ热量,化学方程式为N2H4+2H2O2=N2↑+4H2O。下列说法中错误的是 ( )
| A.肼(N2H4)分子中只存在极性共价键 |
| B.此情况下,液态肼燃烧生成1 mol N2时放出的热量为641.6 kJ |
| C.该反应中肼作还原剂 |
| D.该反应的反应物总能量高于生成物的总能量 |
您最近一年使用:0次
2019-06-10更新
|
996次组卷
|
11卷引用:甘肃省静宁县第一中学2020-2021学年高一下学期第一次月考化学(实)试题
甘肃省静宁县第一中学2020-2021学年高一下学期第一次月考化学(实)试题(已下线)2012-2013学年山东省济宁市任城一中高一3月质量检测化学试卷2014-2015四川省大竹县文星中学高一4月月考化学试卷辽宁省庄河市高级中学2016-2017学年高一下学期期中考试化学试题湖南省双峰县第一中学2017-2018学年高二上期第一次月考化学试题【全国市级联考】湖南省五市十校2018年上学期高一期中考试化学试题河南省周口市扶沟县高级中学2018-2019学年高一下学期第一次月考化学试题【全国百强校】宁夏回族自治区银川一中2018-2019学年高一下学期期中考试化学试题高一必修第二册(人教2019版)第六章 第一节 化学反应与能量变化 课时1 化学反应与能量变化(已下线)6.1.1 化学反应与热能(练好题)(能力提升)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)河南省信阳市2021-2022学年高一下学期期中教学质量检测化学试题



