名校
解题方法
1 . 以太阳能为热源,热化学硫碘循环分解水是一种高效、环保的制氢方法,其流程如图所示。
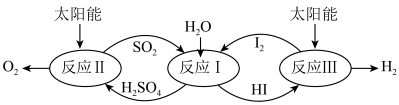
相关反应的热化学方程式为:
反应Ⅰ:SO2(g)+I2(g)+2H2O(l)=2HI(aq)+H2SO4(aq) H1=-213kJ•mol-1
反应Ⅱ:H2SO4(aq)=SO2(g)+H2O(l)+ O2(g) H2=+327kJ•mol-1
O2(g) H2=+327kJ•mol-1
反应Ⅲ:2HI(aq)=H2(g)+I2(g) H3=+172kJ•mol-1
下列说法不正确的是

相关反应的热化学方程式为:
反应Ⅰ:SO2(g)+I2(g)+2H2O(l)=2HI(aq)+H2SO4(aq) H1=-213kJ•mol-1
反应Ⅱ:H2SO4(aq)=SO2(g)+H2O(l)+
 O2(g) H2=+327kJ•mol-1
O2(g) H2=+327kJ•mol-1反应Ⅲ:2HI(aq)=H2(g)+I2(g) H3=+172kJ•mol-1
下列说法不正确的是
| A.该过程实现了太阳能到化学能的转化 |
| B.SO2和I2对总反应起到了催化作用 |
| C.总反应的热化学方程式为2H2O(l)=2H2(g)+O2(g) H=+286kJ•mol-1 |
| D.该过程降低了水分解制氢的活化能,但总反应的H不变 |
您最近一年使用:0次
2020-10-12更新
|
2818次组卷
|
28卷引用:福建省厦门市集美中学2023-2024学年高二上学期10月第一次月考化学试题
福建省厦门市集美中学2023-2024学年高二上学期10月第一次月考化学试题人教版(2019)高二化学选择性必修1第一章 化学反应的热效应 过模拟 2年模拟精编精练湖北省部分省重点中学2020-2021学年高二上学期期中联考化学试题湖北省部分重点中学2020-2021学年高二上学期期中考试化学试题(已下线)高中化学《新教材变化解读与考法剖析》第一章 化学反应的热效应(人教版2019选择性必修1)山东省聊城第三中学2021-2022学年高二上学期第三次质量检测化学试题北京市第三十一中学2021-2022学年高二上学期期中考试化学试题山东省聊城市第二中学2022-2023学年高二上学期第一次月考化学试题北京市北京师范大学燕化附中2022-2023学年高二上学期10月月考化学试题山东省临沂市平邑县第一中学2022-2023学年高二上学期10月月考化学试题湖南省衡阳市第八中学2022-2023学年高二下学期5月月考化学试题湖南省南雅中学2023-2024学年高二上学期第一次月考化学试题江西省宜春市上高二中2023-2024学年高二上学期第一次月考化学试题河北省唐山市丰润区2023-2024学年高二上学期期中考试化学试题【区级联考】北京市海淀区2019届高三第一学期上学期期末考试化学试题【全国百强校】浙江省学军中学2019届高三下学期4月选考模拟冲刺化学试题【全国百强校】内蒙古自治区赤峰二中2018-2019学年高一下学期第二次月考化学试题(已下线)考点24 元素与理论综合——《备战2020年高考精选考点专项突破题集》2019年秋高三化学复习强化练习—— 盖斯定律及其应用河南省实验中学2020届高三12月月考化学试题北京市2020届高三12月月考(新高考选考模式)化学试题北京市2020届高三质量监测化学试题(已下线)考点06 化学能与热能-2020年高考化学命题预测与模拟试题分类精编山东省济南市历城第二中学2021届高三10月份学情检测化学试题(已下线)押山东卷第07题 化学反应与能量-备战2021年高考化学临考题号押题(山东卷)安徽省怀宁中学2020-2021学年高一下学期第一次月考化学试题 湖北省仙桃中学2022-2023学年高一上学期10月月考化学试题(已下线)2023年北京卷高考真题变式题(选择题11-14)
2 . 已知胆矾溶于水溶液温度降低,胆矾分解的热化学方程式为:CuSO4•5H2O(S)=CuSO4(S)+5H2O(l)ΔH=Q1kJ·mol-1;室温下,若将1mol无水硫酸铜溶解为溶液时放热Q2kJ,则:( )
| A.Q1>Q2 | B.Q1=Q2 | C.Q1<Q2 | D.无法比较 |
您最近一年使用:0次
2020-09-20更新
|
274次组卷
|
24卷引用:福建省泉州第十六中学2019-2020学年高二上学期期中考试化学(选考班)试题
福建省泉州第十六中学2019-2020学年高二上学期期中考试化学(选考班)试题2015-2016学年安徽省合肥中科大附中高二下期中理科化学试卷2016-2017学年安徽省淮南二中高二上第一次月考化学试卷河南省南阳市第一中学校2016-2017学年高二下学期第三次月考化学试题河南省南阳市第一中学2016-2017学年高二下学期第三次月考化学试题内蒙古杭锦后旗奋斗中学2017-2018学年高二上学期期末考试化学试题【全国百强校】河南省信阳市高级中学2018-2019学年高二上学期10月月考化学试题1内蒙古乌兰察布市北京八中乌兰察布分校2018-2019学年高二上学期第二次月考调研化学试题浙江省“七彩阳光”新高考研究联盟2018-2019学年高二下学期期中化学试题云南省昆明市官渡区第一中学2019-2020学年高二下学期开学考试化学试题湖南省湘西土家族苗族自治州花垣县边城高级中学2020-2021学年高二上学期入学考试化学试题广东省广州市中山大学附属中学2019-2020学年高二10月月考化学试题大连市普兰店区第一中学2020-2021学年高二上学期第一阶段考试化学试题江苏省苏州实验中学2020-2021学年高二下学期3月份学情调研考试化学试题(已下线)第一章 化学反应与能量 单元综合检测-2021-2022学年高二化学课后培优练(人教版选修4)云南省弥勒市第一中学2021-2022学年高二上学期第二次月考化学试题宁夏吴忠市吴忠中学2022-2023学年高二上学期阶段性测试化学试题(已下线)2012届湖南省四市九校高三上学期第一次联考化学试卷(已下线)2011-2012学年江西省白鹭洲中学高一下学期期中考试化学试卷2017届河北省定州中学高三上月考三化学试卷辽宁省六校协作体2017-2018学年高一下学期期中考试化学试卷辽宁省2017-2018学年度下学期六校协作体高一期中考试化学试题黑龙江省牡丹江市第三高级中学2020届高三上学期第二次月考化学试题上海市2017-2018学年高一化学第一学期综合测试卷二
3 . 工业上,冶炼铁的有关热化学方程式如下:
①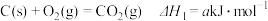 ;
;
②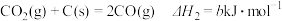 ;
;
③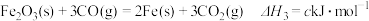
④
上述热化学方程式中,a、b、c、d均不等于0.下列说法不正确的是
①
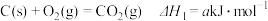 ;
;②
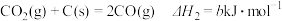 ;
;③
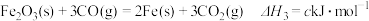
④

上述热化学方程式中,a、b、c、d均不等于0.下列说法不正确的是
A. |
B.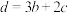 |
C.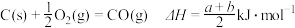 |
D. |
您最近一年使用:0次
2020-09-13更新
|
1715次组卷
|
17卷引用:福建省南安第一中学2019-2020学年高二上学期第一次阶段考试化学试题
福建省南安第一中学2019-2020学年高二上学期第一次阶段考试化学试题【全国校级联考】河南省豫南七校2017-2018学年高二下学期升级摸底考试化学试题2018-2019学年人教版高二化学选修四章:化学反应与能量末测试题(已下线)《2018-2019学年同步单元双基双测AB卷》第一单元 化学反应与能量单元测试(A卷)山西省长治市第二中学2019-2020学年高二上学期第一次月考化学试题安徽省霍邱县第二中学2019-2020学年高二上学期第一次月考化学试题鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第1节 化学反应的热效应 课时3 反应焓变的计算高中必刷题高二选择性必修1第一章 化学反应的热效应 第二节 反应热的计算 课时1 盖斯定律 (1)四川省成都市第七中学2020-2021学年高二上学期十月阶段性考试化学试题湖南省常德市第一中学2020-2021学年高二上学期第2次月考化学试题选择性必修1专题1第一单元 课时2 反应热的测量与计算安徽省皖北县中联盟2021-2022学年 高二上学期10月第一次联考化学试题辽宁省渤海大学附属高级中学2021-2022学年高二上学期期中考试化学试题第二节 反应热的计算 第2课时 反应热的计算1.1.2反应热的测量与计算 课后四川省成都市第七中学2023-2024学年高二上学期10月月考化学试题(已下线)题型102 反应热的大小比较
4 . 1mol白磷转化为红磷放热18.39kJ,已知:
P4(白磷,s)+5O2(g)=2P2O5(s) ΔH= -akJ·mol-1(a>0);
4P(红磷,s)+5O2(g)=2P2O5(s) ΔH=-bkJ·mol-1(b>0);
则a和b的关系是( )
P4(白磷,s)+5O2(g)=2P2O5(s) ΔH= -akJ·mol-1(a>0);
4P(红磷,s)+5O2(g)=2P2O5(s) ΔH=-bkJ·mol-1(b>0);
则a和b的关系是( )
| A.a<b | B.a>b | C.a=b | D.无法确定 |
您最近一年使用:0次
2020-09-11更新
|
232次组卷
|
29卷引用:福建省三明市第一中学2017-2018学年高二上学期第一次月考化学试题
福建省三明市第一中学2017-2018学年高二上学期第一次月考化学试题(已下线)2011-2012学年吉林省长春外国语学校高二第二次月考化学试卷(已下线)2011-2012学年天津一中高二上学期期中考试化学试卷(已下线)2011-2012学年云南大理云龙一中高二上学期期末考试化学试卷(已下线)2011-2012学年安徽省安工大附中、红星中学高二3月联考化学试卷(已下线)2011-2012学年天津市天津一中高二上学期期中考试化学试卷(已下线)2011-2012学年安徽省舒城晓天中学高二下学期质量测试2化学试卷2014-2015学年山西省曲沃中学校高二上学期期中化学试卷2016-2017学年山东省德州市陵城一中高二上10月月考化学试卷山西省运城市康杰中学2017-2018学年高二上学期第一次月考化学试题山东省枣庄市第八中学南校区高二10月份月考化学试题山东省枣庄市第八中学东校区2017-2018学年高二10月月考化学试题河北省邢台第三中学2017-2018学年高二9月月考化学试题山东省锦泽技工学校2017-2018学年高二10月月考化学试题山西省汾阳市第二高级中学2018-2019学年高二上学期第二次半月考化学试题陕西煤铜川市炭建设公司第一中学2018-2019学年高二上学期10月月考化学试题(已下线)2018年10月20日 《每日一题》人教选修4-周末培优江西省上饶市第二中学2018-2019学年高二上学期期中考试化学试题吉林省实验中学2019-2020学年高二上学期第一次月考化学试题内蒙古呼和浩特开来中学2019-2020学年高二上学期期中考试化学试题广东省惠来县葵潭中学2019-2020学年高二上学期第二次月考化学试题甘肃省临夏中学2019-2020学年高二上学期第一次月考化学试题安徽省蚌埠田家炳中学2020-2021学年高二10月月考化学试题甘肃省庆阳市第六中学2020-2021学年高二上学期期中考试化学(理)试题(已下线)2011-2012学年辽宁省抚顺县高级中学高一下学期期中考试化学试卷2014-2015河北省正定中学高一下学期第一次月考化学试卷河北省安平中学2016-2017学年高一下学期升级考试化学试题吉林省长春市第二十九中学2019-2020学年高一下学期期中考试化学试题(理)新疆吾尔自治区哈密市第十五中学2019-2020学年高一下学期期末考试化学试题
5 . 通过以下反应均可获取H2。下列有关说法正确的是( )
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+ O2(g) ΔH1=+571.6 kJ·mol-1
②焦炭与水反应制氢:C(s)+ H2O(g)=CO(g)+ H2(g) ΔH2=+131.3 kJ·mol-1
③甲烷与水反应制氢:CH4(g)+ H2O(g)=CO(g)+3H2(g) ΔH3=+206.1 kJ·mol-1
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+ O2(g) ΔH1=+571.6 kJ·mol-1
②焦炭与水反应制氢:C(s)+ H2O(g)=CO(g)+ H2(g) ΔH2=+131.3 kJ·mol-1
③甲烷与水反应制氢:CH4(g)+ H2O(g)=CO(g)+3H2(g) ΔH3=+206.1 kJ·mol-1
| A.反应①中电能转化为化学能 |
| B.反应②为放热反应 |
| C.反应③使用催化剂,ΔH3减小 |
| D.反应CH4(g)=C(s)+2H2(g)的ΔH=+74.8 kJ·mol-1 |
您最近一年使用:0次
2020-09-02更新
|
3847次组卷
|
106卷引用:福建省南安第一中学2017-2018学年高二上学期期中考试化学试题
福建省南安第一中学2017-2018学年高二上学期期中考试化学试题福建省惠安惠南中学2018-2019学年高二上学期期中考试化学试题福建省福州市福清西山学校高中部2019-2020学年高二上学期期中考试化学试题福建省莆田第七中学2021-2022学年高二上学期期末考试化学试题2016-2017学年湖北省咸宁市高二上学期第一次月考化学试卷2016-2017学年山东省枣庄二中高二第二次月考化学试卷2016-2017学年江西省樟树中学高二上第二次月考化学试卷2016-2017学年云南省曲靖一中高二上期中化学试卷2016-2017学年江西省樟树中学高二上月考二化学试卷2016-2017学年山东省济宁市历城区高二上期中化学试卷2016-2017学年辽宁东北育才学校高二上阶段考二化学卷2016-2017学年江苏省扬州中学高二12月月考化学卷2016-2017学年广东省仲元中学高二上学期期末考试化学(理)试卷江苏省徐州市2016-2017学年高二下学期期中考试化学试题辽宁省辽源市金鼎高级中学2016-2017学年高二上学期期末考试化学试卷吉林省延边安图第一中学2016-2017学年高二练习化学试题山东省济南市外国语学校2017-2018学年高二10月月考(理)化学试题黑龙江省哈尔滨市第六中学2017-2018学年高二上学期期中考试(理)化学试题山东省枣庄市薛城区2017-2018学年高二上学期期末化学试题湖南省醴陵市第一中学2018-2019学年高二上学期入学考试化学试题2018-2019学年人教版高中化学选修四模块综合测评题广东省蓝精灵中学2018-2019学年高二上学期联考化学试题【全国百强校】陕西省西安市第一中学2018-2019学年高二上学期10月月考化学试题甘肃省兰州第一中学2018-2019学年高二(理)上学期期中考试化学试题【校级联考】浙江省温州市“十五校联合体”2018-2019学年高二上学期期中联考化学试题【全国百强校】山东省济南外国语学校三箭分校2018-2019学年高二上学期期中考试化学试题安徽省青阳县第一中学2019-2020学年高二10月月考化学试题安徽省亳州市第十八中学2019-2020学年高二上学期第一次月考化学试题湖北省武汉市汉南区职教中心2019-2020学年高二上学期期中考试化学试题贵州省麻江县第一中学2019-2020学年高二上学期期末考试化学试题海南省海南中学2019-2020学年高二上学期期末考试化学试题福建省厦门市思明区厦门外国语学校2019-2020学年高三上学期周末练习12——化学试题贵州省镇远县二中2019-2020学年高二上学期期末考试化学试题江苏省扬州市江都区大桥高级中学2019-2020学年高二下学期期中考试化学试题湖北省黄冈市黄梅国际育才高级中学2019-2020学年高二上学期期中考试化学试题河南省安阳市林州市第一中学2020-2021学年高二上学期开学考试(实验班)化学试题江苏省启东中学2020-2021学年高二上学期期初考试化学试题(已下线)1.3.2 反应热的计算(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)1.3.1 盖斯定律(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第1章 综合检测高中必刷题高二选择性必修1第一章 化学反应的热效应 第一章素养检测(已下线)1.3.2+反应热的计算-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)江苏省扬州中学2018-2019学年高二上学期12月月考试题 化学 Word版(已下线)【南昌新东方】9.湾里一中 梁莎陕西省西安市第八十九中学2018-2019学年高二上学期期中考试化学试题江苏省徐州市沛县2020-2021学年高二上学期第一次学情调研化学(选修)试题江西省九江市浔阳区九江市第七中学2020-2021学年高二上学期期中考试化学试题(已下线)练习2 盖斯定律与化学反应热的计算-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)江苏省盐城市阜宁中学2020-2021学年高二上学期期末考试化学试题江苏省吴江汾湖高级中学2020-2021学年高二下学期阶段性教学质量检测化学试题江苏省宜兴市张渚高级中学2020-2021学年高二下学期第一学段质量检测化学试题重庆市南开中学2020-2021学年二上学期期末考试化学试题山东省曲阜市第一中学2017-2018学年高二上学期第一次月考化学试题北京市昌平区新学道临川学校2021-2022学年高二上学期第一次月考化学试题山西省朔州市怀仁县大地学校2020-2021学年高二上学期第一次月考化学试题河北省保定市徐水综合高级中学2021-2022学年高二上学期第二次月考化学试题江苏省盐城市第一中学、阜宁中学2021-2022学年高二上学期期中考试化学试题河南省南阳市第六完全学校高级中学2022-2023学年高二上学期9月考试化学试题广西桂林市第十八中学2021-2022学年高二下学期开学考试化学试题山东省济宁市泗水县2021-2022学年高二上学期期中考试化学试题河南省安阳市第三十九中学2022-2023学年高二上学期第二次考试化学试题海南省三亚华侨学校(南新校区)2021-2022学年高二上学期期中考试化学试题天津市河东区 2022-2023 学年高二上学期期末质量检测化学试题广东省江门市第一中学2023-2024学年高二上学期第一次段考化学试题江苏省南菁高级中学2023-2024学年高二上学期9月调研化学试题2016年全国普通高等学校招生统一考试化学(江苏卷精编版)2015-2016学年吉林省松原市油田高中高一下期末化学试卷2017届河北沧州市第一中学高三上学期第一次月考化学试题2017届河北省沧州市第一中学高三上周测化学试卷2017届河北省石家庄二中高三上第二期联考化学试卷2017届河南省开封市高三上学期10月定位考试化学试卷2017届广西桂林十八中高三上10月月考化学试卷2017届河南省郑州一中高三上期中化学试卷2017届辽宁省沈阳二中高三上期中化学试卷2017届宁夏银川一中高三上月考四化学试卷2017届宁夏六盘山高级中学高三上月考二化学卷辽宁省鞍山市第一中学2016-2017学年高一下学期期中考试化学试题苏教版2017届高三单元精练检测六化学试题2018版化学(苏教版)高考总复习专题六对接高考精练--化学反应的热效应黑龙江省大庆实验中学2018届高三上学期期中考试理科综合化学试题(已下线)《考前20天终极攻略》-5月24日 盖斯定律及反应热的有关计算(已下线)解密08 化学反应与热能(教师版)——备战2018年高考化学之高频考点解密人教版2017届高三单元精练检测六化学试题(已下线)2019高考备考二轮复习精品资料-专题8 化学反应中与能量变化(教学案)(已下线)考点08 化学反应中的热效应——备战2019年浙江新高考化学考点2016年全国普通高等学校招生统一考试化学(江苏卷参考版)(已下线)2019年4月8日 《每日一题》三轮复习——反应热的计算与盖斯定律云南省建水县第二中学2020届高三上学期开学考试化学试题2020届高三化学二轮冲刺新题专练——盖斯定律的应用2云南省昭通市绥江县二中2019-2020学年高三上学期期末考试理综化学试题(已下线)专题九 化学能与热能(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训(已下线)广东省深圳中学2020届高三3月份教学质量监测卷理综化学试题2020届四川省成都市第七中学高三二月份网络教学质量监测卷化学试题安徽省合肥市第一中学2020年高中毕业班教学质量监测卷理科综合化学试题湖北省武汉市华中师范大学第一附属中学2020届高三下学期四月份网络教学质量监测理科综合化学试题湖南省长沙市第一中学2019-2020学年高一下学期第三次月考化学试题吉林省白城市洮南市第一中学2019-2020学年高一下学期第三次月考化学试题黑龙江省哈尔滨市第一中学校2021届高三上学期开学测试化学试题河北省唐山市第十一中学2021届高三9月入学检测化学试题吉林省松原市前郭尔罗斯蒙古族自治县第五中学2021届高三下学期5月月考化学试题(已下线)第15讲 化学反应的热效应(练) — 2022年高考化学一轮复习讲练测(新教材新高考)湖北省武汉市华中师范大学第一附属中学2020届高三3月份网络教学质量监测卷理综化学试题湖南省长沙市第一中学、广东省深圳实验学校2021-2022学年高三上学期联考化学试题 (已下线)第14周 晚练题-备战2022年高考化学周测与晚练(新高考专用)湖北省十堰市2016-2017学年高一下学期期末调研考试化学试题湖南省常德市第一中学 2023届高三7月摸底考试化学试题
名校
6 . 火箭推进器中装有还原剂液态肼(N2H4)和氧化剂过氧化氢(H2O2),当它们混合时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.65kJ的热量。回答下列问题:
(1)过氧化氢的结构式是__________ 。
(2)该反应的热化学方程式为___________ 。
(3)已知H2O(l)=H2O(g) ∆H=+44kJ/mol,则32g液态肼与足量液态过氧化氢反应生成氮气和液态水时,∆H=_________ 。
(4)实验室可用次氯酸钠溶液与氨气反应制备液态肼,已知生成物之一是常见的盐,则反应的化学方程式为__________ 。
(5)已知: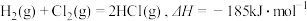 ,几种化学键的键能如下表所示,则a=
,几种化学键的键能如下表所示,则a=_________ 。
(1)过氧化氢的结构式是
(2)该反应的热化学方程式为
(3)已知H2O(l)=H2O(g) ∆H=+44kJ/mol,则32g液态肼与足量液态过氧化氢反应生成氮气和液态水时,∆H=
(4)实验室可用次氯酸钠溶液与氨气反应制备液态肼,已知生成物之一是常见的盐,则反应的化学方程式为
(5)已知:
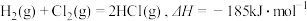 ,几种化学键的键能如下表所示,则a=
,几种化学键的键能如下表所示,则a=共价键 |
|
|
|
键能/( | 436 | 247 | a |
您最近一年使用:0次
2020-08-25更新
|
455次组卷
|
5卷引用:福建省福州第一中学2022-2023学年高二上学期12月月考化学试题
福建省福州第一中学2022-2023学年高二上学期12月月考化学试题 (已下线)第一章 化学反应的热效应(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)辽宁省盘锦市第二高级中学2020-2021学年高二上学期第一次阶段性考试化学试题湖北省仙桃、天门、潜江2019-2020学年高一下学期期末考试化学试题吉林省吉化第一高级中学校2021-2022学年高一下学期复课检测化学试题
7 . 煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后再使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的热化学方程式为
a.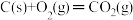 ΔH=E1①
ΔH=E1①
b.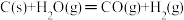 ΔH=E2②
ΔH=E2②
 ΔH=E3③
ΔH=E3③
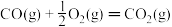 ΔH=E4④
ΔH=E4④
(1)上述四个热化学方程式中哪个反应的ΔH>0?______ (填序号)。
(2)等质量的煤分别通过以上两种不同的途径产生的可利用的总能量关系正确的是____ (填字母)。
A.a比b多 B.a比b少 C.a与b在理论上相同
(3)根据能量守恒定律,E1、E2、E3、E4之间的关系为E1=__________________ 。
(4)已知:①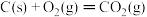 ΔH1=-393.5kJ/mol
ΔH1=-393.5kJ/mol
②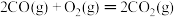 ΔH2=-566kJ/mol
ΔH2=-566kJ/mol
③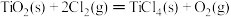 ΔH3=+141kJ/mol
ΔH3=+141kJ/mol
则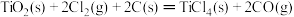 的ΔH=
的ΔH=_____________________ 。
a.
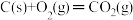 ΔH=E1①
ΔH=E1①b.
 ΔH=E2②
ΔH=E2② ΔH=E3③
ΔH=E3③ 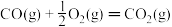 ΔH=E4④
ΔH=E4④(1)上述四个热化学方程式中哪个反应的ΔH>0?
(2)等质量的煤分别通过以上两种不同的途径产生的可利用的总能量关系正确的是
A.a比b多 B.a比b少 C.a与b在理论上相同
(3)根据能量守恒定律,E1、E2、E3、E4之间的关系为E1=
(4)已知:①
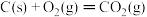 ΔH1=-393.5kJ/mol
ΔH1=-393.5kJ/mol②
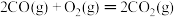 ΔH2=-566kJ/mol
ΔH2=-566kJ/mol③
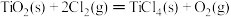 ΔH3=+141kJ/mol
ΔH3=+141kJ/mol 则
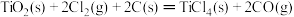 的ΔH=
的ΔH=
您最近一年使用:0次
2020-08-21更新
|
165次组卷
|
4卷引用:福建省南安市柳城中学2020-2021学年高二上学期第一次月考化学试题
2014高三·全国·专题练习
名校
解题方法
8 . 在25℃、101kPa条件下,C(s)、H2(g)、CH3COOH(l)的燃烧热分别为393.5kJ·mol-1、285.8kJ·mol-1、870.3kJ·mol-1,则2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热为( )
| A.-488.3kJ·mol-1 | B.+488.3kJ·mol-1 |
| C.-191kJ·mol-1 | D.+191kJ·mol-1 |
您最近一年使用:0次
2020-08-20更新
|
2573次组卷
|
64卷引用:福建省南安市柳城中学2020-2021学年高二上学期第一次月考化学试题
福建省南安市柳城中学2020-2021学年高二上学期第一次月考化学试题(已下线)2014年高中化学人教版选修四第一章 化学反应与能量练习卷2016-2017学年江西省师大附中高二上第一次月考化学试卷2016-2017学年甘肃省天水一中高二上月考一化学试卷内蒙古巴彦淖尔市第一中学2017-2018学年高二9月月考化学试题A内蒙古巴彦淖尔市第一中学2017-2018学年高二9月月考化学试题B甘肃省会宁县第四中学2017-2018学年高二上学期期中考试化学试题河南省杞县2018-2019学年高二上学期10月月考化学试题【全国百强校】广西壮族自治区桂林市第十八中学2018-2019学年高二(理)上学期期中考试化学试题辽宁省阜新市第二高级中学2019-2020学年高二上学期第一次月考化学试题山西大学附中2019-2020学年高二上学期第一次月考化学试题辽宁省实验中学东戴河分校2019-2020学年高二10月月考化学试题河北省鹿泉第一中学2019-2020学年高二9月月考化学试题安徽省青阳县第一中学2019-2020学年高二9月月考化学试题四川省武胜烈面中学2019-2020学年高二10月月考化学试题江西省南昌市八一中学、洪都中学、十七中三校2019-2020学年高二10月联考化学试题云南省玉溪市玉溪一中2019-2020学年高二上学期第一次月考化学试题黑龙江省哈尔滨师范大学青冈实验中学校2018-2019学年高二上学期开学考试化学试题辽宁省辽阳市辽阳县集美中学2020-2021学年高二上学期第一次月考化学试题(已下线)第01章 化学反应的热效应(A卷基础强化篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)山东省临沂市沂水一中2020-2021学年高二9月月考化学试题陕西省渭南市澄城县城关中学2020-2021学年高二上学期第一次月考化学试题陕西省咸阳百灵中学2020-2021学年高二上学期第一次月考化学试题宁夏吴忠中学2020-2021学年高二10月月考理综化学试题湖南省长沙县第九中学2020-2021学年高二上学期第一次月考化学试题广东省深圳市第七高级中学2020-2021学年高二上学期第一学段考试化学试题陕西省西安市第一中学2020-2021学年高二上学期第一次月考化学试题贵州省思南中学2020-2021学年高二上学期期中考试化学试题(已下线)练习1 化学反应的热效应-2020-2021学年【补习教材·寒假作业】高二化学(苏教版)天津市静海区第一中学2020-2021学年高二11月考化学试题河北省衡水市武邑武罗学校2020-2021学年高二上学期期中考试化学试题湖北i省华中师范大学潜江附属中学2020-2021学年高二上学期入学考试化学试题河南省开封市五县2021-2022学年高二上学期月考联考化学试题广西南宁市宾阳县宾阳中学2021-2022学年高二上学期10月月考化学试题黑龙江省鸡东县第二中学2021-2022学年高二上学期期中考试化学(理)试题江苏省盐城市伍佑中学2021-2022学年高二下学期第一次阶段考试化学试题(已下线)第1章基础巩固测评卷-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)天津市实验中学滨海学校2021-2022学年高二上学期期中质量监测化学试题河南省南阳市第六完全学校高级中学2022-2023学年高二上学期9月半月考化学试题四川省邻水实验学校2021-2022学年高二上学期期中考试化学试题陕西省延安市黄龙县中学2021-2022学年高二上学期第一次月考化学试题四川省凉山彝族自治州2022-2023学年高二上学期期末检测化学试题(已下线)【知识图鉴】单元讲练测选择性必修1第1单元01讲核心(已下线)专题01 反应热、焓变与热化学方程式【考题猜想】(6大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)浙江省海宁市高级中学2022-2023学年高二上学期10月月考化学试题湖北省十堰市部分普通高中2023-2024学年高二上学期11月期中考试化学试题吉林省东北师范大学连山实验高中2023-2024学年高二上学期第一次月考化学试题四川省泸州市泸县第五中学2023-2024学年高二下学期6月月考化学试题(已下线)2014年高考化学苏教版总复习 6-1 化学反应中的热效应练习卷(已下线)2013-2014黑龙江省鹤岗一中高一下学期期中考试化学试卷2015-2016学年黑龙江牡丹江一中高一下期中化学试卷2017届山西省重点中学协作体高三上学期开学考试化学试卷2017届河北邯郸市大名一中高三上学期第二次月考化学试卷2016-2017学年河北省张家口市第一中学高一3月月考(理)化学试卷黑龙江省肇东市第一中学2016-2017学年高一下学期期中考试化学试题吉林省扶余一中2016-2017学年高一下学期期末考试化学试题吉林省扶余市第一中学2016-2017学年高一下学期期末考试化学试题2018届高三一轮复习化学:微考点46-盖斯定律的全面应用四川省成都市七中实验学校2018届高三上学期入学考试化学试题(已下线)2019年9月11日《每日一题》2020年一轮复习—— 反应热的计算2019年秋高三化学复习强化练习—— 盖斯定律及其应用2020届高三化学知识点强化训练—化学能与热能江苏省淮安市涟水县第一中学2020届高三上学期第二次月考化学试题天津市河东区第八中学2021届高三上学期期中化学试题
9 . 依据图示关系,下列说法不正确的是
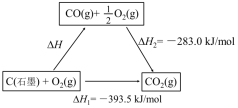

| A.石墨燃烧是放热反应 |
| B.1molC(石墨)和1molCO分别在足量O2中燃烧,全部转化为CO2,前者放热多 |
| C.C(石墨)+CO2(g)=2CO(g) ΔH=ΔH1-ΔH2 |
| D.化学反应的ΔH,只与反应体系的始态和终态有关,与反应途径无关 |
您最近一年使用:0次
2020-08-19更新
|
7650次组卷
|
53卷引用:福建省厦门市湖滨中学2021-2022学年高二上学期期中考试化学试题
福建省厦门市湖滨中学2021-2022学年高二上学期期中考试化学试题辽宁省辽阳市辽阳县集美中学2020-2021学年高二上学期第一次月考化学试题北京首都师范大学附属中学2020-2021学年高二上学期期中考试化学试题北京市一零一中学2020-2021学年高二上学期期中考试化学试题(已下线)1.2 反应热的计算-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)高中化学《新教材变化解读与考法剖析》第一章 化学反应的热效应(人教版2019选择性必修1)山东省济宁曲阜市第一中学2021-2022学年高二10月月考化学试题甘肃省张掖市第二中学2021-2022学年高二上学期10月月考(B班)化学试题甘肃省张掖市第二中学2021-2022学年高二上学期10月月考(A班)化学试题云南省玉溪市第二中学2021-2022学年高二上学期期中考试化学试题云南省玉溪市江川区第二中学2021-2022学年高二上学期期中考试化学试题北京师范大学附属中学2021-2022学年高二上学期期中考试化学试题北京市第四中学顺义分校2021-2022学年高二上学期期中考试化学试题北京市第七中学2022-2023学年高二上学期期中化学试题广东省广州大学附属中学2022-2023学年高二上学期期中考试化学试题(已下线)【2022】【高二上】【期中考】【高中化学】59(已下线)【2022】【高二化学】【期中考】-178广东省广州真光中学2021-2022学年高二上学期期中考试化学试题广东省广州市协和中学等3校2022-2023学年高二上学期(12月)期末考试化学试题作业(三) 反应热的计算第一章 化学反应的热效应 第二节 反应热的计算宁夏回族自治区中宁县第一中学2022-2023学年高二上学期10月月考化学试题北京市八一学校2022-2023学年高二上学期期中考试化学试题北京汇文中学2023-2024学年高二上学期期中考试化学试题北京市第十一中学2022-2023学年高二上学期期中考试化学试卷北京市第一六一中学2023-2024学年高二上学期10月月考化学试题北京师范大学附属中学2023-2024学年高二上学期期末考试化学试卷2020年北京市高考化学试卷浙江省金丽衢十二校2021届高三上学期第一次联考化学试题(已下线)小题必刷24 盖斯定律及反应热计算——2021年高考化学一轮复习小题必刷(通用版)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)热点7 化学能与热能-2021年高考化学【热点·重点·难点】专练(新高考)新疆维吾尔自治区巴州二中2021届高三第六次月考化学试题(已下线)课时29 盖斯定律及反应热计算-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)北京市中国农业大学附属中学2020-2021学年高一下学期期中学业水平调研化学试题2020年北京高考化学真题变式题11-19(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)回归教材重难点05 化学反应中的能量变化-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)广东省大联考2021-2022学年高一下学期期中检测化学试题天津市静海区四校2021-2022学年高三上学期12月阶段性检测化学试题天津市南开区2021-2022学年高一下学期期末阶段性质量检测化学试题吉林省吉化第一高级中学校2021-2022学年高一下学期复课检测化学试题(已下线)考点17 化学反应的热效应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第24练 反应热-2023年高考化学一轮复习小题多维练(全国通用)(已下线)专题15 反应热计算的几种类型-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第六章 化学反应与能量 第34讲 反应热的计算(已下线)题型13 突破反应热图象(已下线)专题08 化学反应中的能量变化(已下线)第2讲 盖斯定律 反应热的计算
10 . 向湿法炼锌的电解液中同时加入Cu和CuSO4,可生成CuCl沉淀除去Cl-,反应原理如下:
Cu(s)+Cu2+(aq)⇌2Cu+(aq)△H1=akJ•mol-1
Cl-(aq)+Cu+(aq)⇌CuCl(s)△H2=bkJ•mol-1
(1)反应Cu(s)+Cu2+(aq)+2Cl-(aq)⇌2CuCl(s) △H=_________ 。
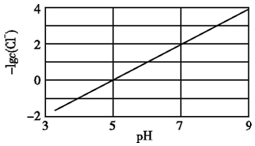
(2)实验测得电解液pH对溶液中残留 的影响如上图所示。当pH=7时,溶液中
的影响如上图所示。当pH=7时,溶液中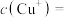
_________ 。
(3)兴趣小组在CuCl2溶液中加入过量KI固体,观察到有白色沉淀生成。推测该白色沉淀中一定含有的物质是___________ ,原因是 ______________________________ 。(已知常温下CuCl、CuI、CuI2的相关信息见表。)
Cu(s)+Cu2+(aq)⇌2Cu+(aq)△H1=akJ•mol-1
Cl-(aq)+Cu+(aq)⇌CuCl(s)△H2=bkJ•mol-1

(1)反应Cu(s)+Cu2+(aq)+2Cl-(aq)⇌2CuCl(s) △H=
(2)实验测得电解液pH对溶液中残留
 的影响如上图所示。当pH=7时,溶液中
的影响如上图所示。当pH=7时,溶液中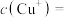
(3)兴趣小组在CuCl2溶液中加入过量KI固体,观察到有白色沉淀生成。推测该白色沉淀中一定含有的物质是
| 物质 | CuCl | CuI | CuI2 |
 |  |  | - |
| 颜色 | 白色 | 白色 | 金黄色 |
您最近一年使用:0次







