解题方法
1 . I.碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质,请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:

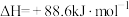
则M、N相比,较稳定的是___________ 。
(2)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,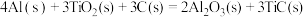
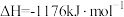 ,则反应过程中,每转移
,则反应过程中,每转移 电子放出的热量为
电子放出的热量为___________ kJ。
(3) 、
、 、C都是优质的能源物质,它们燃烧的热化学方程式分别为
、C都是优质的能源物质,它们燃烧的热化学方程式分别为
①
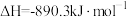 ;
;
②
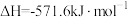 ;
;
③
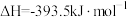 ;
;
已知 、
、 组成的混合气体
组成的混合气体 ,又
,又 与
与 的物质的量之比
的物质的量之比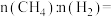 3:2,则该混合气体完全燃烧后放出的热量为
3:2,则该混合气体完全燃烧后放出的热量为___________ kJ; 的反应热无法直接测量,但通过上述反应可求出其反应热
的反应热无法直接测量,但通过上述反应可求出其反应热
___________  。
。
II. 的盐酸与
的盐酸与 的
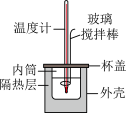
的 溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和反应反应热,回答下列问题:
溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和反应反应热,回答下列问题:
(4)实验中若改用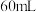
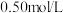 的盐酸与
的盐酸与
 的氢氧化钠溶液进行反应,若实验操作均正确,则所求中和热
的氢氧化钠溶液进行反应,若实验操作均正确,则所求中和热___________ (填“相等”或“不相等”)。
(5)下列说法正确的是___________(填字母)。
(1)有机物M经过太阳光光照可转化成N,转化过程如下:

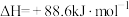
则M、N相比,较稳定的是
(2)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,
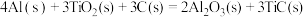
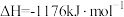 ,则反应过程中,每转移
,则反应过程中,每转移 电子放出的热量为
电子放出的热量为(3)
 、
、 、C都是优质的能源物质,它们燃烧的热化学方程式分别为
、C都是优质的能源物质,它们燃烧的热化学方程式分别为①

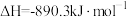 ;
;②

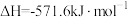 ;
;③

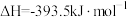 ;
;已知
 、
、 组成的混合气体
组成的混合气体 ,又
,又 与
与 的物质的量之比
的物质的量之比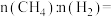 3:2,则该混合气体完全燃烧后放出的热量为
3:2,则该混合气体完全燃烧后放出的热量为 的反应热无法直接测量,但通过上述反应可求出其反应热
的反应热无法直接测量,但通过上述反应可求出其反应热
 。
。II.
 的盐酸与
的盐酸与 的
的 溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和反应反应热,回答下列问题:
溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和反应反应热,回答下列问题:
(4)实验中若改用
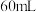
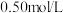 的盐酸与
的盐酸与
 的氢氧化钠溶液进行反应,若实验操作均正确,则所求中和热
的氢氧化钠溶液进行反应,若实验操作均正确,则所求中和热(5)下列说法正确的是___________(填字母)。
| A.玻璃搅拌棒可用铜丝搅拌棒替代 |
| B.向内筒中加入稀碱时,应当缓慢而匀速地加入 |
| C.实验中如果用相同体积、相同浓度的醋酸代替盐酸,测得的中和热数值将偏小 |
| D.将用量筒量取好的稀盐酸加入内筒后,应当快速用水冲洗量筒内壁剩余的稀盐酸至内筒中,以免造成测量误差 |
您最近一年使用:0次
名校
解题方法
2 . 二氧化碳催化加氢制甲醇有利于减少温室气体排放。涉及的主要反应如下:
Ⅰ.

Ⅱ.
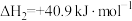
Ⅲ.
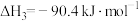
(1)
_______  ,该反应一般认为通过反应Ⅱ和反应Ⅲ两步来实现,若反应Ⅱ为慢反应,下列示意图中能体现上述反应能量变化的是
,该反应一般认为通过反应Ⅱ和反应Ⅲ两步来实现,若反应Ⅱ为慢反应,下列示意图中能体现上述反应能量变化的是_______ (填标号)。
A.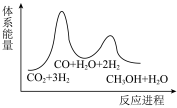 B.
B.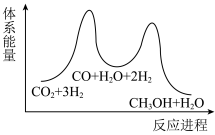
C.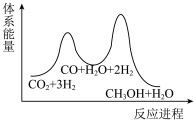 D.
D.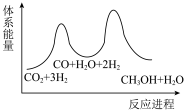
(2)一定条件下,恒容密闭容器中 和
和 发生上述反应。下列说法正确的是_______。
发生上述反应。下列说法正确的是_______。
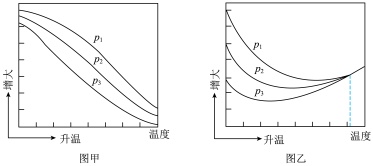
(3)不同压强下,按照 投料,实验测得
投料,实验测得 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如下图所示。
的平衡产率随温度的变化关系如下图所示。
已知: 的平衡转化率
的平衡转化率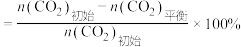
 的平衡产率
的平衡产率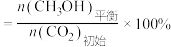
其中纵坐标表示 平衡转化率的是图
平衡转化率的是图_______ (填“甲”或“乙”),压强 、
、 、
、 由大到小的顺序为
由大到小的顺序为_______ ,图乙中 温度时,三条曲线几乎交于一点的原因是
温度时,三条曲线几乎交于一点的原因是_______ 。
(4)乙醇是重要的有机化工原料,可由乙烯气相直接水合法或间接水合法生产。热化学方程式为:C2H4(g)+H2O(g) CH3CH2OH(g) ΔH=-45.5kJ·mol-1,下图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系[其中n(H2O)∶n(C2H4)=1∶1]。
CH3CH2OH(g) ΔH=-45.5kJ·mol-1,下图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系[其中n(H2O)∶n(C2H4)=1∶1]。
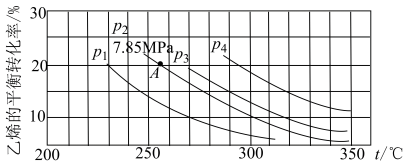
计算乙烯水合制乙醇反应在图中A点的平衡常数Kp=_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
Ⅰ.


Ⅱ.

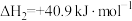
Ⅲ.

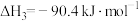
(1)

 ,该反应一般认为通过反应Ⅱ和反应Ⅲ两步来实现,若反应Ⅱ为慢反应,下列示意图中能体现上述反应能量变化的是
,该反应一般认为通过反应Ⅱ和反应Ⅲ两步来实现,若反应Ⅱ为慢反应,下列示意图中能体现上述反应能量变化的是A.
 B.
B.
C.
 D.
D.
(2)一定条件下,恒容密闭容器中
 和
和 发生上述反应。下列说法正确的是_______。
发生上述反应。下列说法正确的是_______。| A.当混合气体密度不变时说明体系达到平衡状态 |
| B.反应达到平衡状态后通入氦气,体系压强增大,反应速率不变,平衡不移动 |
| C.使用高效催化剂,可提高甲醇的生产效率,但不能改变甲醇的平衡产率 |
| D.实际生产中温度越低越有利于甲醇的合成 |
(3)不同压强下,按照
 投料,实验测得
投料,实验测得 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如下图所示。
的平衡产率随温度的变化关系如下图所示。
已知:
 的平衡转化率
的平衡转化率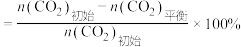
 的平衡产率
的平衡产率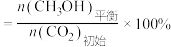
其中纵坐标表示
 平衡转化率的是图
平衡转化率的是图 、
、 、
、 由大到小的顺序为
由大到小的顺序为 温度时,三条曲线几乎交于一点的原因是
温度时,三条曲线几乎交于一点的原因是(4)乙醇是重要的有机化工原料,可由乙烯气相直接水合法或间接水合法生产。热化学方程式为:C2H4(g)+H2O(g)
 CH3CH2OH(g) ΔH=-45.5kJ·mol-1,下图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系[其中n(H2O)∶n(C2H4)=1∶1]。
CH3CH2OH(g) ΔH=-45.5kJ·mol-1,下图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系[其中n(H2O)∶n(C2H4)=1∶1]。
计算乙烯水合制乙醇反应在图中A点的平衡常数Kp=
您最近一年使用:0次
名校
解题方法
3 . 按要求完成下列问题
(1)向某恒温体积固定的密闭容器中加入0.6mol A、0.2mol C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示(已知反应前后容器压强保持不变)。
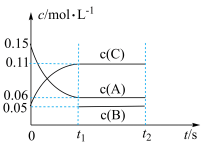
①平衡时A的转化率为___________ ;
②写出该反应的化学方程式___________ ;
③B的起始物质的量是___________ ;
(2)一定条件下,在水溶液中1molCl-、ClO (x=1、2、3、4)的能量(kJ)相对大小(微粒的价态和对应的能量座标)如图所示:
(x=1、2、3、4)的能量(kJ)相对大小(微粒的价态和对应的能量座标)如图所示:
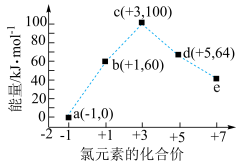
①这些微粒里最不稳定的是___________ (填离子符号)
②写出a+d→b的热化学方程式:___________ 。
(3)甲烷水蒸气催化重整是制高纯氢的方法之一。已知反应器中存在如下反应:
ⅰ.CH4(g)+2H2O(g)=CO2(g)+4H2(g) ΔH1
ⅱ.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2
ⅲ.CH4(g)=C(s)+2H2(g) ΔH3
①ⅲ为积炭反应,常温下不能自发,请判断该反应ΔH3___________ 0(填“>”、“<”或“=”)
②若想利用盖斯定律计算出ΔH3的具体值时,除了ΔH1和ΔH2之外,还需要知道反应___________ ΔH4(写一个合适的方程式,注明物质的状态)。
(1)向某恒温体积固定的密闭容器中加入0.6mol A、0.2mol C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示(已知反应前后容器压强保持不变)。

①平衡时A的转化率为
②写出该反应的化学方程式
③B的起始物质的量是
(2)一定条件下,在水溶液中1molCl-、ClO
 (x=1、2、3、4)的能量(kJ)相对大小(微粒的价态和对应的能量座标)如图所示:
(x=1、2、3、4)的能量(kJ)相对大小(微粒的价态和对应的能量座标)如图所示:
①这些微粒里最不稳定的是
②写出a+d→b的热化学方程式:
(3)甲烷水蒸气催化重整是制高纯氢的方法之一。已知反应器中存在如下反应:
ⅰ.CH4(g)+2H2O(g)=CO2(g)+4H2(g) ΔH1
ⅱ.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2
ⅲ.CH4(g)=C(s)+2H2(g) ΔH3
①ⅲ为积炭反应,常温下不能自发,请判断该反应ΔH3
②若想利用盖斯定律计算出ΔH3的具体值时,除了ΔH1和ΔH2之外,还需要知道反应
您最近一年使用:0次
4 . 几种物质间的转化焓变如图所示,下列说法不正确 的是
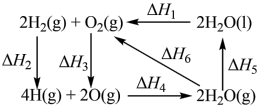

| A.ΔH3>ΔH4 | B.ΔH1>ΔH6 |
| C.ΔH1+ΔH2+ΔH3+ΔH4+ΔH5=0 | D.H—H的键能为ΔH2 |
您最近一年使用:0次
2023-11-11更新
|
180次组卷
|
2卷引用:福建省福州市八县一中2023-2024学年高二上学期11月期中化学试题
名校
解题方法
5 . Ⅰ.在载人航天器中,可以利用 与
与 的反应,将航天员呼出的
的反应,将航天员呼出的 转化为
转化为 等,然后通过电解
等,然后通过电解 得到
得到 ,从而实现
,从而实现 的再生。已知:
的再生。已知:
①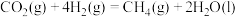

②
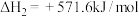
(1)请写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式___________ 。
Ⅱ.将 盐酸和
盐酸和 未知浓度的
未知浓度的 溶液混合均匀后测量并记录溶液的温度,实验结果如图所示,实验中始终保持
溶液混合均匀后测量并记录溶液的温度,实验结果如图所示,实验中始终保持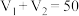 。
。
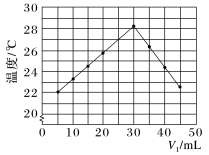
(2)下列叙述正确的是___________。
(3)中和反应的反应热的理论值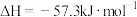 ,写出表示稀盐酸和
,写出表示稀盐酸和 溶液反应的中和热的热化学方程式
溶液反应的中和热的热化学方程式___________ 。下列操作可能使测得的 偏大的是
偏大的是___________ (填序号)。
①室温低于 时进行实验
时进行实验
②分多次把 溶液倒入盛有盐酸的小烧杯中
溶液倒入盛有盐酸的小烧杯中
③实验时用环形铜丝搅拌棒代替搅拌器
(4)在做测定中和反应的反应热实验时,应使用仪器的正确组合是___________。
①天平 ②量筒 ③烧杯 ④滴定管 ⑤温度计 ⑥试管 ⑦酒精灯
 与
与 的反应,将航天员呼出的
的反应,将航天员呼出的 转化为
转化为 等,然后通过电解
等,然后通过电解 得到
得到 ,从而实现
,从而实现 的再生。已知:
的再生。已知:①
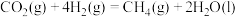

②

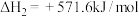
(1)请写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式
Ⅱ.将
 盐酸和
盐酸和 未知浓度的
未知浓度的 溶液混合均匀后测量并记录溶液的温度,实验结果如图所示,实验中始终保持
溶液混合均匀后测量并记录溶液的温度,实验结果如图所示,实验中始终保持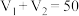 。
。
(2)下列叙述正确的是___________。
| A.该实验表明化学能可转化为热能 | B.做该实验时环境温度为 |
C. 溶液的浓度约为 溶液的浓度约为 | D.该实验表明有水生成的反应都是放热反应 |
(3)中和反应的反应热的理论值
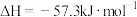 ,写出表示稀盐酸和
,写出表示稀盐酸和 溶液反应的中和热的热化学方程式
溶液反应的中和热的热化学方程式 偏大的是
偏大的是①室温低于
 时进行实验
时进行实验②分多次把
 溶液倒入盛有盐酸的小烧杯中
溶液倒入盛有盐酸的小烧杯中③实验时用环形铜丝搅拌棒代替搅拌器
(4)在做测定中和反应的反应热实验时,应使用仪器的正确组合是___________。
①天平 ②量筒 ③烧杯 ④滴定管 ⑤温度计 ⑥试管 ⑦酒精灯
| A.①②④ | B.②③⑤ | C.②③④⑦ | D.全部 |
您最近一年使用:0次
2023-11-11更新
|
75次组卷
|
2卷引用:福建省厦门大学附属科技中学2023-2024学年高二上学期第一次月考化学试题
6 . 甲醇(CH3OH)是重要的能源物质,研究甲醇具有重要意义。
(1) ,
,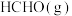 燃烧热
燃烧热 分别
分别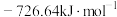 和
和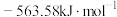 ,则
,则 与
与 反应生成
反应生成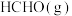 和
和 热化学反应方程式:
热化学反应方程式:___________ 。
(2)利用工业废气中的CO2可制取甲醇,其反应为: 常温常压下已知下列反应的能量变化如图1所示:
常温常压下已知下列反应的能量变化如图1所示:
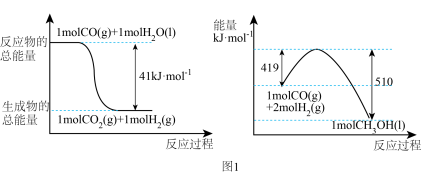
写出由二氧化碳和氢气制备甲醇的热化学方程式:___________ 。
(3)①为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了 的
的 晶体,在高温下它能传导
晶体,在高温下它能传导 离子。电池工作时正极反应式为
离子。电池工作时正极反应式为___________ 。
②若以该电池为电源,用石墨做电极电解100mL含有如下离子的溶液。
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象);阳极上收集到氧气的物质的量为___________ mol。
(4)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后将 氧化成
氧化成 ,然后以
,然后以 作氧化剂把水中的甲醇氧化成
作氧化剂把水中的甲醇氧化成 而净化。实验室用图2装置模拟上述过程:
而净化。实验室用图2装置模拟上述过程:
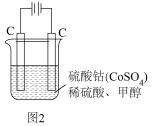
写出阳极电极反应式:___________ 。
(1)
 ,
,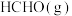 燃烧热
燃烧热 分别
分别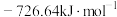 和
和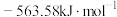 ,则
,则 与
与 反应生成
反应生成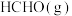 和
和 热化学反应方程式:
热化学反应方程式:(2)利用工业废气中的CO2可制取甲醇,其反应为:
 常温常压下已知下列反应的能量变化如图1所示:
常温常压下已知下列反应的能量变化如图1所示:
写出由二氧化碳和氢气制备甲醇的热化学方程式:
(3)①为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了
 的
的 晶体,在高温下它能传导
晶体,在高温下它能传导 离子。电池工作时正极反应式为
离子。电池工作时正极反应式为②若以该电池为电源,用石墨做电极电解100mL含有如下离子的溶液。
| 离子 | 铜离子 | 氢离子 | 氯离子 | 硫酸根离子 |
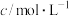 | 1 | 4 | 4 | 1 |
(4)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后将
 氧化成
氧化成 ,然后以
,然后以 作氧化剂把水中的甲醇氧化成
作氧化剂把水中的甲醇氧化成 而净化。实验室用图2装置模拟上述过程:
而净化。实验室用图2装置模拟上述过程:
写出阳极电极反应式:
您最近一年使用:0次
名校
7 . 甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、 和
和 )在催化剂作用下可合成甲醇,发生的主要反应如下:
)在催化剂作用下可合成甲醇,发生的主要反应如下:
Ⅰ.
 kJ⋅mol
kJ⋅mol ;
;
Ⅱ.
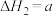 kJ⋅mol
kJ⋅mol ;
;
Ⅲ.
 kJ⋅mol
kJ⋅mol 。
。
(1)
___________ 。
(2)将2.0 mol 和3.0 mol
和3.0 mol  通入容积为3 L的恒容密闭容器中,在一定条件下发生反应Ⅱ,测得
通入容积为3 L的恒容密闭容器中,在一定条件下发生反应Ⅱ,测得 的平衡转化率与温度的关系如图所示。
的平衡转化率与温度的关系如图所示。
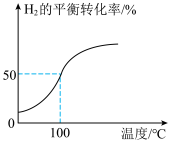
①100℃时反应达到平衡所需的时间为5 min,则反应从起始至5 min内,用 表示该反应的平均反应速率为
表示该反应的平均反应速率为___________ ;平衡后向容器中再通入3 mol Ar,平衡___________ (填“正向”“逆向”或“不”)移动。
②100℃时,反应Ⅱ的平衡常数
___________ 。
③若改变条件使平衡常数增大,则从改变条件至再次平衡正反应速率的变化为___________ 。
(3)甲醇会对水质造成一定的污染,有一种电化学法可消除稀硫酸和甲醇这种污染,其原理如下:通电后,将 氧化成
氧化成 ,下图然后以
,下图然后以 作氧化剂,将水中的甲醇氧化成
作氧化剂,将水中的甲醇氧化成 而净化。实验室用如图装置模拟上述过程。
而净化。实验室用如图装置模拟上述过程。
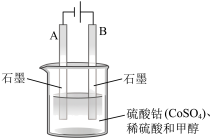
①写出阳极的电极反应式:___________ 。
②写出除去甲醇的离子方程式:___________ 。
 和
和 )在催化剂作用下可合成甲醇,发生的主要反应如下:
)在催化剂作用下可合成甲醇,发生的主要反应如下:Ⅰ.

 kJ⋅mol
kJ⋅mol ;
;Ⅱ.

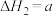 kJ⋅mol
kJ⋅mol ;
;Ⅲ.

 kJ⋅mol
kJ⋅mol 。
。(1)

(2)将2.0 mol
 和3.0 mol
和3.0 mol  通入容积为3 L的恒容密闭容器中,在一定条件下发生反应Ⅱ,测得
通入容积为3 L的恒容密闭容器中,在一定条件下发生反应Ⅱ,测得 的平衡转化率与温度的关系如图所示。
的平衡转化率与温度的关系如图所示。
①100℃时反应达到平衡所需的时间为5 min,则反应从起始至5 min内,用
 表示该反应的平均反应速率为
表示该反应的平均反应速率为②100℃时,反应Ⅱ的平衡常数

③若改变条件使平衡常数增大,则从改变条件至再次平衡正反应速率的变化为
(3)甲醇会对水质造成一定的污染,有一种电化学法可消除稀硫酸和甲醇这种污染,其原理如下:通电后,将
 氧化成
氧化成 ,下图然后以
,下图然后以 作氧化剂,将水中的甲醇氧化成
作氧化剂,将水中的甲醇氧化成 而净化。实验室用如图装置模拟上述过程。
而净化。实验室用如图装置模拟上述过程。
①写出阳极的电极反应式:
②写出除去甲醇的离子方程式:
您最近一年使用:0次
名校
解题方法
8 . 已知反应① 和反应②
和反应② 在T℃时的平衡常数分别为
在T℃时的平衡常数分别为 和
和 ,该温度下反应③
,该温度下反应③ 的平衡常数为
的平衡常数为 。则下列说法正确的是
。则下列说法正确的是
 和反应②
和反应② 在T℃时的平衡常数分别为
在T℃时的平衡常数分别为 和
和 ,该温度下反应③
,该温度下反应③ 的平衡常数为
的平衡常数为 。则下列说法正确的是
。则下列说法正确的是A.反应①的平衡常数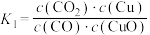 |
B.反应②中,增大氢气浓度,平衡正移, 增大 增大 |
C.对于反应③,T℃时,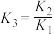 |
| D.对于反应③,恒容时,温度升高,K值减小,则该反应为放热反应 |
您最近一年使用:0次
9 . 镁和卤素单质( )反应的相对能量变化如图所示,下列说法正确的是
)反应的相对能量变化如图所示,下列说法正确的是
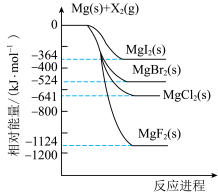
 )反应的相对能量变化如图所示,下列说法正确的是
)反应的相对能量变化如图所示,下列说法正确的是
A.热稳定性: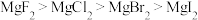 |
| B.1mol碘晶体与足量的Mg充分反应,放热364kJ |
C.工业上常用电解 溶液的方法冶炼金属Mg 溶液的方法冶炼金属Mg |
D.由图可知, 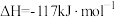 |
您最近一年使用:0次
2023-10-28更新
|
226次组卷
|
2卷引用:福建省漳州市东山县2023-2024学年高二上学期期中考试化学试题
名校
解题方法
10 . 如图1、图2分别表示 和
和 分解时的能量变化情况(单位:kJ)。下列说法错误的是
分解时的能量变化情况(单位:kJ)。下列说法错误的是
 和
和 分解时的能量变化情况(单位:kJ)。下列说法错误的是
分解时的能量变化情况(单位:kJ)。下列说法错误的是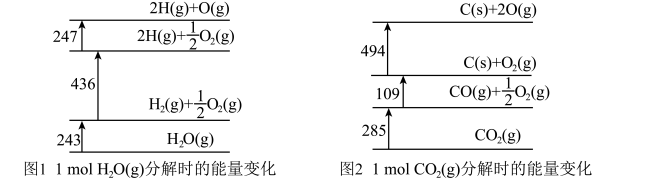
A.CO的燃烧热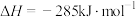 |
B. 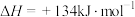 |
C.O=O的键能为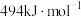 |
D.无法求得 的反应热 的反应热 |
您最近一年使用:0次
2023-10-27更新
|
469次组卷
|
11卷引用:福建省厦门外国语学校2023-2024学年高二上学期期中考试化学试题
福建省厦门外国语学校2023-2024学年高二上学期期中考试化学试题江西省上饶市广信中学2023-2024学年高二上学期11月月考化学试题(已下线)寒假作业01 化学反应的热效应-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)河南省豫北名校2024届高三毕业班上学期一轮复习联考(二)化学试题山西省部分学校2023-2024学年高三上学期10月月考(一轮复习联考(二))化学试题河北省石家庄部分高中2023-2024学年高三上学期10月期中考试化学试题甘肃省部分校2024届高三上学期10月月考化学试题辽宁省部分学校2023-2024学年高三上学期一轮复习联考(二)化学试题重庆市百师联盟2024届高三一轮复习联考(二)河北省保定市唐县第一中学2023-2024学年高三上学期11月期中考试化学试题(已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)



