1 . 碘与氢气反应的热化学方程式是:①
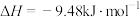 ,②
,②
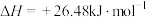 ,下列说法正确的是
,下列说法正确的是

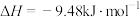 ,②
,②
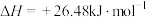 ,下列说法正确的是
,下列说法正确的是A.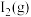 和 和 完全反应生成 完全反应生成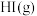 时放热 时放热 |
B. 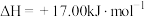 |
| C.②的反应物总能量比①的反应物总能量低 |
D.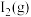 比 比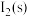 稳定 稳定 |
您最近一年使用:0次
名校
2 . 为实现我国承诺的“碳达峰、碳中和”目标,中国科学院提出了“液态阳光”方案,即将工业生产过程中排放的二氧化碳转化为甲醇,其中反应之一是:
 。回答下列问题:
。回答下列问题:
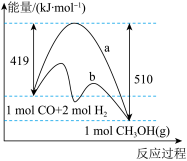
(1)该反应的能量变化如图所示,反应的
______ ,曲线______ (填“a”或“b”)表示使用了催化剂。
(2)相同温度下,若已知反应 的平衡常数为
的平衡常数为 ,反应
,反应 的平衡常数为
的平衡常数为 ,则反应
,则反应 的化学平衡常数K=
的化学平衡常数K=______ (用含 和
和 的代数式表示)。
的代数式表示)。
(3)在恒温恒容密闭容器中按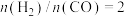 加入反应起始物
加入反应起始物
Ⅰ.下列描述不能说明反应达到平衡状态的是______
A.容器内压强不再变化 B.氢气的转化率达到最大值
C.容器内CO与 的浓度相等 D.容器内CO的体积分数不再变化
的浓度相等 D.容器内CO的体积分数不再变化
II.若CO的平衡转化率[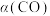 ]随温度的变化曲线如图所示,R、S两点平衡常数大小:
]随温度的变化曲线如图所示,R、S两点平衡常数大小:
______  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。 温度下,测得起始压强
温度下,测得起始压强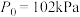 ,达平衡时
,达平衡时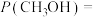
______ kPa。


 。回答下列问题:
。回答下列问题:(1)该反应的能量变化如图所示,反应的


(2)相同温度下,若已知反应
 的平衡常数为
的平衡常数为 ,反应
,反应 的平衡常数为
的平衡常数为 ,则反应
,则反应 的化学平衡常数K=
的化学平衡常数K= 和
和 的代数式表示)。
的代数式表示)。(3)在恒温恒容密闭容器中按
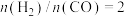 加入反应起始物
加入反应起始物Ⅰ.下列描述不能说明反应达到平衡状态的是
A.容器内压强不再变化 B.氢气的转化率达到最大值
C.容器内CO与
 的浓度相等 D.容器内CO的体积分数不再变化
的浓度相等 D.容器内CO的体积分数不再变化II.若CO的平衡转化率[
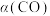 ]随温度的变化曲线如图所示,R、S两点平衡常数大小:
]随温度的变化曲线如图所示,R、S两点平衡常数大小:
 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。 温度下,测得起始压强
温度下,测得起始压强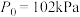 ,达平衡时
,达平衡时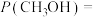

您最近一年使用:0次
名校
解题方法
3 . 回答下列问题:
(1)已知下列热化学方程式:
①
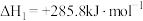
②
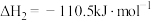
③
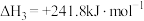
上述反应中属于放热反应的是__________ 。
(2)①的反应过程是太阳光催化分解水制氢气,该反应中主要能量转化形式为_________ 。
a.太阳能转化为化学能 b.化学能转化为电能
(3)若反应③使用催化剂,那么 将
将_______ (填“增大”“减小”或“不变”)
(4)反应 的
的
______  。
。
(5) 气态高能燃料乙硼烷
气态高能燃料乙硼烷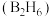 在氧气中燃烧,生成固态三氧化二硼
在氧气中燃烧,生成固态三氧化二硼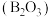 和气态水,释放
和气态水,释放 的热。
的热。
①写出反应的热化学方程式____________ 。
②11.2L(标准状况)气态乙硼烷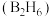 完全燃烧生成液态水生成的热
完全燃烧生成液态水生成的热_______  。
。
(1)已知下列热化学方程式:
①

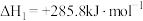
②

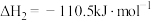
③

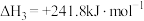
上述反应中属于放热反应的是
(2)①的反应过程是太阳光催化分解水制氢气,该反应中主要能量转化形式为
a.太阳能转化为化学能 b.化学能转化为电能
(3)若反应③使用催化剂,那么
 将
将(4)反应
 的
的
 。
。(5)
 气态高能燃料乙硼烷
气态高能燃料乙硼烷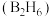 在氧气中燃烧,生成固态三氧化二硼
在氧气中燃烧,生成固态三氧化二硼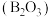 和气态水,释放
和气态水,释放 的热。
的热。①写出反应的热化学方程式
②11.2L(标准状况)气态乙硼烷
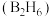 完全燃烧生成液态水生成的热
完全燃烧生成液态水生成的热 。
。
您最近一年使用:0次
4 . 化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于吸热反应的是___________(填字母)。
(2)获取能量变化的途径
①通过化学键的键能计算。已知:
计算可得: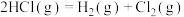 ∆H=
∆H=___________ kJ/mol
②通过盖斯定律可计算。已知在25℃、101kPa时:
I.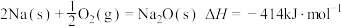
II.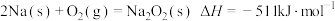
写出Na2O2与Na反应生成Na2O的热化学方程式:___________ 。
(3)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。
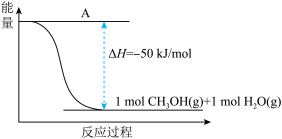
该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的∆H___________ (填“变大”“变小”或“不变”)。
(4)有机物M经过太阳光光照可转化成N,转化过程如下:
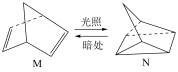
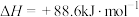
则M、N相比,较稳定的是___________ 。
(1)下列反应中,属于吸热反应的是___________(填字母)。
| A.NaOH与盐酸反应 | B.甲烷的燃烧反应 |
| C.Ba(OH)2∙8H2O与氯化铵反应 | D.锌与盐酸反应 |
(2)获取能量变化的途径
①通过化学键的键能计算。已知:
| 化学键种类 |  |  |  |
| 键能(kJ/mol) | 436 | 247 | 434 |
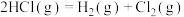 ∆H=
∆H=②通过盖斯定律可计算。已知在25℃、101kPa时:
I.
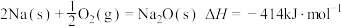
II.
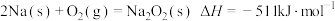
写出Na2O2与Na反应生成Na2O的热化学方程式:
(3)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。

该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的∆H
(4)有机物M经过太阳光光照可转化成N,转化过程如下:

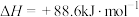
则M、N相比,较稳定的是
您最近一年使用:0次
名校
5 . 温室气体让地球发烧,倡导低碳生活,是一种可持续发展的环保责任,将 应用于生产中实现其综合利用是目前的研究热点。
应用于生产中实现其综合利用是目前的研究热点。
(1)在催化作用下由 和
和 转化为
转化为 的反应历程示意图如下图。
的反应历程示意图如下图。

在合成 的反应历程中,下列有关说法正确的是
的反应历程中,下列有关说法正确的是___________ (填字母)。
a.该催化剂使反应的平衡常数增大
b. 过程中,有
过程中,有 键断裂和
键断裂和 键形成
键形成
c.生成乙酸的反应原子利用率等于100%
d.
(2)以 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:
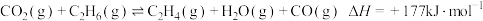 (主反应)
(主反应)
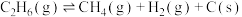
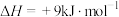 (副反应)
(副反应)
①主反应的反应历程可分为如下两步,反应过程中能量变化如图所示:

i.

ii.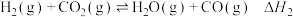

___________ ,主反应的决速步骤为___________ (填“反应i”或“反应ii”)。
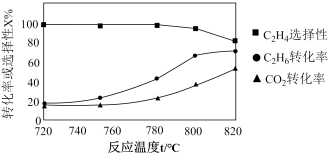
②向恒压密闭容器中充入 和
和 ,温度对催化剂K—Fe—Mn/Si—2性能的影响如图所示,工业生产中主反应应选择的温度是
,温度对催化剂K—Fe—Mn/Si—2性能的影响如图所示,工业生产中主反应应选择的温度是___________ 。
 应用于生产中实现其综合利用是目前的研究热点。
应用于生产中实现其综合利用是目前的研究热点。(1)在催化作用下由
 和
和 转化为
转化为 的反应历程示意图如下图。
的反应历程示意图如下图。
在合成
 的反应历程中,下列有关说法正确的是
的反应历程中,下列有关说法正确的是a.该催化剂使反应的平衡常数增大
b.
 过程中,有
过程中,有 键断裂和
键断裂和 键形成
键形成c.生成乙酸的反应原子利用率等于100%
d.

(2)以
 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下: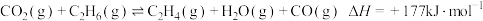 (主反应)
(主反应)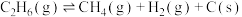
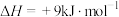 (副反应)
(副反应)①主反应的反应历程可分为如下两步,反应过程中能量变化如图所示:

i.


ii.
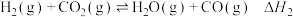

②向恒压密闭容器中充入
 和
和 ,温度对催化剂K—Fe—Mn/Si—2性能的影响如图所示,工业生产中主反应应选择的温度是
,温度对催化剂K—Fe—Mn/Si—2性能的影响如图所示,工业生产中主反应应选择的温度是
您最近一年使用:0次
名校
解题方法
6 . 回答下列问题
(1)已知反应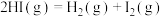 的
的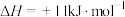 ,1
,1
 、1
、1
 分子中化学键断裂时分别需要吸收436
分子中化学键断裂时分别需要吸收436 、151
、151 的能量,则1
的能量,则1
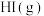 分子中化学键断裂时需吸收的能量为
分子中化学键断裂时需吸收的能量为___________  。
。
(2)已知:
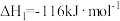

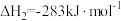

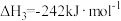
则表示1 气态甲醇完全燃烧生成
气态甲醇完全燃烧生成 和水蒸气时的热化学方程式为
和水蒸气时的热化学方程式为___________ 。
(3)25℃时有甲、乙、丙三种溶液,甲为 溶液,乙为
溶液,乙为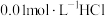 溶液,丙为
溶液,丙为 溶液,请回答下列问题:
溶液,请回答下列问题:
①甲溶液的
___________ 。乙溶液中由水电离出的
___________  。
。
②写出丙的电离方程式___________ 。
③用 的HCl和
的HCl和 两溶液分别与25mL甲完全中和,则消耗这两种酸的体积大小关系为
两溶液分别与25mL甲完全中和,则消耗这两种酸的体积大小关系为
___________  (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
(4)室温时,向 的醋酸溶液中加入等体积的
的醋酸溶液中加入等体积的 的
的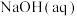 ,充分反应后所得溶液的
,充分反应后所得溶液的 ,所得溶液中
,所得溶液中
___________  。
。
(1)已知反应
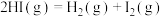 的
的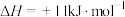 ,1
,1
 、1
、1
 分子中化学键断裂时分别需要吸收436
分子中化学键断裂时分别需要吸收436 、151
、151 的能量,则1
的能量,则1
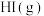 分子中化学键断裂时需吸收的能量为
分子中化学键断裂时需吸收的能量为 。
。(2)已知:

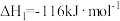

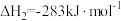

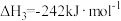
则表示1
 气态甲醇完全燃烧生成
气态甲醇完全燃烧生成 和水蒸气时的热化学方程式为
和水蒸气时的热化学方程式为(3)25℃时有甲、乙、丙三种溶液,甲为
 溶液,乙为
溶液,乙为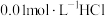 溶液,丙为
溶液,丙为 溶液,请回答下列问题:
溶液,请回答下列问题:①甲溶液的


 。
。②写出丙的电离方程式
③用
 的HCl和
的HCl和 两溶液分别与25mL甲完全中和,则消耗这两种酸的体积大小关系为
两溶液分别与25mL甲完全中和,则消耗这两种酸的体积大小关系为
 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。(4)室温时,向
 的醋酸溶液中加入等体积的
的醋酸溶液中加入等体积的 的
的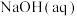 ,充分反应后所得溶液的
,充分反应后所得溶液的 ,所得溶液中
,所得溶液中
 。
。
您最近一年使用:0次
名校
7 . 天然气经 和
和 重整制合成气,再由合成气制备甲醇的相关反应如下:
重整制合成气,再由合成气制备甲醇的相关反应如下:
①主反应: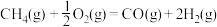
 ;
;
②副反应:
 ;
;
③主反应:
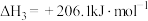
④主反应: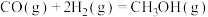
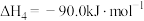 ;
;
⑤主反应: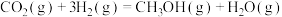
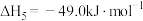 。下列说法不正确的是
。下列说法不正确的是
 和
和 重整制合成气,再由合成气制备甲醇的相关反应如下:
重整制合成气,再由合成气制备甲醇的相关反应如下:①主反应:
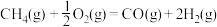
 ;
;②副反应:

 ;
;③主反应:

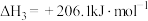
④主反应:
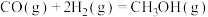
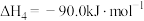 ;
;⑤主反应:
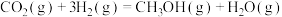
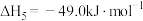 。下列说法不正确的是
。下列说法不正确的是A. 大于 大于 |
| B.反应①为反应③提供能量 |
C.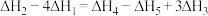 |
D. 为放热反应 为放热反应 |
您最近一年使用:0次
名校
8 . Ⅰ.2018年,美国退出了《巴黎协定》实行再工业化战略,而中国却加大了环保力度,生动诠释了我国负责任的大国形象。近年我国大力加强温室气体 催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。
催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。
(1)已知: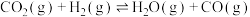
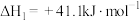

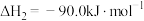
写出 催化氢化合成甲醇的热化学方程式:
催化氢化合成甲醇的热化学方程式:___________ 。
(2)250℃,在体积为2.0L的恒容密闭容器中加入 、
、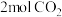 和催化剂,10min时反应达到平衡,测得
和催化剂,10min时反应达到平衡,测得 。
。
①前10min的平均反应速率
___________  。
。
②下列选项中,能使化学反应速率增大的是___________ (填字母)。
A.增大 的浓度B.减小
的浓度B.减小 的浓度
的浓度
C.降低反应温度D.缩小反应容器体积
Ⅱ.某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:实验原理为
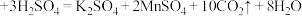 ,实验内容及记录如下:
,实验内容及记录如下:
(3)根据上表中的实验数据,可以得到的结论是___________ 。
(4)忽略混合前后溶液体积的微小变化,实验1在1.5min内的平均反应速率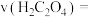
___________  。
。
 催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。
催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。(1)已知:
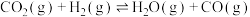
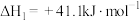

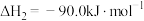
写出
 催化氢化合成甲醇的热化学方程式:
催化氢化合成甲醇的热化学方程式:(2)250℃,在体积为2.0L的恒容密闭容器中加入
 、
、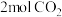 和催化剂,10min时反应达到平衡,测得
和催化剂,10min时反应达到平衡,测得 。
。①前10min的平均反应速率

 。
。②下列选项中,能使化学反应速率增大的是
A.增大
 的浓度B.减小
的浓度B.减小 的浓度
的浓度C.降低反应温度D.缩小反应容器体积
Ⅱ.某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:实验原理为

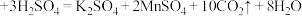 ,实验内容及记录如下:
,实验内容及记录如下:| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 溶液紫色褪去所需时间/min | |||
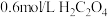 溶液 | H₂O | 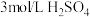 溶液 | 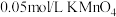 溶液 | ||
| 1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
| 2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
| 3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |
(3)根据上表中的实验数据,可以得到的结论是
(4)忽略混合前后溶液体积的微小变化,实验1在1.5min内的平均反应速率
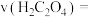
 。
。
您最近一年使用:0次
10-11高一下·辽宁大连·期末
名校
解题方法
9 . 灰锡(以粉末状存在)和白锡是锡的两种同素异形体。下列说法正确的是
已知:①
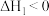
②
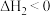
③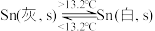
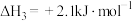
已知:①

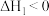
②

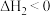
③
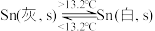
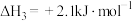
A.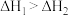 |
| B.锡在常温下以灰锡状态存在 |
| C.灰锡转化为白锡的反应是放热反应 |
D.锡制器皿长期处在低于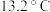 的环境中,会自行毁坏 的环境中,会自行毁坏 |
您最近一年使用:0次
2023-12-18更新
|
111次组卷
|
89卷引用:福建省泉州第十六中学2019-2020学年高二10月份月考化学试题
福建省泉州第十六中学2019-2020学年高二10月份月考化学试题福建省平潭翰英中学2021-2022学年高二上学期第一次月考(选考)化学试题(已下线)2011-2012天津南开中学高二第一学期期中考试理科化学试卷(已下线)2011-2012学年安徽省舒城晓天中学高二下学期质量测试2化学试卷(已下线)2014-2015学年广东东莞市第七中学高二上学期第一次月考化学试卷2015-2016学年山西太原五中高二上第一周考理科化学试卷2015-2016学年山东寿光中学高二上10月月考化学试卷2015-2016学年黑龙江哈尔滨附属中学高二上期中化学试卷2016-2017学年河北冀州中学高二上第一次月考化学试卷云南省姚安县第一中学2017-2018学年高二10月月考化学试题江西省南康中学2017-2018学年高二上学期第一次月考化学试题浙江省嘉兴市第一中学2017-2018学年高二上学期期中考试化学试题云南省峨山彝族自治县第一中学2017-2018学年高二上学期11月考试化学试题(已下线)黄金30题系列 高二化学(选修4) 小题好拿分【提升版】【全国校级联考】浙江省金华市十校2017-2018学年高二下学期期末联考化学试题湖南辰溪博雅实验学校2018-2019学年高二8月月考化学试题浙江省宁波市北仑中学2018-2019学年高二上学期期初返校考试化学试题云南省曲靖市会泽县一中2018-2019学年高二上学期第一次半月考化学试题安徽省芜湖市顶峰美术学校2018-2019学年高二上学期第一次月考化学试题陕西省西安市远东第一中学2018-2019学年高二上学期10月月考化学试题吉林省白城市通榆县第一中学2019-2020学年高二上学期第一次月考化学试题山西省晋中市平遥县第二中学2019-2020学年高二10月月考化学试题福建2020届高三化学总复习专题训练——选修四化学反应原理测试湖南省长沙市第一中学2019-2020学年高二上学期第一次月考化学试题四川省乐山市2019-2020学年高二上学期期末教学质量检测化学试题(已下线)1.1.3 反应焓变的计算 练习——【高中新教材同步备课】鲁科版高中化学选择性必修1(已下线)第01章 化学反应的热效应(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)吉林省辽源市田家炳高级中学校2020-2021学年高二上学期第一次月考化学试题陕西省汉中市洋县中学2020-2021学年高二上学期第一次月考化学试题广东省汕头市澄海中学2020-2021学年高二上学期期中考试化学(选考)试题江西省赣州市南康区南康中学2020-2021学年高二上学期第三次大考化学试题河北省张家口市宣化第一中学2020-2021学年高二上学期1月月考化学试题云南省通海县一中2020-2021学年高二下学期期中考试化学试题(已下线)第一节 化学反应与能量变化 (第2课时 热化学方程式 中和热的测定)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(已下线)1.1.2 热化学方程式-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)1.1.2 热化学方程式 燃烧热-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)安徽省合肥新城高升学校2021-2022学年高二上学期第一次月考化学试题江西省九江一中2020-2021学年高二上学期月考化学试题河北省藁城新冀明中学2021-2022学年高二上学期10月月考化学试题内蒙古赤峰市第二中学2021-2022学年高二上学期第一次月考化学试题广东省珠海市第二中学2021-2022学年高二上学期期中考试化学试题河北省衡水市第十四中学(西校区)2021-2022学年高二上学期二调考试化学试题江西省六校2021-2022学年高二上学期期末联考化学试题四川省遂宁市射洪中学校2021—2022学年高二上学期第三次(12月)月考化学试题宁夏银川市第二中学2021-2022学年高二下学期第一次月考化学试题内蒙古包头市第四中学2021-2022学年高二上学期期中考试化学试题河南省豫西顶级名校2021-2022学年高二下学期4月联考化学试题第二节 反应热的计算 第1课时 盖斯定律(已下线)第04讲 第一章《化学反应的热效应》单元测试(培优提升)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)1.2 反应热的计算-同步学习必备知识江西省丰城市第九中学2021-2022学年高二上学期期中考试(日新班)化学试题江西省金溪县第一中学2022-2023年度高二上学期第一次月考化学试题河南省通许县一中2022—2023年高二上学期第一次月考化学试题安徽省芜湖市无为襄安中学2022-2023高二上学期第一次月考化学试题陕西省安康市2022-2023学年高二上学期11月期中化学试题宁夏回族自治区银川一中2022-2023学年高二上学期期中考试化学试题浙江省金华市江南中学等两校2022-2023学年高二上学期12月阶段测试化学试题河南省南乐县第一高级中学2021-2022学年高二上学期9月半月考化学试题广东仲元中学2021-2022学年高二上学期开学检测 化学试题广东省广州大学附属中学2022-2023学年高二上学期期中考试化学试题安徽省马鞍山市第二十二中学2022-2023学年高二上学期阶段检测化学试题内蒙古自治区包头市第九中学2022-2023学年高二上学期期末考试化学试题广东省广州市第八十六中学2022-2023学年高二上学期期中考试化学试题广东华侨中学2022-2023学年高二上学期期中考试化学试题作业(三) 反应热的计算作业(三) 反应焓变的计算河南省开封市祥符高级中学2023-2024学年高二上学期第一次月考化学试题黑龙江省佳木斯市第一中学2023-2024学年高二上学期10月月考化学试题宁夏回族自治区石嘴山市第三中学2023-2024学年高二9月月考化学试题河南省焦作市博爱县第一中学2023-2024学年高二上学期10月月考化学试题广东省广州市越秀区第七中学2023-2024学年高二上学期10月月考化学试题广东省佛山市顺德区罗定邦中学2023-2024学年高二上学期期中考试化学试题广东省深圳市罗湖外语学校2023-2024学年高二上学期期中考试化学试题山西省朔州市怀仁市第九中学高中部2023-2024学年高二上学期11月期中化学试题云南省腾冲市第八中学2022-2023学年高二下学期第三次月考化学试题黑龙江省方正县高楞高级中学校2023-2024学年高二上学期期中化学试题(已下线)2010~2011学年辽宁省瓦房店市高级中学高一下学期期末考试(已下线)2011-2012学年湖北武汉部分重点中学高一下学期期末考试化学题(已下线)2013-2014黑龙江省哈六中学高一下学期期中考试化学试卷高中化学人教版 选修四 第一章 化学反应与能量 第三节 化学反应热的计算 化学反应热的计算第一课时(盖斯定律)【全国百强校】黑龙江省牡丹江市第一高级中学2017-2018学年高一下学期期末考试化学试题海南省海口市海南中学2020届高三下学期第七次月考化学试题海南省海南中学2020届高三下学期第七次月考化学试题河北省石家庄市第二十三中学2020-2021学年高一第二学期5月月考化学试题吉林省长春市十一高中2020-2021学年高一下学期第三学程考试化学试题河北省石家庄市第二中学2021-2022学年高一下学期期中考试化学试题安徽省安庆二中2022-2023学年高一下学期5月月考化学试题湖南省常德市汉寿县第一中学2023-2024学年高三下学期开学化学试题河北省石家庄卓越中学2023-2024学年高一下学期期中考试化学试题
名校
解题方法
10 . 二氧化碳加氢制甲烷过程中的主要反应为
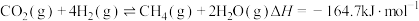
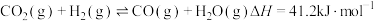
在密闭容器中,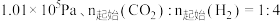 时,
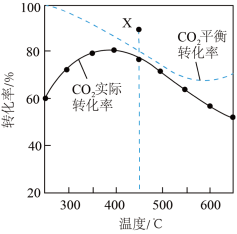
时, 平衡转化率、在催化剂作用下反应相同时间所测得的
平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率随温度的变化如图所示。
实际转化率随温度的变化如图所示。 的选择性可表示为
的选择性可表示为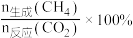 。下列说法正确的是
。下列说法正确的是
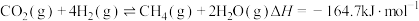
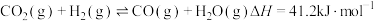
在密闭容器中,
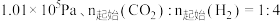 时,
时, 平衡转化率、在催化剂作用下反应相同时间所测得的
平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率随温度的变化如图所示。
实际转化率随温度的变化如图所示。 的选择性可表示为
的选择性可表示为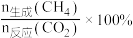 。下列说法正确的是
。下列说法正确的是
A.反应 的焓变 的焓变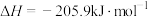 |
B. 的平衡选择性随着温度的升高而增加 的平衡选择性随着温度的升高而增加 |
C.用该催化剂催化二氧化碳反应的最佳温度范围约为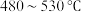 |
D. 时,提高 时,提高 的值或增大压强,均能使 的值或增大压强,均能使 平衡转化率达到X点的值 平衡转化率达到X点的值 |
您最近一年使用:0次



