1 . 根据已知,回答下列问题。
(1)在 、
、 下,
下, 甲烷燃烧生成
甲烷燃烧生成 和液态水时放热
和液态水时放热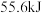 。则表示甲烷燃烧热的热化学方程式为
。则表示甲烷燃烧热的热化学方程式为______ 。
(2)常温常压下,断裂 (理想)气体分子化学键所吸收的能量或形成
(理想)气体分子化学键所吸收的能量或形成 (理想)气体分子化学键所放出的能量称为键能,下表是一些键能数
(理想)气体分子化学键所放出的能量称为键能,下表是一些键能数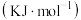
根据键能数据计算以下反应的反应热: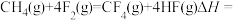
______ 。
(3)随着科学技术的进步,人们研制了多种甲醇质子交换膜燃料电池,以满足不同的需求。有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是
A.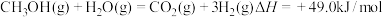
B.
由上述方程式可知, 的燃烧热
的燃烧热______ (填“大于”、“等于”或“小于”)
(4)火箭的常规燃料是液态四氧化二氮和液态肼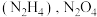 作氧化剂,有人认为若用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
作氧化剂,有人认为若用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
已知:


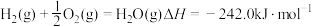
请写出肼和氟气反应的热化学方程式:______ 。
(1)在
 、
、 下,
下, 甲烷燃烧生成
甲烷燃烧生成 和液态水时放热
和液态水时放热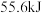 。则表示甲烷燃烧热的热化学方程式为
。则表示甲烷燃烧热的热化学方程式为(2)常温常压下,断裂
 (理想)气体分子化学键所吸收的能量或形成
(理想)气体分子化学键所吸收的能量或形成 (理想)气体分子化学键所放出的能量称为键能,下表是一些键能数
(理想)气体分子化学键所放出的能量称为键能,下表是一些键能数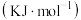
化学键 | 键能 | 化学键 | 键能 | 化学键 | 键能 |
C-H | 414 | C-F | 489 | H-F | 565 |
| 436 |
| 391 |
| 158 |
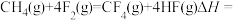
(3)随着科学技术的进步,人们研制了多种甲醇质子交换膜燃料电池,以满足不同的需求。有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是
A.
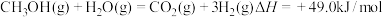
B.

由上述方程式可知,
 的燃烧热
的燃烧热
(4)火箭的常规燃料是液态四氧化二氮和液态肼
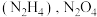 作氧化剂,有人认为若用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
作氧化剂,有人认为若用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。已知:


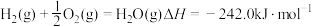
请写出肼和氟气反应的热化学方程式:
您最近一年使用:0次
名校
解题方法
2 . 完成下列问题
(1)土壤中的微生物可将大气中的 经两步反应氧化成
经两步反应氧化成 ,第一步反应的能量变化如图1所示。
,第一步反应的能量变化如图1所示。
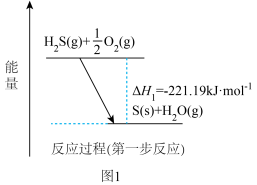
已知: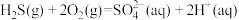
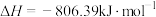
写出第二步反应的热化学方程式:___________ 。
(2)①远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的___________ 腐蚀。
②利用如图2装置,可以模拟铁的电化学防护。若X为碳棒,为减缓铁的腐蚀,开关K应置于___________ 处。若X为锌,开关K置于M处,该电化学防护法称为___________ 。
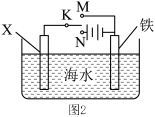
(3)以反应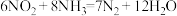 为原理设计电池(如图3所示,a、b电极均为惰性电极),既能有效消除氮氧化物的排放,减小环境污染,又能充分利用化学资源。(阳离子交换膜只允许阳离子通过)
为原理设计电池(如图3所示,a、b电极均为惰性电极),既能有效消除氮氧化物的排放,减小环境污染,又能充分利用化学资源。(阳离子交换膜只允许阳离子通过)

①电池工作时,电解质溶液中的 穿过阳离子交换膜向
穿过阳离子交换膜向___________ (填“a”或“b”)电极移动。
②b电极上的电极反应式为___________ 。
③电池工作一段时间后转移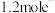 ,左侧工作室溶液的pH
,左侧工作室溶液的pH___________ (填“变大”、“变小”或“不变”),处理的 体积为
体积为___________ L(标准状况下)。
(1)土壤中的微生物可将大气中的
 经两步反应氧化成
经两步反应氧化成 ,第一步反应的能量变化如图1所示。
,第一步反应的能量变化如图1所示。
已知:
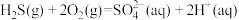
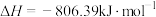
写出第二步反应的热化学方程式:
(2)①远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的
②利用如图2装置,可以模拟铁的电化学防护。若X为碳棒,为减缓铁的腐蚀,开关K应置于

(3)以反应
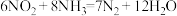 为原理设计电池(如图3所示,a、b电极均为惰性电极),既能有效消除氮氧化物的排放,减小环境污染,又能充分利用化学资源。(阳离子交换膜只允许阳离子通过)
为原理设计电池(如图3所示,a、b电极均为惰性电极),既能有效消除氮氧化物的排放,减小环境污染,又能充分利用化学资源。(阳离子交换膜只允许阳离子通过)
①电池工作时,电解质溶液中的
 穿过阳离子交换膜向
穿过阳离子交换膜向②b电极上的电极反应式为
③电池工作一段时间后转移
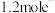 ,左侧工作室溶液的pH
,左侧工作室溶液的pH 体积为
体积为
您最近一年使用:0次
名校
3 . 已知:NO和 转化为
转化为 的反应机理如下:
的反应机理如下:
① (快)
(快)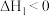 平衡常数
平衡常数
②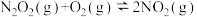 (慢)
(慢)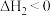 平衡常数
平衡常数
下列说法正确的是
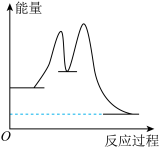
 转化为
转化为 的反应机理如下:
的反应机理如下:①
 (快)
(快)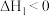 平衡常数
平衡常数
②
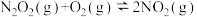 (慢)
(慢)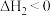 平衡常数
平衡常数
下列说法正确的是

A. 的 的 |
B.反应②的速率大小决定 的反应速率 的反应速率 |
| C.反应过程中的能量变化可用上图表示 |
D. 的平衡常数 的平衡常数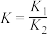 |
您最近一年使用:0次
2023-12-14更新
|
126次组卷
|
2卷引用:福建省福州第七中学2023-2024学年高二上学期期中考试化学试题
名校
4 . 完成下列问题。
(1)已知:①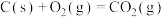
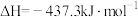
②
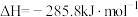
③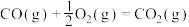
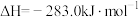
则固态碳和水蒸气反应生成CO和 的热化学方程式为
的热化学方程式为___________ 。
(2)工业上,二氧化碳和氢气在催化剂作用下可以制备甲醇:
CO2(g) + 3H2(g) CH3OH(g) + H2O (g) ΔH
CH3OH(g) + H2O (g) ΔH 0
0
①该反应能在___________ (填“高温”、“低温”或“任何温度”)下自发。
②向2L的恒容密闭容器中充入1molCO2(g),3mol H2(g)欲同时提高CO2的平衡转化率和反应速率,下列措施可能有效的是___________ (填标号)。
a.降低温度并及时分离出产物 b.再向容器中充入1mol H2(g)
c.适当降低温度并加入合适的催化剂
(3)由CO2和H2合成CH3OH 的反应:CO2(g)+3H2(g) CH3OH(g) + H2O(g) ΔH
CH3OH(g) + H2O(g) ΔH 0,在10L的恒容密闭容器中投入0.5mol CO2和1.75mol H2,在不同条件下发生上述反应,测得平衡时甲醇的物质的量随温度、压强的变化如图所示,
0,在10L的恒容密闭容器中投入0.5mol CO2和1.75mol H2,在不同条件下发生上述反应,测得平衡时甲醇的物质的量随温度、压强的变化如图所示,
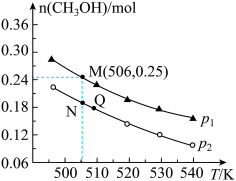
①图中压强p1___________ p2( “>”或“<”)
②M、N、Q三点平衡常数K由大到小顺序为___________ 。
③N点时,该反应的平衡常数K=___________ 。
(1)已知:①
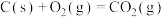
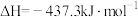
②

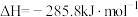
③
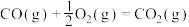
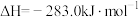
则固态碳和水蒸气反应生成CO和
 的热化学方程式为
的热化学方程式为(2)工业上,二氧化碳和氢气在催化剂作用下可以制备甲醇:
CO2(g) + 3H2(g)
 CH3OH(g) + H2O (g) ΔH
CH3OH(g) + H2O (g) ΔH 0
0①该反应能在
②向2L的恒容密闭容器中充入1molCO2(g),3mol H2(g)欲同时提高CO2的平衡转化率和反应速率,下列措施可能有效的是
a.降低温度并及时分离出产物 b.再向容器中充入1mol H2(g)
c.适当降低温度并加入合适的催化剂
(3)由CO2和H2合成CH3OH 的反应:CO2(g)+3H2(g)
 CH3OH(g) + H2O(g) ΔH
CH3OH(g) + H2O(g) ΔH 0,在10L的恒容密闭容器中投入0.5mol CO2和1.75mol H2,在不同条件下发生上述反应,测得平衡时甲醇的物质的量随温度、压强的变化如图所示,
0,在10L的恒容密闭容器中投入0.5mol CO2和1.75mol H2,在不同条件下发生上述反应,测得平衡时甲醇的物质的量随温度、压强的变化如图所示,
①图中压强p1
②M、N、Q三点平衡常数K由大到小顺序为
③N点时,该反应的平衡常数K=
您最近一年使用:0次
5 . 已知: 与不足量的
与不足量的 反应时,生成S和
反应时,生成S和 。根据以下三个热化学方程式:
。根据以下三个热化学方程式:
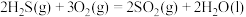
 ①
①

 ②
②

 ③
③
 、
、 、
、 三者大小关系正确的是
三者大小关系正确的是
 与不足量的
与不足量的 反应时,生成S和
反应时,生成S和 。根据以下三个热化学方程式:
。根据以下三个热化学方程式: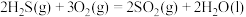
 ①
①
 ②
②
 ③
③ 、
、 、
、 三者大小关系正确的是
三者大小关系正确的是A.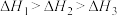 | B.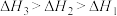 |
C.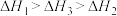 | D.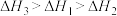 |
您最近一年使用:0次
2023-12-03更新
|
477次组卷
|
24卷引用:福建省福州格致中学2021-2022学年高二上学期第一阶段测试化学试题(10月)
福建省福州格致中学2021-2022学年高二上学期第一阶段测试化学试题(10月)江西省上饶县中学2017-2018学年高二上学期补考化学试题重庆市第三十中学2018-2019学年高二上学期第三次月考化学试题甘肃省古浪县第二中学2019-2020学年高二上学期基础知识竞赛化学试题山西省怀仁市2021-2022学年高二上学期期中化学试题广西钦州市2021-2022学年高二上学期期末考试化学试题第二节 反应热的计算 第2课时 反应热的计算甘肃省甘南藏族自治州合作第一中学2021-2022学年高二上学期期中考试化学试题(理)河南省濮阳市元龙高级中学2021-2022学年高二上学期期中考试化学试题贵州省部分学校2022-2023学年高二上学期10月联考化学试题贵州省“三新”改革联盟校联考2022-2023学年高二上学期期中考试化学试题陕西省咸阳市实验中学2021-2022学年高二上学期第三次月考化学试题湖南省怀化市雅礼实验学校2022-2023学年高二上学期第一次月考化学试题河南省洛阳市第一中学2022-2023学年高二上学期期末检测化学试题章末检测卷(一) 化学反应的热效应广东省广州市执信中学2023-2024学年高二上学期10月选考化学试题安徽省无为襄安中学2022-2023学年高二下学期开学考试化学试题山东省聊城市2023-2024学年高二上学期11月期中考试化学试题天津市南开区2023-2024学年高二上学期11月期中考试化学试题陕西省咸阳市兴平市西郊高级中学2023-2024学年高二上学期期中考试化学试题(已下线)寒假作业01 化学反应的热效应-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)江西省抚州市资溪县第一中学2023-2024学年高二上学期11月期中化学试题安徽省淮北市第一中学2023-2024学年高二下学期寒假自主学习质量评估化学试题江苏省淮安市涟水县第一中学2020届高三上学期第二次月考化学试题
名校
解题方法
6 . 甲醇( )是一种重要的化工原料,广泛应用于化工生产,也可以用作燃料。
)是一种重要的化工原料,广泛应用于化工生产,也可以用作燃料。
已知:
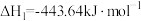

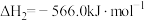
(1)试写出 在氧气中完全燃烧生成
在氧气中完全燃烧生成 和
和 的热化学方程式:
的热化学方程式:___________ 。
(2)某公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月。其中B电极的电极材料为碳,如图是一个电化学过程的示意图。请填空:

①放电时,甲醇在___________ (填“正”或“负”)极发生反应,正极的电极反应式为___________ ;
②工作时,B极的电极反应式为___________ ,当电路中通过0.1mol电子时,A极的质量___________ (填增加或减小)___________ g。
(3)某同学设计了一种用电解法制取 的实验装置(如图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法不正确的是___________(填序号)。
的实验装置(如图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法不正确的是___________(填序号)。
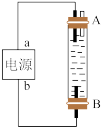
 )是一种重要的化工原料,广泛应用于化工生产,也可以用作燃料。
)是一种重要的化工原料,广泛应用于化工生产,也可以用作燃料。已知:

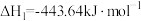

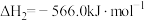
(1)试写出
 在氧气中完全燃烧生成
在氧气中完全燃烧生成 和
和 的热化学方程式:
的热化学方程式:(2)某公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月。其中B电极的电极材料为碳,如图是一个电化学过程的示意图。请填空:

①放电时,甲醇在
②工作时,B极的电极反应式为
(3)某同学设计了一种用电解法制取
 的实验装置(如图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法不正确的是___________(填序号)。
的实验装置(如图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法不正确的是___________(填序号)。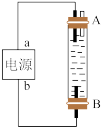
| A.a为电源正极,b为电源负极 | B.可以用NaCl溶液作为电解质溶液 |
| C.A、B两端都必须用铁作电极 | D.阴极发生的反应为 |
您最近一年使用:0次
2023-11-29更新
|
185次组卷
|
3卷引用:福建省福州高级中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
7 . 实现碳达峰、碳中和是贯彻新发展理念的内在要求,因此二氧化碳的合理利用成为研究热点,有效方式之一就是二氧化碳直接加氢合成高附加值产品。
(1)一定条件下,可用二氧化碳加氢合成甲醇。
已知CO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H= -50kJ·mol-1 ,该反应经过如下步骤来实现:
CH3OH(g)+H2O(g) ∆H= -50kJ·mol-1 ,该反应经过如下步骤来实现:
I.CO2(g)+H2(g) CO(g)+H2O(g) ∆H1= +40.9kJ·mol-1
CO(g)+H2O(g) ∆H1= +40.9kJ·mol-1
II.CO(g)+2H2(g) CH3OH(g) ∆H2
CH3OH(g) ∆H2
①求∆H2=___________ kJ·mol-1
②已知反应I是整个反应的决速步,下列示意图中能体现上述反应能量变化的是___________ (填标号)。
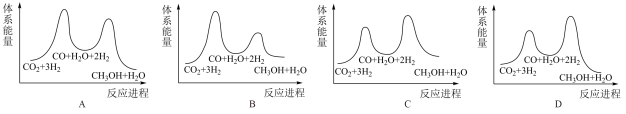
(2)一定条件下也可用二氧化碳加氢合成甲烷:4H2(g)+CO2(g) CH4(g)+2H2O(g)。
CH4(g)+2H2O(g)。
①在绝热恒容密闭容器中,一定能说明该反应达到平衡状态的是___________ (填字母)。
A.v正(H2)=v逆(CH4) B.t min内断裂H-H的数目与断裂O—H数目相等
C.容器温度保持不变 D.当H2(g)与CO2(g)物质的量之比保持4:1不变
一定温度下在2L恒温恒容密闭容器中初始加入2.0mol CO2和一定量H2,发生上述反应数据如下:
②则3min时容器中CH4的物质的量浓度为___________ ,该温度下反应的化学平衡常数为___________ 。
③保持温度不变,在达平衡后,向容器中再加入H2(g)和CH4(g)各1mol,则此时v(正)___________ v(逆)(填“>”、“<”或“=”)。
(3)最近科学家开发出一种新系统,“溶解”水中的二氧化碳,发生电化学反应,生成电能和氢气,其工作原理如图所示。
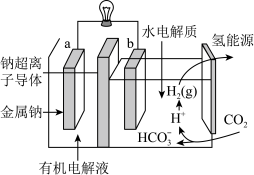
①有机电解液是有机溶剂加特定的盐加热制成,该装置的有机电解液___________ (填“能”或“不能”)用乙醇做溶剂。
②写出二氧化碳生成氢气的电极反应式:___________ 。
(1)一定条件下,可用二氧化碳加氢合成甲醇。
已知CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ∆H= -50kJ·mol-1 ,该反应经过如下步骤来实现:
CH3OH(g)+H2O(g) ∆H= -50kJ·mol-1 ,该反应经过如下步骤来实现:I.CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H1= +40.9kJ·mol-1
CO(g)+H2O(g) ∆H1= +40.9kJ·mol-1II.CO(g)+2H2(g)
 CH3OH(g) ∆H2
CH3OH(g) ∆H2①求∆H2=
②已知反应I是整个反应的决速步,下列示意图中能体现上述反应能量变化的是

(2)一定条件下也可用二氧化碳加氢合成甲烷:4H2(g)+CO2(g)
 CH4(g)+2H2O(g)。
CH4(g)+2H2O(g)。①在绝热恒容密闭容器中,一定能说明该反应达到平衡状态的是
A.v正(H2)=v逆(CH4) B.t min内断裂H-H的数目与断裂O—H数目相等
C.容器温度保持不变 D.当H2(g)与CO2(g)物质的量之比保持4:1不变
一定温度下在2L恒温恒容密闭容器中初始加入2.0mol CO2和一定量H2,发生上述反应数据如下:
| t(min) | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| n(CO2)(mol) | 2.0 | 1.5 | 1.1 | 0.8 | 0.6 | 0.5 | 0.5 |
| n(H2)(mol) | 3.2 |
③保持温度不变,在达平衡后,向容器中再加入H2(g)和CH4(g)各1mol,则此时v(正)
(3)最近科学家开发出一种新系统,“溶解”水中的二氧化碳,发生电化学反应,生成电能和氢气,其工作原理如图所示。

①有机电解液是有机溶剂加特定的盐加热制成,该装置的有机电解液
②写出二氧化碳生成氢气的电极反应式:
您最近一年使用:0次
8 . 完成下列问题。
(1)在一定温度下,向体积为2L的恒容密闭容器中充入一定量的A、B发生化学变化(除物质D为固体外,其余的物质均为气体),各物质的含量随时间的变化情况如图所示,回答下列问题:
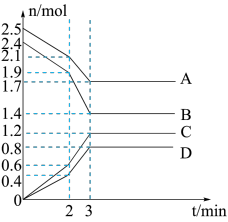
①写出该反应的化学方程式:___________ 。
② 内用D表示的化学反应速率
内用D表示的化学反应速率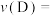
_______ 。
③该反应在 时改变了某一条件,则该条件可能为
时改变了某一条件,则该条件可能为___________ 。
(2)甲醇既是重要的化工原料,又可作为燃料,工业上将 催化加氢生产甲醇,发生如下反应:
催化加氢生产甲醇,发生如下反应:
反应Ⅰ: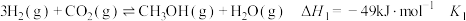
反应Ⅱ: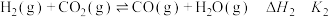
反应Ⅲ: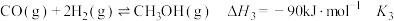
①
___________  ;相同条件下,反应Ⅲ的平衡常数
;相同条件下,反应Ⅲ的平衡常数
___________ (用平衡常数 、
、 表示)。
表示)。
②采用真空封管法制备磷化硼纳米颗粒,成功实现了高选择性电催化还原 制备甲醇,该反应历程如图所示。
制备甲醇,该反应历程如图所示。
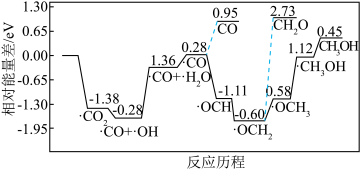
上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中___________ (填字母)的能量变化。
A. B.
B.
C. D.
D.
(1)在一定温度下,向体积为2L的恒容密闭容器中充入一定量的A、B发生化学变化(除物质D为固体外,其余的物质均为气体),各物质的含量随时间的变化情况如图所示,回答下列问题:

①写出该反应的化学方程式:
②
 内用D表示的化学反应速率
内用D表示的化学反应速率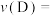
③该反应在
 时改变了某一条件,则该条件可能为
时改变了某一条件,则该条件可能为(2)甲醇既是重要的化工原料,又可作为燃料,工业上将
 催化加氢生产甲醇,发生如下反应:
催化加氢生产甲醇,发生如下反应:反应Ⅰ:
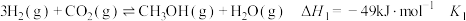
反应Ⅱ:
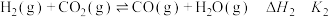
反应Ⅲ:
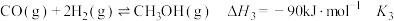
①

 ;相同条件下,反应Ⅲ的平衡常数
;相同条件下,反应Ⅲ的平衡常数
 、
、 表示)。
表示)。②采用真空封管法制备磷化硼纳米颗粒,成功实现了高选择性电催化还原
 制备甲醇,该反应历程如图所示。
制备甲醇,该反应历程如图所示。
上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中
A.
 B.
B.
C.
 D.
D.
您最近一年使用:0次
名校
9 . NO在医药化工行业有着十分重要的应用。
Ⅰ.工业上主要采用氨催化氧化法生产NO:
主反应: △H1
△H1
副反应: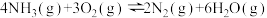 △H2=-1265kJ·mol-1
△H2=-1265kJ·mol-1
(1)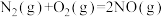 △H=+180kJ·mol-1,则△H1=
△H=+180kJ·mol-1,则△H1=_____ 。
(2)在不同的氨初始含量下,催化剂表面的反应速率与温度的关系如图。
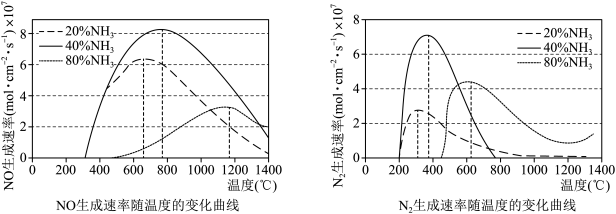
由图知,生产NO的最佳条件为_____。
(3)在一定的氨初始含量下,温度升高一段时间后,体系中 减小,可能的原因是
减小,可能的原因是_____ 。
Ⅱ.NO是空气污染物之一,以硫酸钠溶液为电解质,泡沫Cu为阴极,利用电化学装置实现NO的消除,阴极反应的模拟能量变化如图。
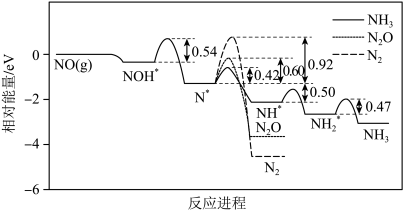
(4)从反应速率角度推断NO最终还原产物主要为_____ ,阴极的主要电极反应式为_____ 。
Ⅲ.用NO生产亚硝酰氯,反应如下: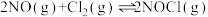 △H<0
△H<0
(5)提高NO平衡转化率可采取的措施是_____。
(6)一定温度下,在恒容密闭容器中,NO(g)和Cl2(g)按物质的量之比为2∶1进行反应,体系初始总压为p0,NO的平衡转化率为α,则平衡常数Kp=_____ (以分压表示,分压=总压×物质的量分数,用含p0、α代数式表示)。
Ⅰ.工业上主要采用氨催化氧化法生产NO:
主反应:
 △H1
△H1副反应:
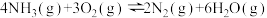 △H2=-1265kJ·mol-1
△H2=-1265kJ·mol-1(1)
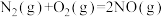 △H=+180kJ·mol-1,则△H1=
△H=+180kJ·mol-1,则△H1=(2)在不同的氨初始含量下,催化剂表面的反应速率与温度的关系如图。

由图知,生产NO的最佳条件为_____。
| A.氨含量20%、反应温度650℃ |
| B.氨含量40%、反应温度750℃ |
| C.氨含量80%、反应温度1150℃ |
| D.氨含量20%、反应温度750℃ |
(3)在一定的氨初始含量下,温度升高一段时间后,体系中
 减小,可能的原因是
减小,可能的原因是Ⅱ.NO是空气污染物之一,以硫酸钠溶液为电解质,泡沫Cu为阴极,利用电化学装置实现NO的消除,阴极反应的模拟能量变化如图。

(4)从反应速率角度推断NO最终还原产物主要为
Ⅲ.用NO生产亚硝酰氯,反应如下:
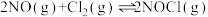 △H<0
△H<0(5)提高NO平衡转化率可采取的措施是_____。
| A.降低温度 | B.增大NO的浓度 | C.增大压强 | D.加入合适的催化剂 |
(6)一定温度下,在恒容密闭容器中,NO(g)和Cl2(g)按物质的量之比为2∶1进行反应,体系初始总压为p0,NO的平衡转化率为α,则平衡常数Kp=
您最近一年使用:0次
10 . 氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。
(1)已知: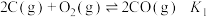 ,
,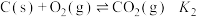 ,
,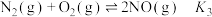 ,则反应
,则反应 的
的
___________ 。(用 、
、 、
、 表示)
表示)
(2)向容积为2L的密闭容器中加入活性炭(足量)和NO,发生反应 ,NO和
,NO和 的物质的量变化如下表所示。
的物质的量变化如下表所示。
①0~5min内,以 表示的该反应速率
表示的该反应速率
___________ ,最终达平衡时NO的转化率
___________ ,该温度T℃下的平衡常数
___________ 。
②保持温度T℃不变,向该2L密闭容器中加入该四种反应混合物各2mol,该时刻,正、逆反应速率的大小关系为: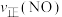
___________ 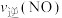 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)已知下列反应在298K时的反应焓变:
①
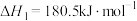
②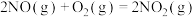
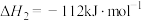
③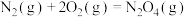
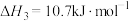
写出 转化为
转化为 的热化学方程式:
的热化学方程式:___________ 。
(1)已知:
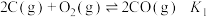 ,
,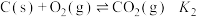 ,
,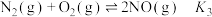 ,则反应
,则反应 的
的
 、
、 、
、 表示)
表示)(2)向容积为2L的密闭容器中加入活性炭(足量)和NO,发生反应
 ,NO和
,NO和 的物质的量变化如下表所示。
的物质的量变化如下表所示。| 条件 | 保持温度为T/℃ | ||||||
| 时间 | 0min | 5min | 10min | 15min | 20min | 25min | 30min |
| NO物质的量/mol |  |  |  | 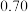 | 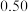 |  |  |
 物质的量/mol 物质的量/mol | 0 |  | 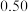 |  |  | 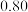 | 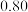 |
 表示的该反应速率
表示的该反应速率


②保持温度T℃不变,向该2L密闭容器中加入该四种反应混合物各2mol,该时刻,正、逆反应速率的大小关系为:
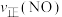
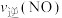 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)已知下列反应在298K时的反应焓变:
①

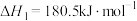
②
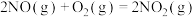
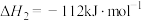
③
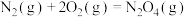
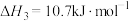
写出
 转化为
转化为 的热化学方程式:
的热化学方程式:
您最近一年使用:0次






