9-10高二下·福建福州·期末
1 . (1)火箭发射时可用肼(N2H4)为燃料,以二氧化氮作氧化剂,它们相互反应生成氮气和水蒸气。
已知:N2(g) + 2O2(g)= 2NO2(g) △H =" +67.7" kJ/mol;
N2H4(g)+ O2(g)=N2(g)+2H2O(g) △H=-534 kJ/mol
则N2H4和NO2反应生成氮气和水蒸气的热化学方程式为___________________ 。
(2)已知:常温下0.1mol/L的某酸H2A的pH=4,则该酸为_____ 酸(填“强”或“弱”), H2A的电离方程式为_______________________________________ ,该溶液中由水电离出的c(H+)=____________________ 。
(3)一定温度下,两种酸:a、盐酸 b、醋酸:
①当两种酸的物质的量浓度相同时,c(H+):a________ b(填“>”、“<”或“=”,下同)。
②在pH相同、体积相同的两种酸溶液中加入过量的铁粉,反应结束时生成H2的总体积: a______________ b。
③将pH相同,体积相同的两种酸溶液分别加水稀释100倍,所得溶液的pH值:a________ b
已知:N2(g) + 2O2(g)= 2NO2(g) △H =" +67.7" kJ/mol;
N2H4(g)+ O2(g)=N2(g)+2H2O(g) △H=-534 kJ/mol
则N2H4和NO2反应生成氮气和水蒸气的热化学方程式为
(2)已知:常温下0.1mol/L的某酸H2A的pH=4,则该酸为
(3)一定温度下,两种酸:a、盐酸 b、醋酸:
①当两种酸的物质的量浓度相同时,c(H+):a
②在pH相同、体积相同的两种酸溶液中加入过量的铁粉,反应结束时生成H2的总体积: a
③将pH相同,体积相同的两种酸溶液分别加水稀释100倍,所得溶液的pH值:a
您最近一年使用:0次
13-14高三·全国·课时练习
名校
解题方法
2 . 碳是形成化合物种类最多的元素,其单质及其部分化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
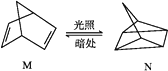
ΔH=+88.6 kJ·mol-1,则M、N相比,较稳定的是__________ 。
(2)CH3OH+O2(g) =CO2(g)+2H2O(g) ΔH=-akJ·mol-1,则a________ (填“>”“<”或“=”)238.6。(已知甲醇的燃烧热为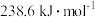 )
)
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:____________________________ 。
(4)将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s) ===2Al2O3(s)+3TiC(s) ΔH= -1 176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为_____________ 。
(1)有机物M经过太阳光光照可转化成N,转化过程如下:

ΔH=+88.6 kJ·mol-1,则M、N相比,较稳定的是
(2)CH3OH+O2(g) =CO2(g)+2H2O(g) ΔH=-akJ·mol-1,则a
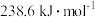 )
) (3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
(4)将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s) ===2Al2O3(s)+3TiC(s) ΔH= -1 176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为
您最近一年使用:0次
2016-12-08更新
|
2134次组卷
|
14卷引用:【全国百强校】福建省三明市第一中学2018-2019学年高二上学期第一次月考化学试题
【全国百强校】福建省三明市第一中学2018-2019学年高二上学期第一次月考化学试题山西省实验中学2017-2018学年高二上学期10月月考化学试题重庆市九校联盟2017-2018学年高二上学期期中考试化学试题【全国百强校】广东仲元中学2017-2018学年高二下学期期中考试(理)化学试题2018-2019学年人教版高二化学选修四章:化学反应与能量末测试题2018-2019学年人教版高中化学选修四 章末综合测评1 化学反应与能量河南省鹤壁市淇县第一中学2018-2019学年高二(普通班)上学期第一次月考化学试题(已下线)《2018-2019学年同步单元双基双测AB卷》第一单元 化学反应与能量单元测试(A卷)高二人教版选修4 期末学业测评(二)(已下线)2014年高考化学一轮复习课后规范训练6-1练习卷(已下线)二轮复习 专题8 化学反应中与能量变化 押题专练河北省安平中学2017-2018学年高一下学期期末考试化学试题1四川省成都经济技术开发区实验中学校2019届高三上学期入学考试化学试题辽宁省普兰店市第一中学2019届高三上学期期中考试化学试题
12-13高二上·福建龙岩·期末
3 . 为了减少CO对大气的污染,某研究性学习小组拟研究CO和H2O反应转化为绿色能源H2,已知:2CO(g)+O2(g)==2CO2(g) △H=-566KJ/mol
2H2(g)+O2(g)==2H2O(g) △H=-483.6KJ/mol H2O(g)="=" H2O(l) △H=-44.0KJ/mol
(1)1mol氢气燃烧生成液态水时放出的热为____________
(2)写出CO和 H2O(g)作用生成CO2和H2的热化学方程式_________________________ 。
(3)往1L体积不变的容器中加入0.200molCO和1.00molH2O(g),在t℃时反应并达到平衡,若该反应的化学平衡常数K=1,则t℃时CO的转化率为___________ ;反应达到平衡后,升高温度,此时平衡常数将___________ (填“变大”、“变小”或“不变”),平衡将向__________ (填“正”或“逆”)反应方向移动。
(4)H2是一种理想的绿色能源,可作燃料电池;若该氢氧燃料电池以KOH为电解质溶液,其负极的电极反应式是_______________________________________________ 。
2H2(g)+O2(g)==2H2O(g) △H=-483.6KJ/mol H2O(g)="=" H2O(l) △H=-44.0KJ/mol
(1)1mol氢气燃烧生成液态水时放出的热为
(2)写出CO和 H2O(g)作用生成CO2和H2的热化学方程式
(3)往1L体积不变的容器中加入0.200molCO和1.00molH2O(g),在t℃时反应并达到平衡,若该反应的化学平衡常数K=1,则t℃时CO的转化率为
(4)H2是一种理想的绿色能源,可作燃料电池;若该氢氧燃料电池以KOH为电解质溶液,其负极的电极反应式是
您最近一年使用:0次
2016-12-08更新
|
1014次组卷
|
4卷引用:2011-2012学年福建省龙岩一中上学期高二期末考试化学试卷
(已下线)2011-2012学年福建省龙岩一中上学期高二期末考试化学试卷江西省赣州市赣县区第三中学2020-2021学年高二(实验重点班)9月月考化学试题辽宁省大石桥市第三高级中学2020-2021学年高二12月月考化学试题(已下线)第12单元 电化学基础(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷
12-13高二上·福建泉州·期末
4 . (1)已知:2SO2(g)+ O2 (g)  2SO3 (g) △H =-196.6kJ·mol-1
2SO3 (g) △H =-196.6kJ·mol-1
2NO(g)+ O2 (g) 2NO2 (g) △H =-113.0kJ·mol-1
2NO2 (g) △H =-113.0kJ·mol-1
则反应NO2(g)+ SO2 (g) SO3 (g) +NO(g)的△H =
SO3 (g) +NO(g)的△H =_______ kJ·mol-1
一定条件下,将NO2与SO2按体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是_______ 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3与NO的体积比保持不变
d。每消耗1molSO3的同时生成1molNO2
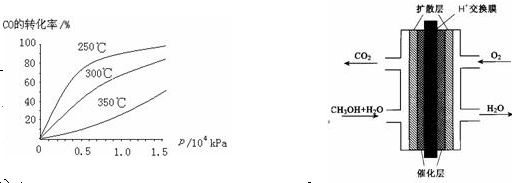
(2)CO可用于合成甲醇,反应方程式为CO(g)+ 2H2 (g) CH3OH (g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应△H
CH3OH (g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应△H _______ 0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是_______ 。
(3)甲醇(CH3OH)燃料电池的结构示意图如右上。甲醇进入_______ 极(填“正”或“负”),正极发生的电极反应为_______ 。
(4)101 kPa时,若16 gCH3OH完全燃烧生成液态水,放出热量为363.25 kJ/mol,则甲醇燃烧的热化学方程式为_______ 。
 2SO3 (g) △H =-196.6kJ·mol-1
2SO3 (g) △H =-196.6kJ·mol-12NO(g)+ O2 (g)
 2NO2 (g) △H =-113.0kJ·mol-1
2NO2 (g) △H =-113.0kJ·mol-1则反应NO2(g)+ SO2 (g)
 SO3 (g) +NO(g)的△H =
SO3 (g) +NO(g)的△H =一定条件下,将NO2与SO2按体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3与NO的体积比保持不变
d。每消耗1molSO3的同时生成1molNO2
(2)CO可用于合成甲醇,反应方程式为CO(g)+ 2H2 (g)
 CH3OH (g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应△H
CH3OH (g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应△H 
(3)甲醇(CH3OH)燃料电池的结构示意图如右上。甲醇进入
(4)101 kPa时,若16 gCH3OH完全燃烧生成液态水,放出热量为363.25 kJ/mol,则甲醇燃烧的热化学方程式为
您最近一年使用:0次
11-12高二上·福建福州·阶段练习
5 . 已知:在298K、100kPa时,
①C(s,石墨)+O2(g) = CO2(g) △H1 = -400 kJ·mol-1;
②2H2(g)+O2(g) = 2H2O(l) △H2 = -570 kJ·mol-1;
③2C2H2(g)+5O2(g) = 4CO2(g)+ 2H2O(l) △H3 = -2600 kJ·mol-1;
写出298K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的热化学方程式_______ 。
①C(s,石墨)+O2(g) = CO2(g) △H1 = -400 kJ·mol-1;
②2H2(g)+O2(g) = 2H2O(l) △H2 = -570 kJ·mol-1;
③2C2H2(g)+5O2(g) = 4CO2(g)+ 2H2O(l) △H3 = -2600 kJ·mol-1;
写出298K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的热化学方程式
您最近一年使用:0次
11-12高二上·福建·期中
6 . (1)已知①C2H5OH(g)+3O2(g)==2CO2(g)+3H2O(g) △H1=akJ·mol-1;
②H2O(g)==H2O(1) △H2=bkJ·mol-1;
③C2H5OH(g)==C2H5OH(1) △H3=ckJ·mol-1,
写出 C2H5OH(1)完全燃烧生成CO2(g)和H2O(1)的热化学方程式__________________
(2)已知下列热化学方程式:
① H2(g)+1/2O2(g)=H2O(g) ΔH=-241.8 kJ/mol
② C(s)+1/2O2(g)=CO(g) ΔH=-110.5 kJ/moL
则水煤气能源的制取原理:C(s)+H2O(g)=H2(g)+CO (g) ΔH=______ kJ/moL
②H2O(g)==H2O(1) △H2=bkJ·mol-1;
③C2H5OH(g)==C2H5OH(1) △H3=ckJ·mol-1,
写出 C2H5OH(1)完全燃烧生成CO2(g)和H2O(1)的热化学方程式
(2)已知下列热化学方程式:
① H2(g)+1/2O2(g)=H2O(g) ΔH=-241.8 kJ/mol
② C(s)+1/2O2(g)=CO(g) ΔH=-110.5 kJ/moL
则水煤气能源的制取原理:C(s)+H2O(g)=H2(g)+CO (g) ΔH=
您最近一年使用:0次
10-11高二上·福建厦门·阶段练习
7 . 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
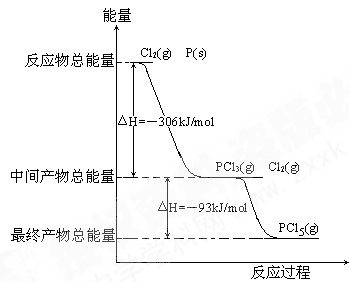
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式______________________________ 。
(2)PCl5分解成PCl3和Cl2的热化学方程式______________________________ ,上述分解反应是一个可逆反应,温度T1时,在密闭容器中加入0.80molPCl5,反应达到平衡时PCl5还剩0.60mol,其分解率α1[分解率即分解量除起始量]等于___________ ;。
(3)P和Cl2分两步反应生成1molPCl5的△H3=_________ ,P和Cl2一步反应生成1molPCl5的△H4______ △H3(填“大于”、“小于”或“等于”)。
(4)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是_____________ 。

根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式
(2)PCl5分解成PCl3和Cl2的热化学方程式
(3)P和Cl2分两步反应生成1molPCl5的△H3=
(4)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是
您最近一年使用:0次
9-10高二下·福建·期末
8 . 已知25℃、101kpa时,一些物质的燃烧热为:
(1)写出该条件下CH3OH(l)完全燃烧的热化学方程式:_____________ 。
(2)根据盖斯定律完成下列热化学方程式CO(g)+ 2H2(g)= CH3OH(l) △H=__________ 。
| 化学式 | CO(g) | H2(g) | CH3OH(l) |
| △H/(kJ/mol) | -283.0 | -285.8 | -726.5 |
(1)写出该条件下CH3OH(l)完全燃烧的热化学方程式:
(2)根据盖斯定律完成下列热化学方程式CO(g)+ 2H2(g)= CH3OH(l) △H=
您最近一年使用:0次
真题
9 . W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数一次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子核外有7个原子轨道填充了电子,Z能形成红色(或砖红色)的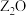 和黑色的ZO两种氧化物。
和黑色的ZO两种氧化物。
(1)W位于元素周期表第_________ 周期第_________ 族。W的气态氢化物稳定性比

__________ (填“强”或“弱”)。
(2)Y的基态原子核外电子排布式是________ ,Y的第一电离能比X的__________ (填“大”或“小”)。
(3)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是
_________________________________________________________________________ 。
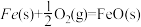
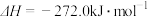
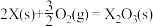
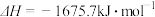
X的单质和FeO反应的热化学方程式是_________________________________________ 。
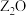 和黑色的ZO两种氧化物。
和黑色的ZO两种氧化物。(1)W位于元素周期表第

(2)Y的基态原子核外电子排布式是
(3)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是
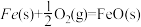
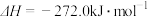
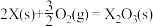
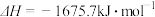
X的单质和FeO反应的热化学方程式是
您最近一年使用:0次



