1 . 2SO2(g)+O2(g) 2SO3(g) ΔH=akJ•mol-1,反应过程的能量变化如图所示。已知1molSO2(g)完全转化为1molSO3(g)放热99kJ。请回答:
2SO3(g) ΔH=akJ•mol-1,反应过程的能量变化如图所示。已知1molSO2(g)完全转化为1molSO3(g)放热99kJ。请回答:

(1)a=_____ kJ•mol-1.
(2)该反应常用V2O5作催化剂使图中ΔH_____ (填“升高”“降低”或“不变”)。
(3)已知单质硫的燃烧热为296kJ•mol-1,写出反应的热化学方程式:_____ 。
(4)工业上用H2和Cl2反应制HCl,各键能数据为:H—H:436kJ/mol,Cl—Cl:243kJ/mol,H—Cl:431kJ/mol。该反应的热化学方程式是_____ 。
(5)已知:①C(s)+O2(g)=CO2(g) ΔH=ΔH1;②2CO(g)+O2(g)=2CO2(g) ΔH=ΔH2;③TiO2(g)+2Cl2(g)=TiCl4(s)+O2(g) ΔH=ΔH3;则TiO2(g)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=_____ 。(列出关于ΔH1、ΔH2、ΔH3的表达式)
 2SO3(g) ΔH=akJ•mol-1,反应过程的能量变化如图所示。已知1molSO2(g)完全转化为1molSO3(g)放热99kJ。请回答:
2SO3(g) ΔH=akJ•mol-1,反应过程的能量变化如图所示。已知1molSO2(g)完全转化为1molSO3(g)放热99kJ。请回答:
(1)a=
(2)该反应常用V2O5作催化剂使图中ΔH
(3)已知单质硫的燃烧热为296kJ•mol-1,写出反应的热化学方程式:
(4)工业上用H2和Cl2反应制HCl,各键能数据为:H—H:436kJ/mol,Cl—Cl:243kJ/mol,H—Cl:431kJ/mol。该反应的热化学方程式是
(5)已知:①C(s)+O2(g)=CO2(g) ΔH=ΔH1;②2CO(g)+O2(g)=2CO2(g) ΔH=ΔH2;③TiO2(g)+2Cl2(g)=TiCl4(s)+O2(g) ΔH=ΔH3;则TiO2(g)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=
您最近一年使用:0次
解题方法
2 . 雾霾天气多次肆虐我国中东部地区。汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为2NO(g)+2CO(g) 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
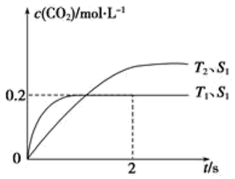
据此判断:
①该反应的ΔH___________ 0(填“>”或“<”),ΔS___________ 0(填“>”或“<”)
②在T1温度下,0~2 s内的平均反应速率v(N2)=___________ 。
③当固体催化剂的质量一定时,增大其表面积可提高化学 反应速率。若增大催化剂的表面积,则CO转化率___________ (填“增大”,“减少”或“不变”)
(2)工业上可采用CH3OH CO + 2H2的方法来制取高纯度的CO和H2。我国研究人员采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用 * 标注。下图为计算机模拟的各步反应的能量变化示意图:
CO + 2H2的方法来制取高纯度的CO和H2。我国研究人员采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用 * 标注。下图为计算机模拟的各步反应的能量变化示意图:
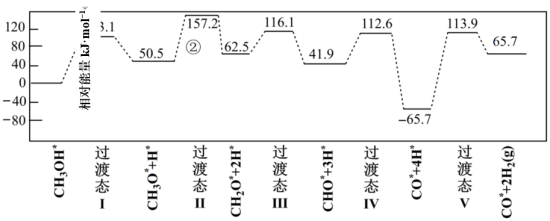
该历程中最大能垒(活化能)E正=___________ kJ·mol−1,该历程中,放热最多的步骤的化学方程式为___________ 。
(1)汽车尾气净化的主要原理为2NO(g)+2CO(g)
 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
据此判断:
①该反应的ΔH
②在T1温度下,0~2 s内的平均反应速率v(N2)=
③当固体催化剂的质量一定时,增大其表面积可提高化学 反应速率。若增大催化剂的表面积,则CO转化率
(2)工业上可采用CH3OH
 CO + 2H2的方法来制取高纯度的CO和H2。我国研究人员采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用 * 标注。下图为计算机模拟的各步反应的能量变化示意图:
CO + 2H2的方法来制取高纯度的CO和H2。我国研究人员采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用 * 标注。下图为计算机模拟的各步反应的能量变化示意图:
该历程中最大能垒(活化能)E正=
您最近一年使用:0次
名校
解题方法
3 . 按照要求写出下列热化学方程式。
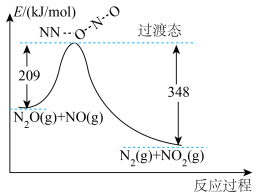
(1)由 和NO反应生成
和NO反应生成 和
和 的能量变化如图所示。写出该反应的热化学方程式
的能量变化如图所示。写出该反应的热化学方程式____________ 。
(2)已知稀溶液中,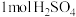 与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示
与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示 与NaOH反应的中和热的热化学方程式
与NaOH反应的中和热的热化学方程式____________ 。
(3)将 转化为
转化为 是工业冶炼金属钛的主要反应之一。已知:
是工业冶炼金属钛的主要反应之一。已知:

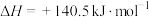
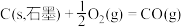
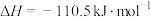
则反应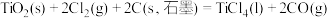 的
的 是
是______ 。
(1)由
 和NO反应生成
和NO反应生成 和
和 的能量变化如图所示。写出该反应的热化学方程式
的能量变化如图所示。写出该反应的热化学方程式
(2)已知稀溶液中,
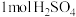 与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示
与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示 与NaOH反应的中和热的热化学方程式
与NaOH反应的中和热的热化学方程式(3)将
 转化为
转化为 是工业冶炼金属钛的主要反应之一。已知:
是工业冶炼金属钛的主要反应之一。已知:
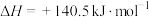
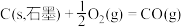
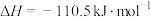
则反应
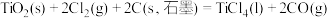 的
的 是
是
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题:
(1)已知下列热化学方程式:
①
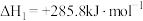
②
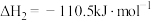
③
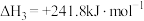
上述反应中属于放热反应的是__________ 。
(2)①的反应过程是太阳光催化分解水制氢气,该反应中主要能量转化形式为_________ 。
a.太阳能转化为化学能 b.化学能转化为电能
(3)若反应③使用催化剂,那么 将
将_______ (填“增大”“减小”或“不变”)
(4)反应 的
的
______  。
。
(5) 气态高能燃料乙硼烷
气态高能燃料乙硼烷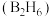 在氧气中燃烧,生成固态三氧化二硼
在氧气中燃烧,生成固态三氧化二硼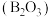 和气态水,释放
和气态水,释放 的热。
的热。
①写出反应的热化学方程式____________ 。
②11.2L(标准状况)气态乙硼烷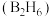 完全燃烧生成液态水生成的热
完全燃烧生成液态水生成的热_______  。
。
(1)已知下列热化学方程式:
①

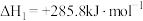
②

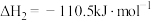
③

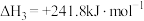
上述反应中属于放热反应的是
(2)①的反应过程是太阳光催化分解水制氢气,该反应中主要能量转化形式为
a.太阳能转化为化学能 b.化学能转化为电能
(3)若反应③使用催化剂,那么
 将
将(4)反应
 的
的
 。
。(5)
 气态高能燃料乙硼烷
气态高能燃料乙硼烷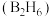 在氧气中燃烧,生成固态三氧化二硼
在氧气中燃烧,生成固态三氧化二硼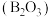 和气态水,释放
和气态水,释放 的热。
的热。①写出反应的热化学方程式
②11.2L(标准状况)气态乙硼烷
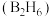 完全燃烧生成液态水生成的热
完全燃烧生成液态水生成的热 。
。
您最近一年使用:0次
5 . 化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于吸热反应的是___________(填字母)。
(2)获取能量变化的途径
①通过化学键的键能计算。已知:
计算可得: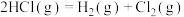 ∆H=
∆H=___________ kJ/mol
②通过盖斯定律可计算。已知在25℃、101kPa时:
I.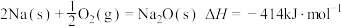
II.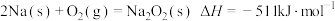
写出Na2O2与Na反应生成Na2O的热化学方程式:___________ 。
(3)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。
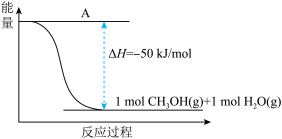
该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的∆H___________ (填“变大”“变小”或“不变”)。
(4)有机物M经过太阳光光照可转化成N,转化过程如下:
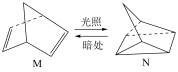
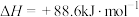
则M、N相比,较稳定的是___________ 。
(1)下列反应中,属于吸热反应的是___________(填字母)。
| A.NaOH与盐酸反应 | B.甲烷的燃烧反应 |
| C.Ba(OH)2∙8H2O与氯化铵反应 | D.锌与盐酸反应 |
(2)获取能量变化的途径
①通过化学键的键能计算。已知:
| 化学键种类 |  |  |  |
| 键能(kJ/mol) | 436 | 247 | 434 |
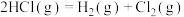 ∆H=
∆H=②通过盖斯定律可计算。已知在25℃、101kPa时:
I.
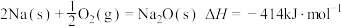
II.
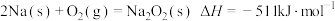
写出Na2O2与Na反应生成Na2O的热化学方程式:
(3)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。

该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的∆H
(4)有机物M经过太阳光光照可转化成N,转化过程如下:

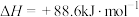
则M、N相比,较稳定的是
您最近一年使用:0次
名校
6 . 氨气催化氧化生产硝酸,硝酸厂常用催化还原法处理尾气:催化剂存在时用H2将NO2还原为N2。
已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol
N2(g)+2O2(g)=2NO2(g) ΔH=+67.7kJ/mol
则反应4H2(g)+2NO2(g)=N2(g)+4H2O(g)的反应热ΔH=________ 。
已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol
N2(g)+2O2(g)=2NO2(g) ΔH=+67.7kJ/mol
则反应4H2(g)+2NO2(g)=N2(g)+4H2O(g)的反应热ΔH=
您最近一年使用:0次
名校
解题方法
7 . Ⅰ.在载人航天器中,可以利用 与
与 的反应,将航天员呼出的
的反应,将航天员呼出的 转化为
转化为 等,然后通过电解
等,然后通过电解 得到
得到 ,从而实现
,从而实现 的再生。已知:
的再生。已知:
①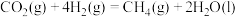

②
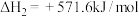
(1)请写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式___________ 。
Ⅱ.将 盐酸和
盐酸和 未知浓度的
未知浓度的 溶液混合均匀后测量并记录溶液的温度,实验结果如图所示,实验中始终保持
溶液混合均匀后测量并记录溶液的温度,实验结果如图所示,实验中始终保持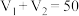 。
。
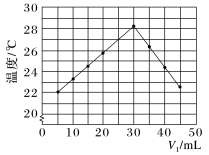
(2)下列叙述正确的是___________。
(3)中和反应的反应热的理论值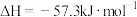 ,写出表示稀盐酸和
,写出表示稀盐酸和 溶液反应的中和热的热化学方程式
溶液反应的中和热的热化学方程式___________ 。下列操作可能使测得的 偏大的是
偏大的是___________ (填序号)。
①室温低于 时进行实验
时进行实验
②分多次把 溶液倒入盛有盐酸的小烧杯中
溶液倒入盛有盐酸的小烧杯中
③实验时用环形铜丝搅拌棒代替搅拌器
(4)在做测定中和反应的反应热实验时,应使用仪器的正确组合是___________。
①天平 ②量筒 ③烧杯 ④滴定管 ⑤温度计 ⑥试管 ⑦酒精灯
 与
与 的反应,将航天员呼出的
的反应,将航天员呼出的 转化为
转化为 等,然后通过电解
等,然后通过电解 得到
得到 ,从而实现
,从而实现 的再生。已知:
的再生。已知:①
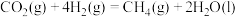

②

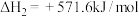
(1)请写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式
Ⅱ.将
 盐酸和
盐酸和 未知浓度的
未知浓度的 溶液混合均匀后测量并记录溶液的温度,实验结果如图所示,实验中始终保持
溶液混合均匀后测量并记录溶液的温度,实验结果如图所示,实验中始终保持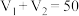 。
。
(2)下列叙述正确的是___________。
| A.该实验表明化学能可转化为热能 | B.做该实验时环境温度为 |
C. 溶液的浓度约为 溶液的浓度约为 | D.该实验表明有水生成的反应都是放热反应 |
(3)中和反应的反应热的理论值
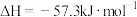 ,写出表示稀盐酸和
,写出表示稀盐酸和 溶液反应的中和热的热化学方程式
溶液反应的中和热的热化学方程式 偏大的是
偏大的是①室温低于
 时进行实验
时进行实验②分多次把
 溶液倒入盛有盐酸的小烧杯中
溶液倒入盛有盐酸的小烧杯中③实验时用环形铜丝搅拌棒代替搅拌器
(4)在做测定中和反应的反应热实验时,应使用仪器的正确组合是___________。
①天平 ②量筒 ③烧杯 ④滴定管 ⑤温度计 ⑥试管 ⑦酒精灯
| A.①②④ | B.②③⑤ | C.②③④⑦ | D.全部 |
您最近一年使用:0次
2023-11-11更新
|
73次组卷
|
2卷引用:福建省厦门大学附属科技中学2023-2024学年高二上学期第一次月考化学试题
名校
8 . 完成下列问题。
(1)实验测得16g甲醇 在氧气中充分燃烧生成二氧化碳气体和液态水时释放出363.25kJ的热量,试写出甲醇完全燃烧的热化学方程式:
在氧气中充分燃烧生成二氧化碳气体和液态水时释放出363.25kJ的热量,试写出甲醇完全燃烧的热化学方程式:___________ 。
(2)合成氨反应
 ,能量变化如图所示:
,能量变化如图所示:

①该反应通常用铁作催化剂,加催化剂会使图中
___________ (填“变大”“变小”或“不变”)。
②有关键能数据如下:
试根据表中所列键能数据计算a为___________ 。
(3)现根据下列的3个热化学反应方程式:
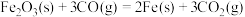

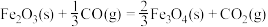
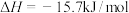

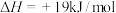
试写出CO气体还原FeO固体得到Fe固体和 气体的热化学反应方程式:
气体的热化学反应方程式:___________ 。
(1)实验测得16g甲醇
 在氧气中充分燃烧生成二氧化碳气体和液态水时释放出363.25kJ的热量,试写出甲醇完全燃烧的热化学方程式:
在氧气中充分燃烧生成二氧化碳气体和液态水时释放出363.25kJ的热量,试写出甲醇完全燃烧的热化学方程式:(2)合成氨反应

 ,能量变化如图所示:
,能量变化如图所示:
①该反应通常用铁作催化剂,加催化剂会使图中

②有关键能数据如下:
| 化学键 | H-H | N-H | N≡N |
键能( ) ) | 436 | 391 | 945 |
(3)现根据下列的3个热化学反应方程式:
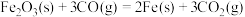

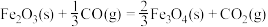
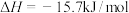

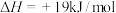
试写出CO气体还原FeO固体得到Fe固体和
 气体的热化学反应方程式:
气体的热化学反应方程式:
您最近一年使用:0次
名校
9 . 火箭推进器中装有还原剂液态肼(N2H4)和氧化剂过氧化氢(H2O2),当它们混合时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.65kJ的热量。回答下列问题:
(1)过氧化氢的电子式是___________ 。
(2)该反应的热化学方程式为___________ 。
(3)实验室可用次氯酸钠溶液与氨气反应制备液态肼,已知生成物之一是常见的盐,则反应的化学方程式为___________ 。
(4)在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
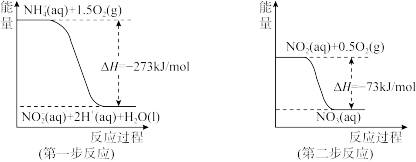
①第一步反应是___________ (填“放热”或“吸热”)反应,判断依据是___________ 。
②1 mol NH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的反应热ΔH是
(aq)的反应热ΔH是___________ 。
(5)已知: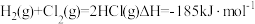 ,几种化学键的键能如下表所示,则a=
,几种化学键的键能如下表所示,则a=___________ 。
(1)过氧化氢的电子式是
(2)该反应的热化学方程式为
(3)实验室可用次氯酸钠溶液与氨气反应制备液态肼,已知生成物之一是常见的盐,则反应的化学方程式为
(4)在微生物作用的条件下,NH
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
①第一步反应是
②1 mol NH
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的反应热ΔH是
(aq)的反应热ΔH是(5)已知:
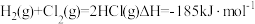 ,几种化学键的键能如下表所示,则a=
,几种化学键的键能如下表所示,则a=| 共价键 | H-H | Cl-Cl | H-Cl |
键能/( ) ) | 436 | 247 | a |
您最近一年使用:0次
2023-10-24更新
|
206次组卷
|
2卷引用:福建省漳州市东山县2023-2024学年高二上学期期中考试化学试题
名校
解题方法
10 . 依题意回答下列问题。
(1)标准状况下,0.3mol C2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7 kJ热量,请写出表示C2H2摩尔燃烧焓的热化学方程式:_______ 。
(2)用肼(N2H4)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①N2(g)+2O2(g)=N2O4(g) ΔH=+10.7 kJ·mol-1
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1
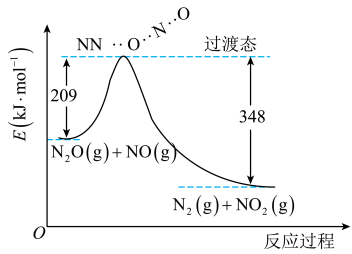
写出气态肼和N2O4反应的热化学方程式:_______ 。
(1)标准状况下,0.3mol C2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7 kJ热量,请写出表示C2H2摩尔燃烧焓的热化学方程式:
(2)用肼(N2H4)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①N2(g)+2O2(g)=N2O4(g) ΔH=+10.7 kJ·mol-1
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1

写出气态肼和N2O4反应的热化学方程式:
您最近一年使用:0次



