名校
解题方法
1 . 按要求书写热化学方程式

(1)一定条件下,由SO2和CO反应生成S和CO2的能量变化如图所示,写出该反应的热化学方程式_________
(2)CO(g)和CH3OH(l)的燃烧热ΔH分别为- 283.0 kJ·mol -1和-726.5 kJ·mol-1。则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为__________
(3)已知H2O(g)=H2O(l) ΔH = - 44 kJ·mol-1
则表示氢气燃烧热的热化学方程式为_____________________________

(1)一定条件下,由SO2和CO反应生成S和CO2的能量变化如图所示,写出该反应的热化学方程式
(2)CO(g)和CH3OH(l)的燃烧热ΔH分别为- 283.0 kJ·mol -1和-726.5 kJ·mol-1。则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
(3)已知H2O(g)=H2O(l) ΔH = - 44 kJ·mol-1
| 化学键 | O=O(g) | H—H | H—O |
| 键能/(kJ·mol-1) | 496 | 436 | 463 |
您最近一年使用:0次
2020-10-15更新
|
244次组卷
|
2卷引用:福建省南安市柳城中学2021-2022学年高二上学期期中考试化学试题
名校
2 . 火箭推进器中装有还原剂液态肼(N2H4)和氧化剂过氧化氢(H2O2),当它们混合时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.65kJ的热量。回答下列问题:
(1)过氧化氢的结构式是__________ 。
(2)该反应的热化学方程式为___________ 。
(3)已知H2O(l)=H2O(g) ∆H=+44kJ/mol,则32g液态肼与足量液态过氧化氢反应生成氮气和液态水时,∆H=_________ 。
(4)实验室可用次氯酸钠溶液与氨气反应制备液态肼,已知生成物之一是常见的盐,则反应的化学方程式为__________ 。
(5)已知: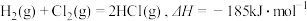 ,几种化学键的键能如下表所示,则a=
,几种化学键的键能如下表所示,则a=_________ 。
(1)过氧化氢的结构式是
(2)该反应的热化学方程式为
(3)已知H2O(l)=H2O(g) ∆H=+44kJ/mol,则32g液态肼与足量液态过氧化氢反应生成氮气和液态水时,∆H=
(4)实验室可用次氯酸钠溶液与氨气反应制备液态肼,已知生成物之一是常见的盐,则反应的化学方程式为
(5)已知:
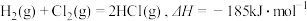 ,几种化学键的键能如下表所示,则a=
,几种化学键的键能如下表所示,则a=共价键 |
|
|
|
键能/( | 436 | 247 | a |
您最近一年使用:0次
2020-08-25更新
|
455次组卷
|
5卷引用:福建省福州第一中学2022-2023学年高二上学期12月月考化学试题
福建省福州第一中学2022-2023学年高二上学期12月月考化学试题 (已下线)第一章 化学反应的热效应(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)辽宁省盘锦市第二高级中学2020-2021学年高二上学期第一次阶段性考试化学试题湖北省仙桃、天门、潜江2019-2020学年高一下学期期末考试化学试题吉林省吉化第一高级中学校2021-2022学年高一下学期复课检测化学试题
3 . 煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后再使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的热化学方程式为
a.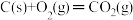 ΔH=E1①
ΔH=E1①
b.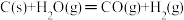 ΔH=E2②
ΔH=E2②
 ΔH=E3③
ΔH=E3③
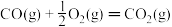 ΔH=E4④
ΔH=E4④
(1)上述四个热化学方程式中哪个反应的ΔH>0?______ (填序号)。
(2)等质量的煤分别通过以上两种不同的途径产生的可利用的总能量关系正确的是____ (填字母)。
A.a比b多 B.a比b少 C.a与b在理论上相同
(3)根据能量守恒定律,E1、E2、E3、E4之间的关系为E1=__________________ 。
(4)已知:①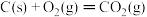 ΔH1=-393.5kJ/mol
ΔH1=-393.5kJ/mol
②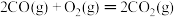 ΔH2=-566kJ/mol
ΔH2=-566kJ/mol
③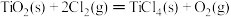 ΔH3=+141kJ/mol
ΔH3=+141kJ/mol
则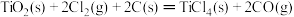 的ΔH=
的ΔH=_____________________ 。
a.
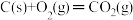 ΔH=E1①
ΔH=E1①b.
 ΔH=E2②
ΔH=E2② ΔH=E3③
ΔH=E3③ 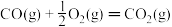 ΔH=E4④
ΔH=E4④(1)上述四个热化学方程式中哪个反应的ΔH>0?
(2)等质量的煤分别通过以上两种不同的途径产生的可利用的总能量关系正确的是
A.a比b多 B.a比b少 C.a与b在理论上相同
(3)根据能量守恒定律,E1、E2、E3、E4之间的关系为E1=
(4)已知:①
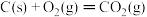 ΔH1=-393.5kJ/mol
ΔH1=-393.5kJ/mol②
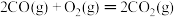 ΔH2=-566kJ/mol
ΔH2=-566kJ/mol③
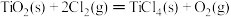 ΔH3=+141kJ/mol
ΔH3=+141kJ/mol 则
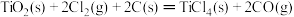 的ΔH=
的ΔH=
您最近一年使用:0次
2020-08-21更新
|
165次组卷
|
4卷引用:福建省南安市柳城中学2020-2021学年高二上学期第一次月考化学试题
4 . 向湿法炼锌的电解液中同时加入Cu和CuSO4,可生成CuCl沉淀除去Cl-,反应原理如下:
Cu(s)+Cu2+(aq)⇌2Cu+(aq)△H1=akJ•mol-1
Cl-(aq)+Cu+(aq)⇌CuCl(s)△H2=bkJ•mol-1
(1)反应Cu(s)+Cu2+(aq)+2Cl-(aq)⇌2CuCl(s) △H=_________ 。
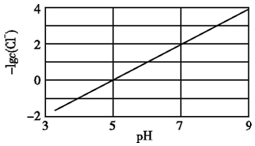
(2)实验测得电解液pH对溶液中残留 的影响如上图所示。当pH=7时,溶液中
的影响如上图所示。当pH=7时,溶液中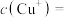
_________ 。
(3)兴趣小组在CuCl2溶液中加入过量KI固体,观察到有白色沉淀生成。推测该白色沉淀中一定含有的物质是___________ ,原因是 ______________________________ 。(已知常温下CuCl、CuI、CuI2的相关信息见表。)
Cu(s)+Cu2+(aq)⇌2Cu+(aq)△H1=akJ•mol-1
Cl-(aq)+Cu+(aq)⇌CuCl(s)△H2=bkJ•mol-1

(1)反应Cu(s)+Cu2+(aq)+2Cl-(aq)⇌2CuCl(s) △H=
(2)实验测得电解液pH对溶液中残留
 的影响如上图所示。当pH=7时,溶液中
的影响如上图所示。当pH=7时,溶液中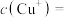
(3)兴趣小组在CuCl2溶液中加入过量KI固体,观察到有白色沉淀生成。推测该白色沉淀中一定含有的物质是
| 物质 | CuCl | CuI | CuI2 |
 |  |  | - |
| 颜色 | 白色 | 白色 | 金黄色 |
您最近一年使用:0次
名校
解题方法
5 . 碳是常见的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程:
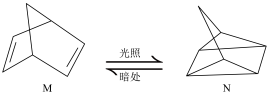
ΔH=+88.6kJ·mol-1。则M、N相比,较稳定的是_____ 。
(2)已知CH3OH(l)的燃烧热ΔH=-726.5kJ·mol-1,CH3OH(l)+ O2(g)===CO2(g)+2H2(g)ΔH=-akJ·mol-1,则a
O2(g)===CO2(g)+2H2(g)ΔH=-akJ·mol-1,则a________ 726.5(填“>”“<”或“=”)。
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)===2Al2O3(s)+3TiC(s) ΔH=-1176kJ·mol-1,则反应过程中,每转移1mol电子放出的热量为________ 。
(4)煤气化制合成气(CO和H2)
已知:①C(s)+H2O(g) CO(g)+H2(g)ΔH1=+131.3kJ·mol-1
CO(g)+H2(g)ΔH1=+131.3kJ·mol-1
②C(s)+2H2O(g) CO2(g)+2H2(g)ΔH2=+90kJ·mol-1
CO2(g)+2H2(g)ΔH2=+90kJ·mol-1
则一氧化碳与水蒸气反应生成二氧化碳和氢气的热化学方程式是________ 。
(1)有机物M经过太阳光光照可转化成N,转化过程:

ΔH=+88.6kJ·mol-1。则M、N相比,较稳定的是
(2)已知CH3OH(l)的燃烧热ΔH=-726.5kJ·mol-1,CH3OH(l)+
 O2(g)===CO2(g)+2H2(g)ΔH=-akJ·mol-1,则a
O2(g)===CO2(g)+2H2(g)ΔH=-akJ·mol-1,则a(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)===2Al2O3(s)+3TiC(s) ΔH=-1176kJ·mol-1,则反应过程中,每转移1mol电子放出的热量为
(4)煤气化制合成气(CO和H2)
已知:①C(s)+H2O(g)
 CO(g)+H2(g)ΔH1=+131.3kJ·mol-1
CO(g)+H2(g)ΔH1=+131.3kJ·mol-1②C(s)+2H2O(g)
 CO2(g)+2H2(g)ΔH2=+90kJ·mol-1
CO2(g)+2H2(g)ΔH2=+90kJ·mol-1则一氧化碳与水蒸气反应生成二氧化碳和氢气的热化学方程式是
您最近一年使用:0次
2014·全国·一模
名校
解题方法
6 . 参考下列图表和有关要求回答问题:
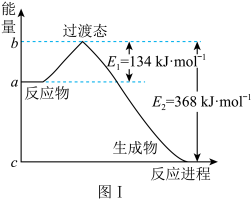
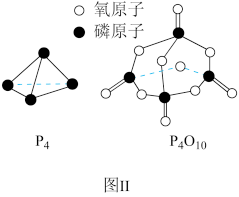
(1)图Ⅰ是 1mol NO2(g)和 1 mol CO(g)反应生成 CO2和NO 过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是_____ (填“增大”“减小”或“不变”,下同),ΔH 的变化是_____ 。请写出 NO2和 CO反应的热化学方程式:_____ 。
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)ΔH=+49.0 kJ·mol-1
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1
又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1则甲醇燃烧生成液态水的热化学方程式:_____ 。
(3)下表是部分化学键的键能数据:
已知 1 mol 白磷(P4)完全燃烧放热为 dkJ,白磷及其完全燃烧的产物结构如图Ⅱ所示,则表中 x=_____ kJ·mol-1(用含有 a、b、c、d 的代数式表示)。


(1)图Ⅰ是 1mol NO2(g)和 1 mol CO(g)反应生成 CO2和NO 过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)ΔH=+49.0 kJ·mol-1
②CH3OH(g)+
 O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1则甲醇燃烧生成液态水的热化学方程式:
(3)下表是部分化学键的键能数据:
| 化学键 | P—P | P—O | O=O | P=O |
| 键能/kJ·mol-1 | a | b | c | x |
已知 1 mol 白磷(P4)完全燃烧放热为 dkJ,白磷及其完全燃烧的产物结构如图Ⅱ所示,则表中 x=
您最近一年使用:0次
2020-05-04更新
|
298次组卷
|
16卷引用:福建省泉州市泉港区第一中学2017-2018学年高二上学期期中考试化学试题
福建省泉州市泉港区第一中学2017-2018学年高二上学期期中考试化学试题2016-2017学年四川省乐山市高二上学期教学质检化学试卷2016-2017学年四川省雅安中学高二下学期开学考试化学试卷河南省南阳市第一中学2016-2017学年高二下学期第二次月考(5月)化学试题湖南省醴陵市第一中学2018-2019学年高二上学期入学考试化学试题四川省蓬溪县蓬南中学2019-2020学年高二上学期第四次月考化学试题安徽省滁州市定远县育才学校2019-2020学年高二(普通班)上学期第三次月考化学试题云南省曲靖市会泽县第一中学2019-2020学年高二上学期第一次段考化学试题北京市朝阳区陈经纶中学 2019-2020学年高二下学期期中自主检测化学试题陕西省咸阳百灵中学2020-2021学年高二上学期第一次月考化学试题江西省赣州市会昌县会昌中学2020-2021学年高二上学期第一次月考化学试题(已下线)【南昌新东方】9.湾里一中 梁莎陕西省子洲中学2019-2020学年高二下学期第一次月考化学试题甘肃省靖远县第二中学2021-2022学年高二上学期期中考试化学(理)试题(已下线)2014高考名师推荐化学盖斯定律及其应用2016-2017学年江苏省启东中学高一上月考二化学试卷
11-12高二上·河南焦作·期中
7 . 丙烷燃烧可以通过以下两种途径:
途径Ⅰ:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-a kJ/mol
途径Ⅱ:C3H8(g)=C3H6(g)+H2(g) ΔH=+b kJ/mol
2C3H6(g)+9O2(g)=6CO2(g)+6H2O(l) ΔH=-c kJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH=-d kJ/mol (a、b、c、d 均为正值)
请回答下列问题:
(1)判断等量的丙烷通过两种途径放出的热量,途径Ⅰ放出的热量________ (填“大于 ”、“等于 ” 或“小于 ”)途径Ⅱ放出的热量。
(2)由于C3H8(g)=C3H6(g)+H2(g)的反应中,反应物具有的总能量_____ (填“大于”、“等 于”或“小于 ”)生成物具有的总能量,那么在化学反应时,反应物就需要_____ (填“放出 ” 或“吸收 ”)能量才能转化为生成物,因此其反应条件是____ ;
(3)b与a、c、d 的数学关系式是_____________________________________ 。
途径Ⅰ:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-a kJ/mol
途径Ⅱ:C3H8(g)=C3H6(g)+H2(g) ΔH=+b kJ/mol
2C3H6(g)+9O2(g)=6CO2(g)+6H2O(l) ΔH=-c kJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH=-d kJ/mol (a、b、c、d 均为正值)
请回答下列问题:
(1)判断等量的丙烷通过两种途径放出的热量,途径Ⅰ放出的热量
(2)由于C3H8(g)=C3H6(g)+H2(g)的反应中,反应物具有的总能量
(3)b与a、c、d 的数学关系式是
您最近一年使用:0次
2020-04-30更新
|
145次组卷
|
13卷引用:福建省莆田第十五中学2018-2019学年高二上学期期中考试化学试题
福建省莆田第十五中学2018-2019学年高二上学期期中考试化学试题(已下线)2011-2012学年河南省焦作市修武一中分校高二上学期期中考试化学试卷(已下线)2012-2013学年吉林省松原市扶余县一中高二第一次月考化学试卷(已下线)2014—2015学年湖北武汉新洲三中高二10月月考化学(A卷)试卷2015-2016学年四川省新津中学高二10月月考化学试卷西藏日喀则市第二高级中学2017-2018学年高二上学期期中考试化学试题内蒙古巴彦淖尔市第一中学2017-2018学年高二9月月考化学试题B甘肃省临泽县第一中学2018-2019学年高二上学期期中考试化学试题山东省济宁市第二中学2019-2020学年高二上学期第一次月考化学试题山西省祁县第二中学2019-2020学年高二10月月考化学试题陕西省宝鸡市金台区2019-2020学年高二上学期期中检测化学试题青海省西宁市海湖中学2020-2021学年高二上学期第一阶段测试化学试题新疆岳普湖县2021-2022学年高二下学期第一次学情调研测试化学试题
名校
解题方法
8 . 碳及其化合物在化工生产中有着广泛的应用。
I.为解决大气中CO2的含量增大的问题,某科学家提出如下构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,在合成塔中经化学反应使废气中的CO2转变为燃料甲醇。部分技术流程如下:
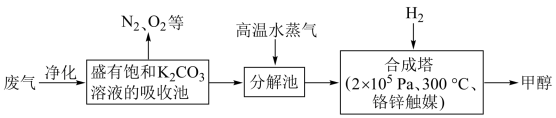
(1)吸收池中反应的化学方程式为K2CO3+CO2+H2O=2KHCO3,△H<0。该反应为可逆反应,从平衡移动原理分析,低温有利于提高原料气的平衡转化率。而实际生产中采用300℃的温度,其原因是____________________ ,_________________________
(2)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H1=-890.3kJ/mol
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ/mol
如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4。写出CO2(g)与H2(g)反应生CH4(g)与液态水的热化学方程式_____________ 。
II.某兴趣小组模拟工业合成甲醇的反应:CO(g)+2H2(g) CH3OH(g),在容积固定为2L的密闭容器中充入1mol CO和2mol H2,加入合适的催化剂(催化剂体积忽略不计)后开始反应。测得容器内的压强随时间变化如下:
CH3OH(g),在容积固定为2L的密闭容器中充入1mol CO和2mol H2,加入合适的催化剂(催化剂体积忽略不计)后开始反应。测得容器内的压强随时间变化如下:
(1)从反应开始到20min时,以CO表示反应速率为___________________
(2)下列描述能说明反应达到平衡 是
是_______
A.装置内CO和H2的浓度比值不再改变
B.容器内气体的平均摩尔质量保持不变
C.容器内气体的压强保持不变
D.容器内气体密度保持不变
(3)该温度下平衡常数K=_______ ,若达到平衡后加入少量CH3OH(g),此时平衡常数K值将_________ (填“增大”、“减小”或“不变”)
(4)该反应达到平衡后,再向容器中充入1mol CO和2mol H2,此时CO的转化率将_____ (填“增大”、“减小”或“不变”)
I.为解决大气中CO2的含量增大的问题,某科学家提出如下构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,在合成塔中经化学反应使废气中的CO2转变为燃料甲醇。部分技术流程如下:

(1)吸收池中反应的化学方程式为K2CO3+CO2+H2O=2KHCO3,△H<0。该反应为可逆反应,从平衡移动原理分析,低温有利于提高原料气的平衡转化率。而实际生产中采用300℃的温度,其原因是
(2)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H1=-890.3kJ/mol
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ/mol
如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4。写出CO2(g)与H2(g)反应生CH4(g)与液态水的热化学方程式
II.某兴趣小组模拟工业合成甲醇的反应:CO(g)+2H2(g)
 CH3OH(g),在容积固定为2L的密闭容器中充入1mol CO和2mol H2,加入合适的催化剂(催化剂体积忽略不计)后开始反应。测得容器内的压强随时间变化如下:
CH3OH(g),在容积固定为2L的密闭容器中充入1mol CO和2mol H2,加入合适的催化剂(催化剂体积忽略不计)后开始反应。测得容器内的压强随时间变化如下:| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/Mpa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
(1)从反应开始到20min时,以CO表示反应速率为
(2)下列描述能说明反应达到平衡
 是
是A.装置内CO和H2的浓度比值不再改变
B.容器内气体的平均摩尔质量保持不变
C.容器内气体的压强保持不变
D.容器内气体密度保持不变
(3)该温度下平衡常数K=
(4)该反应达到平衡后,再向容器中充入1mol CO和2mol H2,此时CO的转化率将
您最近一年使用:0次
名校
解题方法
9 . (1)25℃下,纯水中c(H+)=1×10-7 mol·L-1,则此时c(OH-)=______________ ,该温度下向纯水中加盐酸,使溶液中的c(H+)=1×10-3 mol·L-1,则此时溶液的pH=_______________ 。若25℃下,向纯水中加入NaOH固体,使溶液的pH=13,此时溶液中c(OH-)=___________ 。 与纯水的电离相似,液氨中也存在着微弱的电离:2NH3  NH4++NH2-,请写出液氨的电离平衡常数表达式K =
NH4++NH2-,请写出液氨的电离平衡常数表达式K =____________________________ 。
(2)同素异形体相互转化的反应热相当少而转化速率慢,有时还很不完全,测定时很 困难,现可依据盖斯定律进行计算。已知:
P4 (白磷,s) + 5O2 (g) = 2P2O5 (s); △H1 =-283.2 kJ·mol-1 ①
4P (红磷,s) + 5O2 (g) = 2P2O5 (s); △H2 =-184.0kJ·mol-1 ②
由热化学方程式看来,更稳定的磷的同素异形体是______ (填“白磷”或“红磷”) ,试写出白磷转化成红磷的热化学方程式______________________________________ 。
 NH4++NH2-,请写出液氨的电离平衡常数表达式K =
NH4++NH2-,请写出液氨的电离平衡常数表达式K =(2)同素异形体相互转化的反应热相当少而转化速率慢,有时还很不完全,测定时很 困难,现可依据盖斯定律进行计算。已知:
P4 (白磷,s) + 5O2 (g) = 2P2O5 (s); △H1 =-283.2 kJ·mol-1 ①
4P (红磷,s) + 5O2 (g) = 2P2O5 (s); △H2 =-184.0kJ·mol-1 ②
由热化学方程式看来,更稳定的磷的同素异形体是
您最近一年使用:0次
10 . 碳、氮是中学化学重要的非金属元素,在生产、生活中有广泛的应用。
(1)治理汽车尾气中NO和CO的一种方法是:在汽车的排气管道上安装一个催化转化装置,使NO与CO反应,产物都是空气中的主要成分。写出该反应的热化学方程式___ 。
已知:①N2(g)+O2(g)=2NO(g)△H=+179.5kJ/mol
②2NO(g)+O2(g)=2NO2(g)△H=-112.3kJ/mol
③NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234kJ/mol
(2)已知植物光合作用发生的反应如下:
6CO2(g)+6H2O(l) C6H12O6(s)+6O2(g)△H=+669.62 kJ/mol
C6H12O6(s)+6O2(g)△H=+669.62 kJ/mol
该反应达到化学平衡后,若改变下列条件,CO2转化率增大的是___ 。
a.增大CO2的浓度b.取走一半C6H12O6c.加入催化剂d.适当升高温度
(3)N2O5的分解反应2N2O5(g) 4NO2(g)+O2(g),由实验测得在67℃时N2O5的浓度随时间的变化如下:
4NO2(g)+O2(g),由实验测得在67℃时N2O5的浓度随时间的变化如下:
计算在0~2min时段,化学反应速率v(NO2)=___ mol•L-1•min-1。
(4)新的研究表明,可以将CO2转化为炭黑进行回收利用,反应原理如图所示。
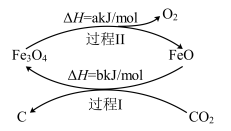
①在转化过程中起催化作用的物质是___ ;
②写出总反应的化学方程式___ 。
(5)工业上以NH3和CO2为原料合成尿素[CO(NH2)2),反应的化学方程式如下:2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(l)
CO(NH2)2(l)+H2O(l)
根据上述反应,填写下列空白
①已知该反应可以自发进行,则△H___ 0。(填“>”、“<”或“=”);
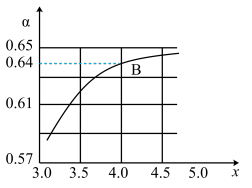
②一定温度和压强下,若原料气中的NH3和CO2的物质的量之比 =x,如图是x与CO2的平衡转化率(α)的关系。α随着x增大而增大的原因是
=x,如图是x与CO2的平衡转化率(α)的关系。α随着x增大而增大的原因是___ ;B点处,NH3的平衡转化率为___ 。
③一定温度下,在3L定容密闭容器中充入NH3和CO2,若x=2,当反应后气体压强变为起始时气体压强的 时达到平衡,测得此时生成尿素90g。该反应的平衡常数K=
时达到平衡,测得此时生成尿素90g。该反应的平衡常数K=___ 。
(1)治理汽车尾气中NO和CO的一种方法是:在汽车的排气管道上安装一个催化转化装置,使NO与CO反应,产物都是空气中的主要成分。写出该反应的热化学方程式
已知:①N2(g)+O2(g)=2NO(g)△H=+179.5kJ/mol
②2NO(g)+O2(g)=2NO2(g)△H=-112.3kJ/mol
③NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234kJ/mol
(2)已知植物光合作用发生的反应如下:
6CO2(g)+6H2O(l)
 C6H12O6(s)+6O2(g)△H=+669.62 kJ/mol
C6H12O6(s)+6O2(g)△H=+669.62 kJ/mol该反应达到化学平衡后,若改变下列条件,CO2转化率增大的是
a.增大CO2的浓度b.取走一半C6H12O6c.加入催化剂d.适当升高温度
(3)N2O5的分解反应2N2O5(g)
 4NO2(g)+O2(g),由实验测得在67℃时N2O5的浓度随时间的变化如下:
4NO2(g)+O2(g),由实验测得在67℃时N2O5的浓度随时间的变化如下:| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
| C(N2O5)/(mol·L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
(4)新的研究表明,可以将CO2转化为炭黑进行回收利用,反应原理如图所示。

①在转化过程中起催化作用的物质是
②写出总反应的化学方程式
(5)工业上以NH3和CO2为原料合成尿素[CO(NH2)2),反应的化学方程式如下:2NH3(g)+CO2(g)
 CO(NH2)2(l)+H2O(l)
CO(NH2)2(l)+H2O(l)根据上述反应,填写下列空白
①已知该反应可以自发进行,则△H
②一定温度和压强下,若原料气中的NH3和CO2的物质的量之比
 =x,如图是x与CO2的平衡转化率(α)的关系。α随着x增大而增大的原因是
=x,如图是x与CO2的平衡转化率(α)的关系。α随着x增大而增大的原因是
③一定温度下,在3L定容密闭容器中充入NH3和CO2,若x=2,当反应后气体压强变为起始时气体压强的
 时达到平衡,测得此时生成尿素90g。该反应的平衡常数K=
时达到平衡,测得此时生成尿素90g。该反应的平衡常数K=
您最近一年使用:0次
2019-12-06更新
|
709次组卷
|
6卷引用:福建省南安市华侨中学2023-2024学年高二上学期10月月考化学试题







