1 . 控制CO2的排放是防止温室效应等不良气候现象产生的有效途径。
(1)高炉炼铁中用CO还原Fe2O3得到Fe,同时会排放大量的CO2和烟尘,必须进行严格的控制。已知:①C(石墨,s)+CO2(g)=2CO(g) ΔH=+172.5kJ⋅mol-1;②3C(石墨,s)+Fe2O3(s)=2Fe(s)+3CO(g) ΔH=+489.0kJ⋅mol-1,则CO还原Fe2O3的热化学方程式为___________ 。
(2)在恒温恒容密闭容器中充入一定量CO与Fe2O3发生该反应。
①以下能说明该可逆反应达到平衡状态的是___________ (选填字母)。
A.混合气体的密度不变 B.容器内气体压强一定
C.CO与CO2浓度比为1:1 D.Fe2O3与Fe的质量比不变
②当达到平衡后,再充入一定量CO,平衡___________ (填“正向”、“逆向”或“不”)移动,则达到新平衡后CO的转化率___________ (填“增大”、“减小”或“不变”)。
③下列措施中能使平衡时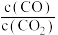 增大的是
增大的是___________ (填字母)。
A.升高温度 B.增大压强 C.充入一定量的CO2 D.再加入一定量铁粉
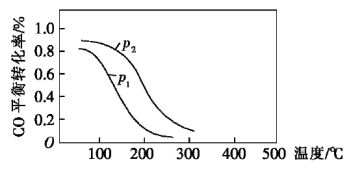
(3)可将炼铁产生的CO2与CH4反应得到气体燃料,其反应原理为:CO2(g)+CH4(g) 2CO(g)+2H2(g)。某小组向体积是1L的刚性密闭容器中充入物质的量均是1mol的CH4与CO2,反应过程中CO2的平衡转化率与温度、压强的关系如图所示。
2CO(g)+2H2(g)。某小组向体积是1L的刚性密闭容器中充入物质的量均是1mol的CH4与CO2,反应过程中CO2的平衡转化率与温度、压强的关系如图所示。
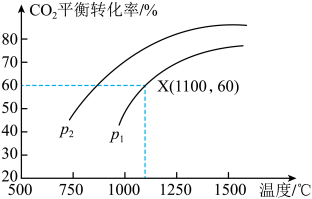
①压强:p1___________ p2(填“>”或“<”)。
②1100℃、p1条件下,20min时反应达到平衡状态,则0-20min内CO的反应速率V(CO)=___________ ,反应的平衡常数Kp=___________ (用含p1的代数式表示,Kp为以分压表示的平衡常数,分压=总压×物质的量分数);
(1)高炉炼铁中用CO还原Fe2O3得到Fe,同时会排放大量的CO2和烟尘,必须进行严格的控制。已知:①C(石墨,s)+CO2(g)=2CO(g) ΔH=+172.5kJ⋅mol-1;②3C(石墨,s)+Fe2O3(s)=2Fe(s)+3CO(g) ΔH=+489.0kJ⋅mol-1,则CO还原Fe2O3的热化学方程式为
(2)在恒温恒容密闭容器中充入一定量CO与Fe2O3发生该反应。
①以下能说明该可逆反应达到平衡状态的是
A.混合气体的密度不变 B.容器内气体压强一定
C.CO与CO2浓度比为1:1 D.Fe2O3与Fe的质量比不变
②当达到平衡后,再充入一定量CO,平衡
③下列措施中能使平衡时
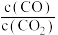 增大的是
增大的是A.升高温度 B.增大压强 C.充入一定量的CO2 D.再加入一定量铁粉
(3)可将炼铁产生的CO2与CH4反应得到气体燃料,其反应原理为:CO2(g)+CH4(g)
 2CO(g)+2H2(g)。某小组向体积是1L的刚性密闭容器中充入物质的量均是1mol的CH4与CO2,反应过程中CO2的平衡转化率与温度、压强的关系如图所示。
2CO(g)+2H2(g)。某小组向体积是1L的刚性密闭容器中充入物质的量均是1mol的CH4与CO2,反应过程中CO2的平衡转化率与温度、压强的关系如图所示。
①压强:p1
②1100℃、p1条件下,20min时反应达到平衡状态,则0-20min内CO的反应速率V(CO)=
您最近一年使用:0次
名校
解题方法
2 . 山东“十四五”规划提出“推动绿色发展,绘就绿水青山齐鲁画卷”。 加氢可缓解
加氢可缓解 带来的环境压力,同时带来巨大的经济效益。
带来的环境压力,同时带来巨大的经济效益。 加氢过程,主要发生的三个竞争反应为:
加氢过程,主要发生的三个竞争反应为:
反应Ⅰ:
反应Ⅱ: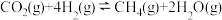
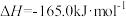
反应Ⅲ:
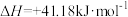
回答下列问题:
(1)①由CO、H2合成甲醇的热化学方程式为_______ 。
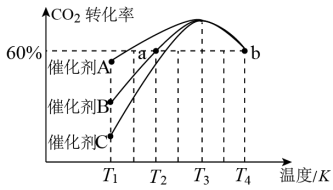
②相同时间内,在不同催化剂下用CO2和H2合成甲醇(其他条件均相同),CO2的转化率随温度变化如图所示,其中活化能最低的反应所用的催化剂是催化剂_______ (填“A”、“B”或“C”)。
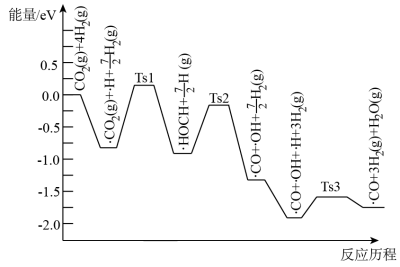
③在 催化剂表面上反应Ⅱ的前三步反应历程如图所示(吸附在
催化剂表面上反应Ⅱ的前三步反应历程如图所示(吸附在 催化剂表面用“∙”标注,Ts表示过渡态),则物质吸附在催化剂表面,形成过渡态的过程会
催化剂表面用“∙”标注,Ts表示过渡态),则物质吸附在催化剂表面,形成过渡态的过程会_______ (填“放出热量”或“吸收热量”),反应历程中最小能垒(活化能)步骤的化学方程式为_______ 。
(2)我国科学家研究了不同反应温度对含碳产物组成的影响。在反应器中按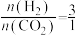 ,通入H2和CO2,分别在0.1MPa和1MPa下进行反应。实验中温度对平衡组成体系的(CO2、CO、CH4)三种物质分析,其CO和CH4的影响如下图所示(该反应条件下甲醇产量极低,因此忽略“反应I”,只考虑反应Ⅱ和反应III)。
,通入H2和CO2,分别在0.1MPa和1MPa下进行反应。实验中温度对平衡组成体系的(CO2、CO、CH4)三种物质分析,其CO和CH4的影响如下图所示(该反应条件下甲醇产量极低,因此忽略“反应I”,只考虑反应Ⅱ和反应III)。

①lMPa时,表示CH4和CO平衡组成随温度变化关系的曲线分别是_______ 、_______ 。M点平衡组成含量高于N点的原因是_______ 。
②当CH4和CO平衡组成均为40%时,该温度下反应Ⅲ的平衡常数Kp为_______ 。
 加氢可缓解
加氢可缓解 带来的环境压力,同时带来巨大的经济效益。
带来的环境压力,同时带来巨大的经济效益。 加氢过程,主要发生的三个竞争反应为:
加氢过程,主要发生的三个竞争反应为:反应Ⅰ:

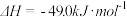
反应Ⅱ:
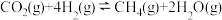
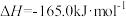
反应Ⅲ:

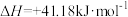
回答下列问题:
(1)①由CO、H2合成甲醇的热化学方程式为
②相同时间内,在不同催化剂下用CO2和H2合成甲醇(其他条件均相同),CO2的转化率随温度变化如图所示,其中活化能最低的反应所用的催化剂是催化剂

③在
 催化剂表面上反应Ⅱ的前三步反应历程如图所示(吸附在
催化剂表面上反应Ⅱ的前三步反应历程如图所示(吸附在 催化剂表面用“∙”标注,Ts表示过渡态),则物质吸附在催化剂表面,形成过渡态的过程会
催化剂表面用“∙”标注,Ts表示过渡态),则物质吸附在催化剂表面,形成过渡态的过程会
(2)我国科学家研究了不同反应温度对含碳产物组成的影响。在反应器中按
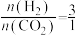 ,通入H2和CO2,分别在0.1MPa和1MPa下进行反应。实验中温度对平衡组成体系的(CO2、CO、CH4)三种物质分析,其CO和CH4的影响如下图所示(该反应条件下甲醇产量极低,因此忽略“反应I”,只考虑反应Ⅱ和反应III)。
,通入H2和CO2,分别在0.1MPa和1MPa下进行反应。实验中温度对平衡组成体系的(CO2、CO、CH4)三种物质分析,其CO和CH4的影响如下图所示(该反应条件下甲醇产量极低,因此忽略“反应I”,只考虑反应Ⅱ和反应III)。
①lMPa时,表示CH4和CO平衡组成随温度变化关系的曲线分别是
②当CH4和CO平衡组成均为40%时,该温度下反应Ⅲ的平衡常数Kp为
您最近一年使用:0次
名校
解题方法
3 . 页岩气是从页岩层中开采的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和 ),
), 与
与 通入聚焦太阳能反应器,发生反应
通入聚焦太阳能反应器,发生反应
 。已知:
。已知:
①

②

③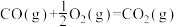

则
___________ (用含 、
、 、
、 的代数式表示)
的代数式表示)
(2)用合成气生成甲醇的反应为
 ,在10L恒容密闭容器中按物质的量之比1:2充入CO和
,在10L恒容密闭容器中按物质的量之比1:2充入CO和 ,测得CO的平衡转化率与温度和压强的关系如图所示:
,测得CO的平衡转化率与温度和压强的关系如图所示:
200℃时 随时间的变化如下表所示:
随时间的变化如下表所示:
①该反应的平衡常数表达式为
___________ ;
___________ (填“>”“<”或“=”)0。
②写出一条可同时提高反应速率和CO转化率的措施:___________ 。
③下列说法正确的是___________ (填字母)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强: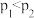
④0~1min内用 表示的反应速率
表示的反应速率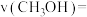
___________  。
。
⑤向上述200℃达到平衡的恒容密闭容器中再加入2 mol CO、4 mol 、2 mol
、2 mol  ,保持温度不变,则化学平衡
,保持温度不变,则化学平衡___________ (填“正向”“逆向”或“不”)移动。
(3)甲烷、氧气和KOH溶液可组成燃料电池。充入22.4L(折算为标准状况下)甲烷,测得电路中转移5.6mol电子,则甲烷的利用率为___________ 。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和
 ),
), 与
与 通入聚焦太阳能反应器,发生反应
通入聚焦太阳能反应器,发生反应
 。已知:
。已知:①


②


③
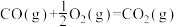

则

 、
、 、
、 的代数式表示)
的代数式表示)(2)用合成气生成甲醇的反应为

 ,在10L恒容密闭容器中按物质的量之比1:2充入CO和
,在10L恒容密闭容器中按物质的量之比1:2充入CO和 ,测得CO的平衡转化率与温度和压强的关系如图所示:
,测得CO的平衡转化率与温度和压强的关系如图所示:
200℃时
 随时间的变化如下表所示:
随时间的变化如下表所示:| t/min | 0 | 1 | 3 | 5 |
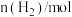 | 8.0 | 5.4 | 4.0 | 4.0 |
①该反应的平衡常数表达式为


②写出一条可同时提高反应速率和CO转化率的措施:
③下列说法正确的是
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强:
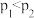
④0~1min内用
 表示的反应速率
表示的反应速率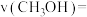
 。
。⑤向上述200℃达到平衡的恒容密闭容器中再加入2 mol CO、4 mol
 、2 mol
、2 mol  ,保持温度不变,则化学平衡
,保持温度不变,则化学平衡(3)甲烷、氧气和KOH溶液可组成燃料电池。充入22.4L(折算为标准状况下)甲烷,测得电路中转移5.6mol电子,则甲烷的利用率为
您最近一年使用:0次
2021-11-23更新
|
222次组卷
|
3卷引用:黑龙江省哈尔滨市第一中学校 2021-2022学年高三上学期期末考试理综化学试题
名校
解题方法
4 . 生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(1)有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。在 下,
下, 氢气完全燃烧生成液态水放出
氢气完全燃烧生成液态水放出 的热量,
的热量,
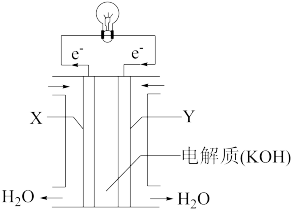
①请写出表示氢气燃烧热的热化学方程式____ 。
②将上述反应设计成下图所示的原电池,其中Y为___ 极(填“正”或“负”),该极电极反应式为___ 。
(2)最新一期国际学术期刊《自然·纳米技术》介绍了我国科学家曾杰团队的成果:在含铂高效催化剂作用下把二氧化碳高效转化清洁液态燃料——甲醇 。
。
①该法利用 制取甲醇的有关化学反应如下:
制取甲醇的有关化学反应如下:
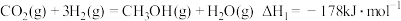
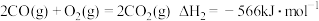
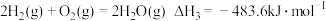
已知:i.断开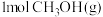 中的化学键共吸收
中的化学键共吸收 的能量
的能量
ii.反应①中部分化学键键能数据如下:
由此计算断开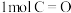 需要吸收
需要吸收____ kJ的能量,
____  。
。
②甲醇燃烧时发生如下反应(a、b、c、d均大于0):
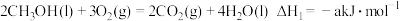
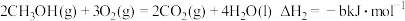
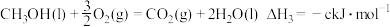
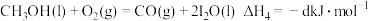
由此知,a、b、c、d由小到大排序为_______ 。
③将甲醇完全燃烧生成液态水的反应设计成原电池,以 为电解质。工作时负极的电极反应式
为电解质。工作时负极的电极反应式__ 。
(1)有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。在
 下,
下, 氢气完全燃烧生成液态水放出
氢气完全燃烧生成液态水放出 的热量,
的热量,①请写出表示氢气燃烧热的热化学方程式
②将上述反应设计成下图所示的原电池,其中Y为

(2)最新一期国际学术期刊《自然·纳米技术》介绍了我国科学家曾杰团队的成果:在含铂高效催化剂作用下把二氧化碳高效转化清洁液态燃料——甲醇
 。
。①该法利用
 制取甲醇的有关化学反应如下:
制取甲醇的有关化学反应如下: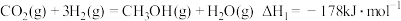
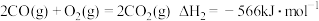
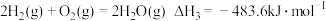
已知:i.断开
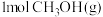 中的化学键共吸收
中的化学键共吸收 的能量
的能量ii.反应①中部分化学键键能数据如下:
| 化学键 | H-H | H-O |
键能/( ) ) | 436 | 463 |
由此计算断开
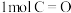 需要吸收
需要吸收
 。
。②甲醇燃烧时发生如下反应(a、b、c、d均大于0):
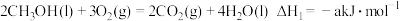
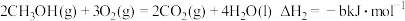
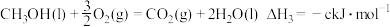
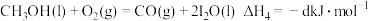
由此知,a、b、c、d由小到大排序为
③将甲醇完全燃烧生成液态水的反应设计成原电池,以
 为电解质。工作时负极的电极反应式
为电解质。工作时负极的电极反应式
您最近一年使用:0次
名校
5 . O2PtF6是一种深红色固体,由英国化学家巴特列克发现,属于离子化合物,其晶体可用O PtF
PtF (s)表示。该晶体形成过程中的能量变化如图所示:(已知△H<0)
(s)表示。该晶体形成过程中的能量变化如图所示:(已知△H<0)
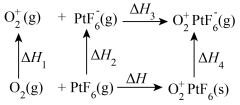
下列说法正确的是
 PtF
PtF (s)表示。该晶体形成过程中的能量变化如图所示:(已知△H<0)
(s)表示。该晶体形成过程中的能量变化如图所示:(已知△H<0)
下列说法正确的是
| A.△H1<0,△H2>0 | B.△H+△H1+△H2+△H3+△H4=0 |
| C.△H3<0,△H4>0 | D.△H4<△H1+△H2+△H3 |
您最近一年使用:0次
2021-09-05更新
|
221次组卷
|
3卷引用:黑龙江省哈尔滨市第九中学校2022届高三上学期适应性考试化学试题
6 . 回答下列问题
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g) NH2COONH4(s) ΔH1
NH2COONH4(s) ΔH1
反应Ⅱ:NH2COONH4(s) CO(NH2)2(s)+H2O(g) ΔH2=+72.49 kJ·mol-1
CO(NH2)2(s)+H2O(g) ΔH2=+72.49 kJ·mol-1
总反应:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) ΔH3=-86.98 kJ·mol-1
CO(NH2)2(s)+H2O(g) ΔH3=-86.98 kJ·mol-1
则反应Ⅰ的ΔH1=___________ kJ·mol-1。
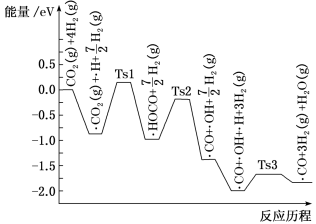
(2)氢气可将CO2还原为甲烷,反应为CO2(g)+4H2(g) CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示,其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会
CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示,其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会___________ (填“放出热量”或“吸收热量”);反应历程中最小能垒步骤的化学方程式为___________ 。
(3)已知CO(g)、CH4(g)、CH3CHO(l)的燃烧热分别为283.0 kJ·mol-1、890.31 kJ·mol-1、1167.9 kJ·mol-1,则乙醛的分解反应CH3CHO(l) CH4(g)+CO(g)的ΔH=
CH4(g)+CO(g)的ΔH=___________ 。
(4)已知断开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式是___________ 。
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g)
 NH2COONH4(s) ΔH1
NH2COONH4(s) ΔH1反应Ⅱ:NH2COONH4(s)
 CO(NH2)2(s)+H2O(g) ΔH2=+72.49 kJ·mol-1
CO(NH2)2(s)+H2O(g) ΔH2=+72.49 kJ·mol-1总反应:2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g) ΔH3=-86.98 kJ·mol-1
CO(NH2)2(s)+H2O(g) ΔH3=-86.98 kJ·mol-1则反应Ⅰ的ΔH1=
(2)氢气可将CO2还原为甲烷,反应为CO2(g)+4H2(g)
 CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示,其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会
CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示,其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会
(3)已知CO(g)、CH4(g)、CH3CHO(l)的燃烧热分别为283.0 kJ·mol-1、890.31 kJ·mol-1、1167.9 kJ·mol-1,则乙醛的分解反应CH3CHO(l)
 CH4(g)+CO(g)的ΔH=
CH4(g)+CO(g)的ΔH=(4)已知断开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式是
您最近一年使用:0次
名校
解题方法
7 . 工业上常用CO作还原剂还原铁矿石制得铁单质,实验室中可以用 还原
还原 制得铁粉。
制得铁粉。
已知:①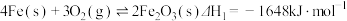
②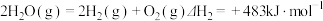
③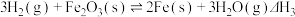
(1)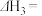
___________ ;
___________ 。(写表达式)
(2) 可以用碳和水蒸气反应制取,反应的热化学方程式为
可以用碳和水蒸气反应制取,反应的热化学方程式为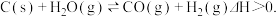 一定条件下该反应达到平衡时,温度、压强对
一定条件下该反应达到平衡时,温度、压强对 产率的影响如图1所示。
产率的影响如图1所示。
① 表示
表示 ___________  填“温度”或“压强”
填“温度”或“压强”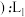
___________  填“
填“ ”、“
”、“ ”或“
”或“ ”
”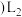 。
。
②在一恒容绝热容器中加入一定量的 和
和 发生反应:
发生反应: ,下列物理量不再改变时一定能说明反应达到平衡状态的是
,下列物理量不再改变时一定能说明反应达到平衡状态的是 ___________  填标号
填标号
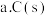 的质量
的质量 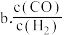
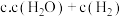
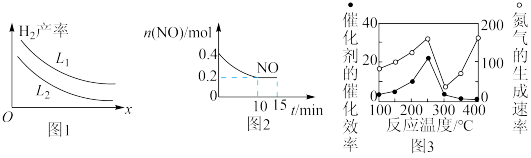
(3)实验证明用活性炭还原法能处理氮的氧化物,有关反应为 。某研究小组向某2L密闭容器中加入足量的活性炭和一定量的
。某研究小组向某2L密闭容器中加入足量的活性炭和一定量的 ,保持温度和体积不变,反应过程
,保持温度和体积不变,反应过程 中
中 的物质的量随时间的变化如图2所示。
的物质的量随时间的变化如图2所示。
①从反应开始到10min时,以 表示的平均反应速率
表示的平均反应速率
___________ 。该温度时反应的平衡常数
___________ 。
②固定压强为p,在不同温度下催化剂的催化效率与氮气的生成速率的关系如图3所示。当氮气的生成速率主要取决于温度时,其影响范围是___________ 。
 还原
还原 制得铁粉。
制得铁粉。已知:①
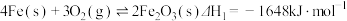
②
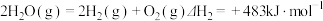
③
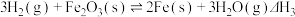
(1)
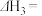

(2)
 可以用碳和水蒸气反应制取,反应的热化学方程式为
可以用碳和水蒸气反应制取,反应的热化学方程式为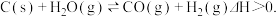 一定条件下该反应达到平衡时,温度、压强对
一定条件下该反应达到平衡时,温度、压强对 产率的影响如图1所示。
产率的影响如图1所示。
①
 表示
表示  填“温度”或“压强”
填“温度”或“压强”
 填“
填“ ”、“
”、“ ”或“
”或“ ”
”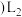 。
。②在一恒容绝热容器中加入一定量的
 和
和 发生反应:
发生反应: ,下列物理量不再改变时一定能说明反应达到平衡状态的是
,下列物理量不再改变时一定能说明反应达到平衡状态的是  填标号
填标号
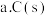 的质量
的质量 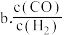
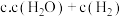
(3)实验证明用活性炭还原法能处理氮的氧化物,有关反应为
 。某研究小组向某2L密闭容器中加入足量的活性炭和一定量的
。某研究小组向某2L密闭容器中加入足量的活性炭和一定量的 ,保持温度和体积不变,反应过程
,保持温度和体积不变,反应过程 中
中 的物质的量随时间的变化如图2所示。
的物质的量随时间的变化如图2所示。①从反应开始到10min时,以
 表示的平均反应速率
表示的平均反应速率

②固定压强为p,在不同温度下催化剂的催化效率与氮气的生成速率的关系如图3所示。当氮气的生成速率主要取决于温度时,其影响范围是
您最近一年使用:0次
8 . 请按要求回答下列问题。
(1)写出下列物质在水溶液中的电离方程式
①HClO:_______ ;
②H2SO3:_______ ;
③NaHCO3:_______ ;
④Cu(OH)2:_______ 。
(2)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为_______ 。
(3)在25 ℃、101 kPa时,H2在O2中完全燃烧生成2.00 mol H2O(l)放出571.6 kJ的热量,表示H2燃烧热的热化学方程式为_______ 。
(4)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+260 kJ·mol-1①
已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1②
则CH4与O2反应生成CO和H2的热化学方程式为_______ 。
(1)写出下列物质在水溶液中的电离方程式
①HClO:
②H2SO3:
③NaHCO3:
④Cu(OH)2:
(2)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为
(3)在25 ℃、101 kPa时,H2在O2中完全燃烧生成2.00 mol H2O(l)放出571.6 kJ的热量,表示H2燃烧热的热化学方程式为
(4)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+260 kJ·mol-1①
已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1②
则CH4与O2反应生成CO和H2的热化学方程式为
您最近一年使用:0次
名校
9 . 按要求书写下列方程式:
(1)制备粗硅的化学方程式___________ 。
(2)碱性锌锰干电池的正极反应式___________ 。
(3)用氢氧化钠溶液处理NO2尾气的化学方程式___________ 。
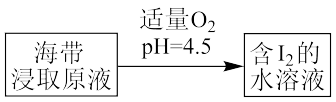
(4)海带提取碘下图所示步骤中反应的离子方程式___________ 。
(5)甲硅烷(SiH4)常温下是无色气体遇空气能自燃,生成二氧化硅和水。已知101kPa 25℃时,测得1g SiH4自燃放出热量44.6kJ/mol。写出其热化学方程式___________ 。
(1)制备粗硅的化学方程式
(2)碱性锌锰干电池的正极反应式
(3)用氢氧化钠溶液处理NO2尾气的化学方程式
(4)海带提取碘下图所示步骤中反应的离子方程式

(5)甲硅烷(SiH4)常温下是无色气体遇空气能自燃,生成二氧化硅和水。已知101kPa 25℃时,测得1g SiH4自燃放出热量44.6kJ/mol。写出其热化学方程式
您最近一年使用:0次
名校
10 . NOx(主要指NO和NO2)是大气主要污染物之一。有效去除大气中的NOx是环境保护的重要课题,研究NOx之间的转化也具有重要意义。
用水吸收NOx的相关热化学方程式如下:
(1)2NO2(g)+H2O(l)=HNO3(aq)+HNO2(aq)ΔH=-116.1kJ·mol-1
3HNO2(aq)=HNO3(aq)+2NO(g)+H2O(l)ΔH=+75.9kJ·mol-1
反应3NO2(g)+H2O(l)=2HNO3(aq)+NO(g)的ΔH=____ kJ·mol-1。
(2)已知反应2NO(g)+2CO(g) N2(g)+2CO2(g)。v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2)·c2(CO2)(k正、k逆为速率常数)。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比m=
N2(g)+2CO2(g)。v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2)·c2(CO2)(k正、k逆为速率常数)。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比m=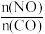 的关系如图所示。
的关系如图所示。

①达到平衡后,仅升高温度,k正增大的倍数__ (填“>”“<”或“=”)k逆增大的倍数。
②下列说法正确的是___ 。
A.投料比:m1<m2<m3
B.汽车排气管中的催化剂可提高NO的平衡转化率
C.当投料比m=2时,NO转化率比CO转化率小
D.当体系中CO2和CO物质的量浓度之比保持不变时,反应达到平衡状态
(3)已知:N2O4(g) 2NO2(g)ΔH>0将一定量N2O4气体充入刚性密闭容器中,控制反应温度为T1。t1时刻反应达到平衡,混合气体平衡总压强为p,N2O4气体的平衡转化率为75%,则反应N2O4(g)
2NO2(g)ΔH>0将一定量N2O4气体充入刚性密闭容器中,控制反应温度为T1。t1时刻反应达到平衡,混合气体平衡总压强为p,N2O4气体的平衡转化率为75%,则反应N2O4(g) 2NO2(g)的平衡常数Kp=
2NO2(g)的平衡常数Kp=___ (对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp,如p(B)=p·x(B),p为平衡总压强,x(B)为平衡系统中B的物质的量分数)。
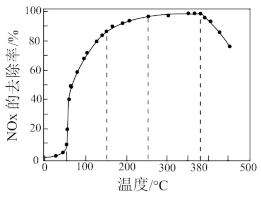
(4)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。将一定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂M的反应器中反应(如图所示)。

反应相同时间NOx的去除率随反应温度的变化曲线如图所示。
在50~250℃范围内随着温度的升高,NOx的去除率先迅速上升的主要原因是___ ;后来上升缓慢的主要原因是___ ;当反应温度高于380℃时,NOx的去除率迅速下降的原因可能是___ 。
用水吸收NOx的相关热化学方程式如下:
(1)2NO2(g)+H2O(l)=HNO3(aq)+HNO2(aq)ΔH=-116.1kJ·mol-1
3HNO2(aq)=HNO3(aq)+2NO(g)+H2O(l)ΔH=+75.9kJ·mol-1
反应3NO2(g)+H2O(l)=2HNO3(aq)+NO(g)的ΔH=
(2)已知反应2NO(g)+2CO(g)
 N2(g)+2CO2(g)。v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2)·c2(CO2)(k正、k逆为速率常数)。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比m=
N2(g)+2CO2(g)。v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2)·c2(CO2)(k正、k逆为速率常数)。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比m=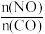 的关系如图所示。
的关系如图所示。
①达到平衡后,仅升高温度,k正增大的倍数
②下列说法正确的是
A.投料比:m1<m2<m3
B.汽车排气管中的催化剂可提高NO的平衡转化率
C.当投料比m=2时,NO转化率比CO转化率小
D.当体系中CO2和CO物质的量浓度之比保持不变时,反应达到平衡状态
(3)已知:N2O4(g)
 2NO2(g)ΔH>0将一定量N2O4气体充入刚性密闭容器中,控制反应温度为T1。t1时刻反应达到平衡,混合气体平衡总压强为p,N2O4气体的平衡转化率为75%,则反应N2O4(g)
2NO2(g)ΔH>0将一定量N2O4气体充入刚性密闭容器中,控制反应温度为T1。t1时刻反应达到平衡,混合气体平衡总压强为p,N2O4气体的平衡转化率为75%,则反应N2O4(g) 2NO2(g)的平衡常数Kp=
2NO2(g)的平衡常数Kp=(4)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。将一定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂M的反应器中反应(如图所示)。

反应相同时间NOx的去除率随反应温度的变化曲线如图所示。
在50~250℃范围内随着温度的升高,NOx的去除率先迅速上升的主要原因是

您最近一年使用:0次



