1 . 钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为 ,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
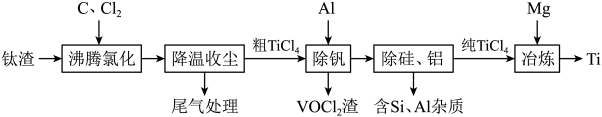
已知“降温收尘”后,粗 中含有的几种物质的沸点:
中含有的几种物质的沸点:
回答下列问题:
(1)已知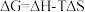 ,
, 的值只决定于反应体系的始态和终态,忽略
的值只决定于反应体系的始态和终态,忽略 、
、 随温度的变化。若
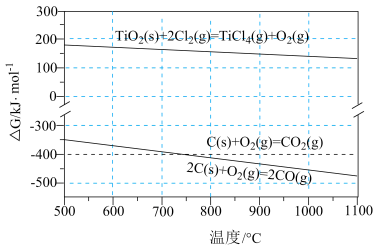
随温度的变化。若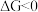 ,则该反应可以自发进行。根据下图判断:
,则该反应可以自发进行。根据下图判断: 时,下列反应不能自发进行的是_______。
时,下列反应不能自发进行的是_______。
(2) 与C、
与C、 ,在
,在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
①该温度下, 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为_______ ;
②随着温度升高,尾气中 的含量升高,原因是
的含量升高,原因是_______ 。
(3)“除钒”过程中的化学方程式为_______ ;“除硅、铝”过程中,分离 中含
中含 、
、 杂质的方法是
杂质的方法是_______ 。
(4)“除钒”和“除硅、铝”的顺序_______ (填“能”或“不能”)交换,理由是_______ 。
(5)下列金属冶炼方法与本工艺流程中加入 冶炼
冶炼 的方法相似的是_______。
的方法相似的是_______。
 ,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
已知“降温收尘”后,粗
 中含有的几种物质的沸点:
中含有的几种物质的沸点:| 物质 |  |  |  |  |
沸点/ | 136 | 127 | 57 | 180 |
(1)已知
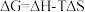 ,
, 的值只决定于反应体系的始态和终态,忽略
的值只决定于反应体系的始态和终态,忽略 、
、 随温度的变化。若
随温度的变化。若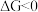 ,则该反应可以自发进行。根据下图判断:
,则该反应可以自发进行。根据下图判断: 时,下列反应不能自发进行的是_______。
时,下列反应不能自发进行的是_______。
A. | B. |
C. | D. |
 与C、
与C、 ,在
,在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
的沸腾炉中充分反应后,混合气体中各组分的分压如下表:| 物质 |  |  |  |  |
分压 | 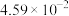 | 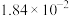 |  |  |
 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为②随着温度升高,尾气中
 的含量升高,原因是
的含量升高,原因是(3)“除钒”过程中的化学方程式为
 中含
中含 、
、 杂质的方法是
杂质的方法是(4)“除钒”和“除硅、铝”的顺序
(5)下列金属冶炼方法与本工艺流程中加入
 冶炼
冶炼 的方法相似的是_______。
的方法相似的是_______。| A.高炉炼铁 | B.电解熔融氯化钠制钠 | C.铝热反应制锰 | D.氧化汞分解制汞 |
您最近一年使用:0次
2022-06-10更新
|
11478次组卷
|
19卷引用:2022年湖北省高考真题变式题16-19
(已下线)2022年湖北省高考真题变式题16-192022年新高考湖南化学高考真题(已下线)2022年湖南卷高考真题变式题(15-19)(已下线)专题14 化学反应原理综合题-2022年高考真题模拟题分项汇编(已下线)专题16 工艺流程题-三年(2020-2022)高考真题分项汇编(已下线)考点24 化学反应的方向-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)2022年海南省高考真题变式题15-19(已下线)易错点08 金属材料-备战2023年高考化学考试易错题(已下线)专题29 无机化工流程综合分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 大题突破3 无机化工流程题题型研究(已下线)题型38 基于金属元素的工艺流程题(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)云南省开远市第一中学校2022-2023学年高二下学期5月月考化学试题(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)福建省厦门第一中学2023-2024学年高二上学期期中考试化学试题河南省周口恒大中学2023-2024学年高二上学期12月月考化学试题
2022·河北·模拟预测
名校
解题方法
2 . 一定条件下HCOOH在Pd催化剂表面脱氢的反应机理、反应历程与能量的关系如图所示:
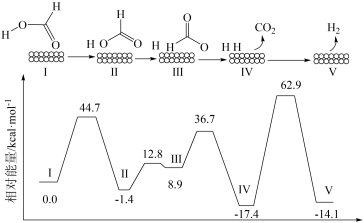
下列说法错误的是

下列说法错误的是
| A.HCOOH催化脱氢反应在该温度下能自发进行 |
| B.在历程Ⅰ~Ⅴ中,由Ⅳ到Ⅴ的反应为决速步骤 |
| C.由反应历程可得出HCOOH中第1个H原子更易脱去 |
| D.在该反应历程中,HCOOH所有的化学键均发生断裂 |
您最近一年使用:0次
名校
3 . 利用CO2催化加氢可制乙烯,反应为2CO2(g)+6H2(g)⇌C2H4(g)+4H2O(g) △H,在两个容积均为1L恒容密闭容器中,分别加入2molCO2、4molH2,分别选用两种催化剂,反应进行相同时间,测得CO2转化率随反应温度的变化如下图所示。下列说法正确的是
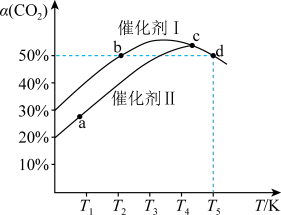

| A.使用催化剂I时反应的活化能低于催化剂II |
| B.△H>0 |
| C.b、d两状态下,化学反应速率相等 |
| D.d状态下,保持其他条件不变,向容器中再加入1molCO2与0.5molC2H4,v(正)<v(逆) |
您最近一年使用:0次
2022-03-30更新
|
1505次组卷
|
12卷引用:湖北省襄阳市第五中学2022届高三下学期适应性考试(二模)化学试题
湖北省襄阳市第五中学2022届高三下学期适应性考试(二模)化学试题江苏省徐州市新沂市第一中学2021-2022学年高三下学期3月月考化学试题(已下线)卷06 小题素养卷-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)(已下线)考点25 化学反应速率与平衡图象-备战2023年高考化学一轮复习考点帮(全国通用)河南省南阳市2022-2023学年高三上学期期中质量评估化学试题学科特色4 化学反应速率、平衡图像(已下线)题型23 平衡常数、平衡转化率图象河南省南阳市2022-2023学年高三上学期11月期中考试化学试题(已下线)考点25 化学反应速率与平衡图象(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)江西省宜春市宜丰中学2023-2024学年高二上学期9月月考化学试题河北省保定市六校联考2023-2024学年高二上学期11月期中考试化学试题(已下线)题型04 化学反应速率与平衡图像分析-2024年高考化学答题技巧与模板构建
4 . 氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气得到氢气。
方法I:氨热分解法制氢气
相关化学键的键能数据
一定温度下,利用催化剂将 分解为
分解为 和
和 。回答下列问题:
。回答下列问题:
(1)反应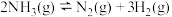

_______  ;
;
(2)已知该反应的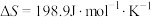 ,在下列哪些温度下反应能自发进行?
,在下列哪些温度下反应能自发进行?_______ (填标号)
A.25℃ B.125℃ C.225℃ D.325℃
(3)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将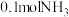 通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
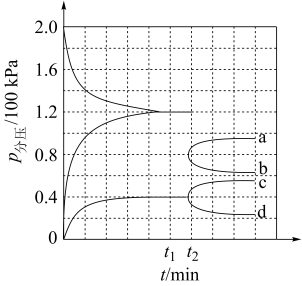
①若保持容器体积不变, 时反应达到平衡,用
时反应达到平衡,用 的浓度变化表示
的浓度变化表示 时间内的反应速率
时间内的反应速率
_______  (用含
(用含 的代数式表示)
的代数式表示)
② 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后
时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 分压变化趋势的曲线是
分压变化趋势的曲线是_______ (用图中a、b、c、d表示),理由是_______ ;
③在该温度下,反应的标准平衡常数
_______ 。(已知:分压=总压×该组分物质的量分数,对于反应 ,
, ,其中
,其中 ,
,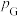 、
、 、
、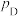 、
、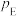 为各组分的平衡分压)。
为各组分的平衡分压)。
方法Ⅱ:氨电解法制氢气
利用电解原理,将氨转化为高纯氢气,其装置如图所示。
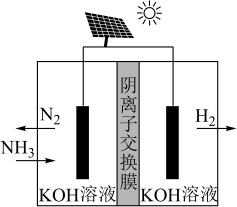
(4)电解过程中 的移动方向为
的移动方向为_______ (填“从左往右”或“从右往左”);
(5)阳极的电极反应式为_______ 。
方法I:氨热分解法制氢气
相关化学键的键能数据
| 化学键 |  |  |  |
键能 | 946 | 436.0 | 390.8 |
 分解为
分解为 和
和 。回答下列问题:
。回答下列问题:(1)反应
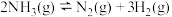

 ;
;(2)已知该反应的
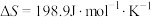 ,在下列哪些温度下反应能自发进行?
,在下列哪些温度下反应能自发进行?A.25℃ B.125℃ C.225℃ D.325℃
(3)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将
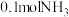 通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
①若保持容器体积不变,
 时反应达到平衡,用
时反应达到平衡,用 的浓度变化表示
的浓度变化表示 时间内的反应速率
时间内的反应速率
 (用含
(用含 的代数式表示)
的代数式表示)②
 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后
时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 分压变化趋势的曲线是
分压变化趋势的曲线是③在该温度下,反应的标准平衡常数

 ,
, ,其中
,其中 ,
,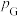 、
、 、
、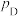 、
、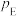 为各组分的平衡分压)。
为各组分的平衡分压)。方法Ⅱ:氨电解法制氢气
利用电解原理,将氨转化为高纯氢气,其装置如图所示。

(4)电解过程中
 的移动方向为
的移动方向为(5)阳极的电极反应式为
您最近一年使用:0次
2021-06-09更新
|
10829次组卷
|
14卷引用:湖北省鄂西南三校2023-2024学年高二下学期3月联考化学试题
湖北省鄂西南三校2023-2024学年高二下学期3月联考化学试题2021年新高考湖南化学高考真题(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(浙江专用)2021年湖南省高考化学试卷变式题11-19(已下线)专题12 化学反应原理综合题—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)回归教材重难点09 化学反应原理综合-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)押新高考卷17题 化学反应原理综合题-备战2022年高考化学临考题号押题(新高考通版)天津市第一中学2022届高三下学期5月月考化学试题(已下线)专题15 化学反应原理综合题-三年(2020-2022)高考真题分项汇编(已下线)考点23 化学平衡常数-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题17 原理综合题(已下线)专题17 原理综合题(已下线)专题15 化学反应原理综合题-2023年高考化学真题题源解密(全国通用)
名校
5 . 二甲醚是一种重要的化工原料,回答下列问题:
(1)已知:①C(s)+ O2(g)=CO(g) ∆H1=-111. 8 kJ/mol;
O2(g)=CO(g) ∆H1=-111. 8 kJ/mol;
②C(s)+ H2O(g)=CO(g) +H2(g) ∆H2 =130 kJ/mol;
③CO(g)+ 2H2(g)=CH3OH(g) ∆H3=- 90.1 kJ/mol;
④2CH3OH(g)=CH3OCH3(g)+H2O(g) ∆H4= -134 kJ/mol。
则CH3OCH3(g)+ O2 (g)=2CO(g)+3H2(g) ∆H=
O2 (g)=2CO(g)+3H2(g) ∆H=______ kJ/mol;该反应能够自发进行所采用的有利条件是______ (填“高温”“低温”或“任意温度”)。
(2)在恒温恒压条件下,化工生产上利用二甲醚与氧气为原料制备合成气,实际生产过程中常常添加一定量的水蒸气,其目的是______ ;研究发现,所得平衡混合气体中H2的体积分数随n(O2)/n(CH3OCH3)变化如图所示,试解释该曲线先变大后减小的原因______ 。
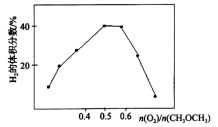
(3)某温度下,在VL的刚性容器中充入4.0molCH3OCH3、2.0molO2及2.0molH2O(g),在催化剂作用下仅发生反应CH3OCH3(g)+ O2(g)
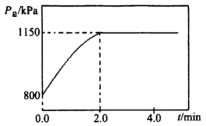
O2(g) 2CO(g)+3H2(g),实验测得容器中压强与时间变化如图所示。则前2.0min内该反应速率v(CH3OCH3)=
2CO(g)+3H2(g),实验测得容器中压强与时间变化如图所示。则前2.0min内该反应速率v(CH3OCH3)=______ mol·min-1;该温度下其分压平衡常数Kp=______ (kPa)3.5(已知 =12.2)。
=12.2)。
(4)二甲醚燃料电池常采用磺酸类质子溶剂,其工作原理如图所示,则负极的电极反应式为______ ,若消耗标准状况下5.6LO2,则理论上左右两室溶液质量变化的差为______ g。

(1)已知:①C(s)+
 O2(g)=CO(g) ∆H1=-111. 8 kJ/mol;
O2(g)=CO(g) ∆H1=-111. 8 kJ/mol;②C(s)+ H2O(g)=CO(g) +H2(g) ∆H2 =130 kJ/mol;
③CO(g)+ 2H2(g)=CH3OH(g) ∆H3=- 90.1 kJ/mol;
④2CH3OH(g)=CH3OCH3(g)+H2O(g) ∆H4= -134 kJ/mol。
则CH3OCH3(g)+
 O2 (g)=2CO(g)+3H2(g) ∆H=
O2 (g)=2CO(g)+3H2(g) ∆H=(2)在恒温恒压条件下,化工生产上利用二甲醚与氧气为原料制备合成气,实际生产过程中常常添加一定量的水蒸气,其目的是

(3)某温度下,在VL的刚性容器中充入4.0molCH3OCH3、2.0molO2及2.0molH2O(g),在催化剂作用下仅发生反应CH3OCH3(g)+
 O2(g)
O2(g) 2CO(g)+3H2(g),实验测得容器中压强与时间变化如图所示。则前2.0min内该反应速率v(CH3OCH3)=
2CO(g)+3H2(g),实验测得容器中压强与时间变化如图所示。则前2.0min内该反应速率v(CH3OCH3)= =12.2)。
=12.2)。
(4)二甲醚燃料电池常采用磺酸类质子溶剂,其工作原理如图所示,则负极的电极反应式为

您最近一年使用:0次
2021-04-04更新
|
648次组卷
|
5卷引用:湖北省华大新高考联盟2021届高三下学期3月教学质量测评(全国卷)理综化学试题
6 . 氯气是现代工业的重要原料,将氯化氢转化为氯气的技术成为科学研究的热车点,回答下列问题:
(1)Deacon发明的直接氧化法为:4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)。可按下列催化过程进行:
Ⅰ.CuCl2(s)=CuCl(s)+ Cl2(g) ΔH1=+83kJ·mol-1
Cl2(g) ΔH1=+83kJ·mol-1
Ⅱ.CuCl(s)+ O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) ΔH2=-20kJ·mol-1
Cl2(g) ΔH2=-20kJ·mol-1
Ⅲ.4HCl(g)+O2(g)=2Cl2(g)+2H2O(g) ΔH3
反应Ⅰ能自发进行的条件是___ 。利用ΔH1和ΔH2计算ΔH3时,还需要利用反应___ 的ΔH。
(2)如图为刚性容器中,进料浓度比c(HCl):c(O2)分别等于1:1、4:1、7:1时HCl平衡转化率随温度变化的关系:

可知反应平衡常数K(400℃)__ K(500℃)(填“大于”或“小于”)。设容器内初始压强为p0,根据进料浓度比c(HCl):c(O2)=4:1的数据,计算400℃时容器内的平衡压强=___ (列出计算式)。按化学计量比进料可以保持反应物高转化率,同时降低产物分离的能耗。进料浓度比c(HCl):c(O2)过低、过高的不利影响分别是___ 。
(3)已知:氯气与NaOH溶液反应可生成NaClO3。有研究表明,生成NaClO3的反应分两步进行:
Ⅰ.2ClO-=ClO2-+Cl-
Ⅱ.ClO2-+ClO-=ClO3-+Cl-
常温下,反应Ⅱ能快速进行,但氯气与NaOH溶液反应很难得到NaClO3,试用碰撞理论解释其原因:___ 。
(4)电解NaClO3水溶液可制备NaClO4,写出阳极反应式:___ 。
(1)Deacon发明的直接氧化法为:4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)。可按下列催化过程进行:
Ⅰ.CuCl2(s)=CuCl(s)+
 Cl2(g) ΔH1=+83kJ·mol-1
Cl2(g) ΔH1=+83kJ·mol-1Ⅱ.CuCl(s)+
 O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) ΔH2=-20kJ·mol-1
Cl2(g) ΔH2=-20kJ·mol-1Ⅲ.4HCl(g)+O2(g)=2Cl2(g)+2H2O(g) ΔH3
反应Ⅰ能自发进行的条件是
(2)如图为刚性容器中,进料浓度比c(HCl):c(O2)分别等于1:1、4:1、7:1时HCl平衡转化率随温度变化的关系:

可知反应平衡常数K(400℃)
(3)已知:氯气与NaOH溶液反应可生成NaClO3。有研究表明,生成NaClO3的反应分两步进行:
Ⅰ.2ClO-=ClO2-+Cl-
Ⅱ.ClO2-+ClO-=ClO3-+Cl-
常温下,反应Ⅱ能快速进行,但氯气与NaOH溶液反应很难得到NaClO3,试用碰撞理论解释其原因:
(4)电解NaClO3水溶液可制备NaClO4,写出阳极反应式:
您最近一年使用:0次
2020-03-27更新
|
410次组卷
|
3卷引用:湖北省宜昌市2020届高三年级3月线上统一调研试题理综化学试题
名校
7 . 氨的合成原理为:N2(g)+3H2(g)⇌2NH3(g)∆H=-92.4kJ·mol-1在500℃、20MPa时,将N2、H2置于一个容积为2L的密闭容器中发生反应,反应过程中各物质的物质的量变化如图。回答下列问题:
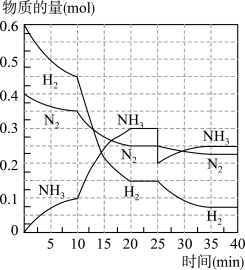
(1)10min内以NH3表示的平均反应速率为_________
(2)在10~20min内,NH3浓度变化的原因可能是_____________
A.加了催化剂
B.缩小容器体积
C.降低温度
D.增加NH3物质的量
(3)第1次平衡:平衡常数K1=__________ (带数据的表达式),第2次平衡时NH3的体积分数为_____________ 。
(4)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fc2O3的TiO2)表面与水发生下列反应:N2(g)+3H2O(l)⇌2NH3+1.5O2(g)∆H=akJ·mol-1,进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
①此合成反应的a______ 0,△S_______ 0;(填“>”、“<”或一”)
②已知N2(g)+3H2(g)⇌2NH3(g)∆H=-92.4kJ·mol-1,2 H2(g)+ O2(g)=2H2O(l) ∆H=-571.kJ·mol-1 则常温下氮气与水反应生成氨气与氧气的热化学方程式为_____________________________

(1)10min内以NH3表示的平均反应速率为
(2)在10~20min内,NH3浓度变化的原因可能是
A.加了催化剂
B.缩小容器体积
C.降低温度
D.增加NH3物质的量
(3)第1次平衡:平衡常数K1=
(4)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fc2O3的TiO2)表面与水发生下列反应:N2(g)+3H2O(l)⇌2NH3+1.5O2(g)∆H=akJ·mol-1,进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
①此合成反应的a
②已知N2(g)+3H2(g)⇌2NH3(g)∆H=-92.4kJ·mol-1,2 H2(g)+ O2(g)=2H2O(l) ∆H=-571.kJ·mol-1 则常温下氮气与水反应生成氨气与氧气的热化学方程式为
您最近一年使用:0次
2019-10-28更新
|
188次组卷
|
2卷引用:湖北省随州一中2019-2020学年高二上学期期中考试化学试题
名校
解题方法
8 . 我国钒钛磁铁矿分布广泛,储量丰富,不仅是铁的重要来源,其中伴生的钛、钒、铝等多种成分还具有很高的利用价值。其尾矿是工业提取钛的重要来源
I.钒钛磁铁矿的尾矿(主要成分为FeTiO3,还含有少量FeO、Al2O3、SiO2 等杂质) 经选矿后得到钛精矿过一系列反应制得TiO2:

(1)氢氧化钠净化尾矿的目的是_________________________________ 。
(2)写出钛精矿中FeTiO3与80%硫酸溶液反应的化学方程式:___________________ 。
Ⅱ.以TiO2 为原料制备金属钛,流程如下: TiO2→TiCl4→Ti
(3)已知反应:TiO2(s)十2Cl2(g)=TiCl4(l)十O2(g) △H=十151kJ/mol,但不能由TiO2和Cl2直接反应(即氯化反应)来制取TiCl4试解释原因:___________________________________ 。
(4)当往氯化反应体系中加入碳后,使得该反应在高温条件下能顺利制得TiCl4,从化学平衡的角度解释其原因___________________________________________ 。
(5)已知碳的燃烧热394kJ/mol,请写出TiO2 与Cl2、C反应制取TiCl4的热化学方程式_____________ 。
Ⅲ.以TiO2为原料可以制备Li4Ti5O12(一种锂离子电池的电极材料),过程如下:

(6)不同温度下,TiO2·xH2O与双氧水、氨水反应达到平衡所得实验结果如下表所示:
该过程的理想温度为_______________ ,分析表中数据,解释TiO2·xH2O的转化率随温度变化的原因:_______________________________________ ,该反应的离子方程式为________________________ 。
I.钒钛磁铁矿的尾矿(主要成分为FeTiO3,还含有少量FeO、Al2O3、SiO2 等杂质) 经选矿后得到钛精矿过一系列反应制得TiO2:

(1)氢氧化钠净化尾矿的目的是
(2)写出钛精矿中FeTiO3与80%硫酸溶液反应的化学方程式:
Ⅱ.以TiO2 为原料制备金属钛,流程如下: TiO2→TiCl4→Ti
(3)已知反应:TiO2(s)十2Cl2(g)=TiCl4(l)十O2(g) △H=十151kJ/mol,但不能由TiO2和Cl2直接反应(即氯化反应)来制取TiCl4试解释原因:
(4)当往氯化反应体系中加入碳后,使得该反应在高温条件下能顺利制得TiCl4,从化学平衡的角度解释其原因
(5)已知碳的燃烧热394kJ/mol,请写出TiO2 与Cl2、C反应制取TiCl4的热化学方程式
Ⅲ.以TiO2为原料可以制备Li4Ti5O12(一种锂离子电池的电极材料),过程如下:

(6)不同温度下,TiO2·xH2O与双氧水、氨水反应达到平衡所得实验结果如下表所示:
| 温度/℃ | 30 | 35 | 40 | 45 | 50 |
| TiO2·xH2O 的转化率 | 80% | 90% | 97% | 93% | 82% |
您最近一年使用:0次
9 . 下列说法不正确的有
| A.常温下反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应△H>0 |
B.H2(g)+I2(g) 2HI(g) △H=-QkJ·mol-1,表示一定条件下有 1molH2和1molI2(g)反应生成2 mol HI (g)时放出QkJ的热量 2HI(g) △H=-QkJ·mol-1,表示一定条件下有 1molH2和1molI2(g)反应生成2 mol HI (g)时放出QkJ的热量 |
| C.过量铁粉与l00mL0.0lmol·L-1的稀盐酸反应,滴入几滴CuSO4溶液能加快反应速率,但不改变产生H2的量 |
| D.改变反应条件使化学平衡向正反应方向移动时反应物的转化率一定增大 |
您最近一年使用:0次
名校
10 . 关于恒容密闭容器进行的反应C(s)+ CO2(g)= 2CO(g)△H >0,下列说法不正确的是
| A.△S>0 |
| B.在低温下能自发进行 |
| C.当混合气体的密度不再发生变化时,反应达到平衡状态 |
| D.达到平衡状态时,升高温度, CO2转化率和反应速率均增大 |
您最近一年使用:0次
2017-11-11更新
|
811次组卷
|
9卷引用:湖北省随州一中2019-2020学年高二上学期期中考试化学试题
湖北省随州一中2019-2020学年高二上学期期中考试化学试题甘肃省会宁县第一中学2017-2018学年高二上学期期中考试(理)化学试题江西省南昌县莲塘一中2018届高三11月质量检测化学试题(已下线)2018-2019学年同步单元双基双测AB卷:第二单元化学反应速率与化学平衡单元测试B卷吉林省长春市一五O中2018-2019学年高二上学期期中考试化学试题湖南省双峰县第一中学2018-2019学年高二下学期第一次月考化学试题吉林省吉林地区普通高中友好学校联合体第三十一届2019-2020学年高二上学期期中考试化学试题内蒙古赤峰市宁城县2019-2020学年高二上学期期末考试化学试题黑龙江省鸡西市第一中学2020-2021学年度高二上学期期末化学试题



