1 . 在某温度下,5L密闭容器内发生如下反应:CH4(g)+H2O (g) CO(g)+3H2(g) △H>0
CO(g)+3H2(g) △H>0
(1)反应中的非极性分子为:______ 、______ 。
(2)一个可逆反应的平衡常数只随温度而变化,请写出该反应的平衡常数表达式______ ,当温度升高,该平衡常数______ (填“增大”、“减小”或“不变”)。
(3)反应20min后生成了18g氢气,甲烷的平均反应速率为______ 。
(4)下列选项中的物理量不变时,一定可以判断反应达到平衡的是______(双选)。
(5)在某一时刻,v正=v逆=v,此时反应达到平衡。若改变一条件,可使得v正<v逆<v,指出可以改变的条件______ ,并说明理由:__________________ 。
A.升高温度 B.增大压强 C.降低温度 D.降低压强
(6)已知CO与H2合成CH3OH是可逆反应:CO+2H2 CH3OH。试求:当投料比n(CO):n(H2)=
CH3OH。试求:当投料比n(CO):n(H2)= ______ 时,平衡时CO与H2的转化率相同。
 CO(g)+3H2(g) △H>0
CO(g)+3H2(g) △H>0(1)反应中的非极性分子为:
(2)一个可逆反应的平衡常数只随温度而变化,请写出该反应的平衡常数表达式
(3)反应20min后生成了18g氢气,甲烷的平均反应速率为
(4)下列选项中的物理量不变时,一定可以判断反应达到平衡的是______(双选)。
| A.氢元素的质量分数 | B.容器内的压强 |
| C.反应的平衡常数 | D.容器内气体的平均分子量 |
A.升高温度 B.增大压强 C.降低温度 D.降低压强
(6)已知CO与H2合成CH3OH是可逆反应:CO+2H2
 CH3OH。试求:当投料比n(CO):n(H2)=
CH3OH。试求:当投料比n(CO):n(H2)=
您最近一年使用:0次
2 . Ⅰ.1909年哈伯在实验室中首次利用氮气与氧气反应合成氨,实现了人工固氮。
(1)一定条件下,氨的平衡含量如下表,哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,主要原因是____________
Ⅱ.在其它条件不变时,不同温度(200℃、400℃、600℃)、压强下,平衡混合物中 的物质的量分数的变化情况如下图所示:
的物质的量分数的变化情况如下图所示:
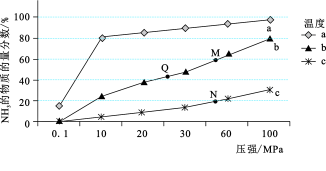
(2)曲线a对应的温度是___________ ;M、N、Q点平衡常数K的大小关系是___________ 。
Ⅲ.最新“人工固氮”的研究报道:常温常压、光照条件下, 在催化剂表面与某物质发生反应,相应的平衡常数表达式为
在催化剂表面与某物质发生反应,相应的平衡常数表达式为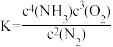 。
。
(3)写出上述反应的化学方程式___________ 。
(4)已知该反应的平衡常数K与温度的关系如图,则此反应的正反应___________ 。(填“吸热“放热”或“不能确定”)
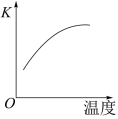
(5)常温下,如果上述反应在体积不变的密闭容器发生,当反应达到平衡时,下列描述正确的是___________。
Ⅳ.工业上,在催化剂条件下,用 作为还原剂将烟气中的
作为还原剂将烟气中的 还原成无害的氮气和水,反应方程式可表示为:
还原成无害的氮气和水,反应方程式可表示为: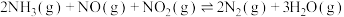 。
。
(6)一定条件下,在容积为 的密闭容器内反应,
的密闭容器内反应, 时达到平衡,生成
时达到平衡,生成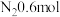 ,则平均反应速率
,则平均反应速率
___________ 。
(7) 的平衡转化率
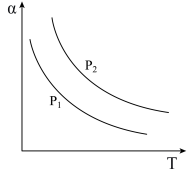
的平衡转化率 与反应温度
与反应温度 和压强
和压强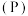 的关系如下图所示,根据图像判断:
的关系如下图所示,根据图像判断:
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(8)温度不变,将容器体积压缩至原来的一半,再次达到新平衡, 的浓度为原来的1.6倍,此时
的浓度为原来的1.6倍,此时 的体积分数相比原平衡状态下
的体积分数相比原平衡状态下___________ 。(填“增大”、“减小”或“保持不变”)
(9)体系的颜色变化能否作为判断上述反应达到平衡的依据,并说明其理由是___________ 。
(1)一定条件下,氨的平衡含量如下表,哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,主要原因是
| 温度/℃ | 压强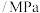 | 氨的平衡含量 |
| 200 | 10 | 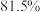 |
| 550 | 10 |  |
Ⅱ.在其它条件不变时,不同温度(200℃、400℃、600℃)、压强下,平衡混合物中
 的物质的量分数的变化情况如下图所示:
的物质的量分数的变化情况如下图所示:
(2)曲线a对应的温度是
Ⅲ.最新“人工固氮”的研究报道:常温常压、光照条件下,
 在催化剂表面与某物质发生反应,相应的平衡常数表达式为
在催化剂表面与某物质发生反应,相应的平衡常数表达式为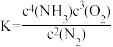 。
。(3)写出上述反应的化学方程式
(4)已知该反应的平衡常数K与温度的关系如图,则此反应的正反应

(5)常温下,如果上述反应在体积不变的密闭容器发生,当反应达到平衡时,下列描述正确的是___________。
| A.容器中气体的平均分子量不随时间而变化 |
B.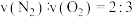 |
| C.容器中气体的密度不随时间而变化 |
| D.再次通入稀有气体,平衡逆向移动 |
Ⅳ.工业上,在催化剂条件下,用
 作为还原剂将烟气中的
作为还原剂将烟气中的 还原成无害的氮气和水,反应方程式可表示为:
还原成无害的氮气和水,反应方程式可表示为: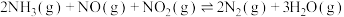 。
。(6)一定条件下,在容积为
 的密闭容器内反应,
的密闭容器内反应, 时达到平衡,生成
时达到平衡,生成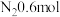 ,则平均反应速率
,则平均反应速率
(7)
 的平衡转化率
的平衡转化率 与反应温度
与反应温度 和压强
和压强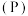 的关系如下图所示,根据图像判断:
的关系如下图所示,根据图像判断:
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(8)温度不变,将容器体积压缩至原来的一半,再次达到新平衡,
 的浓度为原来的1.6倍,此时
的浓度为原来的1.6倍,此时 的体积分数相比原平衡状态下
的体积分数相比原平衡状态下(9)体系的颜色变化能否作为判断上述反应达到平衡的依据,并说明其理由是
您最近一年使用:0次
名校
3 . Ⅰ.根据所学知识,完成下列问题
(1)下列对化学反应速率的理解正确的是_______
(2)下列关于影响化学反应速率的条件的说法正确的是_______
(3)在一定条件下,向某容器中充入 和
和 合成
合成 ,以下叙述错误的是_______
,以下叙述错误的是_______
Ⅱ.已知在2L的密闭固定容器中进行如下可逆反应,各物质的有关数据如下,回答下列问题。

(4)该可逆反应的化学方程式可表示为___________ 。
(5)用物质B来表示0~2s的平均反应速率为___________ 。
(6)下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是___________。
(1)下列对化学反应速率的理解正确的是_______
| A.化学反应速率表示的是化学反应进行的程度 |
| B.化学反应速率可以用单位时间内反应物浓度的变化来表示 |
| C.化学反应速率可以用任何一种反应物或生成物来表示 |
| D.化学反应速率可以是正值,也可以是负值 |
(2)下列关于影响化学反应速率的条件的说法正确的是_______
| A.增大反应物的物质的量,一定会加快反应速率 |
| B.使用催化剂,反应速率加快,但不改变反应的历程 |
| C.反应物浓度是决定化学反应速率的主要因素 |
| D.升高温度,一般能加快化学反应速率 |
(3)在一定条件下,向某容器中充入
 和
和 合成
合成 ,以下叙述错误的是_______
,以下叙述错误的是_______| A.开始反应时,正反应速率最大,逆反应速率为零 |
| B.随着反应的进行,正反应速率逐渐减小,最后减小为零 |
| C.随着反应的进行,逆反应速率逐渐增大,最后保持恒定 |
| D.随着反应的进行,正反应速率逐渐减小,最后与逆反应速率相等且都保持恒定 |
Ⅱ.已知在2L的密闭固定容器中进行如下可逆反应,各物质的有关数据如下,回答下列问题。

(4)该可逆反应的化学方程式可表示为
(5)用物质B来表示0~2s的平均反应速率为
(6)下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是___________。
A. | B.容器内气体的总压强保持不变 |
| C.容器内气体的密度不变 | D. |
您最近一年使用:0次
名校
解题方法
4 . 在密闭容器中充入一定量 ,发生反应:
,发生反应:
 ,如图为
,如图为 气体的平衡转化率与温度、压强的关系。
气体的平衡转化率与温度、压强的关系。
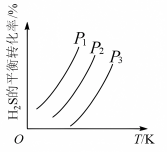
请完成下列填空:
(1)在一定条件下,往2L密闭容器中充入 进行反应,2min时达到平衡状态,此时
进行反应,2min时达到平衡状态,此时 剩余2mol,计算0~2min内
剩余2mol,计算0~2min内 的平均反应速率
的平均反应速率
__________  。图中压强
。图中压强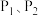 、
、 从大到小顺序为
从大到小顺序为____________________ ,原因是:________________________________________ 。又已知 可转化成羰基碱(COS):
可转化成羰基碱(COS):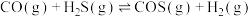

(2)上述反应的平衡常数表达式______________________________ 。
(3)在一恒容的密闭容器中,充入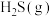 与
与 进行上述反应。下列事实能说明反应达到平衡状态的是
进行上述反应。下列事实能说明反应达到平衡状态的是__________ (选填编号)。
a.生成amolCOS,同时形成amolH-S键 b.消耗 的速率与生成COS速率之比为1:1
的速率与生成COS速率之比为1:1
c.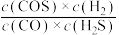 的值不再改变 d.混合气体的平均相对分子质量不再改变
的值不再改变 d.混合气体的平均相对分子质量不再改变
(4)若将标准状况下224mL的 气体通入200mL的
气体通入200mL的 溶液中正好完全反应,现象是
溶液中正好完全反应,现象是______________________________ ,写出反应的离子方程式:______________________________ ,若溶液体积没有发生改变,此时溶液的pH是__________ 。
 ,发生反应:
,发生反应:
 ,如图为
,如图为 气体的平衡转化率与温度、压强的关系。
气体的平衡转化率与温度、压强的关系。
请完成下列填空:
(1)在一定条件下,往2L密闭容器中充入
 进行反应,2min时达到平衡状态,此时
进行反应,2min时达到平衡状态,此时 剩余2mol,计算0~2min内
剩余2mol,计算0~2min内 的平均反应速率
的平均反应速率
 。图中压强
。图中压强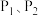 、
、 从大到小顺序为
从大到小顺序为 可转化成羰基碱(COS):
可转化成羰基碱(COS):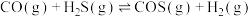

(2)上述反应的平衡常数表达式
(3)在一恒容的密闭容器中,充入
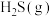 与
与 进行上述反应。下列事实能说明反应达到平衡状态的是
进行上述反应。下列事实能说明反应达到平衡状态的是a.生成amolCOS,同时形成amolH-S键 b.消耗
 的速率与生成COS速率之比为1:1
的速率与生成COS速率之比为1:1c.
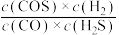 的值不再改变 d.混合气体的平均相对分子质量不再改变
的值不再改变 d.混合气体的平均相对分子质量不再改变(4)若将标准状况下224mL的
 气体通入200mL的
气体通入200mL的 溶液中正好完全反应,现象是
溶液中正好完全反应,现象是
您最近一年使用:0次
5 . 化石燃料燃烧过程中形成 和
和 等污染物,去除污染物的一种方法是在催化剂作用下发生反应:
等污染物,去除污染物的一种方法是在催化剂作用下发生反应: 。某温度下,在容积
。某温度下,在容积 的密闭容器中通入
的密闭容器中通入 和
和 ,测得不同时间
,测得不同时间 的物质的量如下表:
的物质的量如下表:
(1)用 的浓度变化表示
的浓度变化表示 的平均反应速率为
的平均反应速率为_______ 。若要加快反应速率,可以采取的措施有_______ (任写一条)。
(2)下列叙述能说明该反应已经达到平衡状态的是_______。
 和
和 等污染物,去除污染物的一种方法是在催化剂作用下发生反应:
等污染物,去除污染物的一种方法是在催化剂作用下发生反应: 。某温度下,在容积
。某温度下,在容积 的密闭容器中通入
的密闭容器中通入 和
和 ,测得不同时间
,测得不同时间 的物质的量如下表:
的物质的量如下表:时间 | 0 | 1 | 2 | 3 | …… |
 |  |  |  |  | …… |
 的浓度变化表示
的浓度变化表示 的平均反应速率为
的平均反应速率为(2)下列叙述能说明该反应已经达到平衡状态的是_______。
A. 的体积分数不再变化 的体积分数不再变化 | B. 的物质的量不再变化 的物质的量不再变化 |
| C.混合气体的密度不再变化 | D. 和 和 的浓度比保持不变 的浓度比保持不变 |
您最近一年使用:0次
6 . 与氨气相关的化学变化是氮循环和转化的重要一环,对生产、生活有重要的价值。
(1)下图转化途径中属于“固氮”的是___________。

(2)合成氨是目前转化空气中氮最有效的工业方法,其反应历程和能量变化的简图如下:(图中 表示物质吸附在催化剂表面时的状态)
表示物质吸附在催化剂表面时的状态)

①由图可知合成氨反应 的
的
___________  ,对总反应速率影响较大的是步骤
,对总反应速率影响较大的是步骤___________ 。(填写编号)
②若改变某一条件,使合成氨的化学反应速率加快,下列解释正确的是___________ 。
A.升高温度,使单位体积内活化分子百分数增加
B.增加反应物的浓度,使单位体积内活化分子百分数增加
C.使用催化剂,能降低反应活化能,使单位体积内活化分子数增加
D.增大压强,能降低反应的活化能,使单位体积内活化分子数增加
(3)氨是极具前景的氢能载体和性能卓越的“零碳”燃料,利用 的燃烧反应(
的燃烧反应( )能设计成燃料电池,其工作原理如图所示。电极
)能设计成燃料电池,其工作原理如图所示。电极 为
为___________ (选填“正”或“负”)极;电极 的电极反应式为
的电极反应式为___________ ;当正负极共消耗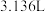 (标准状况)气体时,通过负载的电子数为
(标准状况)气体时,通过负载的电子数为___________ 个。

合成氨厂的可用于合成重要化工原料 ,主要反应为:
,主要反应为: ,向两个容积固定为
,向两个容积固定为 的密闭容器中分别充入比例相同,但总量不同的
的密闭容器中分别充入比例相同,但总量不同的 和气体,
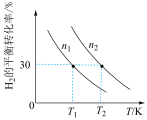
和气体, 的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
(4)①若 时,向容器中充入
时,向容器中充入 气体(
气体( 和
和 ),反应至
),反应至 时达到平衡,则
时达到平衡,则 内
内 的平均反应速率
的平均反应速率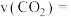
___________ 。
②由上图可判断该反应是___________ (选填“吸热”或“放热”)反应,在___________ (填“较高”或“较低”)温度下有利于该反应自发进行。
③判断图中 、
、 相对大小,并说明理由。
相对大小,并说明理由。___________ 。
(1)下图转化途径中属于“固氮”的是___________。

| A.④⑤⑥ | B.①③④ | C.①⑤⑦ | D.②⑧⑨ |
(2)合成氨是目前转化空气中氮最有效的工业方法,其反应历程和能量变化的简图如下:(图中
 表示物质吸附在催化剂表面时的状态)
表示物质吸附在催化剂表面时的状态)
①由图可知合成氨反应
 的
的
 ,对总反应速率影响较大的是步骤
,对总反应速率影响较大的是步骤②若改变某一条件,使合成氨的化学反应速率加快,下列解释正确的是
A.升高温度,使单位体积内活化分子百分数增加
B.增加反应物的浓度,使单位体积内活化分子百分数增加
C.使用催化剂,能降低反应活化能,使单位体积内活化分子数增加
D.增大压强,能降低反应的活化能,使单位体积内活化分子数增加
(3)氨是极具前景的氢能载体和性能卓越的“零碳”燃料,利用
 的燃烧反应(
的燃烧反应( )能设计成燃料电池,其工作原理如图所示。电极
)能设计成燃料电池,其工作原理如图所示。电极 为
为 的电极反应式为
的电极反应式为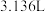 (标准状况)气体时,通过负载的电子数为
(标准状况)气体时,通过负载的电子数为
合成氨厂的可用于合成重要化工原料
 ,主要反应为:
,主要反应为: ,向两个容积固定为
,向两个容积固定为 的密闭容器中分别充入比例相同,但总量不同的
的密闭容器中分别充入比例相同,但总量不同的 和气体,
和气体, 的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
(4)①若
 时,向容器中充入
时,向容器中充入 气体(
气体( 和
和 ),反应至
),反应至 时达到平衡,则
时达到平衡,则 内
内 的平均反应速率
的平均反应速率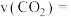
②由上图可判断该反应是
③判断图中
 、
、 相对大小,并说明理由。
相对大小,并说明理由。
您最近一年使用:0次
名校
7 . 图1是哈伯法的流程图,图2是反应历程。

(1)步骤③采用的催化剂是______ ,使用催化剂后
______ (填“增大”、“减小”或“不变”);步骤③中选择500℃的主要原因______ ,步骤①的目的是______ 。
(2)图1中为提高原料转化率而采收的措施是______。
(3)500℃、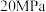 时,将
时,将 和
和 置于一容积为
置于一容积为 的密闭容器中发生反应。反应过程中
的密闭容器中发生反应。反应过程中 、
、 和
和 物质的量变化如图所示,回答下列问题:
物质的量变化如图所示,回答下列问题:

①反应开始到第 ,
, 的平均反应速率为
的平均反应速率为______  。
。
②反应进行到 至
至 时改变的条件可能是
时改变的条件可能是______ 。
A.增大容器体积 B.升温 C.使用了催化剂 D.加入了
③在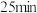 改变条件后,平衡
改变条件后,平衡______ (填“正”或“逆”)向移动,达到新平衡后 的体积分数比原平衡
的体积分数比原平衡______ (填“大”或“小”)。

(1)步骤③采用的催化剂是

(2)图1中为提高原料转化率而采收的措施是______。
| A.①②③ | B.②④⑤ | C.①③⑤ | D.②③④ |
(3)500℃、
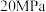 时,将
时,将 和
和 置于一容积为
置于一容积为 的密闭容器中发生反应。反应过程中
的密闭容器中发生反应。反应过程中 、
、 和
和 物质的量变化如图所示,回答下列问题:
物质的量变化如图所示,回答下列问题:
①反应开始到第
 ,
, 的平均反应速率为
的平均反应速率为 。
。②反应进行到
 至
至 时改变的条件可能是
时改变的条件可能是A.增大容器体积 B.升温 C.使用了催化剂 D.加入了

③在
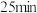 改变条件后,平衡
改变条件后,平衡 的体积分数比原平衡
的体积分数比原平衡
您最近一年使用:0次
名校
8 . 科学家对汽车尾气进行无害化处理反应为: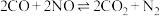 。一定条件下,在
。一定条件下,在 密闭容器中充入
密闭容器中充入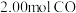 和
和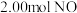 ,一段时间后测得
,一段时间后测得 、
、 浓度随时间变化如图1所示,
浓度随时间变化如图1所示, 的平衡转化率与温度、起始投料比m的关系如图2所示,图中起始投料比
的平衡转化率与温度、起始投料比m的关系如图2所示,图中起始投料比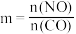 ,完成问题:
,完成问题:
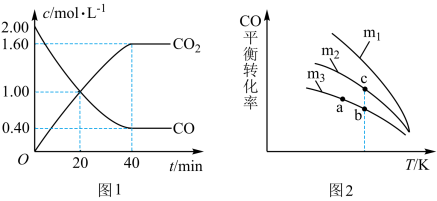
(1)该反应的化学平衡常数表达式是___________ 。根据图1,用 表示该反应达平衡过程中的平均反应速率是
表示该反应达平衡过程中的平均反应速率是___________  。
。
(2)已知:反应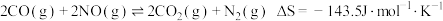 ,每生成14克
,每生成14克 时放出
时放出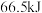 热量试写出上述反应的热化学方程式:
热量试写出上述反应的热化学方程式:___________ 。该反应在___________ 填入选项符号(A.高于、B.低于)___________  (填写温度数值)时,反应可以自发进行。
(填写温度数值)时,反应可以自发进行。
(3)图2中a、b、c三点对应的平衡常数 、
、 、
、 相对大小关系是
相对大小关系是___________ 。
(4)写出一条结论,可表明该反应已经达到平衡状态___________ 。
(5)下列关于该可逆反应的说法不正确的是___________。
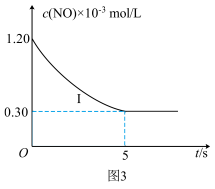
(6)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了验证倠化剂比表面积对反应速率的影响规律,在温度为 时,某同学设计了以下实验:
时,某同学设计了以下实验:
在图3中画出表中实验II条件下混合气体中 的浓度随时间变化的曲线
的浓度随时间变化的曲线___________ 。
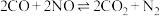 。一定条件下,在
。一定条件下,在 密闭容器中充入
密闭容器中充入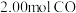 和
和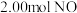 ,一段时间后测得
,一段时间后测得 、
、 浓度随时间变化如图1所示,
浓度随时间变化如图1所示, 的平衡转化率与温度、起始投料比m的关系如图2所示,图中起始投料比
的平衡转化率与温度、起始投料比m的关系如图2所示,图中起始投料比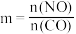 ,完成问题:
,完成问题:
(1)该反应的化学平衡常数表达式是
 表示该反应达平衡过程中的平均反应速率是
表示该反应达平衡过程中的平均反应速率是 。
。(2)已知:反应
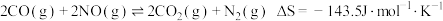 ,每生成14克
,每生成14克 时放出
时放出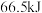 热量试写出上述反应的热化学方程式:
热量试写出上述反应的热化学方程式: (填写温度数值)时,反应可以自发进行。
(填写温度数值)时,反应可以自发进行。(3)图2中a、b、c三点对应的平衡常数
 、
、 、
、 相对大小关系是
相对大小关系是(4)写出一条结论,可表明该反应已经达到平衡状态
(5)下列关于该可逆反应的说法不正确的是___________。
A.其他条件不变,若充入 ,达到新平衡时, ,达到新平衡时, 、 、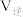 均增大 均增大 |
B.加入催化剂可提高 的平衡转化率 的平衡转化率 |
| C.若适当增大压强,则平衡正向移动 |
D.其他条件不变,若容器体积扩大一倍,达到新平衡时,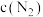 小于原来的一半 小于原来的一半 |
(6)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了验证倠化剂比表面积对反应速率的影响规律,在温度为
 时,某同学设计了以下实验:
时,某同学设计了以下实验:| 编号 | 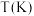 |  的初始浓度 的初始浓度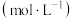 |  的初始浓度 的初始浓度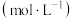 | 催化剂的比表面积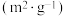 |
 |  |  | 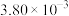 | 75 |
 |  |  | 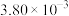 | 50 |
 的浓度随时间变化的曲线
的浓度随时间变化的曲线
您最近一年使用:0次
名校
9 . 随着我国碳中和、碳达峰目标的确定, 的综合利用备受关注。
的综合利用备受关注。
已知 为放热反应,在固定容积为2.0L的密闭容器中充入0.8mol的
为放热反应,在固定容积为2.0L的密闭容器中充入0.8mol的 和2.4mol的
和2.4mol的 ,测得
,测得 和
和 的物质的量随时间变化如图。请回答:
的物质的量随时间变化如图。请回答:

(1)下列措施能加快反应速率的是___________。
(2)0-2min 的反应速率为
的反应速率为___________ 。
(3)第9分钟时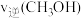
___________ (填“ ”“
”“ ”或“
”或“ ”)第3分钟时
”)第3分钟时 。
。
(4)恒容密闭条件下,能说明反应已达平衡状态的是___________。
(5)欲增大平衡时 的转化率,可采取的措施是
的转化率,可采取的措施是___________ 、___________ 。(任填2项)
(6)已知T℃下 的平衡常数
的平衡常数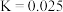 。保持容器温度不变,向1L的某密闭容器中充入
。保持容器温度不变,向1L的某密闭容器中充入 、
、 、
、 、
、 各1mol,反应一段时间后测得
各1mol,反应一段时间后测得 ,判断此时该可逆反应是否达到平衡,并说明理由(若末达到平衡需说明平衡移动方向)。
,判断此时该可逆反应是否达到平衡,并说明理由(若末达到平衡需说明平衡移动方向)。___________ 。
 的综合利用备受关注。
的综合利用备受关注。已知
 为放热反应,在固定容积为2.0L的密闭容器中充入0.8mol的
为放热反应,在固定容积为2.0L的密闭容器中充入0.8mol的 和2.4mol的
和2.4mol的 ,测得
,测得 和
和 的物质的量随时间变化如图。请回答:
的物质的量随时间变化如图。请回答:
(1)下列措施能加快反应速率的是___________。
A.往容器中充入 增大压强 增大压强 | B.及时分离出 |
| C.升高温度 | D.选择高效的催化剂 |
(2)0-2min
 的反应速率为
的反应速率为(3)第9分钟时
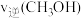
 ”“
”“ ”或“
”或“ ”)第3分钟时
”)第3分钟时 。
。(4)恒容密闭条件下,能说明反应已达平衡状态的是___________。
A.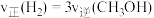 | B.混合气体的平均相对分子量不变 |
C.容器中 浓度与 浓度与 浓度之比为 浓度之比为 | D.混合气体的密度保持不变 |
(5)欲增大平衡时
 的转化率,可采取的措施是
的转化率,可采取的措施是(6)已知T℃下
 的平衡常数
的平衡常数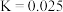 。保持容器温度不变,向1L的某密闭容器中充入
。保持容器温度不变,向1L的某密闭容器中充入 、
、 、
、 、
、 各1mol,反应一段时间后测得
各1mol,反应一段时间后测得 ,判断此时该可逆反应是否达到平衡,并说明理由(若末达到平衡需说明平衡移动方向)。
,判断此时该可逆反应是否达到平衡,并说明理由(若末达到平衡需说明平衡移动方向)。
您最近一年使用:0次
名校
解题方法
10 . 氨的用途十分广泛,如氨是制造硝酸和氮肥的重要原科。工业合成氨是人类科学技术的一项重大突破。回答下列问题:
(1)合成氨反应的历程和能量的变化如图所示,符号“·”可视为催化剂。________  。
。
(2)在不同条件下进行合成氨反应,下列反应速率由大到小的顺序是______ (填选项序号)。
①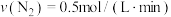 ②
②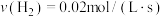
③ ④
④
(3)对于合成氨反应而言,只控制一个变量,下列图像合理的是___________(填选项字母)。
(4)一定温度下,向 恒容密闭容器中充入
恒容密闭容器中充入 、
、 发生反应,
发生反应, 的浓度随时间变化情况如表所示:
的浓度随时间变化情况如表所示:
 内,用
内,用 表示的平均反应速率为
表示的平均反应速率为_______ ;平衡常数
______ (结果保留一位小数);若维持温度不变,向另一 恒容密闭容器中充入
恒容密闭容器中充入 、
、 和
和 各
各 时,该反应的
时,该反应的
_____ (填 “>”“<”或“=”) 。
。
(1)合成氨反应的历程和能量的变化如图所示,符号“·”可视为催化剂。

 。
。(2)在不同条件下进行合成氨反应,下列反应速率由大到小的顺序是
①
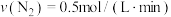 ②
②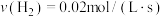
③
 ④
④
(3)对于合成氨反应而言,只控制一个变量,下列图像合理的是___________(填选项字母)。
A. | B. |
C. | D. |
(4)一定温度下,向
 恒容密闭容器中充入
恒容密闭容器中充入 、
、 发生反应,
发生反应, 的浓度随时间变化情况如表所示:
的浓度随时间变化情况如表所示:| 时间/min | 5 | 10 | 15 | 20 | 25 |
浓度/ | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 |
 内,用
内,用 表示的平均反应速率为
表示的平均反应速率为
 恒容密闭容器中充入
恒容密闭容器中充入 、
、 和
和 各
各 时,该反应的
时,该反应的
 。
。
您最近一年使用:0次



