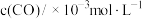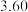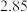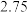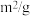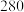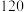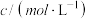名校
1 . 利用催化技术可将汽车尾气中的CO和NO转化为 和
和 ,化学方程式:
,化学方程式: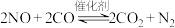 。
。
(1)某温度下,在恒容的密闭容器中通入CO和NO,测得不同时间CO的浓度如下表:
用CO的浓度变化表示0-2s的平均反应速率为______  。
。
(2)下列可说明反应达到平衡状态的是______ 。
a.CO的浓度不再改变
b.容器中的气体质量保持不变
c.NO、CO、 、
、 的浓度之比为2∶2∶2∶1
的浓度之比为2∶2∶2∶1
d.相同时间内,反应消耗2molNO同时消耗
(3)反应物初始浓度相同时,实验温度为280℃和360℃,进行以下实验:
【实验分析与结论】
①补全表格a.______ ,b.______ ,c.______ 。
②测得 ,对比实验Ⅰ、Ⅲ,可得结论:
,对比实验Ⅰ、Ⅲ,可得结论:______ 。
③通过实验可得到“温度相同时,增大催化剂的比表面积,可增大尾气的转化速率”的结论,证据是对比实验Ⅰ、Ⅱ,
______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
 和
和 ,化学方程式:
,化学方程式: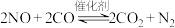 。
。(1)某温度下,在恒容的密闭容器中通入CO和NO,测得不同时间CO的浓度如下表:
时间 |
|
|
|
| …… |
|
|
|
|
| …… |
 。
。(2)下列可说明反应达到平衡状态的是
a.CO的浓度不再改变
b.容器中的气体质量保持不变
c.NO、CO、
 、
、 的浓度之比为2∶2∶2∶1
的浓度之比为2∶2∶2∶1d.相同时间内,反应消耗2molNO同时消耗

(3)反应物初始浓度相同时,实验温度为280℃和360℃,进行以下实验:
实验编号 | 实验目的 |
| 同种催化剂的比表面积 | 达平衡时所用的时间 |
Ⅰ | 对照实验 |
|
|
|
Ⅱ |
|
|
|
|
Ⅲ | 研究温度对尾气转化速率的影响 |
|
|
|
①补全表格a.
②测得
 ,对比实验Ⅰ、Ⅲ,可得结论:
,对比实验Ⅰ、Ⅲ,可得结论:③通过实验可得到“温度相同时,增大催化剂的比表面积,可增大尾气的转化速率”的结论,证据是对比实验Ⅰ、Ⅱ,

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
您最近一年使用:0次
2024-05-08更新
|
96次组卷
|
5卷引用:北京市第十四中学2022-2023学年高一下学期期中化学试题
北京市第十四中学2022-2023学年高一下学期期中化学试题北京市第三中学2022-2023学年高一下学期期中考试化学试题北京市西城区2020-2021学年高一下学期期末联考化学试题北京市第二十二中学2023-2024学年高一下学期期中考试化学试题(已下线)重难点02 速率与平衡综合题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)
2 . 历史上诺贝尔化学奖曾经3次颁给研究合成氨的化学家。合成氨的原理为  。回答下列问题。
。回答下列问题。
(1)t℃时,向填充有催化剂、体积为2L 的刚性容器中充入一定量的 和N2合成氨,实验中测得 c(NH3)随时间的变化如表所示:
和N2合成氨,实验中测得 c(NH3)随时间的变化如表所示:
5~15min内 N2的平均反应速率  =
=___________ 
下列情况能说明反应达到平衡状态的是________ (填标号)。
A.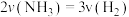 B. 混合气体的相对分子质量不再变化
B. 混合气体的相对分子质量不再变化
C. N2体积分数不再变化 D. 混合气体的密度保持不变
(2)如表列出了在不同温度和压强下,反应达到平衡时) 的百分含量
的百分含量  。
。
①从表中数据得出,最优的条件是___________ 。
②工业上通常选择在400~500℃和10~30MPa条件下合成氨, 原因是___________ 。
 。回答下列问题。
。回答下列问题。(1)t℃时,向填充有催化剂、体积为2L 的刚性容器中充入一定量的
 和N2合成氨,实验中测得 c(NH3)随时间的变化如表所示:
和N2合成氨,实验中测得 c(NH3)随时间的变化如表所示:| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol·L⁻¹ | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
 =
=
下列情况能说明反应达到平衡状态的是
A.
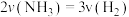 B. 混合气体的相对分子质量不再变化
B. 混合气体的相对分子质量不再变化C. N2体积分数不再变化 D. 混合气体的密度保持不变
(2)如表列出了在不同温度和压强下,反应达到平衡时)
 的百分含量
的百分含量  。
。压强/MPa 温度/℃ | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.5 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
②工业上通常选择在400~500℃和10~30MPa条件下合成氨, 原因是
您最近一年使用:0次
名校
解题方法
3 . 二氧化碳的捕集和转化是科学研究中的热点问题,我国科研人员提出了由 和
和 转化为
转化为 和
和 的反应历程,其示意图如图。
的反应历程,其示意图如图。
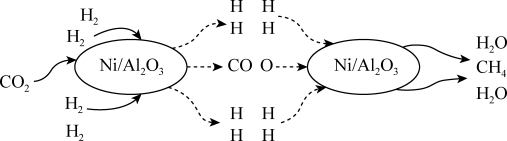
(1)根据信息可知该可逆反应的化学方程式为 ,催化剂
,催化剂
___________ (填“能”或“不能”) 提高平衡转化率。
提高平衡转化率。
(2)200℃下,在一密闭容器中充入一定量的 与
与 发生反应
发生反应 。一段时间后反应达平衡若其他条件不变,温度从200℃升至400℃,反应重新达到平衡时,
。一段时间后反应达平衡若其他条件不变,温度从200℃升至400℃,反应重新达到平衡时, 的体积分数增加。下列说法正确的是
的体积分数增加。下列说法正确的是___________ (填字母)。
a.该反应的 b.200℃下,减小
b.200℃下,减小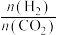 的值,
的值, 的平衡转化率升高
的平衡转化率升高
c.平衡常数大小:K(400℃)>K(200℃) d.反应达到平衡时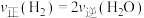
(3)一定条件下,反应体系中 平衡转化率
平衡转化率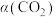 与L和X的关系如图所示,L和X表示温度或压强。
与L和X的关系如图所示,L和X表示温度或压强。
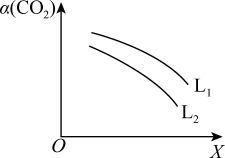
①L表示的物理量是___________ 。
②
___________  (填“<”或“>”),判断理由是
(填“<”或“>”),判断理由是___________ 。
(4)向1L恒容密闭容器中加入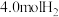 ,
,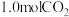 ,控制条件(催化剂、温度为
,控制条件(催化剂、温度为 )使之发生上述反应,测得容器内气体的压强随时间的变化如图所示:
)使之发生上述反应,测得容器内气体的压强随时间的变化如图所示:
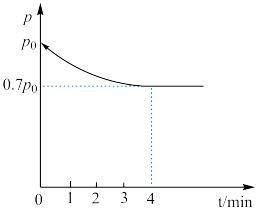
①求4min内 的反应速率
的反应速率
___________ 。
②此温度下,该反应的化学平衡常数
___________ 。
(5)下列情况,不能用勒夏特列原理解释的是___________ (填字母)。
a. 、
、 、HI平衡混合气体加压后颜色变深
、HI平衡混合气体加压后颜色变深
b.夏天,打开冰镇啤酒瓶,立即冒出大量泡沫
c.生活中,用饱和碳酸钠溶液洗去锅碗瓢盆上的油污,且热溶液的效果更好
d.在醋酸溶液中,加入一些醋酸钠固体使溶液的pH增大
 和
和 转化为
转化为 和
和 的反应历程,其示意图如图。
的反应历程,其示意图如图。
(1)根据信息可知该可逆反应的化学方程式为
 ,催化剂
,催化剂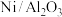
 提高平衡转化率。
提高平衡转化率。(2)200℃下,在一密闭容器中充入一定量的
 与
与 发生反应
发生反应 。一段时间后反应达平衡若其他条件不变,温度从200℃升至400℃,反应重新达到平衡时,
。一段时间后反应达平衡若其他条件不变,温度从200℃升至400℃,反应重新达到平衡时, 的体积分数增加。下列说法正确的是
的体积分数增加。下列说法正确的是a.该反应的
 b.200℃下,减小
b.200℃下,减小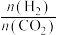 的值,
的值, 的平衡转化率升高
的平衡转化率升高c.平衡常数大小:K(400℃)>K(200℃) d.反应达到平衡时
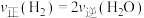
(3)一定条件下,反应体系中
 平衡转化率
平衡转化率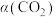 与L和X的关系如图所示,L和X表示温度或压强。
与L和X的关系如图所示,L和X表示温度或压强。
①L表示的物理量是
②

 (填“<”或“>”),判断理由是
(填“<”或“>”),判断理由是(4)向1L恒容密闭容器中加入
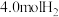 ,
,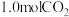 ,控制条件(催化剂、温度为
,控制条件(催化剂、温度为 )使之发生上述反应,测得容器内气体的压强随时间的变化如图所示:
)使之发生上述反应,测得容器内气体的压强随时间的变化如图所示:
①求4min内
 的反应速率
的反应速率②此温度下,该反应的化学平衡常数

(5)下列情况,不能用勒夏特列原理解释的是
a.
 、
、 、HI平衡混合气体加压后颜色变深
、HI平衡混合气体加压后颜色变深b.夏天,打开冰镇啤酒瓶,立即冒出大量泡沫
c.生活中,用饱和碳酸钠溶液洗去锅碗瓢盆上的油污,且热溶液的效果更好
d.在醋酸溶液中,加入一些醋酸钠固体使溶液的pH增大
您最近一年使用:0次
名校
4 . NO2的储存和还原技术能有效降低柴油发动机在空气过量时排放的NO2,原理如图1所示。用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,如图2所示。
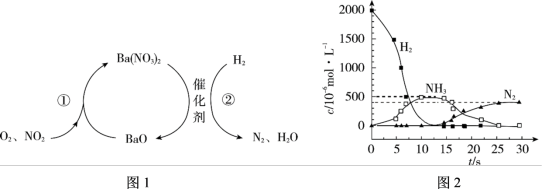
下列说法不正确 的是

下列说法
| A.反应①为4NO2 + O2 + 2BaO = 2Ba(NO3)2 |
| B.储存和还原技术也能降低尾气排放的NO |
| C.0~12.5 s内,氢气的消耗速率为v(H2) = 1.6 × 10﹣4 mol/(L·s) |
| D.反应②分两步进行, 第一步反应消耗的H2与Ba(NO3)2的物质的量之比是1∶8 |
您最近一年使用:0次
名校
解题方法
5 . 研究催化剂对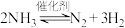 反应速率的影响。恒温恒容时,c(NH3)随时间的变化如下。
反应速率的影响。恒温恒容时,c(NH3)随时间的变化如下。
下列说法不正确 的是
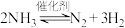 反应速率的影响。恒温恒容时,c(NH3)随时间的变化如下。
反应速率的影响。恒温恒容时,c(NH3)随时间的变化如下。| 时间/min 催化剂 c(NH3)/(×10−3 mol·L−1) | 0 | 20 | 40 | 60 | 80 |
| 催化剂Ⅰ | 2.40 | 2.00 | 1.60 | 1.20 | 0.80 |
| 催化剂Ⅱ | 2.40 | 1.60 | 0.80 | 0.40 | 0.40 |
| A.使用催化剂Ⅰ,0~20 min的平均反应速率v(N2)=1.00×10−5 mol·L−1·min−1 |
B.使用催化剂Ⅰ,达平衡后容器内的压强是初始时的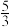 倍 倍 |
| C.相同条件下,使用催化剂Ⅱ可使该反应的活化能降低更多,反应更快 |
| D.相同条件下,使用催化剂Ⅱ不会使该反应的化学平衡常数更大 |
您最近一年使用:0次
解题方法
6 . 人工合成氨反应:N2(g)+3H2(g) 2NH3(g) ∆H<0,在5L密闭容器中进行此反应,30秒后NH3的物质的量增加了0.3mol。下列说法
2NH3(g) ∆H<0,在5L密闭容器中进行此反应,30秒后NH3的物质的量增加了0.3mol。下列说法不正确 的是
 2NH3(g) ∆H<0,在5L密闭容器中进行此反应,30秒后NH3的物质的量增加了0.3mol。下列说法
2NH3(g) ∆H<0,在5L密闭容器中进行此反应,30秒后NH3的物质的量增加了0.3mol。下列说法| A.30秒内v(N2)=0.001mol·L-1·s-1 |
| B.当容器内气体压强不再变化时,反应达到平衡 |
| C.其他条件不变,升高温度能加快反应速率,但降低N2的平衡转化率 |
| D.其他条件不变,使用催化剂能同时提高反应速率和该反应的平衡常数 |
您最近一年使用:0次
7 . 某温度时,H2(g)+CO2(g) H2O(g) + CO(g) K=1.该温度下,在甲、乙、丙、丁四个恒容密闭容器中,投入H2和CO2,起始浓度如下:
H2O(g) + CO(g) K=1.该温度下,在甲、乙、丙、丁四个恒容密闭容器中,投入H2和CO2,起始浓度如下:
5 min时达到平衡。平衡时,下列推断不正确的是
 H2O(g) + CO(g) K=1.该温度下,在甲、乙、丙、丁四个恒容密闭容器中,投入H2和CO2,起始浓度如下:
H2O(g) + CO(g) K=1.该温度下,在甲、乙、丙、丁四个恒容密闭容器中,投入H2和CO2,起始浓度如下:| 起始浓度 | 甲 | 乙 | 丙 | 丁 |
| c(H2)/(mol/L) | 0.10 | 0.10 | 0.20 | 0.20 |
| c(CO2)/(mol/L) | 0.10 | 0.20 | 0.10 | 0.20 |
| A.5min时,甲中v(CO2)=0.01 mol/(L·mn) | B.乙中CO2转化率等于丙中H2转化率 |
| C.丁中各物质的物质的量相等 | D.甲、乙、丁中c(H2)关系为甲<乙<丁 |
您最近一年使用:0次
8 . 二甲醚(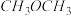 )是一种洁净液体燃料,工业上以CO和H2为原料生产
)是一种洁净液体燃料,工业上以CO和H2为原料生产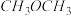 。工业制备二甲醚在催化反应室中(压强:2.0~10.0 MIPa.温度:230-280℃)
。工业制备二甲醚在催化反应室中(压强:2.0~10.0 MIPa.温度:230-280℃)
进行下列反应:
反应i: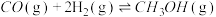
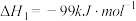
反应ii: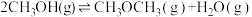
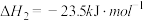
反应iii:
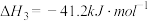
(1)在该条件下,若反应i的起始浓度分别为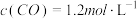 ,
,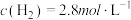 ,8min后达到化学平衡状态,CO的转化率为50%,则8min内CO的平均反应速率为
,8min后达到化学平衡状态,CO的转化率为50%,则8min内CO的平均反应速率为______
(2)在t℃时.反应ii的平衡常数为400,此温度下,在1L的密闭容器中加入一定的甲醇,反应到某时刻测得各组分的物质的量浓度如下:
此时
______  (填“>”“<”或“=”)
(填“>”“<”或“=”)
(3)催化总反应为: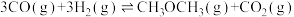

①
______ 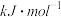
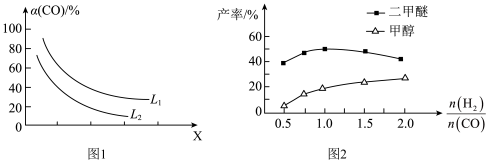
②CO的平衡转化率 (CO)与温度、压强的关系如图I所示.图中X代表
(CO)与温度、压强的关系如图I所示.图中X代表______ (填“温度”或“压强”),
______  (填“>”“<”或“=)。
(填“>”“<”或“=)。
(4)在催化剂的作用下同时进行三个反应,发现随着起始投料比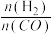 的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图2的变化趋势。解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因
的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图2的变化趋势。解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因______ 。
(5)二甲醚( )空气燃料电池是一种高效、轻污染的车载电池,其工作原理如图3所示。
)空气燃料电池是一种高效、轻污染的车载电池,其工作原理如图3所示。
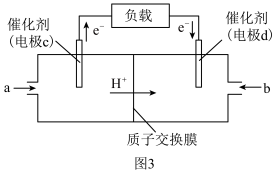
①燃料电池中的正极是______ (填“c”或“d”)电极。
②c电极的电极反应为______ 。
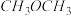 )是一种洁净液体燃料,工业上以CO和H2为原料生产
)是一种洁净液体燃料,工业上以CO和H2为原料生产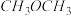 。工业制备二甲醚在催化反应室中(压强:2.0~10.0 MIPa.温度:230-280℃)
。工业制备二甲醚在催化反应室中(压强:2.0~10.0 MIPa.温度:230-280℃)进行下列反应:
反应i:
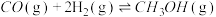
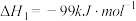
反应ii:
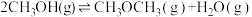
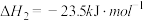
反应iii:

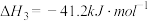
(1)在该条件下,若反应i的起始浓度分别为
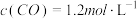 ,
,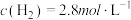 ,8min后达到化学平衡状态,CO的转化率为50%,则8min内CO的平均反应速率为
,8min后达到化学平衡状态,CO的转化率为50%,则8min内CO的平均反应速率为(2)在t℃时.反应ii的平衡常数为400,此温度下,在1L的密闭容器中加入一定的甲醇,反应到某时刻测得各组分的物质的量浓度如下:
物质 |
|
|
|
| 0.05 | 2.0 | 2.0 |

 (填“>”“<”或“=”)
(填“>”“<”或“=”)(3)催化总反应为:
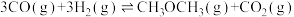

①

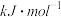
②CO的平衡转化率
 (CO)与温度、压强的关系如图I所示.图中X代表
(CO)与温度、压强的关系如图I所示.图中X代表
 (填“>”“<”或“=)。
(填“>”“<”或“=)。
(4)在催化剂的作用下同时进行三个反应,发现随着起始投料比
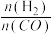 的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图2的变化趋势。解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因
的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图2的变化趋势。解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因(5)二甲醚(
 )空气燃料电池是一种高效、轻污染的车载电池,其工作原理如图3所示。
)空气燃料电池是一种高效、轻污染的车载电池,其工作原理如图3所示。
①燃料电池中的正极是
②c电极的电极反应为
您最近一年使用:0次
2024-01-24更新
|
192次组卷
|
2卷引用:北京市顺义区2023-2024学年高二上学期期末质量监测化学试题
名校
9 . 向体积为10L的恒容密闭容器中通入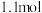
 和
和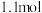
 制备
制备 ,反应原理为
,反应原理为 (
( )。在不同温度(
)。在不同温度(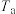 、
、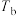 )下测得容器中
)下测得容器中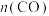 随时间的变化曲线如下图所示。
随时间的变化曲线如下图所示。
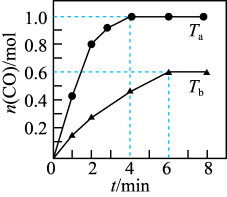
下列说法正确的是
 和
和
 制备
制备 ,反应原理为
,反应原理为 (
( )。在不同温度(
)。在不同温度(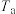 、
、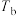 )下测得容器中
)下测得容器中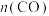 随时间的变化曲线如下图所示。
随时间的变化曲线如下图所示。
下列说法正确的是
A.温度 |
B.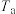 时, 时, 的平衡转化率 的平衡转化率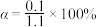 |
C.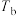 时,加入催化剂,可缩短达平衡的时间并增大平衡时 时,加入催化剂,可缩短达平衡的时间并增大平衡时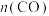 |
D.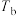 时,若改为恒温恒压容器,平衡时 时,若改为恒温恒压容器,平衡时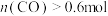 |
您最近一年使用:0次
10 . NH3经一系列反应可以得到HNO3,如下图所示。
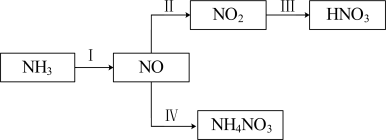
(1)I中,NH3和O2在催化剂作用下反应,其化学方程式是________ 。
(2)Ⅱ中,2NO(g)+O2 2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。
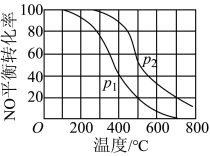
①比较P1、P2的大小关系:______ 。
②随温度升高,该反应平衡常数变化的趋势是______ 。(填“增大”、“减小”或“不变”)
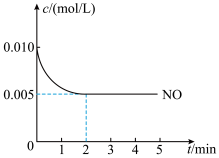
③2NO(g)+O2 2NO2(g)是制造硝酸的重要反应之一、在800℃时,向容积为1L的密闭容器中充入0.010mol NO和0.005molO2,反应过程中NO的浓度随时间变化如下图所示。
2NO2(g)是制造硝酸的重要反应之一、在800℃时,向容积为1L的密闭容器中充入0.010mol NO和0.005molO2,反应过程中NO的浓度随时间变化如下图所示。
a.2min内,v(O2)=________ mol/(L·min)。
b.800℃时,该反应的化学平衡常数为_______ 。
(3)Ⅲ中,降低温度,将NO2(g)转化为N2O4(l),再制备浓硝酸。
①已知:2NO2 (g) N2O4(g) △H1;2NO2 (g)
N2O4(g) △H1;2NO2 (g) N2O2 (l) △H2;下列能量变化示意图中,正确的是(选填字母)
N2O2 (l) △H2;下列能量变化示意图中,正确的是(选填字母) ____ 。
A. B.
B.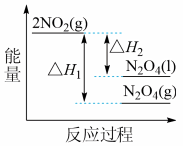 C.
C.
②N2O4与O2、H2O化合的化学方程式是____ 。
(4)Ⅳ中,电解NO制备NH4NO3,其工作原理如图所示:
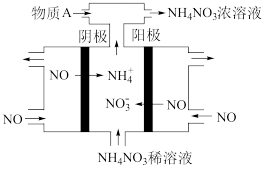
①阳极反应方程式为:___________
②为使电解产物全部转化为NH4NO3,需补充物质A,A是____ 。

(1)I中,NH3和O2在催化剂作用下反应,其化学方程式是
(2)Ⅱ中,2NO(g)+O2
 2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。
①比较P1、P2的大小关系:
②随温度升高,该反应平衡常数变化的趋势是
③2NO(g)+O2
 2NO2(g)是制造硝酸的重要反应之一、在800℃时,向容积为1L的密闭容器中充入0.010mol NO和0.005molO2,反应过程中NO的浓度随时间变化如下图所示。
2NO2(g)是制造硝酸的重要反应之一、在800℃时,向容积为1L的密闭容器中充入0.010mol NO和0.005molO2,反应过程中NO的浓度随时间变化如下图所示。a.2min内,v(O2)=
b.800℃时,该反应的化学平衡常数为

(3)Ⅲ中,降低温度,将NO2(g)转化为N2O4(l),再制备浓硝酸。
①已知:2NO2 (g)
 N2O4(g) △H1;2NO2 (g)
N2O4(g) △H1;2NO2 (g) N2O2 (l) △H2;下列能量变化示意图中,正确的是(选填字母)
N2O2 (l) △H2;下列能量变化示意图中,正确的是(选填字母) A.
 B.
B. C.
C.
②N2O4与O2、H2O化合的化学方程式是
(4)Ⅳ中,电解NO制备NH4NO3,其工作原理如图所示:

①阳极反应方程式为:
②为使电解产物全部转化为NH4NO3,需补充物质A,A是
您最近一年使用:0次