名校
解题方法
1 . 已知CaCO3和盐酸反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,下列措施中可使生成CO2的速率加快的是(不考虑CaCO3与盐酸接触面积改变的影响)
| A.增加CaCO3的量 |
| B.增加盐酸的浓度 |
| C.增加盐酸的量 |
| D.减小CaCl2的浓度 |
您最近一年使用:0次
2023-07-05更新
|
448次组卷
|
11卷引用:【全国百强校】宁夏回族自治区银川一中2018-2019学年高一下学期期中考试化学试题
【全国百强校】宁夏回族自治区银川一中2018-2019学年高一下学期期中考试化学试题四川省广安市岳池县顾县中学2019—2020学年第一学期高二上学期期中测试化学(选修四)试题吉林省汪清县第六中学2016-2017学年高一下学期第二次月考化学试题河北省唐山市开滦第二中学2016-2017学年高二下学期期末考试化学试题人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 第一节 化学反应速率 课时2 影响化学反应速率的因素专题2 第一单元 第2课时 物质的检验 物质性质和变化的探究-高中化学苏教2019版必修第一册海南省三亚华侨学校(南新校区)2021-2022学年高二上学期10月月考化学试题 (已下线)第11讲 物质的性质和变化探究-【暑假自学课】2023年新高一暑假精品课(苏教版2019)江西省吉安市吉州区部分学校联考2022-2023学年高一下学期7月期末考试化学试题云南省大理白族自治州民族中学2022-2023学年高二下学期开学考试化学试题(已下线)6.2.1化学反应的速率-随堂练习
名校
2 . 向绝热恒容密闭容器中通入 和
和 ,在一定条件下发生反应
,在一定条件下发生反应 ,正反应速率随时间变化的示意图如下图,下列结论中正确的个数为
,正反应速率随时间变化的示意图如下图,下列结论中正确的个数为
② 浓度:a点大于c点
浓度:a点大于c点
③反应物的总能量高于生成物的总能量
④逆反应速率图像在此时间段内和上图趋势相同
⑤混合物颜色不再变化,说明反应达到平衡
⑥达到平衡后,改变容器体积增大压强,逆反应速率可能先增大后减小
 和
和 ,在一定条件下发生反应
,在一定条件下发生反应 ,正反应速率随时间变化的示意图如下图,下列结论中正确的个数为
,正反应速率随时间变化的示意图如下图,下列结论中正确的个数为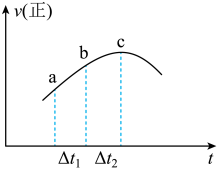
②
 浓度:a点大于c点
浓度:a点大于c点③反应物的总能量高于生成物的总能量
④逆反应速率图像在此时间段内和上图趋势相同
⑤混合物颜色不再变化,说明反应达到平衡
⑥达到平衡后,改变容器体积增大压强,逆反应速率可能先增大后减小
| A.2个 | B.3个 | C.4个 | D.5个 |
您最近一年使用:0次
2023-06-01更新
|
491次组卷
|
4卷引用:宁夏石嘴山市第三中学2023-2024学年高一下学期4月期中考试化学试题
名校
3 . 用0.1mol•L-1稀盐酸与锌反应制取氢气,不能使氢气生成速率增大的是
| A.对该反应体系加热 | B.不用锌片,改用锌粉 |
| C.加入少量NaCl溶液 | D.加入少量2mol•L-1硫酸 |
您最近一年使用:0次
名校
4 . 在一定条件下,可逆反应X(g)+3Y(g) 2Z(g)达到平衡时,测得X和Y转化的转化率均为25%,下列叙述正确的是
2Z(g)达到平衡时,测得X和Y转化的转化率均为25%,下列叙述正确的是
 2Z(g)达到平衡时,测得X和Y转化的转化率均为25%,下列叙述正确的是
2Z(g)达到平衡时,测得X和Y转化的转化率均为25%,下列叙述正确的是| A.升高温度,正反应速率增大,逆反应速率减小 |
| B.开始充入容器中的X、Y物质的量之比为1∶3 |
| C.若Y的反应速率为0.2 mol·L-1·s-1,则Z的反应速率为0.3 mol·L-1·s-1 |
| D.若容器体积不变,向容器中充入氦气,压强增大,反应速率增大 |
您最近一年使用:0次
2023-05-11更新
|
483次组卷
|
3卷引用:宁夏六盘山高级中学2023-2024学年高二上学期期中考试化学试题
名校
5 . 定条件下,发生反应A(g)+B(g) C(g) △H>0,达到平衡后根据下列图像判断:
C(g) △H>0,达到平衡后根据下列图像判断:
A.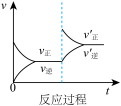 B.
B.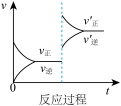 C.
C. D.
D.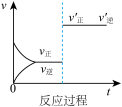 E.
E.
(1)表示升高温度,达到新平衡的是图______ (填“A”、“B”、“C”、“D”或“E”,下同),新平衡中C的质量分数______ (填“增大”、“减小”或“不变”,下同)。
(2)表示降低压强,达到新平衡的是图______ ,A的转化率______ 。
(3)表示减少C的浓度,达到新平衡的是图______ ,表示使用催化剂,达新平衡的是图。
(4)增加A的浓度,达到新平衡的是图______ ,达到平衡后A的转化率______ 。
 C(g) △H>0,达到平衡后根据下列图像判断:
C(g) △H>0,达到平衡后根据下列图像判断:A.
 B.
B. C.
C. D.
D. E.
E.
(1)表示升高温度,达到新平衡的是图
(2)表示降低压强,达到新平衡的是图
(3)表示减少C的浓度,达到新平衡的是图
(4)增加A的浓度,达到新平衡的是图
您最近一年使用:0次
2023-04-24更新
|
266次组卷
|
2卷引用:宁夏青铜峡市宁朔中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
6 . 把在空气中久置的铝片5.0g投入盛有50mL0.1mol/L盐酸的烧杯中,该铝片与盐酸反应,产生氢气的速率v(H2)与反应时间t的关系可用如图所示的坐标曲线来表示,下列推论不正确的是
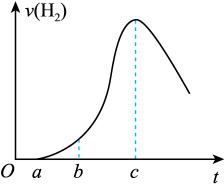

| A.O→a不产生氢气是因为表面的氧化物隔离了铝和稀盐酸 |
| B.b→c段产生氢气的速率增加较快的主要原因之一是温度升高 |
| C.t=c时,反应处于平衡状态 |
| D.t>c时,产生氢气的速率降低的主要原因是溶液中H+浓度下降 |
您最近一年使用:0次
2023-04-22更新
|
391次组卷
|
7卷引用:宁夏银川市育才中学2022-2023学年高一下学期5月期中考试化学试题
名校
解题方法
7 . 某化学研究小组探究外界条件对化学反应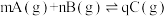 的速率和平衡的影响,如图所示,下列判断错误的是
的速率和平衡的影响,如图所示,下列判断错误的是
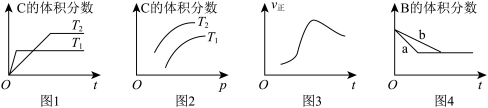
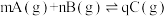 的速率和平衡的影响,如图所示,下列判断错误的是
的速率和平衡的影响,如图所示,下列判断错误的是
A.由图1可知, ,该反应的正反应为放热反应 ,该反应的正反应为放热反应 |
B.由图2可知,该反应的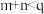 |
| C.图3是绝热条件下正反应速率和时间的图像(从反应物开始投料),由此说明该反应放热 |
| D.图4中,曲线a可能使用了催化剂 |
您最近一年使用:0次
2023-04-01更新
|
462次组卷
|
3卷引用:宁夏青铜峡市宁朔中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
8 . 中医药根植于中华传统文化。下列说法不正确 的是
| A.屠呦呦团队用乙醚从青蒿中提取了青蒿素,采用了萃取的方法 |
| B.中药甘草、金银花、石膏、明矾等的主要化学成分都是有机物 |
| C.汤药存放于冰箱中,可以减小其腐败变质的速率 |
| D.煎制草药不宜使用铁质容器,可能因为草药的有些成分能与铁发生反应影响药效 |
您最近一年使用:0次
2023-03-31更新
|
935次组卷
|
6卷引用:宁夏平罗中学2022-2023学年高二下学期期中考试化学试题
宁夏平罗中学2022-2023学年高二下学期期中考试化学试题北京市西城区2023届一模考试化学试题(已下线)专题01 化学与STSE(已下线)专题05 元素及其化合物北京师范大学附属实验中学2023-2024学年暑期高三第一次督导化学试题广西柳州高级中学2023-2024学年高三上学期8月开学考试化学试题
名校
解题方法
9 . 为保护环境,充分利用钴资源,一种以废旧钴酸锂电池材料(正极材料主要含有LiCoO2、铝箔及金属钢壳)回收钴酸锂的工艺流程如下:
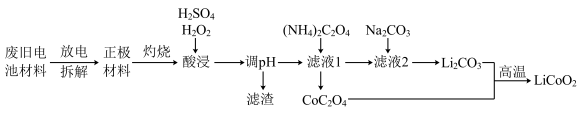
已知一定条件下,部分金属阳离子形成氢氧化物的pH如下表:
请回答下列问题:
(1)废旧钴酸锂电池需经放电、拆解、粉碎预处理。放电方式为电化学放电,可以将废旧电池浸泡在_________ (填标号)中进行放电。粉碎的目的是_________ 。
A. Na2SO4溶液
B.98%的H2SO4溶液
C.酒精
(2)“酸浸”过程中,除加入H2SO4,还要加入H2O2。
①H2O2的作用是_________ (填标号)。
A.做氧化剂
B.做还原剂
C.既做氧化剂又做还原剂
②H2O2促进了LiCoO2在H2SO4中转化为CoSO4,该反应的离子方程式为_________ 。
③相同条件下,“酸浸”时钴的浸出率随温度变化如右图所示,此时温度控制在80°C左右的原因为_________ 。

(3)“调pH”时,溶液应控制的pH范围为_________ ,选用的最佳试剂是_________ (填标号)。
A. H2SO4 B. CoCO3 C.石灰乳 D. NaOH
(4)高温时,CoC2O4和Li2CO3生成LiCoO2的同时放出CO2。此反应的化学方程式为_________ 。

已知一定条件下,部分金属阳离子形成氢氧化物的pH如下表:
| 离子 | Co3+ | Fe3+ | Co2+ | Fe2+ | Al3+ |
| 开始沉淀的pH | 0.3 | 2.7 | 7.2 | 7.6 | 3.6 |
| 完全沉淀的pH | 1.1 | 3.2 | 9.2 | 9.6 | 5.2 |
(1)废旧钴酸锂电池需经放电、拆解、粉碎预处理。放电方式为电化学放电,可以将废旧电池浸泡在
A. Na2SO4溶液
B.98%的H2SO4溶液
C.酒精
(2)“酸浸”过程中,除加入H2SO4,还要加入H2O2。
①H2O2的作用是
A.做氧化剂
B.做还原剂
C.既做氧化剂又做还原剂
②H2O2促进了LiCoO2在H2SO4中转化为CoSO4,该反应的离子方程式为
③相同条件下,“酸浸”时钴的浸出率随温度变化如右图所示,此时温度控制在80°C左右的原因为

(3)“调pH”时,溶液应控制的pH范围为
A. H2SO4 B. CoCO3 C.石灰乳 D. NaOH
(4)高温时,CoC2O4和Li2CO3生成LiCoO2的同时放出CO2。此反应的化学方程式为
您最近一年使用:0次
2023-03-29更新
|
334次组卷
|
2卷引用:宁夏平罗中学2022-2023学年高二下学期期中考试化学试题(重点班)
名校
10 . 近年来光催化处理船舶尾气技术被称为是一种“绿色友好”技术,以 半导体为基底的纳米催化剂,表面经光激发后产生空穴和光生电子,光生空穴被表面吸附水或氢氧根离子捕获生成
半导体为基底的纳米催化剂,表面经光激发后产生空穴和光生电子,光生空穴被表面吸附水或氢氧根离子捕获生成 自由基,光生电子则与
自由基,光生电子则与 等反应在催化剂表面生成
等反应在催化剂表面生成 、
、 等氧化物,这些氧化物作用于尾气中的
等氧化物,这些氧化物作用于尾气中的 、
、 等污染物并将其氧化降解,原理见图。下列说法错误的是
等污染物并将其氧化降解,原理见图。下列说法错误的是
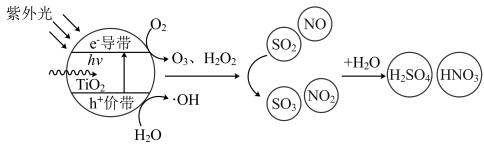
 半导体为基底的纳米催化剂,表面经光激发后产生空穴和光生电子,光生空穴被表面吸附水或氢氧根离子捕获生成
半导体为基底的纳米催化剂,表面经光激发后产生空穴和光生电子,光生空穴被表面吸附水或氢氧根离子捕获生成 自由基,光生电子则与
自由基,光生电子则与 等反应在催化剂表面生成
等反应在催化剂表面生成 、
、 等氧化物,这些氧化物作用于尾气中的
等氧化物,这些氧化物作用于尾气中的 、
、 等污染物并将其氧化降解,原理见图。下列说法错误的是
等污染物并将其氧化降解,原理见图。下列说法错误的是
A.含有氮氧化物、硫氧化物的尾气排放到大气中易形成酸雨, 小于7的雨水为酸雨 小于7的雨水为酸雨 |
B.除 、NO的总反应分别为 、NO的总反应分别为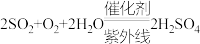 、 、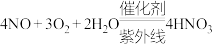 |
| C.催化剂可以改变氮氧化物、硫氧化物被氧化的速率 |
| D.尾气中含有大量有害物质,但经过科学的处理可以转化为多种有实用价值的物质 |
您最近一年使用:0次
2023-03-25更新
|
413次组卷
|
4卷引用:宁夏回族自治区银川一中2022-2023学年高一下学期期中考试化学试题



