名校
1 .  和
和 在催化剂表面合成氨的微观历程及能量变化的示意图如下,用
在催化剂表面合成氨的微观历程及能量变化的示意图如下,用 、
、 、
、 分别表示
分别表示 、
、 、
、 ,已知:
,已知: ,反应释放热量,下列说法正确的是
,反应释放热量,下列说法正确的是

| A.合成氨反应中,反应物断键吸收能量小于生成物形成新键释放的能量 |
B.②→③过程,是吸热过程且只有 键的断裂 键的断裂 |
C.③→④过程,N原子和H原子形成了含有非极性键的 |
D.使用催化剂,对生成 的速率没有影响 的速率没有影响 |
您最近半年使用:0次
解题方法
2 . 水气变换反应(CO+H2O H2+CO2)是工业上大规模制氢的重要方法,HCOOH是中间产物。在密封石英管内完全充满1 mol·L-1 HCOOH水溶液,某温度下HCOOH分解,反应如下。
H2+CO2)是工业上大规模制氢的重要方法,HCOOH是中间产物。在密封石英管内完全充满1 mol·L-1 HCOOH水溶液,某温度下HCOOH分解,反应如下。
i.HCOOH(aq) CO(aq) + H2O(l)
CO(aq) + H2O(l)
ii.HCOOH(aq) CO2(aq) + H2(aq)
CO2(aq) + H2(aq)
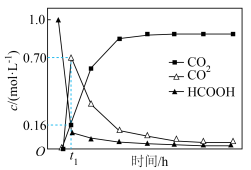
含碳粒子浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。
下列说法不正确 的是
 H2+CO2)是工业上大规模制氢的重要方法,HCOOH是中间产物。在密封石英管内完全充满1 mol·L-1 HCOOH水溶液,某温度下HCOOH分解,反应如下。
H2+CO2)是工业上大规模制氢的重要方法,HCOOH是中间产物。在密封石英管内完全充满1 mol·L-1 HCOOH水溶液,某温度下HCOOH分解,反应如下。i.HCOOH(aq)
 CO(aq) + H2O(l)
CO(aq) + H2O(l)ii.HCOOH(aq)
 CO2(aq) + H2(aq)
CO2(aq) + H2(aq)含碳粒子浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。
下列说法
| A.反应开始至t1,反应速率:i > ii |
| B.t1时,HCOOH的分解率为86% |
| C.相同条件下,若起始时溶液中同时还含有0.1 mol·L-1 盐酸,c(CO)的最大值将变大 |
| D.相同条件下,若起始时溶液中同时还含有0.1 mol·L-1 盐酸,c(CO2)的最大值将变小 |
您最近半年使用:0次
3 . 在催化剂作用下, 分解生成
分解生成 和
和 可能的反应机理如下图所示。
可能的反应机理如下图所示。
 分解生成
分解生成 和
和 可能的反应机理如下图所示。
可能的反应机理如下图所示。
| A.催化剂能降低反应的活化能 |
| B.第一步转化中N与H间形成的化学键是配位键 |
| C.第三步转化涉及极性键的断裂与非极性键的生成 |
D.若用 HCOOD代替 HCOOD代替 ,反应除生成 ,反应除生成 外,还生成 外,还生成 |
您最近半年使用:0次
4 . 我国科学家研发的“液态阳光”计划是:通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢制备甲醇。
主反应: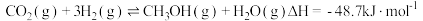
副反应:
将 和
和 按物质的量比
按物质的量比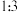 混合,以固定流速通过盛放
混合,以固定流速通过盛放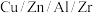 催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。下列说法
催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。下列说法不正确 的是
已知: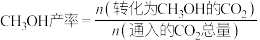
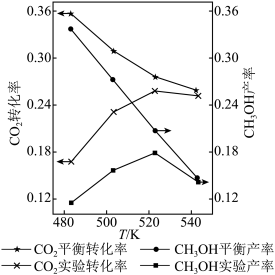
主反应:
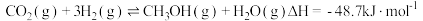
副反应:

将
 和
和 按物质的量比
按物质的量比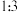 混合,以固定流速通过盛放
混合,以固定流速通过盛放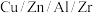 催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。下列说法
催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。下列说法已知:
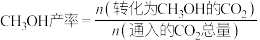

A.由图可知,催化剂活性最好的温度大约在 |
B. 升温到 升温到 ,主反应的反应速率受温度影响更大 ,主反应的反应速率受温度影响更大 |
C.为了提高 的平衡转化率和 的平衡转化率和 的平衡产率,可以选择低温、高压条件 的平衡产率,可以选择低温、高压条件 |
D.温度由 升到 升到 的实验产率降低的原因可能是:温度升高,主反应逆移程度大于副反应正移程度 的实验产率降低的原因可能是:温度升高,主反应逆移程度大于副反应正移程度 |
您最近半年使用:0次
解题方法
5 . 工业上常利用乙苯催化脱氢制备苯乙烯,发生的主反应是:
Ⅰ.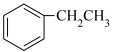 (g)
(g)
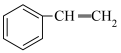 (g)+H2(g) ∆H=+117.6kJ/mol
(g)+H2(g) ∆H=+117.6kJ/mol
同时有副反应发生:
Ⅱ. (g)+H2(g)
(g)+H2(g)
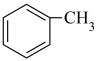 (g)+CH4(g) ∆H=-64.5kJ/mol
(g)+CH4(g) ∆H=-64.5kJ/mol
Ⅲ. (g)
(g) 8C(s)+5H2(g) ∆H=-1.67kJ/mol
8C(s)+5H2(g) ∆H=-1.67kJ/mol
某实验将乙苯和水蒸气混合,以恒定流速通入反应器,经过相同时间,测得乙苯的转化率,苯乙烯的选择性随温度、水蒸气与乙苯质量比的变化关系分别如图1、图2。

资料:苯乙烯的选择性是指生成苯乙烯的物质的量与消耗的乙苯的物质的量的比值。
下列说法不正确 的是
Ⅰ.
 (g)
(g)
 (g)+H2(g) ∆H=+117.6kJ/mol
(g)+H2(g) ∆H=+117.6kJ/mol同时有副反应发生:
Ⅱ.
 (g)+H2(g)
(g)+H2(g)
 (g)+CH4(g) ∆H=-64.5kJ/mol
(g)+CH4(g) ∆H=-64.5kJ/molⅢ.
 (g)
(g) 8C(s)+5H2(g) ∆H=-1.67kJ/mol
8C(s)+5H2(g) ∆H=-1.67kJ/mol某实验将乙苯和水蒸气混合,以恒定流速通入反应器,经过相同时间,测得乙苯的转化率,苯乙烯的选择性随温度、水蒸气与乙苯质量比的变化关系分别如图1、图2。

资料:苯乙烯的选择性是指生成苯乙烯的物质的量与消耗的乙苯的物质的量的比值。
下列说法
| A.从平衡角度分析,高温和低压有利于苯乙烯的制备 |
| B.随温度升高,副反应速率增大的程度比主反应的小 |
| C.乙苯中加入水蒸气,有利于催化剂表面积碳的消除 |
| D.本实验选择水蒸气与乙苯质量比为2:1、反应温度为620℃,是综合考虑乙苯转化率、苯乙烯选择性及能耗等工业实际 |
您最近半年使用:0次
名校
6 . 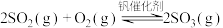
 。当
。当 、
、 和
和 按一定比例混合时,
按一定比例混合时, 平衡转化率
平衡转化率 随温度、压强的变化如下图所示。
随温度、压强的变化如下图所示。
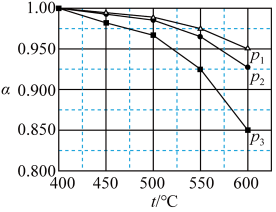
下列说法不正确 的是
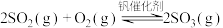
 。当
。当 、
、 和
和 按一定比例混合时,
按一定比例混合时, 平衡转化率
平衡转化率 随温度、压强的变化如下图所示。
随温度、压强的变化如下图所示。
下列说法
A. |
B.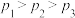 |
| C.钒催化剂能降低反应的活化能,提高反应速率 |
| D.增大压强平衡正向移动,反应平衡常数增大 |
您最近半年使用:0次
名校
7 . 已知H-H的键能为 ,I-I的键能为
,I-I的键能为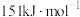 。反应
。反应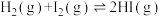 经历了如下反应历程:
经历了如下反应历程:
① ,②
,②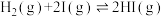 ,反应过程的能量变化如图所示。
,反应过程的能量变化如图所示。

下列说法不正确 的是
 ,I-I的键能为
,I-I的键能为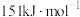 。反应
。反应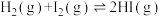 经历了如下反应历程:
经历了如下反应历程:①
 ,②
,②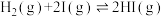 ,反应过程的能量变化如图所示。
,反应过程的能量变化如图所示。
下列说法
A.H-I的键能为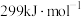 |
| B.升高温度,反应①和反应②的速率均增大 |
C.升高温度,反应②的限度增大,有利于提高 的转化率 的转化率 |
D.为防止反应过程中有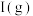 大量累积,应选择合适的催化剂降低反应②的活化能 大量累积,应选择合适的催化剂降低反应②的活化能 |
您最近半年使用:0次
名校
8 . 化学家格哈德·埃特尔证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意图如下:

下列关于合成氨反应的叙述中不正确 的是

下列关于合成氨反应的叙述中
| A.常温下该反应难以进行,是因为常温下生成物的化学键难以形成 |
| B.该过程表明,在化学反应中存在化学键的断裂与形成 |
| C.在催化剂的作用下,反应物的化学键变得容易断裂 |
| D.过程②需吸收能量,过程③则放出能量 |
您最近半年使用:0次
名校
9 . 乙烯和氧气在Ag催化下生成环氧乙烷(EO)和乙醛(AA)的机理如下图所示。吸附在催化剂表面的粒子用*标注,TS表示过渡态(TS2和TS3的能量相差不大)。
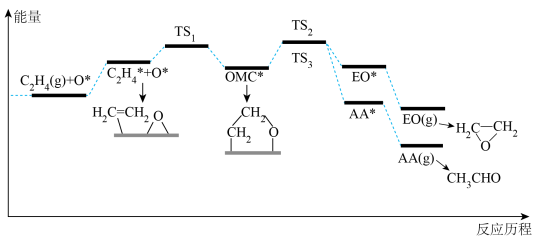
注: 表示Ag催化剂表面
表示Ag催化剂表面
下列说法不正确 的是

注:
 表示Ag催化剂表面
表示Ag催化剂表面下列说法
| A.C2H4(g)吸附在催化剂表面的过程需要吸收能量 |
| B.OMC*→EO(g)和OMC*→AA(g)的过程中均形成了碳氧σ键 |
| C.测得平衡产率:AA>EO,其主要原因是AA比EO更稳定 |
D.EO(g) AA(g)的平衡常数随温度升高而降低 AA(g)的平衡常数随温度升高而降低 |
您最近半年使用:0次
2024-02-23更新
|
183次组卷
|
3卷引用:北京师范大学附属中学2023-2024学年高三下学期开学考化学试题
名校
解题方法
10 . 我国是世界上最早冶炼锌的国家之一,有独立的炼锌发展史。现代炼锌主要采取湿法工艺,以闪锌矿(主要成分为 ,还含铁等元素)、软锰矿(主要成分为
,还含铁等元素)、软锰矿(主要成分为 )为原料联合生产锌和高纯度二氧化锰的一种流程如下:
)为原料联合生产锌和高纯度二氧化锰的一种流程如下:
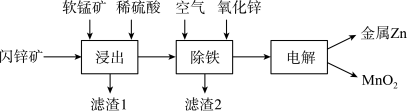
(1)浸出:加入 能促进
能促进 的溶解,提高锌的浸出率,同时生成硫单质。
的溶解,提高锌的浸出率,同时生成硫单质。 的作用类似催化剂,“催化”过程可表示为:
的作用类似催化剂,“催化”过程可表示为:
ⅰ:
ⅱ:……
①写出ⅱ的离子方程式:_______ 。
②下列实验方案可证实上述“催化”过程。将实验方案补充完整。
a.向酸化的 溶液中加入
溶液中加入 溶液,溶液几乎无色,再加入少量
溶液,溶液几乎无色,再加入少量 ,溶液变红。
,溶液变红。
b._______ 。
(2)除铁:已知①进入除铁工艺的溶液的pH约为3;②控制溶液pH为2.5~3.5,使铁主要以 沉淀的形式除去。结合离子方程式说明,通入空气需同时补充适量
沉淀的形式除去。结合离子方程式说明,通入空气需同时补充适量 的理由是
的理由是_______ 。
(3)电解:总反应(未配平): 。若不考虑副反应,为了使溶液中的
。若不考虑副反应,为了使溶液中的 、
、 均恰好完全反应,理论上需要再添加哪种离子?
均恰好完全反应,理论上需要再添加哪种离子?_______ (填“ ”、“
”、“ ”或“都不需要”)。
”或“都不需要”)。
 ,还含铁等元素)、软锰矿(主要成分为
,还含铁等元素)、软锰矿(主要成分为 )为原料联合生产锌和高纯度二氧化锰的一种流程如下:
)为原料联合生产锌和高纯度二氧化锰的一种流程如下:
(1)浸出:加入
 能促进
能促进 的溶解,提高锌的浸出率,同时生成硫单质。
的溶解,提高锌的浸出率,同时生成硫单质。 的作用类似催化剂,“催化”过程可表示为:
的作用类似催化剂,“催化”过程可表示为:ⅰ:

ⅱ:……
①写出ⅱ的离子方程式:
②下列实验方案可证实上述“催化”过程。将实验方案补充完整。
a.向酸化的
 溶液中加入
溶液中加入 溶液,溶液几乎无色,再加入少量
溶液,溶液几乎无色,再加入少量 ,溶液变红。
,溶液变红。b.
(2)除铁:已知①进入除铁工艺的溶液的pH约为3;②控制溶液pH为2.5~3.5,使铁主要以
 沉淀的形式除去。结合离子方程式说明,通入空气需同时补充适量
沉淀的形式除去。结合离子方程式说明,通入空气需同时补充适量 的理由是
的理由是(3)电解:总反应(未配平):
 。若不考虑副反应,为了使溶液中的
。若不考虑副反应,为了使溶液中的 、
、 均恰好完全反应,理论上需要再添加哪种离子?
均恰好完全反应,理论上需要再添加哪种离子? ”、“
”、“ ”或“都不需要”)。
”或“都不需要”)。
您最近半年使用:0次



