名校
解题方法
1 . 某科研人员提出HCHO与 在羟基磷灰石(HAP)表面催化氧化生成
在羟基磷灰石(HAP)表面催化氧化生成 ,
, 的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
 在羟基磷灰石(HAP)表面催化氧化生成
在羟基磷灰石(HAP)表面催化氧化生成 ,
, 的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
A.HAP降低了该反应的焓变( ) ) |
| B.反应过程中,发生了非极性键的断裂和生成 |
C.HCHO在反应过程中,无 键发生断裂 键发生断裂 |
D. 和 和 的中心原子上所含孤电子对数不同 的中心原子上所含孤电子对数不同 |
您最近半年使用:0次
7日内更新
|
253次组卷
|
4卷引用:广西壮族自治区部分学校2023-2024学年高三下学期教学质量监测联考(二模)化学试题
2 . 大气污染物的治理和“碳中和”技术的开发应用成为化学研究的热点。如图表示 在
在 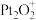 表面与
表面与  反应转化成无害气体的过程。设
反应转化成无害气体的过程。设  为阿伏加德罗常数的值。下列说法
为阿伏加德罗常数的值。下列说法错误 的是
 在
在 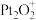 表面与
表面与  反应转化成无害气体的过程。设
反应转化成无害气体的过程。设  为阿伏加德罗常数的值。下列说法
为阿伏加德罗常数的值。下列说法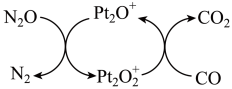
A. 和 和  分子中均有 分子中均有  个 个  键 键 |
B. 转化为 转化为 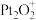 失去的电子数为 失去的电子数为  |
C. 转化成无害气体时的催化剂是 转化成无害气体时的催化剂是 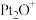 |
| D.题图转化过程中,氮元素被还原,碳元素被氧化 |
您最近半年使用:0次
3 . 下列实验操作或做法正确且能达到目的的是
| 选项 | 实验操作或做法 | 目的 |
| A | 向2 mL0.1 mol/LNa2S溶液中滴加0.1 mol/LZnSO4溶液至不再有沉淀产生,再滴加几滴0.1 mol/LCuSO4溶液,出现黑色沉淀 | 验证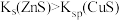 |
| B | 向各盛有5 mLH2O2溶液的两支试管中分别滴入2滴0.1 mol/L的FeCl3溶液和0.1 mol/L的CuSO4溶液 | 比较Fe3+与Cu2+对H2O2分解的催化效果 |
| C | 向盛有淀粉溶液的试管中加入少量稀硫酸,加热,再滴加几滴银氨溶液,水浴加热 | 证明淀粉已发生水解 |
| D | 先用稀硝酸酸化待测液,再滴加BaCl2溶液,生成白色沉淀 | 检验溶液中是否含有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
4 . “肼合成酶”以其中的 配合物为催化中心,可将
配合物为催化中心,可将 与
与 转化为肼
转化为肼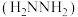 ,其反应历程如下所示。
,其反应历程如下所示。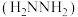 的燃烧热为
的燃烧热为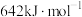 。
。
下列说法正确的是
 配合物为催化中心,可将
配合物为催化中心,可将 与
与 转化为肼
转化为肼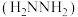 ,其反应历程如下所示。
,其反应历程如下所示。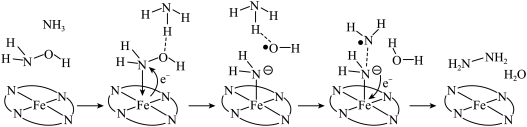
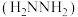 的燃烧热为
的燃烧热为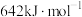 。
。下列说法正确的是
A.反应过程中 元素的化合价发生了变化 元素的化合价发生了变化 |
B.催化中心的 提供孤电子对,N提供空轨道 提供孤电子对,N提供空轨道 |
| C.反应涉及极性键与非极性键的断裂和生成 |
D.肼燃烧热的热化学方程式为: 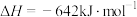 |
您最近半年使用:0次
名校
解题方法
5 . 我国科学家成功利用光伏发电,将电解水获得的 与
与 反应合成甲醇,再由甲醇经若干酶促反应合成淀粉。该研究成果已在国际学术期刊《科学》上发表。回答下列问题:
反应合成甲醇,再由甲醇经若干酶促反应合成淀粉。该研究成果已在国际学术期刊《科学》上发表。回答下列问题:
(1) 人工合成转化为淀粉只需要11步,其中前两步涉及的反应如图所示。
人工合成转化为淀粉只需要11步,其中前两步涉及的反应如图所示。 的
的
__________ (用含 、
、 、
、 、
、 的代数式表示)。
的代数式表示)。
(2)有学者结合实验和计算机模拟结果,得出 的一种反应历程如图所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为
的一种反应历程如图所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为__________ ;TS3对应的步骤适合在__________ (填“高温”或“低温”)条件下进行。 和
和 ,发生反应
,发生反应
 ,在催化剂作用下单位时间内
,在催化剂作用下单位时间内 的转化率与温度、催化剂的关系如图所示。
的转化率与温度、催化剂的关系如图所示。 的生成速率
的生成速率__________ (填“>”“<”或“=”,下同) 的消耗速率;催化效率:Cat2
的消耗速率;催化效率:Cat2__________ Cat1。
②b点之后 的转化率降低,可能的原因是
的转化率降低,可能的原因是__________ 。
(4)已知 催化加氢的主要反应如下:
催化加氢的主要反应如下:
反应Ⅰ.
反应Ⅱ.
①230℃时,将 和
和 按物质的量之比为1:3混合通入恒温刚性密闭容器中,在催化剂作用下同时发生反应Ⅰ和反应Ⅱ,容器内压强随时间的变化如下表所示。
按物质的量之比为1:3混合通入恒温刚性密闭容器中,在催化剂作用下同时发生反应Ⅰ和反应Ⅱ,容器内压强随时间的变化如下表所示。
平衡时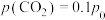 ,则该温度下反应Ⅰ的化学平衡常数
,则该温度下反应Ⅰ的化学平衡常数
__________  (用含
(用含 的代数式表示)。
的代数式表示)。
②二氧化碳催化加氢合成甲醇反应往往伴随副反应Ⅱ。一定温度和压强条件下,为了提高反应速率和甲醇选择性,应当__________ 。
 与
与 反应合成甲醇,再由甲醇经若干酶促反应合成淀粉。该研究成果已在国际学术期刊《科学》上发表。回答下列问题:
反应合成甲醇,再由甲醇经若干酶促反应合成淀粉。该研究成果已在国际学术期刊《科学》上发表。回答下列问题:(1)
 人工合成转化为淀粉只需要11步,其中前两步涉及的反应如图所示。
人工合成转化为淀粉只需要11步,其中前两步涉及的反应如图所示。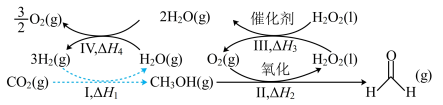
 的
的
 、
、 、
、 、
、 的代数式表示)。
的代数式表示)。(2)有学者结合实验和计算机模拟结果,得出
 的一种反应历程如图所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为
的一种反应历程如图所示,其中吸附在催化剂表面的物种用“·”标注,TS1、TS2、TS3、TS4均为过渡态。决速步骤对应的化学方程式为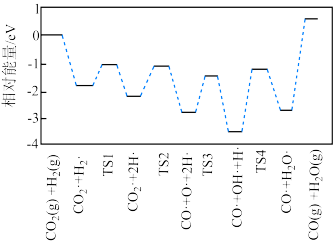
 和
和 ,发生反应
,发生反应
 ,在催化剂作用下单位时间内
,在催化剂作用下单位时间内 的转化率与温度、催化剂的关系如图所示。
的转化率与温度、催化剂的关系如图所示。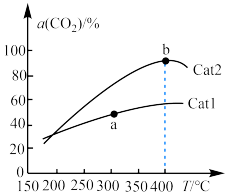
 的生成速率
的生成速率 的消耗速率;催化效率:Cat2
的消耗速率;催化效率:Cat2②b点之后
 的转化率降低,可能的原因是
的转化率降低,可能的原因是(4)已知
 催化加氢的主要反应如下:
催化加氢的主要反应如下:反应Ⅰ.

反应Ⅱ.

①230℃时,将
 和
和 按物质的量之比为1:3混合通入恒温刚性密闭容器中,在催化剂作用下同时发生反应Ⅰ和反应Ⅱ,容器内压强随时间的变化如下表所示。
按物质的量之比为1:3混合通入恒温刚性密闭容器中,在催化剂作用下同时发生反应Ⅰ和反应Ⅱ,容器内压强随时间的变化如下表所示。时间/min | 0 | 20 | 40 | 60 | 80 |
压强/MPa |
|
|
|
|
|
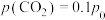 ,则该温度下反应Ⅰ的化学平衡常数
,则该温度下反应Ⅰ的化学平衡常数
 (用含
(用含 的代数式表示)。
的代数式表示)。②二氧化碳催化加氢合成甲醇反应往往伴随副反应Ⅱ。一定温度和压强条件下,为了提高反应速率和甲醇选择性,应当
您最近半年使用:0次
2024-04-07更新
|
292次组卷
|
4卷引用:广西壮族自治区部分学校2023-2024学年高三下学期教学质量监测联考(二模)化学试题
名校
6 . 炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧。活化过程的能量变化模拟计算结果如图所示。活化氧可以快速氧化二氧化硫。下列说法正确的是


| A.该过程中的最大能垒为1.02ev |
| B.炭黑是大气中二氧化硫转化为三氧化硫的催化剂 |
| C.该过程涉及了非极性键的断裂和形成 |
| D.每个氧分子活化成活化氧需要吸收0.29ev的能量 |
您最近半年使用:0次
名校
7 . 反应物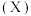 转化为产物
转化为产物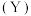 时,能量变化与反应历程的关系如图所示,下列说法正确的是
时,能量变化与反应历程的关系如图所示,下列说法正确的是

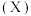 转化为产物
转化为产物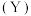 时,能量变化与反应历程的关系如图所示,下列说法正确的是
时,能量变化与反应历程的关系如图所示,下列说法正确的是
| A.该反应是吸热反应 |
B.由图可知 比 比 稳定 稳定 |
C. 是催化剂,可降低反应所需的活化能 是催化剂,可降低反应所需的活化能 |
D.使用催化剂后,反应历程中的决速步为 |
您最近半年使用:0次
名校
解题方法
8 . 下列实验操作、现象、实验结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向两支盛有等浓度等体积 的试管中分别加入等浓度等体积的 的试管中分别加入等浓度等体积的 溶液和 溶液和 溶液 溶液 | 前者产生气泡速率快 |  的催化效果比 的催化效果比 好 好 |
| B | 取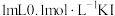 于试管中,加入 于试管中,加入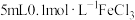 溶液,充分反应后滴入5滴15%的 溶液,充分反应后滴入5滴15%的 溶液 溶液 | 溶液变红 |  与 与 的反应有一定限度 的反应有一定限度 |
| C | 取A、B两试管,各加入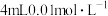 的 的 ,向A中加 ,向A中加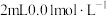 酸性高锰酸钾溶液,同时向B中加入 酸性高锰酸钾溶液,同时向B中加入 酸性高锰酸钾溶液 酸性高锰酸钾溶液 | B试管先褪为无色 | 其他条件不变时,增大反应物的浓度,反应速率加快 |
| D | 向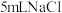 溶液中滴加2滴等浓度的 溶液中滴加2滴等浓度的 出现白色沉淀,过滤后取上层清 液又加入2滴 出现白色沉淀,过滤后取上层清 液又加入2滴 溶液 溶液 | 有黄色沉淀生成 |  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-02-24更新
|
394次组卷
|
3卷引用:2024届广西2024年“贵百河”高三下学期4月新高考模拟二模化学试题
名校
解题方法
9 . 2021年9月,中国科学院天津工业生物技术研究所成果“无细胞化学酶系统催化 合成淀粉”在国际学术期刊《自然》上发表,引发化学界的极大关注。其中部分核心反应转化如图所示。下列叙述正确的是
合成淀粉”在国际学术期刊《自然》上发表,引发化学界的极大关注。其中部分核心反应转化如图所示。下列叙述正确的是
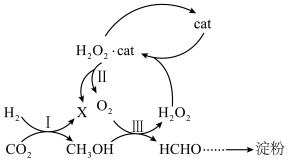
 合成淀粉”在国际学术期刊《自然》上发表,引发化学界的极大关注。其中部分核心反应转化如图所示。下列叙述正确的是
合成淀粉”在国际学术期刊《自然》上发表,引发化学界的极大关注。其中部分核心反应转化如图所示。下列叙述正确的是
A.反应Ⅰ中消耗2mol ,生成 ,生成 为1mol 为1mol |
B.反应Ⅲ需要额外从环境中补充 |
| C.合成过程可采用高温条件,以加快反应速率 |
D.HCHO转化为淀粉[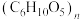 ]的原子利用率可达100% ]的原子利用率可达100% |
您最近半年使用:0次
23-24高三上·黑龙江大庆·期末
名校
解题方法
10 . 晶体硅材料是最主要的光伏材料,随当前信息工程的发展,硅主要用于微电子技术。工业上将粗硅氯化、精馏后得到 和
和 的混合物然后用
的混合物然后用 还原得到高纯硅。还原过程中发生的主要反应为:
还原得到高纯硅。还原过程中发生的主要反应为:
i.
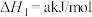
ii.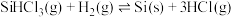
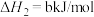
回答下列问题:
(1)已知: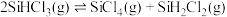
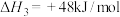 ,
, 还原
还原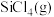 生成
生成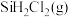 的热化学方程式为
的热化学方程式为___________ 。
(2)在 、
、 温度下,将
温度下,将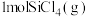 、
、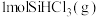 和
和 分别加入体积固定的密闭容器中,在催化条件下发生反应i、ii.测得
分别加入体积固定的密闭容器中,在催化条件下发生反应i、ii.测得 的转化率及体系内的压强随时间的变化关系如图所示。
的转化率及体系内的压强随时间的变化关系如图所示。
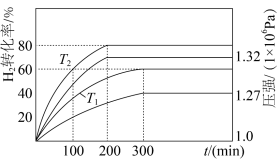
① 温度下,反应达到平衡时
温度下,反应达到平衡时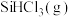 的转化率
的转化率___________ 。
② 温度下,反应i的标准平衡常数
温度下,反应i的标准平衡常数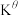 的计算式为
的计算式为___________ 。(已知:分压=总压×该组分物质的量分数,对于反应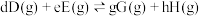 的
的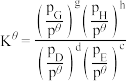 ,其中
,其中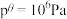 ,
,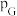 、
、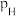 、
、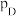 、
、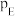 为各组分的平衡分压)。
为各组分的平衡分压)。
③
___________ 0(填“>”或“<”),写出推理过程___________ 。
(3)研究发现,反应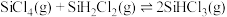 的活化能
的活化能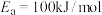 。反应的活化能
。反应的活化能 、速率常数k、温度T满足关系:
、速率常数k、温度T满足关系: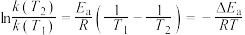 。
。
已知: ;ln10=2.3
;ln10=2.3
①若 ,通过升高温度到595K,才能满足
,通过升高温度到595K,才能满足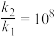 以加快反应速率;
以加快反应速率;
②若T=300K,使用催化剂使活化能降低,满足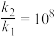 以加快反应速率,
以加快反应速率, 应减小。
应减小。
上述②中 应减小
应减小___________ kJ/mol(保留1位小数);对比①和②你得到的结论是___________ 。
 和
和 的混合物然后用
的混合物然后用 还原得到高纯硅。还原过程中发生的主要反应为:
还原得到高纯硅。还原过程中发生的主要反应为:i.

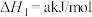
ii.
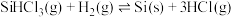
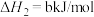
回答下列问题:
(1)已知:
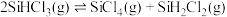
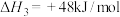 ,
, 还原
还原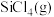 生成
生成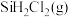 的热化学方程式为
的热化学方程式为(2)在
 、
、 温度下,将
温度下,将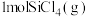 、
、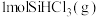 和
和 分别加入体积固定的密闭容器中,在催化条件下发生反应i、ii.测得
分别加入体积固定的密闭容器中,在催化条件下发生反应i、ii.测得 的转化率及体系内的压强随时间的变化关系如图所示。
的转化率及体系内的压强随时间的变化关系如图所示。
①
 温度下,反应达到平衡时
温度下,反应达到平衡时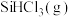 的转化率
的转化率②
 温度下,反应i的标准平衡常数
温度下,反应i的标准平衡常数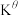 的计算式为
的计算式为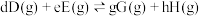 的
的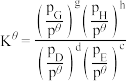 ,其中
,其中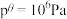 ,
,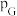 、
、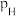 、
、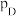 、
、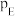 为各组分的平衡分压)。
为各组分的平衡分压)。③

(3)研究发现,反应
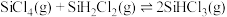 的活化能
的活化能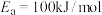 。反应的活化能
。反应的活化能 、速率常数k、温度T满足关系:
、速率常数k、温度T满足关系: 。
。已知:
 ;ln10=2.3
;ln10=2.3①若
 ,通过升高温度到595K,才能满足
,通过升高温度到595K,才能满足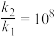 以加快反应速率;
以加快反应速率;②若T=300K,使用催化剂使活化能降低,满足
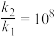 以加快反应速率,
以加快反应速率, 应减小。
应减小。上述②中
 应减小
应减小
您最近半年使用:0次