1 . 用 还原
还原 可合成
可合成 。回答下列问题:
。回答下列问题:
(1)利用 光解水制
光解水制 具有重要的经济价值,原理如图所示。
具有重要的经济价值,原理如图所示。 表面发生的电极反应式为
表面发生的电极反应式为_____ 。
写出 还原
还原 生成
生成 和
和 的热化学方程式:
的热化学方程式:_____ 。
(3)一定条件下,向某恒容密闭容器中充入2
 和3
和3
 反应生成
反应生成 和
和 ,起始时压强为
,起始时压强为 ,测得在相同时间内不同温度下
,测得在相同时间内不同温度下 的转化率如图所示。
的转化率如图所示。_____ 。
② K时,该反应的平衡常数
K时,该反应的平衡常数
_____ (列出计算式即可,不必化简。以分压代替浓度,分压=总压×物质的量分数)。
(4)为了探究浓度对反应速率的影响,473K时,向某恒容密闭容器中充入 和
和 进行实验,实验数据如下表所示:
进行实验,实验数据如下表所示:
该反应速率的通式为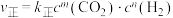 ,
,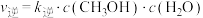 (
( 、
、 是只与温度有关的速率常数)。由表中数据可确定反应速率通式中
是只与温度有关的速率常数)。由表中数据可确定反应速率通式中
_____ 、
_____ 。实验发现,当实验1中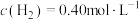 时达到平衡,请计算该温度下此反应的
时达到平衡,请计算该温度下此反应的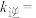
_____ 。
 还原
还原 可合成
可合成 。回答下列问题:
。回答下列问题:(1)利用
 光解水制
光解水制 具有重要的经济价值,原理如图所示。
具有重要的经济价值,原理如图所示。 表面发生的电极反应式为
表面发生的电极反应式为
| 共价键 |  |  |  |  |  |
键能/( ) ) | 464 | 358 | 799 | 432 | 411 |
 还原
还原 生成
生成 和
和 的热化学方程式:
的热化学方程式:(3)一定条件下,向某恒容密闭容器中充入2

 和3
和3
 反应生成
反应生成 和
和 ,起始时压强为
,起始时压强为 ,测得在相同时间内不同温度下
,测得在相同时间内不同温度下 的转化率如图所示。
的转化率如图所示。
②
 K时,该反应的平衡常数
K时,该反应的平衡常数
(4)为了探究浓度对反应速率的影响,473K时,向某恒容密闭容器中充入
 和
和 进行实验,实验数据如下表所示:
进行实验,实验数据如下表所示:| 实验 | 起始浓度/( ) ) | 初始速率/( ) ) | |
 |  | ||
| 1 | 0.25 | 1.00 | 0.45 |
| 2 | 0.25 | 2.00 | 3.60 |
| 3 | 2.00 | 1.00 | 3.6 |
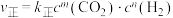 ,
,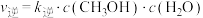 (
( 、
、 是只与温度有关的速率常数)。由表中数据可确定反应速率通式中
是只与温度有关的速率常数)。由表中数据可确定反应速率通式中

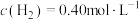 时达到平衡,请计算该温度下此反应的
时达到平衡,请计算该温度下此反应的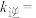
您最近半年使用:0次
解题方法
2 . 光阳极表面修饰的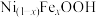 电催化剂可显著降低水氧化半反应的反应能垒,在
电催化剂可显著降低水氧化半反应的反应能垒,在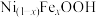 电催化剂作用下光电催化水氧化过程中的质子耦合电荷转移路径如图(Ni已略去;
电催化剂作用下光电催化水氧化过程中的质子耦合电荷转移路径如图(Ni已略去; 代表空穴,具有强氧化性)。下列说法错误的是
代表空穴,具有强氧化性)。下列说法错误的是
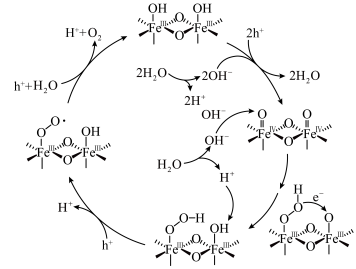
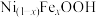 电催化剂可显著降低水氧化半反应的反应能垒,在
电催化剂可显著降低水氧化半反应的反应能垒,在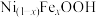 电催化剂作用下光电催化水氧化过程中的质子耦合电荷转移路径如图(Ni已略去;
电催化剂作用下光电催化水氧化过程中的质子耦合电荷转移路径如图(Ni已略去; 代表空穴,具有强氧化性)。下列说法错误的是
代表空穴,具有强氧化性)。下列说法错误的是
| A.上述路径中涉及极性共价键的断裂和形成 |
B.上述路径中 元素与 元素与 元素均体现出两种化合价 元素均体现出两种化合价 |
C.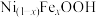 电催化剂中的铁元素位于第Ⅷ族 电催化剂中的铁元素位于第Ⅷ族 |
D.图示光电催化水氧化半反应可表示为 |
您最近半年使用:0次
名校
解题方法
3 . 某研究团队以NO和H2为原料,在Fe基催化下有效地合成NH3.回答下列问题:
已知:①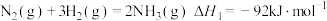
②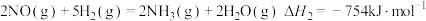
(1)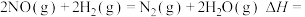
___________  。
。
(2)在一定温度下,向一恒容密闭容器中充入0.2molNO(g)和0.5molH2(g),只发生反应②,达到平衡时生成1.7gNH3(g)。下列叙述正确的是___________ (填标号)。
A.当容器内总压强不变时,该反应达到平衡
B.达到平衡时,反应体系放出的热量为37.7kJ
C.平衡后再充入0.2molNO(g)和0.5molH2(g),NO平衡转化率减小
(3)研究发现, 分两步进行:
分两步进行:
第1步: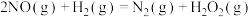 (慢反应);
(慢反应);
第2步:___________ (补充)(快反应)。
加入催化剂,主要是降低第___________ (填“1”或“2”)步反应活化能。
(4) 的反应速率方程式为
的反应速率方程式为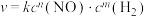 (其中,k为常数,只与温度和催化剂有关)。为了测定反应级数m、n,实验结果如下:
(其中,k为常数,只与温度和催化剂有关)。为了测定反应级数m、n,实验结果如下:
根据上述数据计算:m=___________ ,n=___________ ,c=___________ 。
(5)在一密闭反应器中充入2molNO(g)和5molH2(g),在催化剂10Fe﹣8Cu/TiO2作用下发生反应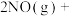
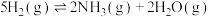 ,
, ,实验测得NO转化率和NH3选择性与温度的关系如图所示。
,实验测得NO转化率和NH3选择性与温度的关系如图所示。

温度高于350℃时,NO转化率增大,但NH3选择性降低,主要原因是___________ 。a点时生成NH3的物质的量为___________ (结果保留3位有效数字)。
(6)某温度下,保持总压强为100kPa,向反应器中充入2molNO(g)和6molH2(g),只发生反应:(a)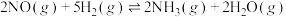 ,(b)
,(b) ,达到平衡时NO转化率为60%,NH3选择性为80%。反应(b)的平衡常数
,达到平衡时NO转化率为60%,NH3选择性为80%。反应(b)的平衡常数
___________  (计算结果保留三位有效数字)。
(计算结果保留三位有效数字)。
已知:①
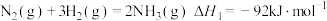
②
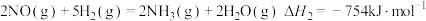
(1)
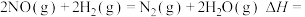
 。
。(2)在一定温度下,向一恒容密闭容器中充入0.2molNO(g)和0.5molH2(g),只发生反应②,达到平衡时生成1.7gNH3(g)。下列叙述正确的是
A.当容器内总压强不变时,该反应达到平衡
B.达到平衡时,反应体系放出的热量为37.7kJ
C.平衡后再充入0.2molNO(g)和0.5molH2(g),NO平衡转化率减小
(3)研究发现,
 分两步进行:
分两步进行:第1步:
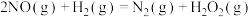 (慢反应);
(慢反应);第2步:
加入催化剂,主要是降低第
(4)
 的反应速率方程式为
的反应速率方程式为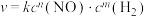 (其中,k为常数,只与温度和催化剂有关)。为了测定反应级数m、n,实验结果如下:
(其中,k为常数,只与温度和催化剂有关)。为了测定反应级数m、n,实验结果如下:| 序号 | 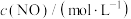 | 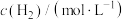 | 速率 |
| I | 0.1 | 0.1 | v |
| II | 0.2 | 0.1 | 4v |
| III | 0.2 | 0.2 | 8v |
| IV | c | 0.4 | 36v |
(5)在一密闭反应器中充入2molNO(g)和5molH2(g),在催化剂10Fe﹣8Cu/TiO2作用下发生反应
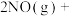
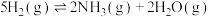 ,
, ,实验测得NO转化率和NH3选择性与温度的关系如图所示。
,实验测得NO转化率和NH3选择性与温度的关系如图所示。
温度高于350℃时,NO转化率增大,但NH3选择性降低,主要原因是
(6)某温度下,保持总压强为100kPa,向反应器中充入2molNO(g)和6molH2(g),只发生反应:(a)
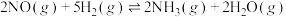 ,(b)
,(b) ,达到平衡时NO转化率为60%,NH3选择性为80%。反应(b)的平衡常数
,达到平衡时NO转化率为60%,NH3选择性为80%。反应(b)的平衡常数
 (计算结果保留三位有效数字)。
(计算结果保留三位有效数字)。
您最近半年使用:0次
2024-01-19更新
|
145次组卷
|
3卷引用:2024届青海省协作联考高三上学期一模理综试题
解题方法
4 . 在室温下,Ti不与O2、H2O、强碱、强酸反应,在高温下可与O2反应。Hunter法是最早研究用来制取金属钛的方法,其流程如下图所示。回答下列问题:
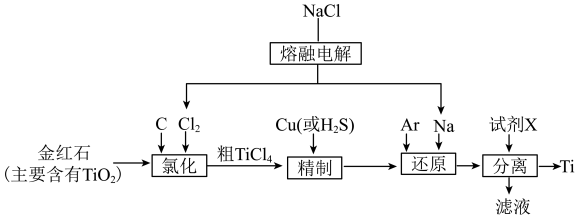
(1)“氯化”是在1000~1050℃下进行,碳被氧化为CO,该反应的化学方程式为___________ 。
(2)“精制”时,粗 中含有大量杂质,可用精馏的方法提纯,对于沸点相近的
中含有大量杂质,可用精馏的方法提纯,对于沸点相近的 杂质可用铜(或
杂质可用铜(或 )将其转化为
)将其转化为 沉淀,反应机理为
沉淀,反应机理为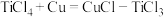 ,
,
 。从总反应看,
。从总反应看, 是该反应的
是该反应的___________ ; 可与
可与 直接反应生成
直接反应生成 ,写出
,写出 与
与 发生反应的化学方程式:
发生反应的化学方程式:___________ 。
(3)“钠还原”是用液态钠还原气态 得到Ti,Ar的作用是
得到Ti,Ar的作用是___________ ;若发生 、
、 等副反应,其原因可能是
等副反应,其原因可能是___________ 。
(4)“分离”时,固体混合物需经取出、破碎、酸浸、过滤、洗涤及干燥等步骤,试剂X为___________ (填名称),滤液循环使用的方法是___________ 。

(1)“氯化”是在1000~1050℃下进行,碳被氧化为CO,该反应的化学方程式为
(2)“精制”时,粗
 中含有大量杂质,可用精馏的方法提纯,对于沸点相近的
中含有大量杂质,可用精馏的方法提纯,对于沸点相近的 杂质可用铜(或
杂质可用铜(或 )将其转化为
)将其转化为 沉淀,反应机理为
沉淀,反应机理为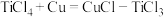 ,
,
 。从总反应看,
。从总反应看, 是该反应的
是该反应的 可与
可与 直接反应生成
直接反应生成 ,写出
,写出 与
与 发生反应的化学方程式:
发生反应的化学方程式:(3)“钠还原”是用液态钠还原气态
 得到Ti,Ar的作用是
得到Ti,Ar的作用是 、
、 等副反应,其原因可能是
等副反应,其原因可能是(4)“分离”时,固体混合物需经取出、破碎、酸浸、过滤、洗涤及干燥等步骤,试剂X为
您最近半年使用:0次
5 . 下列有关说法中正确的是
| A.冰在室温下自动融化成水,是因为体系混乱度降低 |
| B.硫酸工业中采用400~500℃的高温,有利于增大反应正向进行的程度 |
| C.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 |
| D.工业生产中,合成氨采用的压强越高,温度越低,越有利于提高经济效益 |
您最近半年使用:0次
2023-09-10更新
|
142次组卷
|
2卷引用:青海省海东市名校2023-2024学年高三上学期9月联考化学试题
名校
6 . 对于可逆反应mA(g)+nB(s)  pC(g)+qD(g)反应过程中,其他条件不变时,产物D的质量分数D %与温度T或压强p的关系如图所示,下列说法正确的是
pC(g)+qD(g)反应过程中,其他条件不变时,产物D的质量分数D %与温度T或压强p的关系如图所示,下列说法正确的是
 pC(g)+qD(g)反应过程中,其他条件不变时,产物D的质量分数D %与温度T或压强p的关系如图所示,下列说法正确的是
pC(g)+qD(g)反应过程中,其他条件不变时,产物D的质量分数D %与温度T或压强p的关系如图所示,下列说法正确的是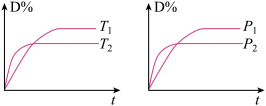
| A.降温,化学平衡向正反应方向移动 |
| B.使用催化剂可使D%有所增加 |
| C.化学方程式中化学计量数m+n<p+q |
| D.升温,A的转化率提高 |
您最近半年使用:0次
2023-04-25更新
|
413次组卷
|
4卷引用:青海省西宁市六校联考2022-2023学年高二上学期期末考试化学试题
青海省西宁市六校联考2022-2023学年高二上学期期末考试化学试题(已下线)专题04 化学平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)安徽省合肥市第一中学2023-2024学年高二上学期12月月考化学试题天津市武清区河西务中学2023-2024学年高二上学期第二次月考化学试卷
名校
解题方法
7 . 下列装置或操作正确且对应的实验能达到实验目的的是
 | 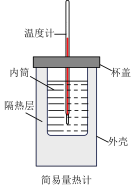 | 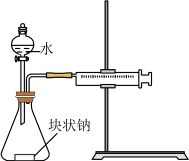 | 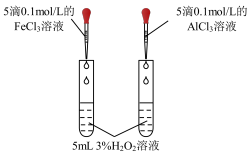 |
| A.测定NaOH溶液的浓度 | B.测定中和反应反应热 | C.通过注射器活塞右移,验证Na与H2O反应放热 | D.研究Fe3+、Al3+对H2O2分解速率的影响 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-01-15更新
|
352次组卷
|
4卷引用:青海省西宁市大通县2023-2024学年高二上学期期末考试化学试题
解题方法
8 . 无论是在环境保护还是工农业生产方面,氮及其化合物一直是我国科研重点。
已知:反应i. 6NO(g)+4NH3(g)⇌5N2(g)+6H2O(g) ΔH1=−1808kJ·mol−1;
反应ii. N2(g)+3H2(g)⇌2NH3(g) ΔH2=−91.4kJ·mol−1。
部分化学键键能如下表所示:
回答下列问题:
(1)NO中氮氧键键能为_______ 。
(2)向2L刚性密闭容器中充入0.06molNO(g)和0.04molNH3(g),发生反应i.不同温度下,测得10min时NO的转化率如图1所示。

①T1K下反应i的平均反应速率v(NO)=_______ mol·L-1·min-1(用含α1的代数式表示);
②NH3和NO(g)的有效碰撞几率M_______ N(填“>”“=”或“<”)原因为_______ ;
③NO转化率先升高后降低的原因为_______ ;
(3)固氮在工农业生产中具有重要意义:
①反应i是工业固氮的反应原理合成氨的速率公式为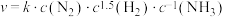 。其中k为反应速率常数:下列条件能影响k值大小的是
。其中k为反应速率常数:下列条件能影响k值大小的是_______ (填选项字母)
A.反应温度 B.反应物的浓度 C.反应压强 D.催化剂
②某固氮反应机理如图2所示:
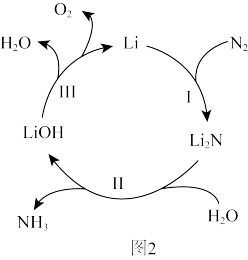
该固氮的总反应方程式为_______ ;已知三步反应的活化能由大到小的顺序为Ⅲ>Ⅰ>Ⅱ则该固氮过程的决速步骤为_______ (填“I”“Ⅱ”或“Ⅲ”);
已知:反应i. 6NO(g)+4NH3(g)⇌5N2(g)+6H2O(g) ΔH1=−1808kJ·mol−1;
反应ii. N2(g)+3H2(g)⇌2NH3(g) ΔH2=−91.4kJ·mol−1。
部分化学键键能如下表所示:
| 化学键 | N—H |  | H—O |
| 键能/ kJ·mol−1 | 390 | 946 | 463 |
(1)NO中氮氧键键能为
(2)向2L刚性密闭容器中充入0.06molNO(g)和0.04molNH3(g),发生反应i.不同温度下,测得10min时NO的转化率如图1所示。

①T1K下反应i的平均反应速率v(NO)=
②NH3和NO(g)的有效碰撞几率M
③NO转化率先升高后降低的原因为
(3)固氮在工农业生产中具有重要意义:
①反应i是工业固氮的反应原理合成氨的速率公式为
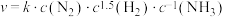 。其中k为反应速率常数:下列条件能影响k值大小的是
。其中k为反应速率常数:下列条件能影响k值大小的是A.反应温度 B.反应物的浓度 C.反应压强 D.催化剂
②某固氮反应机理如图2所示:

该固氮的总反应方程式为
您最近半年使用:0次
名校
解题方法
9 . CO2在Au纳米颗粒表面电催化还原制备CO的方法具有在常温下催化效率高的优点,其反应历程如图所示。下列说法错误的是
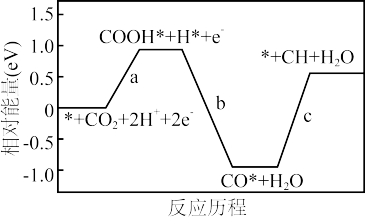

| A.该反应历程为阴极反应历程 |
| B.催化剂降低了反应的活化能 |
| C.高温下一定能提高电催化制备CO的速率 |
| D.电催化还原CO2的电极反应式为CO2+2H++2e−=CO+H2O |
您最近半年使用:0次
2022-12-11更新
|
290次组卷
|
4卷引用:青海省海东市第一中学2022-2023学年高三上学期第一次模拟检测化学试题
青海省海东市第一中学2022-2023学年高三上学期第一次模拟检测化学试题广东省广州市2022-2023学年高二上学期期末考试化学试题(已下线)河南省湘豫名校联考2022-2023学年高三上学期12月期末摸底考试变式汇编(1-8)四川省甘孜藏族自治州泸定中学2023-2024学年高二上学期11月期中考试化学试题
10 . 叔丁基溴在乙醇中反应的能量变化如图所示。
反应1: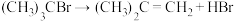
反应2: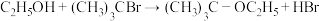
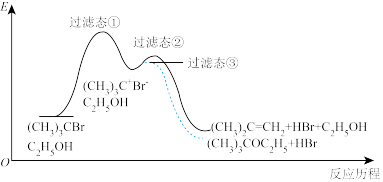
下列说法正确的是
反应1:
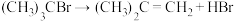
反应2:
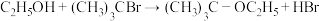

下列说法正确的是
| A.3种过渡态相比①最稳定 |
| B.反应1和反应2的∆H都大于0 |
| C.第一个基元反应是决速步骤 |
D. 是反应1和反应2共同的催化剂 是反应1和反应2共同的催化剂 |
您最近半年使用:0次



