名校
1 . 在铁系催化剂的催化作用下,工业合成氨的反应历程如图所示,其中TS表示过渡态,*表示吸附在催化剂表面。下列说法正确的是

A.决速步骤: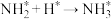 |
| B.氨气脱附过程放热 |
| C.使用铁催化剂可加快反应速率,提高原料平衡转化率 |
D.热化学方程式:  kJ·mol kJ·mol |
您最近半年使用:0次
解题方法
2 . 接触法制硫酸的工艺流程中的关键步骤是SO2的催化氧化: ,在催化剂表面的反应历程如下:
,在催化剂表面的反应历程如下:
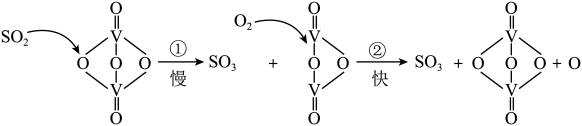
下列说法正确的是
 ,在催化剂表面的反应历程如下:
,在催化剂表面的反应历程如下:
下列说法正确的是
| A.过程中既有V-O键的断裂,又有V-O键的形成 |
| B.该反应的中间产物是V2O5 |
| C.反应①的活化能比反应②大 |
| D.反应放热,为提高SO2转化率,应尽可能在较低温度下反应 |
您最近半年使用:0次
解题方法
3 . 下列对有关事实或解释正确的是
| 编号 | 事实 | 解释 |
| A | 锌与稀盐酸反应,加入氯化钠固体,速率加快 | 增大了氯离子浓度,反应速率加快 |
| B | 锌与稀硫酸反应,滴入较多硫酸铜溶液,生成氢气的速率减慢 | 锌置换铜的反应干扰了锌置换氢的反应,致使生成氢气的速率变慢 |
| C |  的双氧水中加入二氧化锰粉末,分解速率迅速加快 的双氧水中加入二氧化锰粉末,分解速率迅速加快 | 降低了反应的焓变,活化分子数增多,有效碰撞增多,速率加快 |
| D | 面粉生产车间容易发生爆炸 | 固体表面积大,反应速率加快 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
4 . HCHO(g)与O2在催化剂羟基磷灰石(简写为HAP)表面催化生成CO2(g)和H2O(g)的历程示意图如下。下列说法错误的是
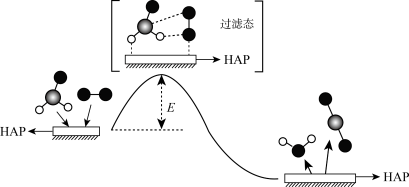

| A.CO2分子的分子空间构型为直线形 |
| B.羟基磷灰石(HAP)的作用是加快反应速率 |
| C.HCHO和H2O分子的VSEPR模型都是四面体形 |
| D.该反应过程既有极性共价键的断裂,也有非极性共价键的断裂 |
您最近半年使用:0次
名校
解题方法
5 . 氢气作为一种清洁能源,一直是能源研究的热点,水煤气变换反应可用于大规模制 ,反应原理如下:
,反应原理如下:
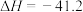 kJ⋅mol
kJ⋅mol
(1)根据下表中提供的数据,计算

 。
。化学键 |
|
|
|
|
键能/kJ·mol | 803 | x | 463 | 436 |
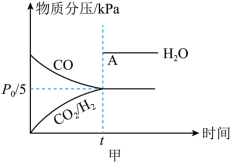
(2)某温度下,在一恒容密闭容器中充入CO和
 ,加入催化剂使其发生上述反应(忽略其他副反应),测得该反应中初始压强为
,加入催化剂使其发生上述反应(忽略其他副反应),测得该反应中初始压强为 ,分压如图甲所示(t时刻前,
,分压如图甲所示(t时刻前, 的分压未给出),则A点坐标为(t,
的分压未给出),则A点坐标为(t,
(3)反应
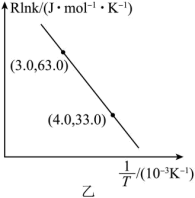
 的Arrhenius经验公式的实验数据如图乙中曲线所示,已知经验公式为
的Arrhenius经验公式的实验数据如图乙中曲线所示,已知经验公式为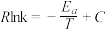 (其中
(其中 为活化能,k为速率常数,R和C为常数)。该反应的活化能
为活化能,k为速率常数,R和C为常数)。该反应的活化能
当使用更高效催化剂时,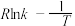
您最近半年使用:0次
6 . 华中师范大学某团队成功制备了单原子 分散于催化剂表面的
分散于催化剂表面的 催化剂,并用于
催化剂,并用于 氧化制备
氧化制备 ,分别在
,分别在 催化剂、
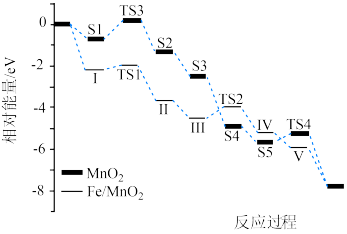
催化剂、 催化剂作用下,测得反应过程中的相对能量变化如图所示。已知:TS代表过渡态,S1~S5、Ⅰ~Ⅴ代表中间产物。下列叙述错误的是
催化剂作用下,测得反应过程中的相对能量变化如图所示。已知:TS代表过渡态,S1~S5、Ⅰ~Ⅴ代表中间产物。下列叙述错误的是
 分散于催化剂表面的
分散于催化剂表面的 催化剂,并用于
催化剂,并用于 氧化制备
氧化制备 ,分别在
,分别在 催化剂、
催化剂、 催化剂作用下,测得反应过程中的相对能量变化如图所示。已知:TS代表过渡态,S1~S5、Ⅰ~Ⅴ代表中间产物。下列叙述错误的是
催化剂作用下,测得反应过程中的相对能量变化如图所示。已知:TS代表过渡态,S1~S5、Ⅰ~Ⅴ代表中间产物。下列叙述错误的是
A. 氧化制备 氧化制备 为放热反应 为放热反应 |
B. 的催化效率低于 的催化效率低于 |
| C.两种催化剂作用下反应热相等 |
D. 催化时总反应速率由S1→S2步骤决定 催化时总反应速率由S1→S2步骤决定 |
您最近半年使用:0次
7 . 某温度下,反应CH2=CH2(g)+H2O(g) CH3CH2OH(g)在密闭容器中达到平衡。下列说法
CH3CH2OH(g)在密闭容器中达到平衡。下列说法错误 的是
 CH3CH2OH(g)在密闭容器中达到平衡。下列说法
CH3CH2OH(g)在密闭容器中达到平衡。下列说法| A.升高温度,v正减小 |
| B.达到平衡时,CH2=CH2的体积分数不再发生变化 |
| C.恒容下,充入一定量的H2O(g),速率增大 |
| D.加入催化剂,可缩短到达平衡的时间 |
您最近半年使用:0次
2024-02-25更新
|
394次组卷
|
2卷引用:海南中学白沙学校2022-2023学年高一下学期期末考试化学试题
名校
8 . 氨主要来源于工业合成氨: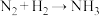 (未配平)。中国科学家研制出新型催化剂,将该反应的温度、压强降至350℃、1MPa.相比于常温、常压。下列措施一定能提高H2的平衡转化率的是
(未配平)。中国科学家研制出新型催化剂,将该反应的温度、压强降至350℃、1MPa.相比于常温、常压。下列措施一定能提高H2的平衡转化率的是
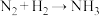 (未配平)。中国科学家研制出新型催化剂,将该反应的温度、压强降至350℃、1MPa.相比于常温、常压。下列措施一定能提高H2的平衡转化率的是
(未配平)。中国科学家研制出新型催化剂,将该反应的温度、压强降至350℃、1MPa.相比于常温、常压。下列措施一定能提高H2的平衡转化率的是| A.采用合适的高效催化剂 | B.采用较高的温度 |
| C.采用较高的压强 | D.增大反应体系中H2的浓度 |
您最近半年使用:0次
名校
9 . 下列四种溶液中,分别加入少量的固体二氧化锰,能产生气体的是
| A.3%的H2O2溶液 | B.1mol/L NaOH溶液 | C.1mol/L KClO3溶液 | D.0.1mol/L盐酸 |
您最近半年使用:0次
名校
10 . 催化剂的作用是
| A.作为反应物参加反应,以增加产量 |
| B.缩短达到平衡的时间 |
| C.只加快正反应的速率 |
| D.减少反应物的消耗 |
您最近半年使用:0次







