名校
解题方法
1 . 燃油汽车尾气中含有CO和氮氧化物,在 的催化作用下,发生反应:
的催化作用下,发生反应: ,可降低污染。其反应历程和相对能量变化如图所示:
,可降低污染。其反应历程和相对能量变化如图所示:不正确 的是
 的催化作用下,发生反应:
的催化作用下,发生反应: ,可降低污染。其反应历程和相对能量变化如图所示:
,可降低污染。其反应历程和相对能量变化如图所示: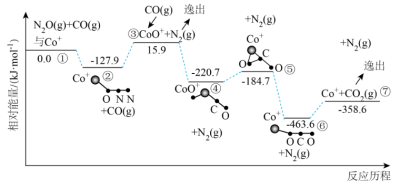
A. 分子的中心原子是N,分子中O—N—N的键角大于 分子的中心原子是N,分子中O—N—N的键角大于 分子中O—N—O的键角 分子中O—N—O的键角 |
| B.历程中决定反应速率的变化过程是②→③ |
C.总反应分两步进行,已知 参与第一步反应,则第二步反应为: 参与第一步反应,则第二步反应为: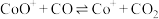 |
D.恒容、绝热下模拟反应: ,体系的温度、 ,体系的温度、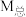 (平均相对分子质量)、压强恒定均能说明反应达到平衡状态 (平均相对分子质量)、压强恒定均能说明反应达到平衡状态 |
您最近半年使用:0次
名校
2 . 化学与生产、生活密切相关。下列事实与化学反应速率无关的
| A.用炉灶燃烧含硫蜂窝煤时加入生石灰 |
| B.做糕点时,在面粉中加入酵母菌发酵 |
| C.在糕点包装内放置除氧剂可以延长食品保质期 |
D.燃烧黄铁矿制备 气体时,把矿石粉碎成颗粒状 气体时,把矿石粉碎成颗粒状 |
您最近半年使用:0次
名校
解题方法
3 . 工业合成氨是最重要的人工固氮途径,发生反应: 。请回答:
。请回答:
(1)已知断开1mol的某化学键所需能量如表所示。若固氮反应中有2mol 生成时,
生成时,______ (填 “吸收”或“放出”)热量______ kJ。
(2)恒温恒压条件下,向密闭容器中投入等物质的量的 和
和 发生反应,下列描述能说明反应已达到化学平衡状态的是______。
发生反应,下列描述能说明反应已达到化学平衡状态的是______。
(3)利用 可消除大气污染物NO,可将反应设计为原电池提供电能,如图所示。该电池中M为原电池的
可消除大气污染物NO,可将反应设计为原电池提供电能,如图所示。该电池中M为原电池的______ 极(填“正”或“负”),其电极方程式为______ 。______ (填“a”、“b”或“c”)______
 。请回答:
。请回答:(1)已知断开1mol的某化学键所需能量如表所示。若固氮反应中有2mol
 生成时,
生成时,化学键 |
|
|
|
能量(kJ) | 436 | 391 | 946 |
(2)恒温恒压条件下,向密闭容器中投入等物质的量的
 和
和 发生反应,下列描述能说明反应已达到化学平衡状态的是______。
发生反应,下列描述能说明反应已达到化学平衡状态的是______。A.反应速率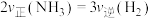 | B.混合气体的密度不再变化 |
| C.混合气体的平均摩尔质量不再变化 | D. 的体积分数不再变化 的体积分数不再变化 |
(3)利用
 可消除大气污染物NO,可将反应设计为原电池提供电能,如图所示。该电池中M为原电池的
可消除大气污染物NO,可将反应设计为原电池提供电能,如图所示。该电池中M为原电池的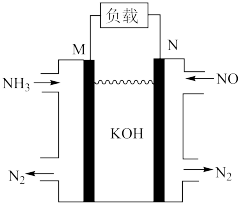


您最近半年使用:0次
解题方法
4 . 邻二醇在酸的作用下能转化为酮(或醛),反应的分步机理和协同机理如下:
①当碳原子上连有推电子基团时,有利于碳正离子(通常指的是价层只有6个电子的碳阳离子,是活性中间体)的稳定。
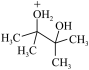
②2,3-二甲基-2,3-丁二醇与酸反应,对应的中间体和生成物相对能量(kJ/mol)如下:
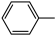
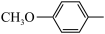
③当碳正离子的相邻碳上有两个不同芳基时,迁移的相对速率与芳基的关系如下表:
下列说法不正确 的是

①当碳原子上连有推电子基团时,有利于碳正离子(通常指的是价层只有6个电子的碳阳离子,是活性中间体)的稳定。
②2,3-二甲基-2,3-丁二醇与酸反应,对应的中间体和生成物相对能量(kJ/mol)如下:
| 过渡态1 | 过渡态2 | 生成物 | |
| 分步机理 | 0.00 | 30.1 | 38.3 | -82.3 |
| 协同机理 | 0.00 | 44.0 | - | -82.3 |
| 芳基 |
|
|
|
| 相对速率 | 0.7 | 1 | 500 |
A.酸性条件下,2,3-二甲基-2,3-丁二醇转化为 主要以分步机理进行 主要以分步机理进行 |
| B.上述转化过程中酸可提高反应速率,但不影响平衡产率 |
| C.乙二醇在酸性条件下只能通过协同机理生成醛,原因是碳正离子中间体不稳定 |
D.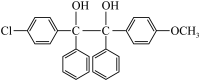 在酸的作用下,产物主要形式为 在酸的作用下,产物主要形式为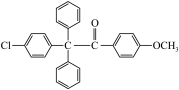 |
您最近半年使用:0次
5 . 在一定温度下,以 为催化剂,氯苯和
为催化剂,氯苯和 在
在 中发生平行反应,分别生成邻二氯苯和对二氯苯
中发生平行反应,分别生成邻二氯苯和对二氯苯
①两产物浓度之比与反应时间无关。
②反应物起始浓度均为 ,反应30min测得氯苯15%转化为邻二氯苯,25%转化为对二氯苯。下列说法
,反应30min测得氯苯15%转化为邻二氯苯,25%转化为对二氯苯。下列说法不正确 的是
 为催化剂,氯苯和
为催化剂,氯苯和 在
在 中发生平行反应,分别生成邻二氯苯和对二氯苯
中发生平行反应,分别生成邻二氯苯和对二氯苯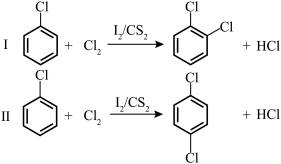
①两产物浓度之比与反应时间无关。
②反应物起始浓度均为
 ,反应30min测得氯苯15%转化为邻二氯苯,25%转化为对二氯苯。下列说法
,反应30min测得氯苯15%转化为邻二氯苯,25%转化为对二氯苯。下列说法| A.反应Ⅰ的活化能大于反应Ⅱ |
| B.保持其他条件不变,改变反应物浓度可以提高产物中邻二氯苯的比例 |
| C.保持其他条件不变,改变催化剂可以提高产物中邻二氯苯的比例 |
| D.保持其他条件不变,适当提高反应温度可以提高产物中邻二氯苯的比例 |
您最近半年使用:0次
2024-04-18更新
|
90次组卷
|
2卷引用:浙江绍兴市2023-2024学年高三下学期选考科目适应性考试化学试题
名校
解题方法
6 . 氧化铟基纳米催化剂 可用于
可用于 选择性加氢制备
选择性加氢制备 ,其反应机理如图所示。下列说法
,其反应机理如图所示。下列说法不正确 的是
 可用于
可用于 选择性加氢制备
选择性加氢制备 ,其反应机理如图所示。下列说法
,其反应机理如图所示。下列说法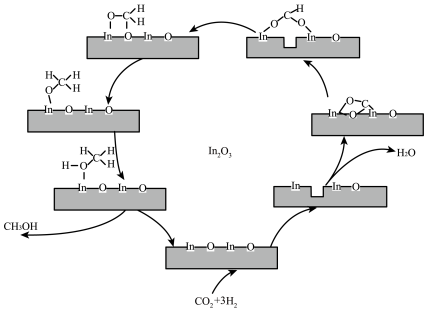
A.该反应每生成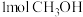 ,转移 ,转移 电子 电子 |
B. 与 与 中,碳原子的杂化方式分别是 中,碳原子的杂化方式分别是 与 与 杂化 杂化 |
C.该反应过程中 只有 只有 键断裂,没有 键断裂,没有 键断裂,但有新 键断裂,但有新 键形成 键形成 |
D.催化剂 ,参与反应生成了过渡态物质,降低了反应的活化能,加快了化学反应速率 ,参与反应生成了过渡态物质,降低了反应的活化能,加快了化学反应速率 |
您最近半年使用:0次
名校
解题方法
7 . 据文献报道:Fe(CO)5催化某反应的一种反应机理如图。下列叙述错误的是
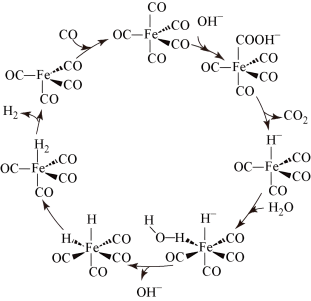
| A.该催化循环中OH-参与了反应 |
| B.该反应可消耗温室气体CO2产生清洁燃料H2 |
| C.Fe(CO)5铁的氧化数为0 |
| D.该催化循环中Fe的成键数目和类型都发生变化 |
您最近半年使用:0次
解题方法
8 . 回收利用 是目前解决空间站供氧问题的有效途径,其物质转化如图:
是目前解决空间站供氧问题的有效途径,其物质转化如图:

反应A为 ,是回收利用
,是回收利用 的关键步骤。
的关键步骤。
发生反应A的过程中,有副反应发生,主要涉及的副反应如下:
Ⅰ.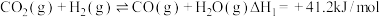
Ⅱ.
(1)反应 的
的
_______  。
。
(2)向某容积为 的恒容密闭容器中充入
的恒容密闭容器中充入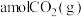 和
和 ,在纳米镍粒子催化剂作用下,假设只发生反应A(不考虑副反应),在相同时间内测得
,在纳米镍粒子催化剂作用下,假设只发生反应A(不考虑副反应),在相同时间内测得 的物质的量分数与温度的变化曲线如图所示(不考虑催化剂失效问题)。
的物质的量分数与温度的变化曲线如图所示(不考虑催化剂失效问题)。
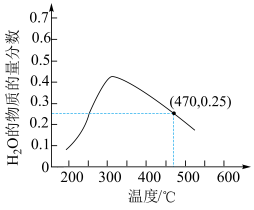
①请用虚线 在上图中画出在250℃-550℃间内,反应 达到平衡时,
达到平衡时, 的物质的量分数随温度变化的曲线
的物质的量分数随温度变化的曲线_______ 。
②在470℃时,反应 的平衡常数
的平衡常数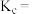
_______  (用含a的最简分数表示)。
(用含a的最简分数表示)。
③实际生产中,温度过高或温度过低均不利于该反应的进行,原因是_______ 。
(3)下列关于空间站内物质转化和能量变化的说法中,不正确 的是_______ (填字母)。
a.反应B的能量变化是电能(或光能) 化学能
化学能
b.目前科学家致力于开发新型催化剂,此催化剂可将 的分解转为放热反应,降低生产
的分解转为放热反应,降低生产 的成本
的成本
c.反应Ⅰ的 ,反应II的
,反应II的
d.镍粒子催化剂的颗粒大小不影响反应速率
(4)用 代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是
代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是_______ 。
 是目前解决空间站供氧问题的有效途径,其物质转化如图:
是目前解决空间站供氧问题的有效途径,其物质转化如图:
反应A为
 ,是回收利用
,是回收利用 的关键步骤。
的关键步骤。发生反应A的过程中,有副反应发生,主要涉及的副反应如下:
Ⅰ.
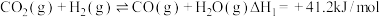
Ⅱ.

(1)反应
 的
的
 。
。(2)向某容积为
 的恒容密闭容器中充入
的恒容密闭容器中充入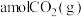 和
和 ,在纳米镍粒子催化剂作用下,假设只发生反应A(不考虑副反应),在相同时间内测得
,在纳米镍粒子催化剂作用下,假设只发生反应A(不考虑副反应),在相同时间内测得 的物质的量分数与温度的变化曲线如图所示(不考虑催化剂失效问题)。
的物质的量分数与温度的变化曲线如图所示(不考虑催化剂失效问题)。
①请用
 达到平衡时,
达到平衡时, 的物质的量分数随温度变化的曲线
的物质的量分数随温度变化的曲线②在470℃时,反应
 的平衡常数
的平衡常数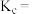
 (用含a的最简分数表示)。
(用含a的最简分数表示)。③实际生产中,温度过高或温度过低均不利于该反应的进行,原因是
(3)下列关于空间站内物质转化和能量变化的说法中,
a.反应B的能量变化是电能(或光能)
 化学能
化学能b.目前科学家致力于开发新型催化剂,此催化剂可将
 的分解转为放热反应,降低生产
的分解转为放热反应,降低生产 的成本
的成本c.反应Ⅰ的
 ,反应II的
,反应II的
d.镍粒子催化剂的颗粒大小不影响反应速率
(4)用
 代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是
代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是
您最近半年使用:0次
解题方法
9 . 下列实验中,操作、现象及结论都正确,且有因果关系的是
选项 | 实验操作 | 现象 | 结论 |
A | 将 | 溶液pH变大 | 稀释后, |
B | 取两支试管,分别加入2mL5%的双氧水,试管1中加入 | 试管1产生气泡快 | 加入 |
C | 向含有ZnS和 | 生成黑色沉淀 |
|
D | 用pH试纸分别测定同浓度 | 测得NaClO溶液pH大 |
|
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
10 . 某反应过程能量变化如图所示,下列说法正确的是
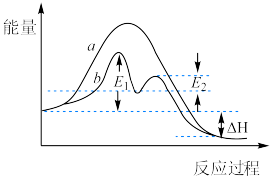

| A.反应过程a有催化剂参与 |
B.该反应为吸热反应,反应热等于 |
C.加入催化剂,可改变该反应的活化能,但不能改变反应的 |
D.有催化剂的条件下,反应的活化能等于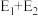 |
您最近半年使用:0次





 溶液由
溶液由 稀释到
稀释到 ,测溶液pH
,测溶液pH 的水解程度增大
的水解程度增大 溶液2滴,试管2中加入
溶液2滴,试管2中加入
 时,双氧水分解反应的活化能较小
时,双氧水分解反应的活化能较小 的悬浊液中滴加
的悬浊液中滴加 溶液
溶液
 和NaClO溶液的pH
和NaClO溶液的pH 水解程度大于
水解程度大于


