1 . 室温下,探究0.1 mol·L-1 FeCl3溶液的性质,下列实验方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向两支试管中分别加入5 mL 5%的H2O2溶液,再向两支试管中滴入3滴浓度均为0.1 mol·L-1 的FeCl3和CuSO4,观察产生气体的速率 | 比较Fe3+和Cu2+的催化效率 |
| B | 向2 mL 0.1 mol·L-1 FeCl3溶液中加入1 mL 0.1 mol·L-1 KI溶液,充分振荡后滴加KSCN溶液,观察颜色变化 | 2Fe3++2I-=2Fe2++I2是否为可逆反应 |
| C | 向苯酚溶液中滴加几滴0.1 mol·L-1 FeCl3溶液,溶液呈紫色 | FeCl3与苯酚发生了氧化还原反应 |
| D | 将5 mL 0.1 mol·L-1 FeCl3溶液和15 mL 0.1 mol·L-1 NaHCO3溶液混合,生成红褐色沉淀和气体 | Fe3+与 发生了双水解反应 发生了双水解反应 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
2 . 氰化氢(HCN,一元弱酸,易挥发)主要应用于电镀、采矿、药物合成等工业生产。HCN,CN-能抑制人体组织细胞内酶的活性,不能直接排放到环境中。
(1)Na2S2O3在临床上常用于氰化物的解毒剂。解毒的原理是 将CN-转化为SCN-和
将CN-转化为SCN-和 。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,
。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,___________ 。
(2)Cu2+可催化过氧化氢氧化废水中的CN-。
①反应不能在酸性条件下进行,原因是___________ 。
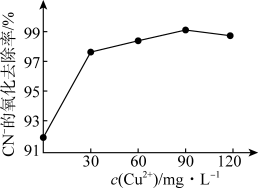
②在含氰废水总景、过氧化氢用量和溶液pH一定的情况下,反应相同时间,测得CN-的氧化去除率随c(Cu2+)的变化与如图所示。c(Cu2+)超过90mg·L-1时,CN-的氧化去除率有所下降,原因是___________ 。 ,其反应的离子方程式为
,其反应的离子方程式为___________ 。
(4)在铜镍为催化剂(Cu、CuO为活性组分,Cu的催化活性效果更好)的条件下,可利用反应:HCN(g)+H2O(g) NH3(g)+CO(g) △H>0
NH3(g)+CO(g) △H>0
除去废气中的HCN。将含相同比例的HCN(g)、H2O(g)、CO(g)[或N2(g)]混合气体分别通过催化剂,反应相同的时间,测得HCN(g)的去除率随温度变化如图所示。200℃时含CO的混合气体中HCN(g)的去除率较高,而400℃时含CO的混合气体中HCN(g)的去除率较低。其原因是___________ 。
(1)Na2S2O3在临床上常用于氰化物的解毒剂。解毒的原理是
 将CN-转化为SCN-和
将CN-转化为SCN-和 。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,
。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,(2)Cu2+可催化过氧化氢氧化废水中的CN-。
①反应不能在酸性条件下进行,原因是
②在含氰废水总景、过氧化氢用量和溶液pH一定的情况下,反应相同时间,测得CN-的氧化去除率随c(Cu2+)的变化与如图所示。c(Cu2+)超过90mg·L-1时,CN-的氧化去除率有所下降,原因是
 ,其反应的离子方程式为
,其反应的离子方程式为(4)在铜镍为催化剂(Cu、CuO为活性组分,Cu的催化活性效果更好)的条件下,可利用反应:HCN(g)+H2O(g)
 NH3(g)+CO(g) △H>0
NH3(g)+CO(g) △H>0除去废气中的HCN。将含相同比例的HCN(g)、H2O(g)、CO(g)[或N2(g)]混合气体分别通过催化剂,反应相同的时间,测得HCN(g)的去除率随温度变化如图所示。200℃时含CO的混合气体中HCN(g)的去除率较高,而400℃时含CO的混合气体中HCN(g)的去除率较低。其原因是

您最近半年使用:0次
名校
3 . 反应2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g);△H<0可实现CO2的资源化,下列说法正确的是
CH3OCH3(g)+3H2O(g);△H<0可实现CO2的资源化,下列说法正确的是
 CH3OCH3(g)+3H2O(g);△H<0可实现CO2的资源化,下列说法正确的是
CH3OCH3(g)+3H2O(g);△H<0可实现CO2的资源化,下列说法正确的是| A.上述反应在任何温度下均可自发进行 |
| B.上述反应反应物的总能量大于生成物的总能量 |
C.上述反应平衡常数K=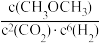 |
| D.上述反应达到平衡后,加入催化剂,平衡正向移动 |
您最近半年使用:0次
名校
4 . CO2/HCOOH循环在氢能的贮存/释放、燃料电池等方面具有重要应用。
(1)CO2催化加氢。在密闭容器中,向含有催化剂的KHCO3溶液(CO2与KOH溶液反应制得)中通入H2生成HCOO−,其离子方程式为_______ ;其他条件不变, 转化为HCOO−的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内,
转化为HCOO−的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内, 催化加氢的转化率迅速上升,其主要原因是
催化加氢的转化率迅速上升,其主要原因是_______ 。_______ ;放电过程中需补充的物质A为_______ (填化学式)。
②图中所示的HCOOH燃料电池放电的本质是通过HCOOH与O2的反应,将化学能转化为电能,其反应的离子方程式为_______ 。
(3)HCOOH催化释氢。在催化剂作用下,HCOOH分解生成CO2和H2可能的反应机理如图所示。_______ (填化学式)。
②研究发现:其他条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳,其具体优点是提高释放氢气的速率,提高释放出氢气的纯度,请分析原因_______ 。
(1)CO2催化加氢。在密闭容器中,向含有催化剂的KHCO3溶液(CO2与KOH溶液反应制得)中通入H2生成HCOO−,其离子方程式为
 转化为HCOO−的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内,
转化为HCOO−的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内, 催化加氢的转化率迅速上升,其主要原因是
催化加氢的转化率迅速上升,其主要原因是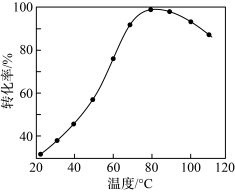
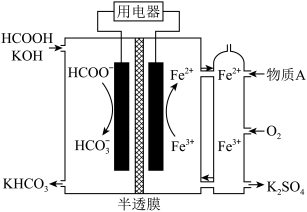
②图中所示的HCOOH燃料电池放电的本质是通过HCOOH与O2的反应,将化学能转化为电能,其反应的离子方程式为
(3)HCOOH催化释氢。在催化剂作用下,HCOOH分解生成CO2和H2可能的反应机理如图所示。
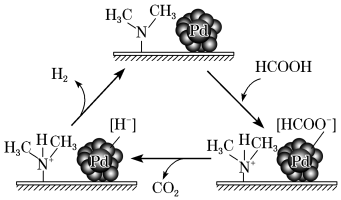
②研究发现:其他条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳,其具体优点是提高释放氢气的速率,提高释放出氢气的纯度,请分析原因
您最近半年使用:0次
名校
解题方法
5 . NH3催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图;研究发现在以Fe2O3为主的催化剂上可能发生的反应过程如图。下列说法正确的是

| A.NH3催化还原NO为吸热反应 |
| B.过程I中NH3断裂N—H键 |
| C.过程Ⅱ中NO为氧化剂,Fe2+为还原剂 |
| D.脱硝的总反应为:4NH3(g)+4NO(g)+2O2(g)⇌4N2(g)+6H2O(g) |
您最近半年使用:0次
解题方法
6 . 在催化剂作用下,HCOOH分解生成 和
和 可能的反应机理如下图所示。下列说法
可能的反应机理如下图所示。下列说法不正确 的是
 和
和 可能的反应机理如下图所示。下列说法
可能的反应机理如下图所示。下列说法
A.若用HCOOK溶液代替HCOOH最终所得气体中 的纯度会降低 的纯度会降低 |
| B.第一步转化N与H间形成配位键 |
| C.若用HCOOK溶液代替HCOOH释氢的速率加快 |
D.若用HCOOD催化释氢,反应除生成 外,还生成HD 外,还生成HD |
您最近半年使用:0次
7 . 空气中 含量的控制和
含量的控制和 资源利用具有重要意义。
资源利用具有重要意义。
(1)利用高炉炼铁尾气中的 制取有机物的过程如下:
制取有机物的过程如下: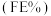 随电解电压的变化如下图1所示:
随电解电压的变化如下图1所示: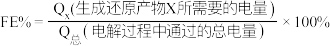 ,选择性
,选择性 .
.
“电解”在质子交换膜电解池中进行,生成 的电极反应式为
的电极反应式为____________ ,当电解电压为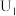 时,生成
时,生成 和
和 的选择性之比为
的选择性之比为____________ .
(2)利用铟氧化物催化 制取
制取 的可能机理如下图2所示,
的可能机理如下图2所示, 无催化活性,形成氧空位后具有较强催化活性,将固定比例的
无催化活性,形成氧空位后具有较强催化活性,将固定比例的 混合气体以不同流速通过装有催化剂的反应管,
混合气体以不同流速通过装有催化剂的反应管, 选择性、
选择性、 转化率随气体流速变化曲线如下图3所示,
转化率随气体流速变化曲线如下图3所示,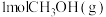 和
和 放出
放出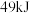 的热量,其热化学方程式为
的热量,其热化学方程式为____________ .
②若原料气中 比例过低、过高均会减弱催化剂活性,原因是
比例过低、过高均会减弱催化剂活性,原因是____________ .
③制取 时,同时发生反应
时,同时发生反应 ,气体流速分别为
,气体流速分别为 和
和 ,相同时间内生成
,相同时间内生成 的质量,前者
的质量,前者____________ 后者(选填“>”、“=”或“<”);保持气体流速不变,反应管内温度从 升高到
升高到 ,测得出口处
,测得出口处 和
和 的物质的量均减小,可能的原因是
的物质的量均减小,可能的原因是____________ .
 含量的控制和
含量的控制和 资源利用具有重要意义。
资源利用具有重要意义。(1)利用高炉炼铁尾气中的
 制取有机物的过程如下:
制取有机物的过程如下: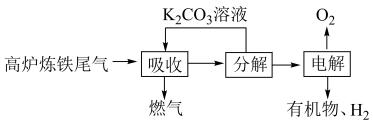
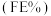 随电解电压的变化如下图1所示:
随电解电压的变化如下图1所示: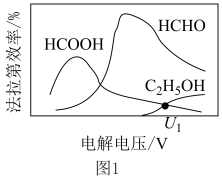
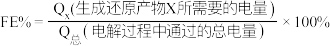 ,选择性
,选择性 .
.“电解”在质子交换膜电解池中进行,生成
 的电极反应式为
的电极反应式为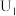 时,生成
时,生成 和
和 的选择性之比为
的选择性之比为(2)利用铟氧化物催化
 制取
制取 的可能机理如下图2所示,
的可能机理如下图2所示, 无催化活性,形成氧空位后具有较强催化活性,将固定比例的
无催化活性,形成氧空位后具有较强催化活性,将固定比例的 混合气体以不同流速通过装有催化剂的反应管,
混合气体以不同流速通过装有催化剂的反应管, 选择性、
选择性、 转化率随气体流速变化曲线如下图3所示,
转化率随气体流速变化曲线如下图3所示,
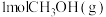 和
和 放出
放出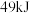 的热量,其热化学方程式为
的热量,其热化学方程式为②若原料气中
 比例过低、过高均会减弱催化剂活性,原因是
比例过低、过高均会减弱催化剂活性,原因是③制取
 时,同时发生反应
时,同时发生反应 ,气体流速分别为
,气体流速分别为 和
和 ,相同时间内生成
,相同时间内生成 的质量,前者
的质量,前者 升高到
升高到 ,测得出口处
,测得出口处 和
和 的物质的量均减小,可能的原因是
的物质的量均减小,可能的原因是
您最近半年使用:0次
名校
8 . 有机物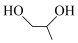 脱氧脱水反应的催化循环机理如下图所示.下列说法正确的是
脱氧脱水反应的催化循环机理如下图所示.下列说法正确的是

A.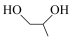 的系统名称为丙二醇 的系统名称为丙二醇 |
B. 为该反应的中间产物 为该反应的中间产物 |
C.过程④中有 键发生断裂 键发生断裂 |
D.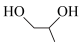 分解的产物有 分解的产物有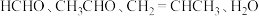 |
您最近半年使用:0次
解题方法
9 . 高砷煤中含有砷硫铁(FeAsS)等物质。燃煤产生的烟气中含NO、 、粉尘等,经过SCR脱硝除去NO,粉尘经沉降得到粉煤灰。
、粉尘等,经过SCR脱硝除去NO,粉尘经沉降得到粉煤灰。
(1)燃煤固硫
①燃用高砷煤时加入生石灰将大部分硫元素转化为___________ (填化学式)留在煤渣中。
②高砷煤燃烧过程中,砷硫铁在高温下被氧化成 释放到烟气中,该反应的化学方程式为
释放到烟气中,该反应的化学方程式为________________ 。
(2)SCR脱硝(脱除烟气中的NO)
在烟气中加入适量氨气,用钒氧化物作催化剂将 、NO、
、NO、 转化为
转化为 。烟气中含有的
。烟气中含有的 会使钒氧化物催化剂中毒。
会使钒氧化物催化剂中毒。
①在SCR脱硝的反应中还原剂为_______________ (填化学式)。
②研究发现砷中毒机理主要是 分子破坏了催化剂的Lewis酸位点,使
分子破坏了催化剂的Lewis酸位点,使 数量减少(产物中As化合价为+3、+5)。请补充完整产物的结构
数量减少(产物中As化合价为+3、+5)。请补充完整产物的结构__________ 。 不易使催化剂中毒。但与
不易使催化剂中毒。但与 相比,
相比, 更不利于脱硝反应的进行,其原因是
更不利于脱硝反应的进行,其原因是_______________ 。
(3)粉煤灰成分研究
粉煤灰可用于水泥工业,粉煤灰中的氨含量( 或铵盐)会影响水泥的性能。
或铵盐)会影响水泥的性能。
①取50.00 g粉煤灰加入NaOH蒸出 ,用20 mL 0.1000 mol⋅L
,用20 mL 0.1000 mol⋅L 的
的 溶液吸收
溶液吸收 ,用0.2000mol⋅L
,用0.2000mol⋅L NaOH溶液滴定过量的
NaOH溶液滴定过量的 至终点,平行滴定3次,平均消耗NaOH溶液10.00 mL,计算粉煤灰中的以
至终点,平行滴定3次,平均消耗NaOH溶液10.00 mL,计算粉煤灰中的以 计的氨含量
计的氨含量___________ (用mg⋅g 表示,写出计算过程)。
表示,写出计算过程)。
②相同烟气所得脱硝粉煤灰(经过SCR脱硝后获得)与未脱硝粉煤灰(直接沉降获得)加水后溶解后,所得浆液pH随时间的变化如图所示。脱硝粉煤灰pH始终比未脱硝粉煤灰低的原因是___________ 。
 、粉尘等,经过SCR脱硝除去NO,粉尘经沉降得到粉煤灰。
、粉尘等,经过SCR脱硝除去NO,粉尘经沉降得到粉煤灰。(1)燃煤固硫
①燃用高砷煤时加入生石灰将大部分硫元素转化为
②高砷煤燃烧过程中,砷硫铁在高温下被氧化成
 释放到烟气中,该反应的化学方程式为
释放到烟气中,该反应的化学方程式为(2)SCR脱硝(脱除烟气中的NO)
在烟气中加入适量氨气,用钒氧化物作催化剂将
 、NO、
、NO、 转化为
转化为 。烟气中含有的
。烟气中含有的 会使钒氧化物催化剂中毒。
会使钒氧化物催化剂中毒。①在SCR脱硝的反应中还原剂为
②研究发现砷中毒机理主要是
 分子破坏了催化剂的Lewis酸位点,使
分子破坏了催化剂的Lewis酸位点,使 数量减少(产物中As化合价为+3、+5)。请补充完整产物的结构
数量减少(产物中As化合价为+3、+5)。请补充完整产物的结构
 不易使催化剂中毒。但与
不易使催化剂中毒。但与 相比,
相比, 更不利于脱硝反应的进行,其原因是
更不利于脱硝反应的进行,其原因是(3)粉煤灰成分研究
粉煤灰可用于水泥工业,粉煤灰中的氨含量(
 或铵盐)会影响水泥的性能。
或铵盐)会影响水泥的性能。①取50.00 g粉煤灰加入NaOH蒸出
 ,用20 mL 0.1000 mol⋅L
,用20 mL 0.1000 mol⋅L 的
的 溶液吸收
溶液吸收 ,用0.2000mol⋅L
,用0.2000mol⋅L NaOH溶液滴定过量的
NaOH溶液滴定过量的 至终点,平行滴定3次,平均消耗NaOH溶液10.00 mL,计算粉煤灰中的以
至终点,平行滴定3次,平均消耗NaOH溶液10.00 mL,计算粉煤灰中的以 计的氨含量
计的氨含量 表示,写出计算过程)。
表示,写出计算过程)。②相同烟气所得脱硝粉煤灰(经过SCR脱硝后获得)与未脱硝粉煤灰(直接沉降获得)加水后溶解后,所得浆液pH随时间的变化如图所示。脱硝粉煤灰pH始终比未脱硝粉煤灰低的原因是

您最近半年使用:0次
7日内更新
|
427次组卷
|
2卷引用:江苏省苏锡常镇四市2024届高三一模考试化学试题
10 . 甲醛释氢对氢能源和含甲醛污水处理有重要意义。
(1)HCHO电催化释氢
催化电解含较低浓度的HCHO、NaOH混合溶液,可获得 与HCOONa(如图所示),其中电极b表面覆盖一种Mo与P形成的化合物(晶胞结构如图所示)作催化剂。
与HCOONa(如图所示),其中电极b表面覆盖一种Mo与P形成的化合物(晶胞结构如图所示)作催化剂。 与
与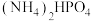 混合物与
混合物与 高温灼烧制得(反应中N元素化合价不变),该反应的化学方程式为
高温灼烧制得(反应中N元素化合价不变),该反应的化学方程式为_________________ 。
②电解时,电极b上同时产生 与
与 的物质的量之比为1∶2,则电极b上的电极反应式为
的物质的量之比为1∶2,则电极b上的电极反应式为_____________ 。
③电解过程中每产生1 mol ,通过阴离子交换膜的
,通过阴离子交换膜的 为
为______ mol。
(2)HCHO水化释氢
45℃时,碱性条件下Ag作催化剂可将甲醛转化为 ,反应的机理如图所示。
,反应的机理如图所示。 表面以防止纳米Ag团聚。其他条件不变,反应相同时间,NaOH浓度对氢气产生快慢的影响如图所示。
表面以防止纳米Ag团聚。其他条件不变,反应相同时间,NaOH浓度对氢气产生快慢的影响如图所示。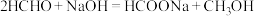 。
。
①若将甲醛中的氢用D原子标记为DCDO,得到的氢气产物为_______ (填化学式)。
②NaOH浓度低于1 mol⋅L 时,NaOH浓度增大产生氢气会加快的原因是
时,NaOH浓度增大产生氢气会加快的原因是__________ 。
③若NaOH浓度过大, 的产生迅速减慢的原因可能是
的产生迅速减慢的原因可能是__________________ 。
(3)甲烷与水在催化剂作用下可产生氢气与碳氧化物,与甲烷水化法制氢气相比,甲醛制氢的优点有______________ 。
(1)HCHO电催化释氢
催化电解含较低浓度的HCHO、NaOH混合溶液,可获得
 与HCOONa(如图所示),其中电极b表面覆盖一种Mo与P形成的化合物(晶胞结构如图所示)作催化剂。
与HCOONa(如图所示),其中电极b表面覆盖一种Mo与P形成的化合物(晶胞结构如图所示)作催化剂。
 与
与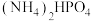 混合物与
混合物与 高温灼烧制得(反应中N元素化合价不变),该反应的化学方程式为
高温灼烧制得(反应中N元素化合价不变),该反应的化学方程式为②电解时,电极b上同时产生
 与
与 的物质的量之比为1∶2,则电极b上的电极反应式为
的物质的量之比为1∶2,则电极b上的电极反应式为③电解过程中每产生1 mol
 ,通过阴离子交换膜的
,通过阴离子交换膜的 为
为(2)HCHO水化释氢
45℃时,碱性条件下Ag作催化剂可将甲醛转化为
 ,反应的机理如图所示。
,反应的机理如图所示。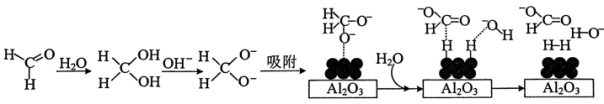
 表面以防止纳米Ag团聚。其他条件不变,反应相同时间,NaOH浓度对氢气产生快慢的影响如图所示。
表面以防止纳米Ag团聚。其他条件不变,反应相同时间,NaOH浓度对氢气产生快慢的影响如图所示。
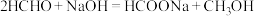 。
。①若将甲醛中的氢用D原子标记为DCDO,得到的氢气产物为
②NaOH浓度低于1 mol⋅L
 时,NaOH浓度增大产生氢气会加快的原因是
时,NaOH浓度增大产生氢气会加快的原因是③若NaOH浓度过大,
 的产生迅速减慢的原因可能是
的产生迅速减慢的原因可能是(3)甲烷与水在催化剂作用下可产生氢气与碳氧化物,与甲烷水化法制氢气相比,甲醛制氢的优点有
您最近半年使用:0次
7日内更新
|
464次组卷
|
2卷引用:江苏省苏锡常镇四市2024届高三一模考试化学试题



