名校
1 . 工业或机动车尾气中的 会造成环境问题,可用多种方法脱除。
会造成环境问题,可用多种方法脱除。
(1)碱液吸收:石灰乳可吸收硝酸工业的尾气(含 ),获得副产品
),获得副产品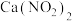 。
。
①等物质的量 与
与 被
被 吸收,反应的化学方程式为
吸收,反应的化学方程式为___________ 。
②下列措施能提高尾气中 和
和 去除率的有
去除率的有___________ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量 溶液
溶液
③该工艺需控制 和
和 的物质的量之比接近
的物质的量之比接近 ,若
,若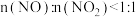 ,则会导致
,则会导致___________ ;若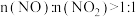 ,则会导致
,则会导致___________ 。
④生产中需保持弱碱性,在酸性溶液中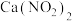 会发生分解,产物之一是
会发生分解,产物之一是 ,其反应的离子方程式为
,其反应的离子方程式为___________ 。
(2)还原法:尿素水溶液热解产生的氨气发生催化反应可去除尾气中的 。
。 与
与 转化生成
转化生成 的反应中,当生成
的反应中,当生成 时,转移的电子数为
时,转移的电子数为___________  。
。
(3)氯化法:“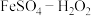 ”试剂可将
”试剂可将 氧化为可溶的
氧化为可溶的 。
。 催化
催化 分解产生有很强的氧化性的
分解产生有很强的氧化性的 ,
, 将
将 氧化为
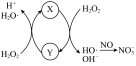
氧化为 的机理如图所示,Y的化学式为
的机理如图所示,Y的化学式为___________ 。
 会造成环境问题,可用多种方法脱除。
会造成环境问题,可用多种方法脱除。(1)碱液吸收:石灰乳可吸收硝酸工业的尾气(含
 ),获得副产品
),获得副产品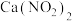 。
。①等物质的量
 与
与 被
被 吸收,反应的化学方程式为
吸收,反应的化学方程式为②下列措施能提高尾气中
 和
和 去除率的有
去除率的有A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量
 溶液
溶液③该工艺需控制
 和
和 的物质的量之比接近
的物质的量之比接近 ,若
,若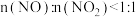 ,则会导致
,则会导致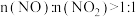 ,则会导致
,则会导致④生产中需保持弱碱性,在酸性溶液中
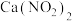 会发生分解,产物之一是
会发生分解,产物之一是 ,其反应的离子方程式为
,其反应的离子方程式为(2)还原法:尿素水溶液热解产生的氨气发生催化反应可去除尾气中的
 。
。 与
与 转化生成
转化生成 的反应中,当生成
的反应中,当生成 时,转移的电子数为
时,转移的电子数为 。
。(3)氯化法:“
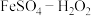 ”试剂可将
”试剂可将 氧化为可溶的
氧化为可溶的 。
。 催化
催化 分解产生有很强的氧化性的
分解产生有很强的氧化性的 ,
, 将
将 氧化为
氧化为 的机理如图所示,Y的化学式为
的机理如图所示,Y的化学式为
您最近半年使用:0次
名校
2 . 钒系催化剂催化脱硝部分机理如图所示,则有关该过程的叙述
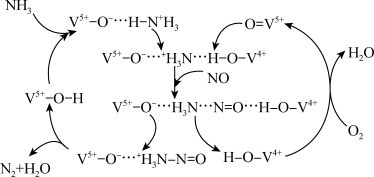
| A.V在流程中的化合价变化为+5→+4→+5 |
| B.V5+-O-···H-N+H3为该反应的一个中间体 |
| C.该反应的整体反应为:6NH3 + 5NO + 2O2 = 4N2 + 9H2O |
| D.反应过程中涉及极性共价键的断裂与形成和非极性共价键的断裂与形成 |
您最近半年使用:0次
3 . 甲醛释氢对氢能源和含甲醛污水处理有重要意义。
(1)HCHO电催化释氢
催化电解含较低浓度的HCHO、NaOH混合溶液,可获得 与HCOONa(如图所示),其中电极b表面覆盖一种Mo与P形成的化合物(晶胞结构如图所示)作催化剂。
与HCOONa(如图所示),其中电极b表面覆盖一种Mo与P形成的化合物(晶胞结构如图所示)作催化剂。 与
与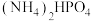 混合物与
混合物与 高温灼烧制得(反应中N元素化合价不变),该反应的化学方程式为
高温灼烧制得(反应中N元素化合价不变),该反应的化学方程式为_________________ 。
②电解时,电极b上同时产生 与
与 的物质的量之比为1∶2,则电极b上的电极反应式为
的物质的量之比为1∶2,则电极b上的电极反应式为_____________ 。
③电解过程中每产生1 mol ,通过阴离子交换膜的
,通过阴离子交换膜的 为
为______ mol。
(2)HCHO水化释氢
45℃时,碱性条件下Ag作催化剂可将甲醛转化为 ,反应的机理如图所示。
,反应的机理如图所示。 表面以防止纳米Ag团聚。其他条件不变,反应相同时间,NaOH浓度对氢气产生快慢的影响如图所示。
表面以防止纳米Ag团聚。其他条件不变,反应相同时间,NaOH浓度对氢气产生快慢的影响如图所示。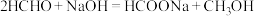 。
。
①若将甲醛中的氢用D原子标记为DCDO,得到的氢气产物为_______ (填化学式)。
②NaOH浓度低于1 mol⋅L 时,NaOH浓度增大产生氢气会加快的原因是
时,NaOH浓度增大产生氢气会加快的原因是__________ 。
③若NaOH浓度过大, 的产生迅速减慢的原因可能是
的产生迅速减慢的原因可能是__________________ 。
(3)甲烷与水在催化剂作用下可产生氢气与碳氧化物,与甲烷水化法制氢气相比,甲醛制氢的优点有______________ 。
(1)HCHO电催化释氢
催化电解含较低浓度的HCHO、NaOH混合溶液,可获得
 与HCOONa(如图所示),其中电极b表面覆盖一种Mo与P形成的化合物(晶胞结构如图所示)作催化剂。
与HCOONa(如图所示),其中电极b表面覆盖一种Mo与P形成的化合物(晶胞结构如图所示)作催化剂。
 与
与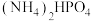 混合物与
混合物与 高温灼烧制得(反应中N元素化合价不变),该反应的化学方程式为
高温灼烧制得(反应中N元素化合价不变),该反应的化学方程式为②电解时,电极b上同时产生
 与
与 的物质的量之比为1∶2,则电极b上的电极反应式为
的物质的量之比为1∶2,则电极b上的电极反应式为③电解过程中每产生1 mol
 ,通过阴离子交换膜的
,通过阴离子交换膜的 为
为(2)HCHO水化释氢
45℃时,碱性条件下Ag作催化剂可将甲醛转化为
 ,反应的机理如图所示。
,反应的机理如图所示。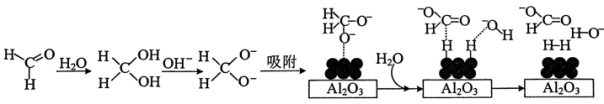
 表面以防止纳米Ag团聚。其他条件不变,反应相同时间,NaOH浓度对氢气产生快慢的影响如图所示。
表面以防止纳米Ag团聚。其他条件不变,反应相同时间,NaOH浓度对氢气产生快慢的影响如图所示。
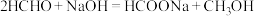 。
。①若将甲醛中的氢用D原子标记为DCDO,得到的氢气产物为
②NaOH浓度低于1 mol⋅L
 时,NaOH浓度增大产生氢气会加快的原因是
时,NaOH浓度增大产生氢气会加快的原因是③若NaOH浓度过大,
 的产生迅速减慢的原因可能是
的产生迅速减慢的原因可能是(3)甲烷与水在催化剂作用下可产生氢气与碳氧化物,与甲烷水化法制氢气相比,甲醛制氢的优点有
您最近半年使用:0次
2024-03-24更新
|
608次组卷
|
3卷引用:江苏省苏锡常镇四市2024届高三一模考试化学试题
4 .  催化重整能够有效去除大气中的
催化重整能够有效去除大气中的 ,是实现“碳中和”的重要途径之一,发生的反应如下:
,是实现“碳中和”的重要途径之一,发生的反应如下:
重整反应:

积炭反应I: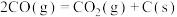

积炭反应II:

在恒压、起始投料比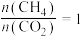 条件下,体系中含碳组分平衡时的物质的量随温度变化关系曲线如图所示。下列说法正确的是
条件下,体系中含碳组分平衡时的物质的量随温度变化关系曲线如图所示。下列说法正确的是

 催化重整能够有效去除大气中的
催化重整能够有效去除大气中的 ,是实现“碳中和”的重要途径之一,发生的反应如下:
,是实现“碳中和”的重要途径之一,发生的反应如下:重整反应:


积炭反应I:
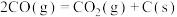

积炭反应II:


在恒压、起始投料比
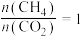 条件下,体系中含碳组分平衡时的物质的量随温度变化关系曲线如图所示。下列说法正确的是
条件下,体系中含碳组分平衡时的物质的量随温度变化关系曲线如图所示。下列说法正确的是
| A.升高温度积碳反应I,正反应速率减小,逆反应速率增大,平衡逆向移动 |
B.曲线B表示 平衡时物质的量随温度的变化 平衡时物质的量随温度的变化 |
C.积炭会导致催化剂失活,降低 的平衡转化率 的平衡转化率 |
D.低于600℃时,降低温度有利于减少积炭的量并去除 气体 气体 |
您最近半年使用:0次
5 . 通过计算机模拟发现,甲醇在钯基催化剂表面制氢( )的反应历程如图所示(用“*”表示吸附在他催化剂表面上的物种)。下列相关说法
)的反应历程如图所示(用“*”表示吸附在他催化剂表面上的物种)。下列相关说法不正确 的是
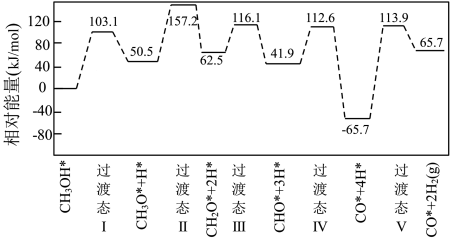
 )的反应历程如图所示(用“*”表示吸附在他催化剂表面上的物种)。下列相关说法
)的反应历程如图所示(用“*”表示吸附在他催化剂表面上的物种)。下列相关说法
A.在经历“过渡态Ⅰ”的过程中 键发生断裂 键发生断裂 |
B.经历“过渡态Ⅱ”的反应 的 的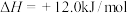 |
| C.经历“过渡态Ⅴ”的反应,控制甲醇制氢的总反应速率 |
D.使用钯基催化剂,能减小反应 的焓变 的焓变 |
您最近半年使用:0次
解题方法
6 . 在酸性条件下,黄铁矿( ,其中S为~1价)催化氧化的反应转化如图所示。
,其中S为~1价)催化氧化的反应转化如图所示。
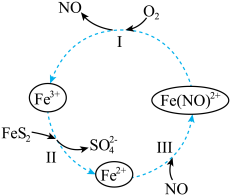
总反应:
(1)分别写出反应Ⅰ、Ⅱ的离子方程式:
①反应Ⅰ:_______ 。
②反应Ⅱ:_______ 。
(2)NO在总反应中的作用是_______ 。
 ,其中S为~1价)催化氧化的反应转化如图所示。
,其中S为~1价)催化氧化的反应转化如图所示。
总反应:

(1)分别写出反应Ⅰ、Ⅱ的离子方程式:
①反应Ⅰ:
②反应Ⅱ:
(2)NO在总反应中的作用是
您最近半年使用:0次
名校
7 . 工业上常采用氨氧化法制硝酸,其流程是将氨和空气混合后通入灼热的铂铑合金网,反应生成NO(g),生成的一氧化氮与残余的氧气继续反应生成二氧化氮:2NO(g)+O2(g) = 2NO2(g);ΔH = -116.4 kJ·mol-1。随后将二氧化氮通入水中制取硝酸。对于反应2NO(g)+O2(g)  2NO2(g),下列说法正确的是
2NO2(g),下列说法正确的是
 2NO2(g),下列说法正确的是
2NO2(g),下列说法正确的是| A.该反应能够自发的原因是ΔS > 0 |
| B.工业上使用合适的催化剂可提高NO2的生产效率 |
| C.升高温度,该反应V(逆)减小,V(正)增大,平衡向逆反应方向移动 |
| D.2 mol NO(g)和1 mol O2(g)中所含化学键能总和比2 mol NO2(g)中大116.4 kJ·mol-1 |
您最近半年使用:0次
8 . 二氧化碳的综合利用具有重要意义。
(1)工业上以 和
和 为原料可以制取合成气(
为原料可以制取合成气( 和
和 )。
)。
①已知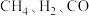 的燃烧热分别为
的燃烧热分别为 ,则反应
,则反应 的
的
________ 。
②将 和
和 以体积比
以体积比 混合后,通过装有催化剂的反应管。下列措施有利于提高
混合后,通过装有催化剂的反应管。下列措施有利于提高 转化率的是
转化率的是________ (填字母)。
a.将反应管控制在催化剂的最大活性温度范围内
b.延长混合气体通过反应管的时间
c.向反应管中加入少量炭粉
(2)电解法转化 可实现
可实现 资源化利用。电解
资源化利用。电解 制
制 的原理如图1所示。
的原理如图1所示。

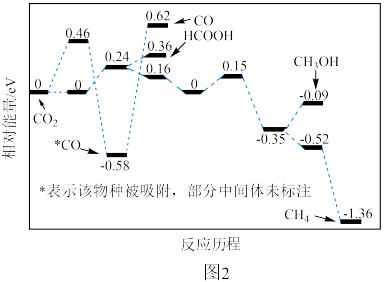
①写出阴极 还原为
还原为 的电极反应式:
的电极反应式:________ 。
②电解一段时间后,阳极区的 溶液浓度降低,其原因是
溶液浓度降低,其原因是________ 。
(3)一种负载活性金属原子催化剂可催化还原 ,在催化剂表面的物质相对能量与反应历程的关系如图2所示。
,在催化剂表面的物质相对能量与反应历程的关系如图2所示。
①反应中催化剂的活性会因为生成 的不断增多而逐渐减弱,原因是
的不断增多而逐渐减弱,原因是________ 。
② 可由中间体
可由中间体 或
或 经过如图3所示2步转化得到。
经过如图3所示2步转化得到。 和
和 的组成相同,催化剂载体中的活性金属带正电性,
的组成相同,催化剂载体中的活性金属带正电性, 与活性金属结合后的相对能量低于
与活性金属结合后的相对能量低于 。在图4方框内画出
。在图4方框内画出 的结构简式
的结构简式________ 。

(1)工业上以
 和
和 为原料可以制取合成气(
为原料可以制取合成气( 和
和 )。
)。①已知
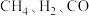 的燃烧热分别为
的燃烧热分别为 ,则反应
,则反应 的
的
②将
 和
和 以体积比
以体积比 混合后,通过装有催化剂的反应管。下列措施有利于提高
混合后,通过装有催化剂的反应管。下列措施有利于提高 转化率的是
转化率的是a.将反应管控制在催化剂的最大活性温度范围内
b.延长混合气体通过反应管的时间
c.向反应管中加入少量炭粉
(2)电解法转化
 可实现
可实现 资源化利用。电解
资源化利用。电解 制
制 的原理如图1所示。
的原理如图1所示。

①写出阴极
 还原为
还原为 的电极反应式:
的电极反应式:②电解一段时间后,阳极区的
 溶液浓度降低,其原因是
溶液浓度降低,其原因是(3)一种负载活性金属原子催化剂可催化还原
 ,在催化剂表面的物质相对能量与反应历程的关系如图2所示。
,在催化剂表面的物质相对能量与反应历程的关系如图2所示。①反应中催化剂的活性会因为生成
 的不断增多而逐渐减弱,原因是
的不断增多而逐渐减弱,原因是②
 可由中间体
可由中间体 或
或 经过如图3所示2步转化得到。
经过如图3所示2步转化得到。 和
和 的组成相同,催化剂载体中的活性金属带正电性,
的组成相同,催化剂载体中的活性金属带正电性, 与活性金属结合后的相对能量低于
与活性金属结合后的相对能量低于 。在图4方框内画出
。在图4方框内画出 的结构简式
的结构简式
您最近半年使用:0次
9 . 一种燃煤烟气中 的捕集和资源再利用技术可通过如下转化过程实现。
的捕集和资源再利用技术可通过如下转化过程实现。
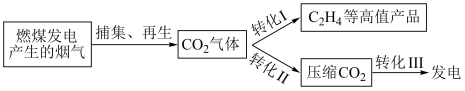
转化I是利用风/太阳能电厂过剩电力,将 转化为
转化为 等高值产品。
等高值产品。
转化II是利用风/太阳能电厂过剩电力驱动压缩机压缩 。
。
转化III是风/太阳能电厂发电低谷时,利用压缩 推动汽轮机,带动发电机发电。
推动汽轮机,带动发电机发电。
(1)利用氨水可捕集烟气中的 捕集、再生过程中含碳物种的变化如图所示。
捕集、再生过程中含碳物种的变化如图所示。

①液相中 发生转化:
发生转化: 。X的结构式为
。X的结构式为___________ 。
②已知: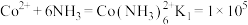

反应 的平衡常数
的平衡常数
___________ 。
③转化后的溶液通过反应 解吸释放
解吸释放 。向两份相同的转化后的溶液中分别加入等体积、等浓度的
。向两份相同的转化后的溶液中分别加入等体积、等浓度的 和
和 溶液,加入
溶液,加入 溶液后释放
溶液后释放 效果更好的原因是
效果更好的原因是___________ 。
(2)以过渡金属作催化剂,利用如图所示装置可实现“转化1”。
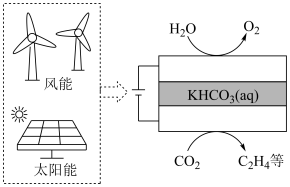
①写出阴极表面的电极反应方程式:___________ 。
②在金属催化剂表面发生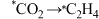 转化的过程可能为
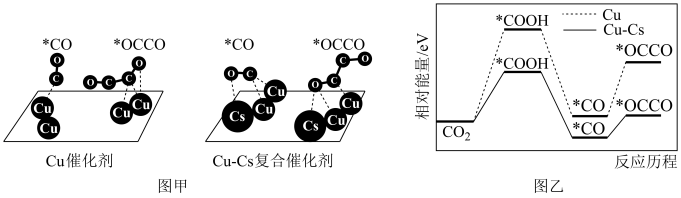
转化的过程可能为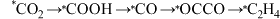 (*表示吸附在催化剂表面)。其中部分物种在催化剂表面的吸附构型如图甲所示,反应历程中的相对能量如图乙所示。与Cu催化剂相比,掺杂了Cs的
(*表示吸附在催化剂表面)。其中部分物种在催化剂表面的吸附构型如图甲所示,反应历程中的相对能量如图乙所示。与Cu催化剂相比,掺杂了Cs的 复合催化剂更有利于
复合催化剂更有利于 的形成,可能原因是
的形成,可能原因是___________ 。
(3)从物质转化与资源综合利用角度分析,本工艺中 的捕集和资源再利用技术的优点是
的捕集和资源再利用技术的优点是___________ 。
 的捕集和资源再利用技术可通过如下转化过程实现。
的捕集和资源再利用技术可通过如下转化过程实现。
转化I是利用风/太阳能电厂过剩电力,将
 转化为
转化为 等高值产品。
等高值产品。转化II是利用风/太阳能电厂过剩电力驱动压缩机压缩
 。
。转化III是风/太阳能电厂发电低谷时,利用压缩
 推动汽轮机,带动发电机发电。
推动汽轮机,带动发电机发电。(1)利用氨水可捕集烟气中的
 捕集、再生过程中含碳物种的变化如图所示。
捕集、再生过程中含碳物种的变化如图所示。
①液相中
 发生转化:
发生转化: 。X的结构式为
。X的结构式为②已知:
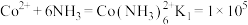

反应
 的平衡常数
的平衡常数
③转化后的溶液通过反应
 解吸释放
解吸释放 。向两份相同的转化后的溶液中分别加入等体积、等浓度的
。向两份相同的转化后的溶液中分别加入等体积、等浓度的 和
和 溶液,加入
溶液,加入 溶液后释放
溶液后释放 效果更好的原因是
效果更好的原因是(2)以过渡金属作催化剂,利用如图所示装置可实现“转化1”。

①写出阴极表面的电极反应方程式:
②在金属催化剂表面发生
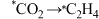 转化的过程可能为
转化的过程可能为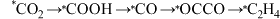 (*表示吸附在催化剂表面)。其中部分物种在催化剂表面的吸附构型如图甲所示,反应历程中的相对能量如图乙所示。与Cu催化剂相比,掺杂了Cs的
(*表示吸附在催化剂表面)。其中部分物种在催化剂表面的吸附构型如图甲所示,反应历程中的相对能量如图乙所示。与Cu催化剂相比,掺杂了Cs的 复合催化剂更有利于
复合催化剂更有利于 的形成,可能原因是
的形成,可能原因是
(3)从物质转化与资源综合利用角度分析,本工艺中
 的捕集和资源再利用技术的优点是
的捕集和资源再利用技术的优点是
您最近半年使用:0次
名校
10 . 氢气是一种理想的绿色清洁能源,氢气的制取是氢能源利用领域的研究热点。
(1)用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O可制H2。
①氧缺位铁酸铜通过两步反应分解水制氢。已知第二步反应为2CuFe2O4=2CuFe2O4-x+xO2↑,则第一步反应的化学方程式为___________ 。
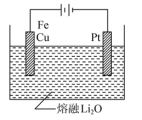
②CuFe2O4可用电化学方法得到,其原理如图所示,则阳极的电极反应式为___________ 。
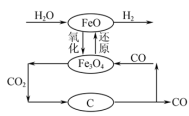
(2)可利用FeO/Fe3O4之间的相互转化,来裂解水制取氢气,其制氢流程如图所示。该工艺制氢的总反应为C(s)+H2O(g)=CO(g)+H2(g),对比水和碳在高温下直接接触反应制氢,分析该工艺制氢的最大优点是___________ 。
(3)硼氢化钠(NaBH4)的强碱溶液在催化剂作用下与水反应可获取氢气,其可能反应机理如图所示。已知:常温下,NaB(OH)4在水中的溶解度不大,易以NaBO2形式结晶析出。
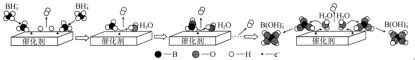
①若用D2O代替H2O,依据反应机理,则反应后生成的气体中含有___________ 。
②其他条件相同时,测得平均每克催化剂使用量下,NaBH4的浓度和放氢速率的变化关系如图所示。随着NaBH4浓度的增大,放氢速率先增大后减小,导致放氢速率下降的原因可能是___________ 。

(1)用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O可制H2。
①氧缺位铁酸铜通过两步反应分解水制氢。已知第二步反应为2CuFe2O4=2CuFe2O4-x+xO2↑,则第一步反应的化学方程式为
②CuFe2O4可用电化学方法得到,其原理如图所示,则阳极的电极反应式为

(2)可利用FeO/Fe3O4之间的相互转化,来裂解水制取氢气,其制氢流程如图所示。该工艺制氢的总反应为C(s)+H2O(g)=CO(g)+H2(g),对比水和碳在高温下直接接触反应制氢,分析该工艺制氢的最大优点是

(3)硼氢化钠(NaBH4)的强碱溶液在催化剂作用下与水反应可获取氢气,其可能反应机理如图所示。已知:常温下,NaB(OH)4在水中的溶解度不大,易以NaBO2形式结晶析出。

①若用D2O代替H2O,依据反应机理,则反应后生成的气体中含有
②其他条件相同时,测得平均每克催化剂使用量下,NaBH4的浓度和放氢速率的变化关系如图所示。随着NaBH4浓度的增大,放氢速率先增大后减小,导致放氢速率下降的原因可能是

您最近半年使用:0次



