1 . 研究CO2、H2的开发利用意义重大。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),反应过程中的能量变化情况如图所示。请按要求回答下列问题:
CH3OH(g)+H2O(g),反应过程中的能量变化情况如图所示。请按要求回答下列问题:
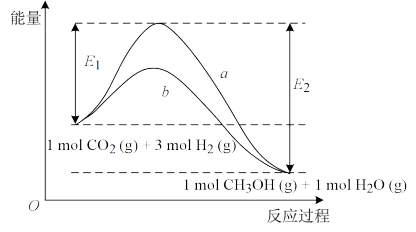
(1)曲线a和曲线b分别表示不使用催化剂和使用催化剂的两种情况。该反应是___ (填“吸热”或“放热”)反应。计算当反应生成2molCH3OH(g)时能量变化是___ (用E1、E2表示)。
(2)选择适宜的催化剂是___ (填“能”或“不能”)改变该反应的能量变化。
(3)下列说法一定正确的是___ (填选项字母)。
A.a与b相比,a表示的反应速度较大
B.反应物断裂化学键吸收的总能量小于生成物形成化学键释放的总能量
C.CO2(g)和H2(g)所具有的总能量一定高于CH3OH(g)和H2O(g)所具有的总能量
(4)推测反应CH3OH(g)+H2O(g) CO2(g)+3H2(g)是
CO2(g)+3H2(g)是___ (填“吸热”或“放热”)反应。
 CH3OH(g)+H2O(g),反应过程中的能量变化情况如图所示。请按要求回答下列问题:
CH3OH(g)+H2O(g),反应过程中的能量变化情况如图所示。请按要求回答下列问题: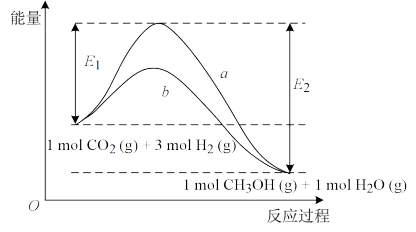
(1)曲线a和曲线b分别表示不使用催化剂和使用催化剂的两种情况。该反应是
(2)选择适宜的催化剂是
(3)下列说法一定正确的是
A.a与b相比,a表示的反应速度较大
B.反应物断裂化学键吸收的总能量小于生成物形成化学键释放的总能量
C.CO2(g)和H2(g)所具有的总能量一定高于CH3OH(g)和H2O(g)所具有的总能量
(4)推测反应CH3OH(g)+H2O(g)
 CO2(g)+3H2(g)是
CO2(g)+3H2(g)是
您最近半年使用:0次
解题方法
2 . 某同学设计了探究影响反应速率因素的如下两组实验,该同学探究的影响因素是
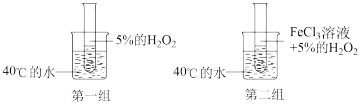
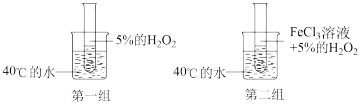
| A.浓度 | B.压强 | C.温度 | D.催化剂 |
您最近半年使用:0次
2020-07-22更新
|
152次组卷
|
3卷引用:海南省东方市琼西中学2019-2020学年高一第二次月考化学试题
名校
解题方法
3 . 中国首条“生态马路”在上海复兴路隧道建成,它运用了“光触媒”技术,在路面涂上一种光催化剂涂料,可将汽车尾气中45%的NO和CO转化成N2 和CO2。下列对此反应的叙述中正确的是
| A.使用光催化剂不改变反应速率 |
| B.该“光触媒”技术可以杜绝“光化学烟雾”的产生 |
| C.升高温度能加快反应速率 |
| D.改变压强对反应速率无影响 |
您最近半年使用:0次
2020-07-01更新
|
626次组卷
|
14卷引用:海南省琼海市嘉积中学2021-2022学年高一下学期期末考试化学试题
海南省琼海市嘉积中学2021-2022学年高一下学期期末考试化学试题辽宁省六校2019-2020学年高一下学期期中考试化学试卷辽宁省阜新市第二高级中学2019-2020学年高一下学期期末考试化学试题河北省邢台市第二中学2020-2021学年高二上学期开学摸底考试化学试题山西省临猗县临晋中学2020-2021学年高二9月月考化学试题(已下线)【浙江新东方】绍兴qw122(已下线)专题06 化学反应速率和化学平衡——备战2021年高考化学纠错笔记江西省赣州市十六县(市)十七校2020-2021学年高一下学期期中联考化学试题甘肃省庆阳市第六中学2020-2021学年高一下学期期中考试化学(理)试题浙江省丽水外国语学校高中部2021-2022学年高二上学期第一次月考(10月)化学试题广东省深圳市宝安中学高中部2020-2021学年高一下学期期中考试化学试卷 辽宁省阜新市第二高级中学2022-2023学年高一下学期期末考试化学试卷广东省东莞市东华高级中学2023-2024学年高一下学期前段考试化学试题广东省广州市育才中学2023-2024学年高一下学期 期中考试化学试题
名校
解题方法
4 . 在 催化作用下,
催化作用下, 被
被 氧化为
氧化为 的机理如下:
的机理如下:
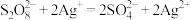 慢
慢
 快
快
下列有关说法正确的是
 催化作用下,
催化作用下, 被
被 氧化为
氧化为 的机理如下:
的机理如下: 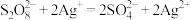 慢
慢 快
快下列有关说法正确的是
A.反应速率与 的浓度有关 的浓度有关 |
B. 也是该反应的催化剂 也是该反应的催化剂 |
C. 能降低该反应的活化能和焓变 能降低该反应的活化能和焓变 |
D.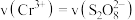 |
您最近半年使用:0次
2020-01-26更新
|
147次组卷
|
9卷引用:海南儋州市第一中学2020-2021学年高二上学期第一次月考化学试题
海南儋州市第一中学2020-2021学年高二上学期第一次月考化学试题河北省衡水中学2016-2017学年高一下学期三调考试化学试题辽宁省大连育明高级中学2018届高三人教版选修四9.8同步测试化学试题(已下线)考点12 化学反应速率化学平衡——《备战2020年高考精选考点专项突破题集》山东省青岛市第58中学2018-2019学年高二上学期期中考试化学试题2020届高三化学二轮冲刺新题专练——影响化学反应速率的因素(提升练)湖南省湘西土家族苗族自治州花垣县边城高级中学2020-2021学年高二上学期入学考试化学试题甘肃省天水市第六中学2019-2020学年高二上学期期末考试化学试题(重点班)广东省佛山市南海区狮山石门高级中学2023-2024学年高二上学期第二次月考化学试题
名校
5 . 下列说法中正确的是( )
| A.NaOH溶液与稀盐酸反应的活化能几乎为零 |
| B.活化分子之间发生的碰撞一定是有效碰撞 |
| C.升高温度和增大压强都可以提高反应体系内活化分子百分数 |
| D.催化剂可以改变反应的活化能,可以提高活化分子百分数,但是不能改变反应热 |
您最近半年使用:0次
名校
6 . 下列关于化学反应速率的说法正确的是( )
| A.反应4Fe(s)+3O2(g)=2Fe2O3(s)常温下可自发进行,该反应为吸热反应 |
| B.0.1mol·L-1盐酸和0.1mol·L-1硝酸与相同形状和大小的大理石反应的速率相同 |
| C.在相同温度下,两个相同的容器中,分别充入相同物质的量的Br2和Cl2,让它们与等量的氢气发生反应,反应速率相同 |
| D.有气体参加的化学反应,若增大压强(即缩小反应容器的容积),可增加活化分子的百分数,从而使反应速率加快 |
您最近半年使用:0次
名校
解题方法
7 . 某课外兴趣小组对H2O2的分解速率做了如下实验探究。
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:用10mL H2O2制取150mLO2所需的时间(秒)
①该研究小组在设计方案时。考虑了浓度、___________ 、____________ 等因素对过氧化氢分解速率的影响。
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响?_______________________ 。
(2)将质量相同但聚集状态不同的MnO2分别加入到5mL 5%(密度为1.0g/cm3)的双氧水中,并用带火星的木条测试。测定结果如下:
① 写出H2O2发生分解的化学反应方程式________________ 。求出实验A中H2O2在5分钟内的平均反应速率________________ 。(结果保留小数点后两位数字)
② 实验结果说明催化剂作用的大小与____________________ 有关。
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:用10mL H2O2制取150mLO2所需的时间(秒)
 | 30% H2O2 | 15% H2O2 | 10% H2O2 | 5% H2O2 |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 360 | 480 | 540 | 720 |
| MnO2催化剂、加热 | 10 | 25 | 60 | 120 |
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响?
(2)将质量相同但聚集状态不同的MnO2分别加入到5mL 5%(密度为1.0g/cm3)的双氧水中,并用带火星的木条测试。测定结果如下:
| 实验 序号 | 催化剂(MnO2) | 操作 情况 | 观察结果 | 反应完成 所需的时间 |
| A | 粉末状 | 混合不振荡 | 剧烈反应,带火星的木条复燃 | 5分钟 |
| B | 块状 | 反应较慢,火星红亮但木条未复燃 | 30分钟 |
② 实验结果说明催化剂作用的大小与
您最近半年使用:0次
名校
解题方法
8 . 下列有关化学反应速率的说法中,不正确的是
| A.实验室用H2O2分解制O2,加入MnO2后,反应速率明显加快 |
| B.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使反应速率增大 |
| C.可用单位时间内氢离子物质的量浓度的变化来表示NaOH和H2SO4反应的速率 |
| D.实验室用碳酸钙和盐酸反应制取CO2,用碳酸钙粉末比块状反应要快 |
您最近半年使用:0次
2020-01-01更新
|
92次组卷
|
2卷引用:海南省文昌中学2019-2020学年高二上学期第二次月考化学试题
9 . 在下列事实中,各是什么因素影响了化学反应的速率。
(1)黄铁矿煅烧时要粉碎成细小颗粒______________ ;
(2)夏天的食品变霉,在冬天不易发生该现象_____________ ;
(3)同浓度同体积的盐酸中放入同样大小的锌粒和镁块,产生气体快慢程度不同__ ;
(4)同样大小的石灰石分别在0.1 mol·L-1的盐酸和1 mol·L-1的盐酸中反应速度不同_____________ ;
(5)熔化的KClO3放出气泡很慢,撒入MnO2少量很快产生气体__________ ;
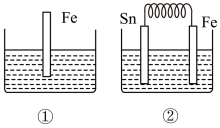
(6)如下图,铁在海水中的腐蚀速度是②比①快______ 。
(1)黄铁矿煅烧时要粉碎成细小颗粒
(2)夏天的食品变霉,在冬天不易发生该现象
(3)同浓度同体积的盐酸中放入同样大小的锌粒和镁块,产生气体快慢程度不同
(4)同样大小的石灰石分别在0.1 mol·L-1的盐酸和1 mol·L-1的盐酸中反应速度不同
(5)熔化的KClO3放出气泡很慢,撒入MnO2少量很快产生气体
(6)如下图,铁在海水中的腐蚀速度是②比①快

您最近半年使用:0次
10 . 控制变量法是化学实验的常用方法之一,下图所示实验探究影响反应速率的因素是


| A.催化剂 | B.温度 |
| C.压强 | D.浓度 |
您最近半年使用:0次
2019-11-05更新
|
206次组卷
|
4卷引用:海南省东方市八所中学2018-2019学年高一下学期期中联考化学试题



