解题方法
1 . 卤代烃在有机物转化过程中有着重要的作用,卤代烃通过不同的反应可以转化成其它类型的化合物,因此研究卤代烃反应的历程及实质很有意义。回答下列问题:
(1)一定温度下,丙烷的氯化、溴化过程中决速步反应能量图及一段时间后产物的选择性如图所示:
_____________  (用
(用 和
和 表示);升高温度时,丙烷的氯化体系中n (1-氯丙烷)与n(2-氯丙烷)的比值
表示);升高温度时,丙烷的氯化体系中n (1-氯丙烷)与n(2-氯丙烷)的比值_________ (填“增大”“减小”或“不变”)。
②以丙烷为原料通过“卤代-水解”过程合成2-丙醇时,为了提高2-丙醇的含量,可以采取的措施为_____________ (填“先氯代再水解”或“先溴代再水解”),理由为_________________________________ 。
(2)丙烯与氯气可发生的反应:
Ⅰ:CH2=CHCH3(g)+Cl2(g) CH2ClCHClCH3(g)
CH2ClCHClCH3(g) 
Ⅱ:CH2=CHCH3(g)+Cl2(g) CH2=CHCH2Cl(g)+HCl(g)
CH2=CHCH2Cl(g)+HCl(g) 
①将 和
和 的混合气体以一定流速通过填充有催化剂的反应器,出口气中含有CH2=CHCH3、Cl2、CH2ClCHClCH3、CH2=CHCH2Cl、HCl。实验测得Cl2的转化率与温度、压强的关系如图所示。已知T1>T2>T3,下列有关说法正确的是
的混合气体以一定流速通过填充有催化剂的反应器,出口气中含有CH2=CHCH3、Cl2、CH2ClCHClCH3、CH2=CHCH2Cl、HCl。实验测得Cl2的转化率与温度、压强的关系如图所示。已知T1>T2>T3,下列有关说法正确的是_________ (填序号)。
B.图中T1、T2、T3时反应均未达到平衡状态
C.达到平衡状态时所需要的时间a>b
D.反应Ⅰ在低温下可以自发进行
②一定温度下,向填充有催化剂的恒容密闭容器中以物质的量之比为2:1充入CH2=CHCH3和Cl2。实验测得反应前容器内气体压强为300kPa,平衡时容器内气体压强为240kPa,HCl的分压为30kPa。则CH2=CHCH3的平衡转化率为_____________ ;反应Ⅱ的平衡常数Kp=_____________ (用平衡时的分压表示)。
③分子筛膜反应器可提高反应Ⅱ的平衡转化率,进而增大CH2=CHCH2Cl的选择性,原理如图所示。分子筛膜反应器可以提高反应Ⅱ的转化率的原因为_________________ 。
(1)一定温度下,丙烷的氯化、溴化过程中决速步反应能量图及一段时间后产物的选择性如图所示:


 (用
(用 和
和 表示);升高温度时,丙烷的氯化体系中n (1-氯丙烷)与n(2-氯丙烷)的比值
表示);升高温度时,丙烷的氯化体系中n (1-氯丙烷)与n(2-氯丙烷)的比值②以丙烷为原料通过“卤代-水解”过程合成2-丙醇时,为了提高2-丙醇的含量,可以采取的措施为
(2)丙烯与氯气可发生的反应:
Ⅰ:CH2=CHCH3(g)+Cl2(g)
 CH2ClCHClCH3(g)
CH2ClCHClCH3(g) 
Ⅱ:CH2=CHCH3(g)+Cl2(g)
 CH2=CHCH2Cl(g)+HCl(g)
CH2=CHCH2Cl(g)+HCl(g) 
①将
 和
和 的混合气体以一定流速通过填充有催化剂的反应器,出口气中含有CH2=CHCH3、Cl2、CH2ClCHClCH3、CH2=CHCH2Cl、HCl。实验测得Cl2的转化率与温度、压强的关系如图所示。已知T1>T2>T3,下列有关说法正确的是
的混合气体以一定流速通过填充有催化剂的反应器,出口气中含有CH2=CHCH3、Cl2、CH2ClCHClCH3、CH2=CHCH2Cl、HCl。实验测得Cl2的转化率与温度、压强的关系如图所示。已知T1>T2>T3,下列有关说法正确的是
B.图中T1、T2、T3时反应均未达到平衡状态
C.达到平衡状态时所需要的时间a>b
D.反应Ⅰ在低温下可以自发进行
②一定温度下,向填充有催化剂的恒容密闭容器中以物质的量之比为2:1充入CH2=CHCH3和Cl2。实验测得反应前容器内气体压强为300kPa,平衡时容器内气体压强为240kPa,HCl的分压为30kPa。则CH2=CHCH3的平衡转化率为
③分子筛膜反应器可提高反应Ⅱ的平衡转化率,进而增大CH2=CHCH2Cl的选择性,原理如图所示。分子筛膜反应器可以提高反应Ⅱ的转化率的原因为

您最近一年使用:0次
2 . 我国向国际社会承诺2030年“碳达峰”,2060年实现“碳中和”。为了实现这些目标,对 的研究成为科技界关注的重点,下面是一些可使
的研究成为科技界关注的重点,下面是一些可使 转化为高附加值化学品的反应,请回答相关问题:
转化为高附加值化学品的反应,请回答相关问题:
(1)工业上以 、
、 为原料生产尿素
为原料生产尿素 ,反应实际分两步进行:
,反应实际分两步进行:
Ⅰ: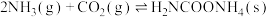
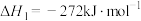
Ⅱ: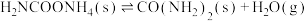

已知:

①请写出以 、
、 为原料,合成尿素和液态水的热化学方程式:
为原料,合成尿素和液态水的热化学方程式:___________ 。
② 时,在
时,在 的密闭容器中充入
的密闭容器中充入 和
和 模拟工业生产,
模拟工业生产, ,如图是
,如图是 平衡转化率(
平衡转化率( )与
)与 的关系。计算图中
的关系。计算图中 点
点 的平衡转化率
的平衡转化率
___________ (填分数)。

(2)二氧化碳催化加氢合成乙烯是综合利用 的热点研究领域。
的热点研究领域。
①在恒温恒容的密闭容器中通入一定量的 和
和 发生反应:
发生反应:
 ,下列能说明该反应达到平衡状态的是
,下列能说明该反应达到平衡状态的是___________ (填字母)。
A.容器内的压强不再发生变化
B.生成的乙烯和水蒸气物质的量之比为
C.断裂 键的同时生成
键的同时生成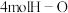 键
键
D.混合气体的总质量不随时间改变
②理论计算表明,原料初始组成 ,在体系压强为
,在体系压强为 ,反应达到平衡时,四种组分的物质的量分数(x)随温度(T)的变化如图所示。表示
,反应达到平衡时,四种组分的物质的量分数(x)随温度(T)的变化如图所示。表示 变化的曲线是
变化的曲线是___________ 。 催化加氢合成
催化加氢合成 反应的
反应的
___________ 0(填“>”或“<”)。

(3) 在催化剂下可与
在催化剂下可与 同时发生如下反应Ⅰ、Ⅱ,得到燃料。
同时发生如下反应Ⅰ、Ⅱ,得到燃料。
Ⅰ.

Ⅱ.

①若要提高反应Ⅰ的选择性,最佳措施是___________ (填字母)。
A.缩小容器体积 B.降低温度 C.升高温度 D.使用合适的催化剂
②在 存在的条件下,保持温度
存在的条件下,保持温度 不变,在一刚性密闭容器中充入一定量的
不变,在一刚性密闭容器中充入一定量的 及
及 ,发生上面两个反应,起始及达平衡时,容器内各气体物质的量如下表:
,发生上面两个反应,起始及达平衡时,容器内各气体物质的量如下表:
若反应Ⅰ、Ⅱ均达平衡时, ,则表中
,则表中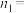
___________ ;若此时 ,则反应Ⅱ的平衡常数
,则反应Ⅱ的平衡常数
___________ 。[已知:气体各组分的分压=总压×其体积分数]
 的研究成为科技界关注的重点,下面是一些可使
的研究成为科技界关注的重点,下面是一些可使 转化为高附加值化学品的反应,请回答相关问题:
转化为高附加值化学品的反应,请回答相关问题:(1)工业上以
 、
、 为原料生产尿素
为原料生产尿素 ,反应实际分两步进行:
,反应实际分两步进行:Ⅰ:
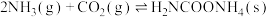
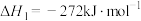
Ⅱ:
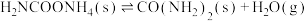

已知:


①请写出以
 、
、 为原料,合成尿素和液态水的热化学方程式:
为原料,合成尿素和液态水的热化学方程式:②
 时,在
时,在 的密闭容器中充入
的密闭容器中充入 和
和 模拟工业生产,
模拟工业生产, ,如图是
,如图是 平衡转化率(
平衡转化率( )与
)与 的关系。计算图中
的关系。计算图中 点
点 的平衡转化率
的平衡转化率

(2)二氧化碳催化加氢合成乙烯是综合利用
 的热点研究领域。
的热点研究领域。①在恒温恒容的密闭容器中通入一定量的
 和
和 发生反应:
发生反应:
 ,下列能说明该反应达到平衡状态的是
,下列能说明该反应达到平衡状态的是A.容器内的压强不再发生变化
B.生成的乙烯和水蒸气物质的量之比为

C.断裂
 键的同时生成
键的同时生成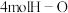 键
键D.混合气体的总质量不随时间改变
②理论计算表明,原料初始组成
 ,在体系压强为
,在体系压强为 ,反应达到平衡时,四种组分的物质的量分数(x)随温度(T)的变化如图所示。表示
,反应达到平衡时,四种组分的物质的量分数(x)随温度(T)的变化如图所示。表示 变化的曲线是
变化的曲线是 催化加氢合成
催化加氢合成 反应的
反应的

(3)
 在催化剂下可与
在催化剂下可与 同时发生如下反应Ⅰ、Ⅱ,得到燃料。
同时发生如下反应Ⅰ、Ⅱ,得到燃料。Ⅰ.


Ⅱ.


①若要提高反应Ⅰ的选择性,最佳措施是
A.缩小容器体积 B.降低温度 C.升高温度 D.使用合适的催化剂
②在
 存在的条件下,保持温度
存在的条件下,保持温度 不变,在一刚性密闭容器中充入一定量的
不变,在一刚性密闭容器中充入一定量的 及
及 ,发生上面两个反应,起始及达平衡时,容器内各气体物质的量如下表:
,发生上面两个反应,起始及达平衡时,容器内各气体物质的量如下表:| 状态 |  |  |  |  |  | 总压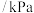 |
起始 | 5 | 7 | 0 | 0 | 0 |  |
平衡 |  |  |  |
 ,则表中
,则表中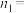
 ,则反应Ⅱ的平衡常数
,则反应Ⅱ的平衡常数
您最近一年使用:0次
名校
3 . 2020年9月22日,国家主席习近平在第七十五届联合国大会上宣布:“中国力争在2030年前 排放达到峰值,努力争取2060年前实现碳中和目标。”中国科学院马延和团队发表于Science上的论文成果显示:实验室条件下,只需4个小时11步就能合成淀粉,其中关键步骤是
排放达到峰值,努力争取2060年前实现碳中和目标。”中国科学院马延和团队发表于Science上的论文成果显示:实验室条件下,只需4个小时11步就能合成淀粉,其中关键步骤是 转化为甲醇:
转化为甲醇: 。
。
1.现研究温度对于甲醇产率的影响。在210℃~290℃,保持原料气中 和
和 的投料比不变,得到甲醇实际产率、平衡产率与温度的关系如图,图中实线代表的是
的投料比不变,得到甲醇实际产率、平衡产率与温度的关系如图,图中实线代表的是___________ 。
2.由此判断
___________ 0(填“>”、“=”或“<”),请分别阐述你做出上述实线选择和判断 的依据
的依据___________ 。
3.该反应的自发条件是___________ 。
A.高温自发 B.低温自发 C.任何温度下都自发
4.恒温恒容条件下,有利于提高 的平衡转化率的措施有
的平衡转化率的措施有
5.向恒温恒容容器中投入2mol  和等量
和等量 ,下列能说明该反应已达平衡状态的是
,下列能说明该反应已达平衡状态的是
 除了能转化为
除了能转化为 外,还可以和
外,还可以和 反应生成CO:
反应生成CO:
其化学平衡常数和温度的关系如下表所示:
6.某温度下,平衡浓度符合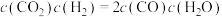 ,此时温度介于___________范围。
,此时温度介于___________范围。
7.在820℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为: 、
、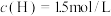 、
、 、
、 ,则下一时刻,反应向___________进行。
,则下一时刻,反应向___________进行。
 排放达到峰值,努力争取2060年前实现碳中和目标。”中国科学院马延和团队发表于Science上的论文成果显示:实验室条件下,只需4个小时11步就能合成淀粉,其中关键步骤是
排放达到峰值,努力争取2060年前实现碳中和目标。”中国科学院马延和团队发表于Science上的论文成果显示:实验室条件下,只需4个小时11步就能合成淀粉,其中关键步骤是 转化为甲醇:
转化为甲醇: 。
。1.现研究温度对于甲醇产率的影响。在210℃~290℃,保持原料气中
 和
和 的投料比不变,得到甲醇实际产率、平衡产率与温度的关系如图,图中实线代表的是
的投料比不变,得到甲醇实际产率、平衡产率与温度的关系如图,图中实线代表的是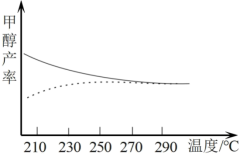
2.由此判断

 的依据
的依据3.该反应的自发条件是
A.高温自发 B.低温自发 C.任何温度下都自发
4.恒温恒容条件下,有利于提高
 的平衡转化率的措施有
的平衡转化率的措施有| A.使用催化剂 | B.加压 |
C.减小 和 和 的初始投料比 的初始投料比 | D.平衡后,同等比例的增加反应物的量 |
 和等量
和等量 ,下列能说明该反应已达平衡状态的是
,下列能说明该反应已达平衡状态的是A. 体积分数保持不变 体积分数保持不变 | B.气体的密度不再变化 |
| C.混合气体的平均摩尔质量不再变化 | D.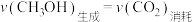 |
 除了能转化为
除了能转化为 外,还可以和
外,还可以和 反应生成CO:
反应生成CO:
其化学平衡常数和温度的关系如下表所示:
| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
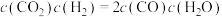 ,此时温度介于___________范围。
,此时温度介于___________范围。| A.<700℃ | B.700-800℃ | C.1000-1200℃ | D.无法判断 |
 、
、 、
、 、
、 ,则下一时刻,反应向___________进行。
,则下一时刻,反应向___________进行。| A.正向 | B.逆向 | C.不移动 | D.无法判断 |
您最近一年使用:0次
名校
解题方法
4 . I.合成氨工业和硫酸工业在国民经济中占有重要地位。
(1)在合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:[Cu(NH3)2]++CO+NH3⇌[Cu(NH3)3CO]+ △H<0。吸收CO后的铜氨液经过适当处理可再生,恢复其吸收CO的能力,可循环使用。铜氨液再生适宜的生产条件是___________。(填选项)
(2)将等物质的量的H2和N2通入绝热恒容密闭容器中发生反应N2(g)+3H2(g)⇌2NH3(g) △H<0,下列选项表明反应一定已达平衡状态的是___________(填标号,下同)。
II.接触法制硫酸的关键反应为SO2的催化氧化,二氧化硫在V2O5作用下的催化氧化是工业上生产硫酸的主要反应。SO2的催化氧化热化学方程式为:2SO2(g)+O2(g)⇌2SO3(g) △H=akJ·mol-1。其催化机理分为三步:
第1步:SO2(g)+V2O5(s)⇌SO3(g)+V2O4(s) △H=bkJ·mol-1
第2步:V2O4(s)+O2(g)+2SO2(g)⇌2VOSO4(s) △H=ckJ·mol-1
第3步:___________。
(3)第3步热化学方程式___________ (△H的值用a、b、c的代数式表示)。
(4)T℃时,将3molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生反应。3min时反应达到平衡,此时测得O2还剩余0.1mol。则达平衡时SO2的转化率为___________ ;从反应开始至达到平衡,用SO3表示反应速率为___________ 。
(5)设O2的平衡分压为p,SO2的平衡转化率为α,用含p和α的代数式表示上述催化氧化反应的Kp=___________ (用平衡分压代替平衡浓度计算)。
(6)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度的关系如下图所示,下列说法正确的是___________。

(7)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如图所示,催化性能最佳的是___________ (填标号)。

(1)在合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:[Cu(NH3)2]++CO+NH3⇌[Cu(NH3)3CO]+ △H<0。吸收CO后的铜氨液经过适当处理可再生,恢复其吸收CO的能力,可循环使用。铜氨液再生适宜的生产条件是___________。(填选项)
| A.高温高压 | B.高温低压 | C.低温低压 | D.低温高压 |
(2)将等物质的量的H2和N2通入绝热恒容密闭容器中发生反应N2(g)+3H2(g)⇌2NH3(g) △H<0,下列选项表明反应一定已达平衡状态的是___________(填标号,下同)。
| A.容器内的压强不再变化 |
| B.相同时间内,断开H-H键的数目和生成N-H键的数目相等 |
| C.容器内气体的浓度c(N2):c(H2):c(NH3)=1:3:2 |
| D.N2的体积分数不再发生变化 |
II.接触法制硫酸的关键反应为SO2的催化氧化,二氧化硫在V2O5作用下的催化氧化是工业上生产硫酸的主要反应。SO2的催化氧化热化学方程式为:2SO2(g)+O2(g)⇌2SO3(g) △H=akJ·mol-1。其催化机理分为三步:
第1步:SO2(g)+V2O5(s)⇌SO3(g)+V2O4(s) △H=bkJ·mol-1
第2步:V2O4(s)+O2(g)+2SO2(g)⇌2VOSO4(s) △H=ckJ·mol-1
第3步:___________。
(3)第3步热化学方程式
(4)T℃时,将3molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生反应。3min时反应达到平衡,此时测得O2还剩余0.1mol。则达平衡时SO2的转化率为
(5)设O2的平衡分压为p,SO2的平衡转化率为α,用含p和α的代数式表示上述催化氧化反应的Kp=
(6)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度的关系如下图所示,下列说法正确的是___________。

| A.温度越高,反应速率越大 |
| B.可根据不同α下的最大速率,选择最佳生产温度 |
| C.α=0.88的曲线代表平衡转化率 |
| D.α越大,反应速率最大值对应温度越低 |
(7)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如图所示,催化性能最佳的是

您最近一年使用:0次
5 . 二氧化碳的回收利用是环保领域研究的热点课题。结合所学知识回答下列问题:
Ⅰ.利用太阳能实现 制取某些物质是一种非常理想的
制取某些物质是一种非常理想的 减排途径。
减排途径。
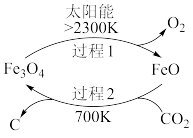
(1)在太阳能的作用下,以 为原料制取炭黑的流程如图所示。其总反应的化学方程式为
为原料制取炭黑的流程如图所示。其总反应的化学方程式为___________ 。
(2)以稀硫酸为电解质溶液,利用太阳能将 转化为低碳烯烃,工作原理如图:
转化为低碳烯烃,工作原理如图:
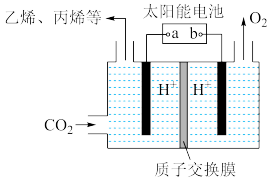
①b是电源的___________ (填“正”或“负”)极。
②生成乙烯( )的电极反应式为
)的电极反应式为___________ 。
③电场作用下,氢离子从___________ (填:“从左到右”或“从右到左”)移动。
Ⅱ.通过化学的方法实现 的资源化利用也是一种非常理想的
的资源化利用也是一种非常理想的 减排途径。
减排途径。
(3)工业上用 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:
 ;
;
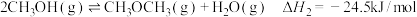 。
。
则 反应的
反应的
___________  。
。
(4)已知该反应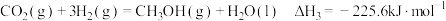 ,在恒温恒压下进行,以下叙述能说明该反应达到平衡状态的是___________(填序号)。
,在恒温恒压下进行,以下叙述能说明该反应达到平衡状态的是___________(填序号)。
(5)工业上用 和
和 反应合成甲醇
反应合成甲醇
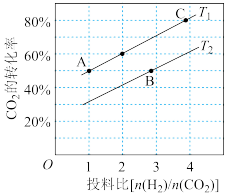
 ,在2L刚性密闭容器中,不同温度、不同投料比时,
,在2L刚性密闭容器中,不同温度、不同投料比时, 的平衡转化率如图所示。
的平衡转化率如图所示。 温度下,将
温度下,将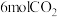 和
和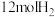 充入该密闭容器中,
充入该密闭容器中, 后反应达到平衡状态,则0-5min内的用甲醇表示的平均反应速率为
后反应达到平衡状态,则0-5min内的用甲醇表示的平均反应速率为___________ ;反应的平衡常数
___________ ,从图中可知:
___________  (填>或<或=,判断的依据是
(填>或<或=,判断的依据是___________ , 、
、 、
、 三者之间的大小关系为
三者之间的大小关系为___________ 。
Ⅰ.利用太阳能实现
 制取某些物质是一种非常理想的
制取某些物质是一种非常理想的 减排途径。
减排途径。(1)在太阳能的作用下,以
 为原料制取炭黑的流程如图所示。其总反应的化学方程式为
为原料制取炭黑的流程如图所示。其总反应的化学方程式为
(2)以稀硫酸为电解质溶液,利用太阳能将
 转化为低碳烯烃,工作原理如图:
转化为低碳烯烃,工作原理如图:
①b是电源的
②生成乙烯(
 )的电极反应式为
)的电极反应式为③电场作用下,氢离子从
Ⅱ.通过化学的方法实现
 的资源化利用也是一种非常理想的
的资源化利用也是一种非常理想的 减排途径。
减排途径。(3)工业上用
 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知: ;
;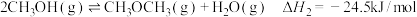 。
。则
 反应的
反应的
 。
。(4)已知该反应
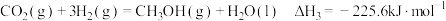 ,在恒温恒压下进行,以下叙述能说明该反应达到平衡状态的是___________(填序号)。
,在恒温恒压下进行,以下叙述能说明该反应达到平衡状态的是___________(填序号)。A. 和 和 的物质的量浓度之比是 的物质的量浓度之比是 |
| B.容器中混合气体的平均摩尔质量保持不变 |
| C.容器中混合气体的体积保持不变 |
D. 的消耗速率等于 的消耗速率等于 的生成速率的3倍 的生成速率的3倍 |
(5)工业上用
 和
和 反应合成甲醇
反应合成甲醇 ,在2L刚性密闭容器中,不同温度、不同投料比时,
,在2L刚性密闭容器中,不同温度、不同投料比时, 的平衡转化率如图所示。
的平衡转化率如图所示。 温度下,将
温度下,将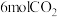 和
和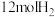 充入该密闭容器中,
充入该密闭容器中, 后反应达到平衡状态,则0-5min内的用甲醇表示的平均反应速率为
后反应达到平衡状态,则0-5min内的用甲醇表示的平均反应速率为

 (填>或<或=,判断的依据是
(填>或<或=,判断的依据是 、
、 、
、 三者之间的大小关系为
三者之间的大小关系为
您最近一年使用:0次
名校
解题方法
6 . 二氧化碳的综合利用是实现碳达峰、碳中和的关键。
I.利用 和
和 合成甲醇,涉及的主要反应如下:
合成甲醇,涉及的主要反应如下:
已知:a.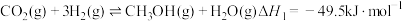
b.
c.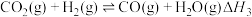
(1)计算
_______ 。
(2)一定条件下,向密闭容器中充入物质的量之比为1:3的 和
和 发生上述反应,使用不同催化剂经相同反应时间,
发生上述反应,使用不同催化剂经相同反应时间, 的转化率和甲醇的选择性随温度的变化如图所示:
的转化率和甲醇的选择性随温度的变化如图所示:

甲醇的选择性
①210-270℃间,在甲醇的选择性上,催化效果较好的是_______ 。
②210-270℃间,催化剂2条件下 的转化率随温度的升高而增大,可能原因为
的转化率随温度的升高而增大,可能原因为_______ 。
II.工业上用 和
和 通过如下反应合成尿素
通过如下反应合成尿素 :
: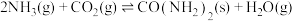 。t℃时,向容积恒定为
。t℃时,向容积恒定为 的密闭容器中充入
的密闭容器中充入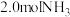 和
和 发生反应。
发生反应。
(3)下列能说明反应达到化学平衡状态的是_______ (填字母)。
a.相同时间内,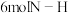 键断裂,同时有
键断裂,同时有 键形成
键形成
b.容器内气体总压强不再变化
c.
d.容器内气体的密度不再改变
(4) 的物质的量随时间的变化如下表所示:
的物质的量随时间的变化如下表所示:
 的平衡转化率为
的平衡转化率为_______ ;t°C时,该反应的平衡常数K=_______ 。
III.中科院研究所利用 和甲酸(HCOOH)的相互转化设计并实现了一种可逆的水系金属二氧化碳电池,结构如图所示:
和甲酸(HCOOH)的相互转化设计并实现了一种可逆的水系金属二氧化碳电池,结构如图所示:
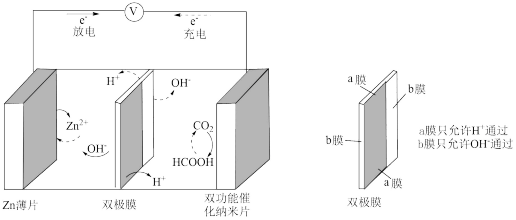
(5)放电时,正极上的电极反应为_______ ;若电池工作时产生a库仑的电量,则理论上消耗锌的质量为_______ g。(已知:转移1mol电子所产生的电量为96500库仑)
I.利用
 和
和 合成甲醇,涉及的主要反应如下:
合成甲醇,涉及的主要反应如下:已知:a.
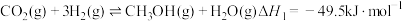
b.

c.
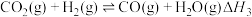
(1)计算

(2)一定条件下,向密闭容器中充入物质的量之比为1:3的
 和
和 发生上述反应,使用不同催化剂经相同反应时间,
发生上述反应,使用不同催化剂经相同反应时间, 的转化率和甲醇的选择性随温度的变化如图所示:
的转化率和甲醇的选择性随温度的变化如图所示:
甲醇的选择性

①210-270℃间,在甲醇的选择性上,催化效果较好的是
②210-270℃间,催化剂2条件下
 的转化率随温度的升高而增大,可能原因为
的转化率随温度的升高而增大,可能原因为II.工业上用
 和
和 通过如下反应合成尿素
通过如下反应合成尿素 :
: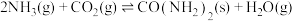 。t℃时,向容积恒定为
。t℃时,向容积恒定为 的密闭容器中充入
的密闭容器中充入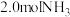 和
和 发生反应。
发生反应。(3)下列能说明反应达到化学平衡状态的是
a.相同时间内,
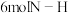 键断裂,同时有
键断裂,同时有 键形成
键形成b.容器内气体总压强不再变化
c.

d.容器内气体的密度不再改变
(4)
 的物质的量随时间的变化如下表所示:
的物质的量随时间的变化如下表所示:| 时间/min | 0 | 30 | 70 | 80 | 100 |
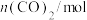 | 1.6 | l.0 | 0.8 | 0.8 | 0.8 |
 的平衡转化率为
的平衡转化率为III.中科院研究所利用
 和甲酸(HCOOH)的相互转化设计并实现了一种可逆的水系金属二氧化碳电池,结构如图所示:
和甲酸(HCOOH)的相互转化设计并实现了一种可逆的水系金属二氧化碳电池,结构如图所示:
(5)放电时,正极上的电极反应为
您最近一年使用:0次
名校
7 . 尿素 是首个由无机物人工合成的有机物.
是首个由无机物人工合成的有机物.
(1)在尿素合成塔中发生的反应可表示为 ;
;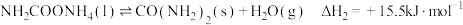 ,已知第一步反应为快速反应,第二步反应为慢速反应,则
,已知第一步反应为快速反应,第二步反应为慢速反应,则
________  ,下列图象能表示尿素合成塔中发生反应的能量变化历程的是
,下列图象能表示尿素合成塔中发生反应的能量变化历程的是________ (填标号).
A.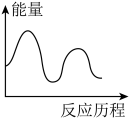 B.
B. 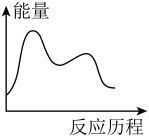 C.
C.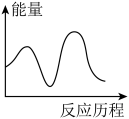 D.
D.
(2)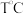 ,在
,在 的密闭容器中,通入
的密闭容器中,通入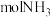 和
和 ,保持体积不变,发生反应,
,保持体积不变,发生反应,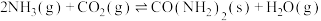 ,
, 时反应刚好达到平衡.测得起始压强为平衡时压强的1.5倍,则:
时反应刚好达到平衡.测得起始压强为平衡时压强的1.5倍,则:
① 的平衡转化率为
的平衡转化率为________ .
②能说明上述反应达到平衡状态的是________ (填标号).
A.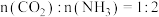 B.混合气体的密度不再发生变化
B.混合气体的密度不再发生变化
C. 的体积分数在混合气体中保持不变 D.单位时间内消耗
的体积分数在混合气体中保持不变 D.单位时间内消耗 ,同时生成
,同时生成
③若 时保持温度和容器的容积不变,再向容器中同时充入
时保持温度和容器的容积不变,再向容器中同时充入 、
、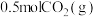 和
和 ,则此时平衡
,则此时平衡________ (填“正向移动”、“逆向移动”或“不移动”).
(3)一定温度下,某恒容密闭容器中发生反应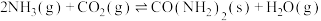 ,若原料气中
,若原料气中 ,测得
,测得 与
与 的平衡转化率
的平衡转化率 的关系如图所示:
的关系如图所示:
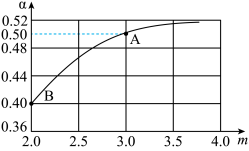
若平衡时 点容器内总压强为
点容器内总压强为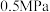 ,则上述反应的平衡常数
,则上述反应的平衡常数
________  .(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
.(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
 是首个由无机物人工合成的有机物.
是首个由无机物人工合成的有机物.(1)在尿素合成塔中发生的反应可表示为
 ;
;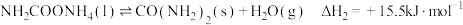 ,已知第一步反应为快速反应,第二步反应为慢速反应,则
,已知第一步反应为快速反应,第二步反应为慢速反应,则
 ,下列图象能表示尿素合成塔中发生反应的能量变化历程的是
,下列图象能表示尿素合成塔中发生反应的能量变化历程的是A.
 B.
B.  C.
C. D.
D.
(2)
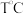 ,在
,在 的密闭容器中,通入
的密闭容器中,通入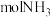 和
和 ,保持体积不变,发生反应,
,保持体积不变,发生反应,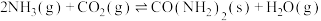 ,
, 时反应刚好达到平衡.测得起始压强为平衡时压强的1.5倍,则:
时反应刚好达到平衡.测得起始压强为平衡时压强的1.5倍,则:①
 的平衡转化率为
的平衡转化率为②能说明上述反应达到平衡状态的是
A.
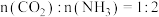 B.混合气体的密度不再发生变化
B.混合气体的密度不再发生变化C.
 的体积分数在混合气体中保持不变 D.单位时间内消耗
的体积分数在混合气体中保持不变 D.单位时间内消耗 ,同时生成
,同时生成
③若
 时保持温度和容器的容积不变,再向容器中同时充入
时保持温度和容器的容积不变,再向容器中同时充入 、
、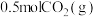 和
和 ,则此时平衡
,则此时平衡(3)一定温度下,某恒容密闭容器中发生反应
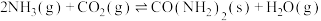 ,若原料气中
,若原料气中 ,测得
,测得 与
与 的平衡转化率
的平衡转化率 的关系如图所示:
的关系如图所示:
若平衡时
 点容器内总压强为
点容器内总压强为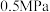 ,则上述反应的平衡常数
,则上述反应的平衡常数
 .(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
.(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
您最近一年使用:0次
8 . 氨的用途十分广泛,是制造硝酸和氮肥的重要原料。
(1)工业合成氨中,合成塔中每产生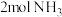 ,放出92.2kJ热量。
,放出92.2kJ热量。

1mol N-H键断裂吸收的能量约等于___________ kJ
(2)一定条件下,在恒温恒容的密闭容器中加入等物质的量 和
和 发生反应生成
发生反应生成 下列状态能说明反应达到平衡的是___________(填标号)。
下列状态能说明反应达到平衡的是___________(填标号)。
(3)以氨为原料生产尿素的方程式为 。
。
①为进一步提高 的平衡转化率,下列措施能达到目的的是
的平衡转化率,下列措施能达到目的的是___________ (填标号)。
A.增大 的浓度 B.增大压强 C.及时转移生成的尿素 D.使用更高效的催化剂
的浓度 B.增大压强 C.及时转移生成的尿素 D.使用更高效的催化剂
②尿素的合成分两步进行:
a.
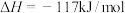
b.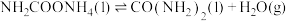

第一步反应速率快,可判断活化能较大的是___________ (填“第一步”或“第二步”)。
③某实验小组为了模拟工业上合成尿素,在恒温恒容的真空密闭容器中充入一定量的 和
和 发生反应:
发生反应: ,反应过程中混合气体中
,反应过程中混合气体中 的体积分数如下图所示。
的体积分数如下图所示。
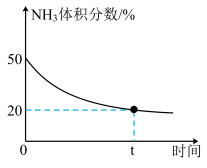
实验测得体系平衡时的压强为10MPa,计算该反应的平衡常数
___________ (已知:分压=总压×体积分数)。
(4)中国首个空间实验室——“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),它是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。a、b、c、d均为Pt电极。
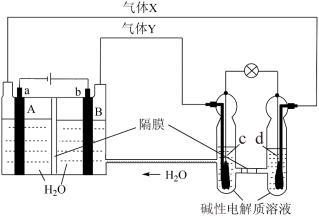
气体X为___________ ,A区pH___________ (填“变大”或“变小”或“不变”)图中右管中的 通过隔膜向
通过隔膜向___________ 电极移动(填“c”或“d”),c是___________ 极,电极上的电极反应为___________ 。
(1)工业合成氨中,合成塔中每产生
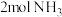 ,放出92.2kJ热量。
,放出92.2kJ热量。
1mol N-H键断裂吸收的能量约等于
(2)一定条件下,在恒温恒容的密闭容器中加入等物质的量
 和
和 发生反应生成
发生反应生成 下列状态能说明反应达到平衡的是___________(填标号)。
下列状态能说明反应达到平衡的是___________(填标号)。| A.容器内压强不变 | B. 的体积分数不变 的体积分数不变 |
| C.气体的密度不再改变 | D. |
(3)以氨为原料生产尿素的方程式为
 。
。①为进一步提高
 的平衡转化率,下列措施能达到目的的是
的平衡转化率,下列措施能达到目的的是A.增大
 的浓度 B.增大压强 C.及时转移生成的尿素 D.使用更高效的催化剂
的浓度 B.增大压强 C.及时转移生成的尿素 D.使用更高效的催化剂②尿素的合成分两步进行:
a.

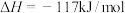
b.
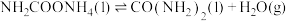

第一步反应速率快,可判断活化能较大的是
③某实验小组为了模拟工业上合成尿素,在恒温恒容的真空密闭容器中充入一定量的
 和
和 发生反应:
发生反应: ,反应过程中混合气体中
,反应过程中混合气体中 的体积分数如下图所示。
的体积分数如下图所示。
实验测得体系平衡时的压强为10MPa,计算该反应的平衡常数

(4)中国首个空间实验室——“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),它是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。a、b、c、d均为Pt电极。

气体X为
 通过隔膜向
通过隔膜向
您最近一年使用:0次
9 . 碳、氮元素及其化合物对生产、生活有重要的意义。回答下列问题:
(1)以 与
与 为原料可合成尿素
为原料可合成尿素 。已知:
。已知:
①
②
③
写出 和
和 合成尿素和液态水的热化学方程式
合成尿素和液态水的热化学方程式______________________________ 。
(2) 可用于富集得到高浓度
可用于富集得到高浓度 。原理是:在
。原理是:在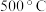 ,低浓度
,低浓度 与
与 接触后生成两种锂盐;平衡后加热至
接触后生成两种锂盐;平衡后加热至 ,反应逆向进行,放出高浓度
,反应逆向进行,放出高浓度 ,
, 再生。
再生。 时反应的化学方程式为
时反应的化学方程式为____________________ 。
(3)在体积为 的密闭恒容容器中,充入
的密闭恒容容器中,充入 和
和 ,发生反应:
,发生反应: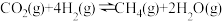 测得温度对
测得温度对 的平衡转化率(
的平衡转化率( )和催化剂催化效率的影响如图所示。
)和催化剂催化效率的影响如图所示。
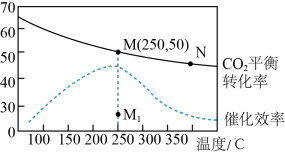
①欲提高 的平衡转化率,可采取的措施有
的平衡转化率,可采取的措施有__________ (填序号)
A.通入惰性气体 B.升高温度 C.增加 浓度 D.增加
浓度 D.增加 浓度
浓度
②下列说法正确的是__________ (填序号)。
A.平衡常数大小:
B.其他条件不变,若不使用催化剂,则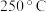 时
时 的平衡转化率可能位于点
的平衡转化率可能位于点
C.其他条件不变,加入催化剂可以降低该反应活化能, 不变
不变
D.当压强或混合气体的密度保持不变时均可证明化学反应已达到平衡状态
③已知M点总压为 ,该反应在此温度下的平衡常数
,该反应在此温度下的平衡常数
__________ 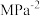 。(
。( 是用平衡分压代替平衡浓度表示的化学平衡常数,气体分压=气体总压×体积分数)
是用平衡分压代替平衡浓度表示的化学平衡常数,气体分压=气体总压×体积分数)
(4)固体氧化物电解池(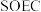 )用于高温共电解
)用于高温共电解 ,既可高效制备合成气(
,既可高效制备合成气( ),又可实现
),又可实现 的减排,其工作原理如图。写出电极c发生的电极反应式:
的减排,其工作原理如图。写出电极c发生的电极反应式:______________________________ 。
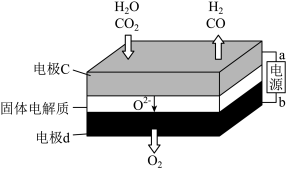
电解生成的合成气在催化剂作用下发生如下反应: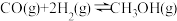 。对此反应进行如下研究:某温度下在一恒压容器中分别充入
。对此反应进行如下研究:某温度下在一恒压容器中分别充入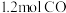 和
和 ,达到平衡时容器体积为
,达到平衡时容器体积为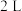 ,且含有
,且含有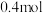
 。此时向容器中再通入
。此时向容器中再通入 气体,则此平衡将
气体,则此平衡将__________ 移动(填“向正反应方向”“不”或“向逆反应方向”)。
(1)以
 与
与 为原料可合成尿素
为原料可合成尿素 。已知:
。已知:①

②

③

写出
 和
和 合成尿素和液态水的热化学方程式
合成尿素和液态水的热化学方程式(2)
 可用于富集得到高浓度
可用于富集得到高浓度 。原理是:在
。原理是:在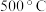 ,低浓度
,低浓度 与
与 接触后生成两种锂盐;平衡后加热至
接触后生成两种锂盐;平衡后加热至 ,反应逆向进行,放出高浓度
,反应逆向进行,放出高浓度 ,
, 再生。
再生。 时反应的化学方程式为
时反应的化学方程式为(3)在体积为
 的密闭恒容容器中,充入
的密闭恒容容器中,充入 和
和 ,发生反应:
,发生反应: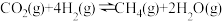 测得温度对
测得温度对 的平衡转化率(
的平衡转化率( )和催化剂催化效率的影响如图所示。
)和催化剂催化效率的影响如图所示。
①欲提高
 的平衡转化率,可采取的措施有
的平衡转化率,可采取的措施有A.通入惰性气体 B.升高温度 C.增加
 浓度 D.增加
浓度 D.增加 浓度
浓度②下列说法正确的是
A.平衡常数大小:

B.其他条件不变,若不使用催化剂,则
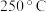 时
时 的平衡转化率可能位于点
的平衡转化率可能位于点
C.其他条件不变,加入催化剂可以降低该反应活化能,
 不变
不变D.当压强或混合气体的密度保持不变时均可证明化学反应已达到平衡状态
③已知M点总压为
 ,该反应在此温度下的平衡常数
,该反应在此温度下的平衡常数
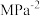 。(
。( 是用平衡分压代替平衡浓度表示的化学平衡常数,气体分压=气体总压×体积分数)
是用平衡分压代替平衡浓度表示的化学平衡常数,气体分压=气体总压×体积分数)(4)固体氧化物电解池(
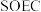 )用于高温共电解
)用于高温共电解 ,既可高效制备合成气(
,既可高效制备合成气( ),又可实现
),又可实现 的减排,其工作原理如图。写出电极c发生的电极反应式:
的减排,其工作原理如图。写出电极c发生的电极反应式:
电解生成的合成气在催化剂作用下发生如下反应:
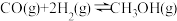 。对此反应进行如下研究:某温度下在一恒压容器中分别充入
。对此反应进行如下研究:某温度下在一恒压容器中分别充入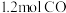 和
和 ,达到平衡时容器体积为
,达到平衡时容器体积为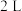 ,且含有
,且含有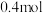
 。此时向容器中再通入
。此时向容器中再通入 气体,则此平衡将
气体,则此平衡将
您最近一年使用:0次
名校
解题方法
10 . 在化学反应的研究和实际应用中,人们除了选择合适的化学反应以实现新期特的物质转化或能量转化,还要关注化学反应进行的快慢和程度,以提高生产效率。
(1)控制条件,让反应在恒容密闭容器中进行如下反应: 。用传感器测得不同时间NO和CO的浓度如表。
。用传感器测得不同时间NO和CO的浓度如表。
前2s内的平均反应速率
___________ ,从表格看,已达化学平衡的时间段为:___________ 。
(2)如图是在一定温度下,某固定容积的密闭容器中充入一定量的 气体后,发生反应
气体后,发生反应 ,已知
,已知 是红棕色气体,
是红棕色气体, 是无色气体。反应速率(v)与时间(t)的关系曲线。
是无色气体。反应速率(v)与时间(t)的关系曲线。
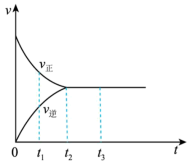
下列叙述正确的是___________ 。
a. 时,反应未达到平衡,
时,反应未达到平衡, 浓度在减小
浓度在减小
b. 时,反应达到平衡,反应不再进行
时,反应达到平衡,反应不再进行
c. 各物质浓度不再变化
各物质浓度不再变化
d. 各物质浓度相等
各物质浓度相等
e. ,
, 浓度增大
浓度增大
f.反应过程中气体的颜色不变
(3)在压强为 条件下,
条件下, 与
与 的混合气体在催化剂作用下能自发放热反应生成甲醇:
的混合气体在催化剂作用下能自发放热反应生成甲醇: 。为了寻得合成甲醇的适宜温度与压强,某同学设计了三组实验,部分实验条件已经填在下面的实验设计表中。表中剩余的实验数据:
。为了寻得合成甲醇的适宜温度与压强,某同学设计了三组实验,部分实验条件已经填在下面的实验设计表中。表中剩余的实验数据:
___________ ,
___________ 。
(4)比较相同浓度的 溶液和不同浓度的
溶液和不同浓度的 溶液反应的反应快慢可通过测定
溶液反应的反应快慢可通过测定___________ 来实现。
(5)在四个不同的容器中,在不同的条件下进行合成氨反应: 根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________
根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________
(1)控制条件,让反应在恒容密闭容器中进行如下反应:
 。用传感器测得不同时间NO和CO的浓度如表。
。用传感器测得不同时间NO和CO的浓度如表。时间 | 0 | 1 | 2 | 3 | 4 | 5 |
 | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
 | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |

(2)如图是在一定温度下,某固定容积的密闭容器中充入一定量的
 气体后,发生反应
气体后,发生反应 ,已知
,已知 是红棕色气体,
是红棕色气体, 是无色气体。反应速率(v)与时间(t)的关系曲线。
是无色气体。反应速率(v)与时间(t)的关系曲线。
下列叙述正确的是
a.
 时,反应未达到平衡,
时,反应未达到平衡, 浓度在减小
浓度在减小b.
 时,反应达到平衡,反应不再进行
时,反应达到平衡,反应不再进行c.
 各物质浓度不再变化
各物质浓度不再变化 d.
 各物质浓度相等
各物质浓度相等e.
 ,
, 浓度增大
浓度增大 f.反应过程中气体的颜色不变
(3)在压强为
 条件下,
条件下, 与
与 的混合气体在催化剂作用下能自发放热反应生成甲醇:
的混合气体在催化剂作用下能自发放热反应生成甲醇: 。为了寻得合成甲醇的适宜温度与压强,某同学设计了三组实验,部分实验条件已经填在下面的实验设计表中。表中剩余的实验数据:
。为了寻得合成甲醇的适宜温度与压强,某同学设计了三组实验,部分实验条件已经填在下面的实验设计表中。表中剩余的实验数据:

| 实验编号 |  (℃) (℃) |  |  |
| ① | 180 |  | 0.1 |
| ② |  |  | 5 |
| ③ | 350 |  | 5 |
 溶液和不同浓度的
溶液和不同浓度的 溶液反应的反应快慢可通过测定
溶液反应的反应快慢可通过测定(5)在四个不同的容器中,在不同的条件下进行合成氨反应:
 根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________
根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________A. | B. |
C. | D. |
您最近一年使用:0次
2023-05-16更新
|
478次组卷
|
2卷引用:广东省广州市白云中学2022-2023学年高一下学期期中考试化学试题



