1 . 天然气、石油钻探过程会释放出CO2、H2S等气体。某种将CO2和H2S共活化的工艺涉及反应如下:
①

②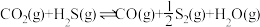

③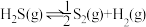
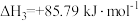
④
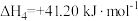
恒压密闭容器中,反应物的平衡转化率、部分生成物的选择性与温度关系如图所示。
已知:i.CO2和H2S的初始物质的量相等:
ii.产率=转化率×选择性:
iii.COS的选择性 ,H2O的选择性
,H2O的选择性 。
。
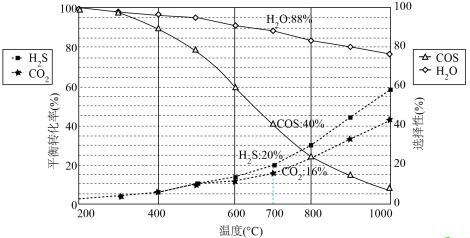
回答下列问题:
(1)COS分子的空间结构为__________ 形。
(2)
_________  。
。
(3)以下温度,COS的产率最高的是__________。
(4)温度高于500℃时,H2S的转化率大于CO2,原因是____________________ 。
(5)可提高S2平衡产率的方法为__________。
(6)700℃时反应①的平衡常数K=__________ (精确到0.01)。
(7)催化剂CeO2-MgO对反应②具有高选择性,通过理论计算得到反应的主要路径如下图所示。表示状态2的为__________ 。

A. B.
B.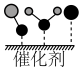 C.
C.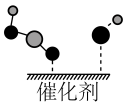
①


②
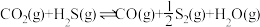

③
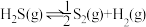
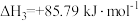
④

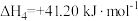
恒压密闭容器中,反应物的平衡转化率、部分生成物的选择性与温度关系如图所示。
已知:i.CO2和H2S的初始物质的量相等:
ii.产率=转化率×选择性:
iii.COS的选择性
 ,H2O的选择性
,H2O的选择性 。
。
回答下列问题:
(1)COS分子的空间结构为
(2)

 。
。(3)以下温度,COS的产率最高的是__________。
A. | B. | C. | D.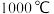 |
(4)温度高于500℃时,H2S的转化率大于CO2,原因是
(5)可提高S2平衡产率的方法为__________。
| A.升高温度 | B.增大压强 | C.降低温度 | D.充入氩气 |
(6)700℃时反应①的平衡常数K=
(7)催化剂CeO2-MgO对反应②具有高选择性,通过理论计算得到反应的主要路径如下图所示。表示状态2的为

A.
 B.
B. C.
C.
您最近一年使用:0次
名校
解题方法
2 . 将X(s)和Y(g)加入密闭容器中,在一定条件下发生反应: 。已知该反应的平衡常数如表所示。下列说法正确的是
。已知该反应的平衡常数如表所示。下列说法正确的是
 。已知该反应的平衡常数如表所示。下列说法正确的是
。已知该反应的平衡常数如表所示。下列说法正确的是| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 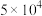 | 2 | 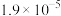 |
| A.上述反应是熵增反应 |
B.25℃时,反应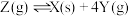 的平衡常数是0.5 的平衡常数是0.5 |
| C.恒温恒容下,向容器中再充入少量Z(g),达到新平衡时,Z的体积百分含量将增大 |
D.在80℃时,测得某时刻Y、Z的浓度均为0.5 ,则此时 ,则此时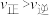 |
您最近一年使用:0次
2023-01-08更新
|
221次组卷
|
4卷引用:黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试变式汇编(11-20)
(已下线)黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试变式汇编(11-20)黑龙江省黑河市第一中学2023-2024学年高二上学期期末考试化学试题安徽省皖北2022~2023学年高二上学期12月联考化学试题河北省沧州运东七县2023-2024学年高二上学期10月期中考试化学试题
名校
解题方法
3 . 利用甲醇 制备一些高附加值产品,是目前研究的热点。
制备一些高附加值产品,是目前研究的热点。
(1)甲醇和水蒸气经催化重整可制得氢气,反应主要过程如下:
反应Ⅰ.

反应Ⅱ.

反应Ⅲ.

①
_________  。
。
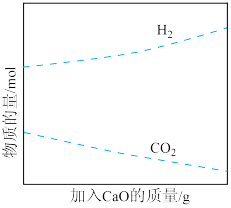
②工业上采用 吸附增强制氢的方法,可以有效提高反应Ⅰ氢气的产率,如图所示,请分析加入
吸附增强制氢的方法,可以有效提高反应Ⅰ氢气的产率,如图所示,请分析加入 提高氢气产率的原因:
提高氢气产率的原因:_________ 。
(2) 和
和 充入一定体积的密闭容器中,在两种温度下发生反应:
充入一定体积的密闭容器中,在两种温度下发生反应: ,测得
,测得 的物质的量随时间的变化如图。
的物质的量随时间的变化如图。

①曲线Ⅰ、Ⅱ对应的平衡常数大小关系为
_________  。(填“>”或“=”或“<”)
。(填“>”或“=”或“<”)
②一定温度下,在容积为 的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
若甲中平衡后气体的压强为开始的0.8倍,则乙容器起始时反应速率
_________  。(填“>”“<”或“=”)。
。(填“>”“<”或“=”)。
③一定温度下,此反应在恒压容器中进行,能判断该反应达到化学平衡状态的依据是_________ 。
a.容器中压强不变
b. 的体积分数不变
的体积分数不变
c.
d.容器中密度不变
e.2个 断裂的同时有3个
断裂的同时有3个 断裂
断裂
(3)已知电离常数 :
: ,
, :
: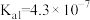 ,
, ,则向
,则向 溶液中通入少量
溶液中通入少量 时的离子方程式为
时的离子方程式为_________ 。
(4)利用人工光合作用,借助太阳能使 和
和 转化为
转化为 ,如图所示,在催化剂b表面发生的电极反应为:
,如图所示,在催化剂b表面发生的电极反应为:_________ 。

 制备一些高附加值产品,是目前研究的热点。
制备一些高附加值产品,是目前研究的热点。(1)甲醇和水蒸气经催化重整可制得氢气,反应主要过程如下:
反应Ⅰ.


反应Ⅱ.


反应Ⅲ.


①

 。
。②工业上采用
 吸附增强制氢的方法,可以有效提高反应Ⅰ氢气的产率,如图所示,请分析加入
吸附增强制氢的方法,可以有效提高反应Ⅰ氢气的产率,如图所示,请分析加入 提高氢气产率的原因:
提高氢气产率的原因:
(2)
 和
和 充入一定体积的密闭容器中,在两种温度下发生反应:
充入一定体积的密闭容器中,在两种温度下发生反应: ,测得
,测得 的物质的量随时间的变化如图。
的物质的量随时间的变化如图。
①曲线Ⅰ、Ⅱ对应的平衡常数大小关系为

 。(填“>”或“=”或“<”)
。(填“>”或“=”或“<”)②一定温度下,在容积为
 的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。| 容器 | 甲 | 乙 |
| 反应物投入量 |  、 、 |  、 、 、 、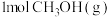 、 、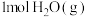 |

 。(填“>”“<”或“=”)。
。(填“>”“<”或“=”)。③一定温度下,此反应在恒压容器中进行,能判断该反应达到化学平衡状态的依据是
a.容器中压强不变
b.
 的体积分数不变
的体积分数不变c.

d.容器中密度不变
e.2个
 断裂的同时有3个
断裂的同时有3个 断裂
断裂(3)已知电离常数
 :
: ,
, :
: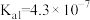 ,
, ,则向
,则向 溶液中通入少量
溶液中通入少量 时的离子方程式为
时的离子方程式为(4)利用人工光合作用,借助太阳能使
 和
和 转化为
转化为 ,如图所示,在催化剂b表面发生的电极反应为:
,如图所示,在催化剂b表面发生的电极反应为:
您最近一年使用:0次
名校
解题方法
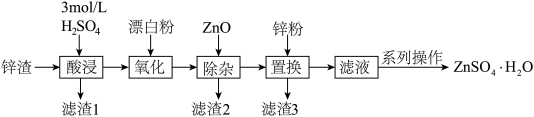
4 . 硫酸锌是一种重要的工业原料,ZnSO4∙H2O可用于制造印染用的媒染剂,木材及皮革保存剂等。以炼锌厂锌渣为原料,含ZnO、FeO、CuO、CdO等,生产ZnSO4∙H2O的流程如下:
已知:①当溶液中剩余离子浓度小于1×10-5 mol∙L-1时,认为生成沉淀的反应进行完全;
②常温下,Ksp[Fe(OH)3]= 4.0×10-38,Ksp[Fe(OH)2]= 4.9×10-17,Ksp[Cu(OH)2]= 2.2×10-20,Ksp[Zn(OH)2]=1×10-17。
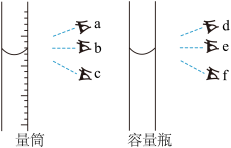
(1)“酸浸”时,需不断通入高温水蒸气,其目的是___________ (填字母)。用18 mol∙L-1的浓硫酸配制3 mol∙L-1H2SO4溶液,下列操作会使所配溶液浓度偏小的是___________ (填字母)。
(2)结合必要的化学反应方程式,从平衡角度解释加入ZnO得到滤渣2的原理:___________ 。除杂过程中,若控制pH=4,溶液中c(Fe3+)=___________ mol∙L-1。结合实际生产情况一般取pH4.5~5.0,pH不宜过大的原因是___________ 。
(3)滤渣3含有Zn和___________ (写化学式)。
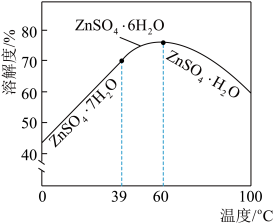
(4)硫酸锌晶体的溶解度与温度的变化如图所示。“系列操作”是:___________ ,洗涤、干燥。

已知:①当溶液中剩余离子浓度小于1×10-5 mol∙L-1时,认为生成沉淀的反应进行完全;
②常温下,Ksp[Fe(OH)3]= 4.0×10-38,Ksp[Fe(OH)2]= 4.9×10-17,Ksp[Cu(OH)2]= 2.2×10-20,Ksp[Zn(OH)2]=1×10-17。
(1)“酸浸”时,需不断通入高温水蒸气,其目的是

(2)结合必要的化学反应方程式,从平衡角度解释加入ZnO得到滤渣2的原理:
(3)滤渣3含有Zn和
(4)硫酸锌晶体的溶解度与温度的变化如图所示。“系列操作”是:

您最近一年使用:0次
2023-01-08更新
|
285次组卷
|
3卷引用:黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试变式汇编(21-24)
(已下线)黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试变式汇编(21-24)山西省名校联考2022-2023学年高二上学期期末考试化学试题福建省宁德市2022-2023学年高二上学期期末居家检测化学试题
名校
解题方法
5 . 温度为 时,在两个容积均为2L的恒容密闭容器中仅发生反应
时,在两个容积均为2L的恒容密闭容器中仅发生反应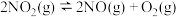 (正反应吸热)。实验测得:v(正)
(正反应吸热)。实验测得:v(正)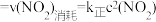 ,v(逆)
,v(逆) ,
, 、
、 为速率常数,受温度影响。下列说法正确的是
为速率常数,受温度影响。下列说法正确的是
 时,在两个容积均为2L的恒容密闭容器中仅发生反应
时,在两个容积均为2L的恒容密闭容器中仅发生反应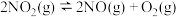 (正反应吸热)。实验测得:v(正)
(正反应吸热)。实验测得:v(正)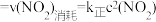 ,v(逆)
,v(逆) ,
, 、
、 为速率常数,受温度影响。下列说法正确的是
为速率常数,受温度影响。下列说法正确的是| 容器编号 | 物质的起始浓度/ | 物质的平衡浓度/ | ||
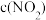 |  |  |  | |
| I | 0.6 | 0 | 0 | 0.2 |
| II | 0.3 | 0.5 | 0.2 | |
A.若容器I两分钟达到平衡,则0~2分钟反应速率 |
| B.达到平衡时,容器I与容器II中的总压强之比4:5 |
| C.容器II中起始时速率v(逆)>v(正) |
D.若改变温度为 ,且 ,且 ,则 ,则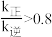 |
您最近一年使用:0次
6 . 环氧乙烷(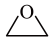 ,别称EO)是重要的杀菌剂和工业合成原料。回答下列问题:
,别称EO)是重要的杀菌剂和工业合成原料。回答下列问题:
(一)乙烯直接氧化法:
反应I:CH2=CH2(g)+ O2(g)→
O2(g)→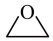 (g) ΔH1
(g) ΔH1
反应II:CH2=CH2(g)+3O2(g)→2CO2(g)+2H2O(g) ΔH2
(1)乙烯与O2在a、b两种催化剂作用下发生反应,催化剂的催化活性(用EO%衡量)及生成EO的选择性(用EO选择性%表示)与温度(T)的变化曲线如图一所示。

①依据图给信息,选择制备环氧乙烷的适宜条件为_____ 。
②M点后曲线下降的原因为_____ 。
③下列说法正确的有_____ (填标号)。
A.催化剂的选择性越高,其达到最高反应活性所需的温度越高
B.不同催化剂达到最高活性时的温度不同
C.催化剂的催化活性与温度成正比
(2)设K 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。反应I、II对应的-lnK
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。反应I、II对应的-lnK 随
随 (温度的倒数)的变化如图二所示。
(温度的倒数)的变化如图二所示。
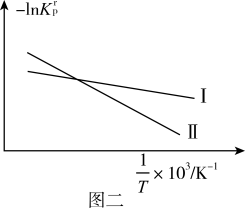
ΔH2_____ 0(填“>”或“<”)。
(二)电化学合成法
(3)科学家利用CO2、水合成环氧乙烷,有利于实现碳中和。总反应为:2CO2+2H2O→ +2.5O2,该过程在两个独立的电解槽中实现,装置如图三所示,在电解槽2中利用氯离子介导制备环氧乙烷,内部结构如图四所示。
+2.5O2,该过程在两个独立的电解槽中实现,装置如图三所示,在电解槽2中利用氯离子介导制备环氧乙烷,内部结构如图四所示。
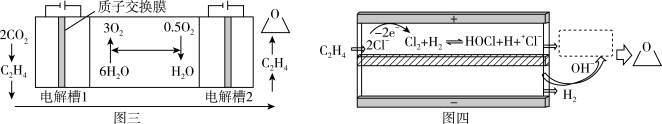
①电解槽1中阴极的电极反应式为_____ 。
②图四虚线框中发生多个反应,有中间产物HOCH2CH2Cl生成,最终生成环氧乙烷,其反应过程可描述为_____ 。
 ,别称EO)是重要的杀菌剂和工业合成原料。回答下列问题:
,别称EO)是重要的杀菌剂和工业合成原料。回答下列问题:(一)乙烯直接氧化法:
反应I:CH2=CH2(g)+
 O2(g)→
O2(g)→ (g) ΔH1
(g) ΔH1反应II:CH2=CH2(g)+3O2(g)→2CO2(g)+2H2O(g) ΔH2
(1)乙烯与O2在a、b两种催化剂作用下发生反应,催化剂的催化活性(用EO%衡量)及生成EO的选择性(用EO选择性%表示)与温度(T)的变化曲线如图一所示。

①依据图给信息,选择制备环氧乙烷的适宜条件为
②M点后曲线下降的原因为
③下列说法正确的有
A.催化剂的选择性越高,其达到最高反应活性所需的温度越高
B.不同催化剂达到最高活性时的温度不同
C.催化剂的催化活性与温度成正比
(2)设K
 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。反应I、II对应的-lnK
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。反应I、II对应的-lnK 随
随 (温度的倒数)的变化如图二所示。
(温度的倒数)的变化如图二所示。
ΔH2
(二)电化学合成法
(3)科学家利用CO2、水合成环氧乙烷,有利于实现碳中和。总反应为:2CO2+2H2O→
 +2.5O2,该过程在两个独立的电解槽中实现,装置如图三所示,在电解槽2中利用氯离子介导制备环氧乙烷,内部结构如图四所示。
+2.5O2,该过程在两个独立的电解槽中实现,装置如图三所示,在电解槽2中利用氯离子介导制备环氧乙烷,内部结构如图四所示。
①电解槽1中阴极的电极反应式为
②图四虚线框中发生多个反应,有中间产物HOCH2CH2Cl生成,最终生成环氧乙烷,其反应过程可描述为
您最近一年使用:0次
名校
7 . 氮及其化合物在工农业生产和生命活动中起着重要的作用。
(1)已知:①
 kJ·mol
kJ·mol
②
 kJ·mol
kJ·mol
③
 kJ·mol
kJ·mol
若某反应的平衡常数表达式为 ,请写出此反应的热化学方程式:
,请写出此反应的热化学方程式:_______ 。
(2)汽车尾气中的NO和CO在一定条件下可发生反应生成无毒的 和
和 。将NO和CO以一定的流速通过两种不同的催化剂(cat1、cat2)进行反应,相同时间内测得的脱氮率(脱氮率即NO的转化率)如图所示,M点
。将NO和CO以一定的流速通过两种不同的催化剂(cat1、cat2)进行反应,相同时间内测得的脱氮率(脱氮率即NO的转化率)如图所示,M点_______ (填“是”或“不是”)对应温度下的平衡脱氮率,理由是_______ 。

(3)某同学设计用NO—空气质子交换膜燃料电池探究将雾霾中的 、NO转化为
、NO转化为 的原理。
的原理。

①燃料电池放电过程中负极的电极反应式为_______ 。
②若甲装置中消耗22.4 L (标况),则乙装置中
(标况),则乙装置中 和NO转化的物质的量共有
和NO转化的物质的量共有_______ mol。
(4)某温度下,在一密闭容器中充入一定量NO(g)发生反应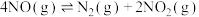
 ,其正反应速率表达式为
,其正反应速率表达式为 (
( 为速率常数,只与温度有关),测得反应速率和NO浓度的数据如表所示。
为速率常数,只与温度有关),测得反应速率和NO浓度的数据如表所示。
则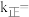
_______  ;下列对于该反应的说法正确的是
;下列对于该反应的说法正确的是_______ (填标号)。
A.当混合气体颜色保持不变时,反应达到化学平衡状态
B.当 的比值保持不变时,反应达到化学平衡状态
的比值保持不变时,反应达到化学平衡状态
C.反应达到化学平衡状态时,每消耗0.1 mol NO就会消耗0.05 mol
D.反应达到平衡状态后,若降低温度,则混合气体的颜色变浅
E.反应达到平衡状态后,若减小压强,则混合气体的平均相对分子质量减小
(1)已知:①

 kJ·mol
kJ·mol
②

 kJ·mol
kJ·mol
③

 kJ·mol
kJ·mol
若某反应的平衡常数表达式为
 ,请写出此反应的热化学方程式:
,请写出此反应的热化学方程式:(2)汽车尾气中的NO和CO在一定条件下可发生反应生成无毒的
 和
和 。将NO和CO以一定的流速通过两种不同的催化剂(cat1、cat2)进行反应,相同时间内测得的脱氮率(脱氮率即NO的转化率)如图所示,M点
。将NO和CO以一定的流速通过两种不同的催化剂(cat1、cat2)进行反应,相同时间内测得的脱氮率(脱氮率即NO的转化率)如图所示,M点
(3)某同学设计用NO—空气质子交换膜燃料电池探究将雾霾中的
 、NO转化为
、NO转化为 的原理。
的原理。
①燃料电池放电过程中负极的电极反应式为
②若甲装置中消耗22.4 L
 (标况),则乙装置中
(标况),则乙装置中 和NO转化的物质的量共有
和NO转化的物质的量共有(4)某温度下,在一密闭容器中充入一定量NO(g)发生反应
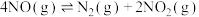
 ,其正反应速率表达式为
,其正反应速率表达式为 (
( 为速率常数,只与温度有关),测得反应速率和NO浓度的数据如表所示。
为速率常数,只与温度有关),测得反应速率和NO浓度的数据如表所示。| 序号 |  |  |
| ① | 0.10 |  |
| ② | 0.20 |  |
| ③ | 0.30 |  |
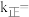
 ;下列对于该反应的说法正确的是
;下列对于该反应的说法正确的是A.当混合气体颜色保持不变时,反应达到化学平衡状态
B.当
 的比值保持不变时,反应达到化学平衡状态
的比值保持不变时,反应达到化学平衡状态C.反应达到化学平衡状态时,每消耗0.1 mol NO就会消耗0.05 mol

D.反应达到平衡状态后,若降低温度,则混合气体的颜色变浅
E.反应达到平衡状态后,若减小压强,则混合气体的平均相对分子质量减小
您最近一年使用:0次
名校
8 . 在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应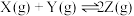
 ,一段时间后达到平衡。反应过程中测定的数据如下表:
,一段时间后达到平衡。反应过程中测定的数据如下表:
下列说法正确的是
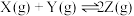
 ,一段时间后达到平衡。反应过程中测定的数据如下表:
,一段时间后达到平衡。反应过程中测定的数据如下表:| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.前4min内反应的平均速率 |
B.其他条件不变,升高温度,反应达到新平衡前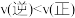 |
| C.该温度下此反应的平衡常数K=1.44 |
| D.其他条件不变,再充入0.2molZ,平衡时X的体积分数增大 |
您最近一年使用:0次
2022-04-14更新
|
493次组卷
|
7卷引用:黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试变式汇编(11-20)
(已下线)黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试变式汇编(11-20)(已下线)专项12 化学反应速率与化学平衡-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)专题10 化学反应速率与平衡-2023年高考化学一轮复习小题多维练(全国通用)黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试化学试题浙江省金华十校2021-2022学年高三下学期4月模拟考试化学试题湖南省衡阳市衡东县第一中学2022届高三下学期期中考试化学试题(已下线)化学(辽宁B卷)-学易金卷:2023年高考第一次模拟考试卷
名校
解题方法
9 . 下列实验装置能达到实验目的的是


| A.用甲装置除去CO2中的少量SO2气体 |
| B.用乙装置完成实验室制取乙酸乙酯 |
| C.用丙装置证明温度对化学平衡的影响 |
| D.用丁装置验证浓硫酸具有脱水性、强氧化性,SO2具有漂白性、氧化性 |
您最近一年使用:0次
2021-10-12更新
|
478次组卷
|
4卷引用:黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试变式汇编(11-20)
(已下线)黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试变式汇编(11-20)陕西省西咸新区黄冈泾河中学2022届高三第1次模拟考试化学试题(已下线)一轮巩固卷7-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)内蒙古赤峰市2021-2022学年高三上学期期末考试化学试题
名校
10 . 如图所示为工业合成氨的流程图。有关说法错误的是


A.步骤③中“ ”是催化剂催化活性的最佳温度 ”是催化剂催化活性的最佳温度 |
B. 晶胞符合分子密堆积 晶胞符合分子密堆积 |
| C.步骤②、④、⑤均有利于提高原料的转化率 |
| D.产品液氨除可生产化肥外,还可用作制冷剂 |
您最近一年使用:0次



