1 . 过氧乙酸是具有重要用途的有机合成氧化剂和化工原料,实验室拟合成过氧乙酸并测定其含量。
(1)浓缩
在图示装置(加热装置已省略)中,由分液漏斗向冷凝管1中滴加30% 溶液,最终得到质量分数约68%的
溶液,最终得到质量分数约68%的 溶液。
溶液。
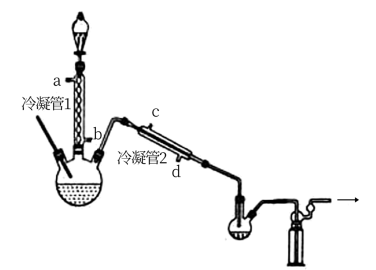
冷凝管1、冷凝管2中进水接口依次为___________ 、___________ (填字母)。
②加热温度不宜超过60℃的原因是___________ 。
(2)合成过氧乙酸
向带有搅拌装置及温度计的500mL三口烧瓶中先加入16g冰醋酸,在搅拌下滴加90g68% 溶液,最后加入4.1mL浓硫酸,搅拌5h,静置20h。
溶液,最后加入4.1mL浓硫酸,搅拌5h,静置20h。
(已知:CH3COOH+H2O2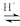
 +H2O)
+H2O)
①用浓缩的68% 溶液代替常见的30%
溶液代替常见的30% 溶液的目的是
溶液的目的是___________ 。
②充分搅拌的目的是___________ 。
(3)过氧乙酸含量的测定
步骤a:称取5.0g过氧乙酸试样(液体),配制成100mL溶液A。
步骤b:在碘量瓶中加入5.0mL 溶液、3滴
溶液、3滴 溶液、5.0mL溶液A,摇匀,用0.01mol/L的
溶液、5.0mL溶液A,摇匀,用0.01mol/L的 溶液滴定至溶液呈微红色。
溶液滴定至溶液呈微红色。
步骤c:向滴定后的溶液中再加1.0gKI(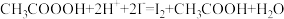 ),摇匀,置于暗处5min,用蒸馏水冲洗瓶盖及四周,加钼酸铵催化剂20mL,摇匀,用淀粉溶液作指示剂,用0.05mol/L的
),摇匀,置于暗处5min,用蒸馏水冲洗瓶盖及四周,加钼酸铵催化剂20mL,摇匀,用淀粉溶液作指示剂,用0.05mol/L的 标准溶液滴定至蓝色刚好褪去(
标准溶液滴定至蓝色刚好褪去( )。重复步骤b,步骤c三次,测得平均消耗
)。重复步骤b,步骤c三次,测得平均消耗 标准溶液的体积为20.00mL。
标准溶液的体积为20.00mL。
①步骤a中配制溶液A时,需要用到的玻璃仪器除烧杯、100mL容量瓶,玻璃棒和量筒外,还需要___________
②设计步骤b的目的是___________
③过氧乙酸的质量分数为___________ %。
(1)浓缩

在图示装置(加热装置已省略)中,由分液漏斗向冷凝管1中滴加30%
 溶液,最终得到质量分数约68%的
溶液,最终得到质量分数约68%的 溶液。
溶液。
冷凝管1、冷凝管2中进水接口依次为
②加热温度不宜超过60℃的原因是
(2)合成过氧乙酸
向带有搅拌装置及温度计的500mL三口烧瓶中先加入16g冰醋酸,在搅拌下滴加90g68%
 溶液,最后加入4.1mL浓硫酸,搅拌5h,静置20h。
溶液,最后加入4.1mL浓硫酸,搅拌5h,静置20h。(已知:CH3COOH+H2O2
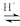
 +H2O)
+H2O)①用浓缩的68%
 溶液代替常见的30%
溶液代替常见的30% 溶液的目的是
溶液的目的是②充分搅拌的目的是
(3)过氧乙酸含量的测定
步骤a:称取5.0g过氧乙酸试样(液体),配制成100mL溶液A。
步骤b:在碘量瓶中加入5.0mL
 溶液、3滴
溶液、3滴 溶液、5.0mL溶液A,摇匀,用0.01mol/L的
溶液、5.0mL溶液A,摇匀,用0.01mol/L的 溶液滴定至溶液呈微红色。
溶液滴定至溶液呈微红色。步骤c:向滴定后的溶液中再加1.0gKI(
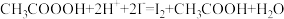 ),摇匀,置于暗处5min,用蒸馏水冲洗瓶盖及四周,加钼酸铵催化剂20mL,摇匀,用淀粉溶液作指示剂,用0.05mol/L的
),摇匀,置于暗处5min,用蒸馏水冲洗瓶盖及四周,加钼酸铵催化剂20mL,摇匀,用淀粉溶液作指示剂,用0.05mol/L的 标准溶液滴定至蓝色刚好褪去(
标准溶液滴定至蓝色刚好褪去( )。重复步骤b,步骤c三次,测得平均消耗
)。重复步骤b,步骤c三次,测得平均消耗 标准溶液的体积为20.00mL。
标准溶液的体积为20.00mL。①步骤a中配制溶液A时,需要用到的玻璃仪器除烧杯、100mL容量瓶,玻璃棒和量筒外,还需要
②设计步骤b的目的是
③过氧乙酸的质量分数为
您最近一年使用:0次
2 . 合成氨工艺的一个重要工序是铜洗,其目的是用铜液 醋酸二氨合铜
醋酸二氨合铜 Ⅰ
Ⅰ ,氨水
,氨水 吸收在生产过程中产生的CO和
吸收在生产过程中产生的CO和 等气体,铜液吸收CO的反应是放热反应,其反应方程式为:
等气体,铜液吸收CO的反应是放热反应,其反应方程式为: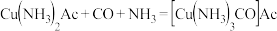 ; 完成下列填空:
; 完成下列填空:
 如果要提高上述反应的反应速率,可以采取的措施是
如果要提高上述反应的反应速率,可以采取的措施是 ______  选填编号
选填编号
 减压
减压  增加
增加 的浓度
的浓度  升温
升温  及时移走产物
及时移走产物
 铜液中的氨可吸收二氧化碳,写出该反应的化学方程式:
铜液中的氨可吸收二氧化碳,写出该反应的化学方程式: ______
 简述铜液吸收CO及铜液再生的操作步骤
简述铜液吸收CO及铜液再生的操作步骤 注明吸收和再生的条件
注明吸收和再生的条件 .
.______
 铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为
铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为 ______ 通过比较 ______ 可判断氮、磷两种元素的非金属性强弱.
 已知
已知 与
与 分子结构相似,
分子结构相似, 的电子式是
的电子式是 ______  熔点高于
熔点高于 ,其原因是
,其原因是 ______
 提取的
提取的 中含少量
中含少量 、SO
、SO 。将产品溶解,加入
。将产品溶解,加入 ,加热至沸,再加入
,加热至沸,再加入 溶液,过滤,蒸发结晶,得到工业氯化铵.加热至沸的目的是
溶液,过滤,蒸发结晶,得到工业氯化铵.加热至沸的目的是 ______ 。滤渣的主要成分是 ______ 、 ______ .
 称取
称取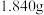 小苏打样品
小苏打样品 含少量
含少量 ,配置成250mL溶液,取
,配置成250mL溶液,取 用
用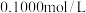 盐酸滴定,消耗盐酸
盐酸滴定,消耗盐酸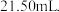 实验中所需的定量仪器出滴定管外,还有
实验中所需的定量仪器出滴定管外,还有 ______ 。选甲基橙而不选酚酞作为指示剂的原因是 ______  样品中
样品中 质量分数为
质量分数为 ______ 。( 保留3位小数)
 将一定量小苏打样品
将一定量小苏打样品 含少量
含少量 溶于足量盐酸,蒸干后称量固体质量,也可测量小苏打的含量。若蒸发过程中有少量液体溅出,则测定结果
溶于足量盐酸,蒸干后称量固体质量,也可测量小苏打的含量。若蒸发过程中有少量液体溅出,则测定结果 ______ 。(选填“偏高”、“偏低”或“不受影响”)
 醋酸二氨合铜
醋酸二氨合铜 Ⅰ
Ⅰ ,氨水
,氨水 吸收在生产过程中产生的CO和
吸收在生产过程中产生的CO和 等气体,铜液吸收CO的反应是放热反应,其反应方程式为:
等气体,铜液吸收CO的反应是放热反应,其反应方程式为: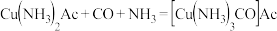 ; 完成下列填空:
; 完成下列填空:  如果要提高上述反应的反应速率,可以采取的措施是
如果要提高上述反应的反应速率,可以采取的措施是  选填编号
选填编号
 减压
减压  增加
增加 的浓度
的浓度  升温
升温  及时移走产物
及时移走产物  铜液中的氨可吸收二氧化碳,写出该反应的化学方程式:
铜液中的氨可吸收二氧化碳,写出该反应的化学方程式:  简述铜液吸收CO及铜液再生的操作步骤
简述铜液吸收CO及铜液再生的操作步骤 注明吸收和再生的条件
注明吸收和再生的条件 .
. 铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为
铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为  已知
已知 与
与 分子结构相似,
分子结构相似, 的电子式是
的电子式是  熔点高于
熔点高于 ,其原因是
,其原因是  提取的
提取的 中含少量
中含少量 、SO
、SO 。将产品溶解,加入
。将产品溶解,加入 ,加热至沸,再加入
,加热至沸,再加入 溶液,过滤,蒸发结晶,得到工业氯化铵.加热至沸的目的是
溶液,过滤,蒸发结晶,得到工业氯化铵.加热至沸的目的是  称取
称取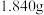 小苏打样品
小苏打样品 含少量
含少量 ,配置成250mL溶液,取
,配置成250mL溶液,取 用
用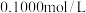 盐酸滴定,消耗盐酸
盐酸滴定,消耗盐酸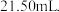 实验中所需的定量仪器出滴定管外,还有
实验中所需的定量仪器出滴定管外,还有  样品中
样品中 质量分数为
质量分数为  将一定量小苏打样品
将一定量小苏打样品 含少量
含少量 溶于足量盐酸,蒸干后称量固体质量,也可测量小苏打的含量。若蒸发过程中有少量液体溅出,则测定结果
溶于足量盐酸,蒸干后称量固体质量,也可测量小苏打的含量。若蒸发过程中有少量液体溅出,则测定结果
您最近一年使用:0次
2019-12-27更新
|
148次组卷
|
2卷引用:2019年秋高三化学复习强化练习—— 酸碱中和滴定
3 . 盐酸羟胺(化学式为 )是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
)是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
实验室以环己酮肟、盐酸为原料制备盐酸羟胺的反应原理如下:
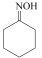 (环己酮肟)
(环己酮肟)
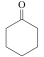 (环己酮)
(环己酮)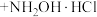
制备盐酸羟胺的实验装置如图所示(加热、搅拌和夹持装置已省略)。
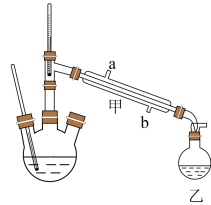
盐酸羟胺在不同温度下的溶解度如下表:
(1)仪器甲中进水口应为___________ 。
A.a处 B.b处 C.a处或b处均可
(2)反应过程中,将环已酮不断蒸出的主要原因是___________ 。
(3)容器乙中收集到环己酮的水溶液,环已酮和水之间存在的相互作用有___________。
(4)反应后,从三口烧瓶的溶液中获取盐酸羟胺的实验方法为___________。
称取0.500g由上述方法制得的盐酸羟胺产品,加水配制成100mL溶液。量取20.00mL于锥形瓶中,加入适量稀硫酸酸化,再加入过量硫酸铁铵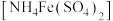 溶液充分反应,接着加入足量磷酸溶液(与
溶液充分反应,接着加入足量磷酸溶液(与 形成无色配合物),最后用
形成无色配合物),最后用 的酸性溶液滴定,达到滴定终点时消耗
的酸性溶液滴定,达到滴定终点时消耗 的酸性溶液的体积为11.35mL。
的酸性溶液的体积为11.35mL。
反应原理为:①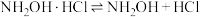
②
③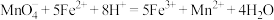
(5)将反应②补充完整,并标出电子转移的方向和数目___________ 。
(6)配制上述盐酸羟胺溶液所需要的定量仪器有___________ 。
A.电子天平 B.100mL容量瓶 C.滴定管 D.量筒
判断滴定终点的现象为___________ 。
(7)通过计算判断该产品的纯度级别___________ 。(写出计算过程)
已知:
 )是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
)是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。实验室以环己酮肟、盐酸为原料制备盐酸羟胺的反应原理如下:
 (环己酮肟)
(环己酮肟)
 (环己酮)
(环己酮)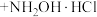
制备盐酸羟胺的实验装置如图所示(加热、搅拌和夹持装置已省略)。

盐酸羟胺在不同温度下的溶解度如下表:
| 温度(℃) | 溶解度(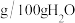 ) ) |
| 20 | 46.7 |
| 40 | 54.9 |
| 60 | 63.2 |
| 80 | 71.1 |
A.a处 B.b处 C.a处或b处均可
(2)反应过程中,将环已酮不断蒸出的主要原因是
(3)容器乙中收集到环己酮的水溶液,环已酮和水之间存在的相互作用有___________。
| A.共价键 | B.离子键 | C.氢键 | D.范德华力 |
| A.冷却结晶 | B.渗析 | C.蒸馏 | D.萃取、分液 |
称取0.500g由上述方法制得的盐酸羟胺产品,加水配制成100mL溶液。量取20.00mL于锥形瓶中,加入适量稀硫酸酸化,再加入过量硫酸铁铵
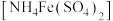 溶液充分反应,接着加入足量磷酸溶液(与
溶液充分反应,接着加入足量磷酸溶液(与 形成无色配合物),最后用
形成无色配合物),最后用 的酸性溶液滴定,达到滴定终点时消耗
的酸性溶液滴定,达到滴定终点时消耗 的酸性溶液的体积为11.35mL。
的酸性溶液的体积为11.35mL。反应原理为:①
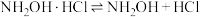
②

③
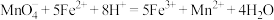
(5)将反应②补充完整,并标出电子转移的方向和数目
(6)配制上述盐酸羟胺溶液所需要的定量仪器有
A.电子天平 B.100mL容量瓶 C.滴定管 D.量筒
判断滴定终点的现象为
(7)通过计算判断该产品的纯度级别
| 纯度级别 | 优级纯 | 分析纯 | 化学纯 |
质量分数 | 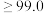 |  |  |

您最近一年使用:0次
2024-01-13更新
|
363次组卷
|
3卷引用:上海市四区联考2023-2024学年高三上学期化学一模试卷
上海市四区联考2023-2024学年高三上学期化学一模试卷(已下线)专题09 化学实验综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)上海市嘉定区第二中学2023-2024学年高三上学期第一次质量调研 化学试卷
4 . 在一定条件下,可逆反应A+B mC变化如下图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后增大容器内压强的变化情况,问:
mC变化如下图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后增大容器内压强的变化情况,问:
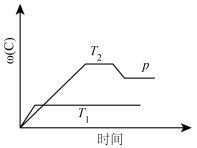
(1)温度T1_____ T2(填“大于”“等于”或“小于”),正反应是_____ (填“吸热”或“放热”)反应。
(2)如果A、B、C均为气体,则m_____ 2(填“大于”“等于”或“小于”)。
(3)当温度和容积不变时,如向平衡体系中加入一定量的某稀有气体,则体系的压强_____ ,平衡_____ 移动。
(4)当温度和压强不变时,如向平衡体系中加入一定量的某稀有气体,平衡_____ 移动。
 mC变化如下图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后增大容器内压强的变化情况,问:
mC变化如下图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后增大容器内压强的变化情况,问:
(1)温度T1
(2)如果A、B、C均为气体,则m
(3)当温度和容积不变时,如向平衡体系中加入一定量的某稀有气体,则体系的压强
(4)当温度和压强不变时,如向平衡体系中加入一定量的某稀有气体,平衡
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
5 . 钒及其化合物在工业上有许多用途。某钒精矿的主要成分及质量分数如下表:
一种从该钒精矿中提取五氧化二钒的流程如下:
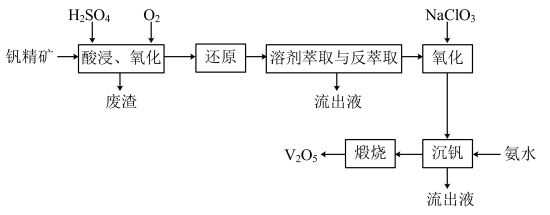
(1)萃取剂对四价钒具有高选择性,且萃取Fe3+而不萃取Fe2+,所以萃取前可用___________ (填名称,下同)对浸出液进行“还原”处理。为检验“还原”后的滤液中是否含有Fe3+,可选用的化学试剂是___________
(2)“溶剂萃取与反萃取”可表示为:VO2++(HR2PO4)2(O) (VOR2PO4)2(O)+2H+。其中(HR2PO4)2(O)为萃取剂,为了提高VO2+的产率,反萃取剂应该呈
(VOR2PO4)2(O)+2H+。其中(HR2PO4)2(O)为萃取剂,为了提高VO2+的产率,反萃取剂应该呈___________ 性(填“酸”“碱”或“中”)。
| 物质 | V2O5 | V2O3 | K2O | SiO2 | Fe2O3 | Al2O3 |
| 质量分数% | 0.81 | 1.70 | 2.11 | 63.91 | 5.86 | 12.51 |

(1)萃取剂对四价钒具有高选择性,且萃取Fe3+而不萃取Fe2+,所以萃取前可用
(2)“溶剂萃取与反萃取”可表示为:VO2++(HR2PO4)2(O)
 (VOR2PO4)2(O)+2H+。其中(HR2PO4)2(O)为萃取剂,为了提高VO2+的产率,反萃取剂应该呈
(VOR2PO4)2(O)+2H+。其中(HR2PO4)2(O)为萃取剂,为了提高VO2+的产率,反萃取剂应该呈
您最近一年使用:0次
解题方法
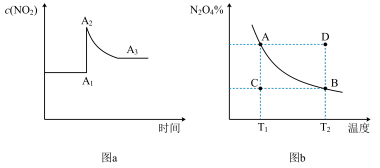
6 . 在密闭容器中发生反应 。图a表示恒温条件下
。图a表示恒温条件下 随时间的变化情况,图b表示恒压条件下,平衡体系中
随时间的变化情况,图b表示恒压条件下,平衡体系中 的质量分数随温度变化情况。下列说法不正确的是
的质量分数随温度变化情况。下列说法不正确的是
 。图a表示恒温条件下
。图a表示恒温条件下 随时间的变化情况,图b表示恒压条件下,平衡体系中
随时间的变化情况,图b表示恒压条件下,平衡体系中 的质量分数随温度变化情况。下列说法不正确的是
的质量分数随温度变化情况。下列说法不正确的是
A.图a中, 变化的原因可能是缩小体积 变化的原因可能是缩小体积 |
B.依据图b分析可知,该化学反应 |
| C.图b中,C→A所需的时间为x,D→B所需时间为y,则x<y |
D.若要测定 的相对分子质量,尽量选择低压、高温条件 的相对分子质量,尽量选择低压、高温条件 |
您最近一年使用:0次
解题方法
7 . 工业上以铬铁矿(主要成分为 ,含Al、Si氧化物等杂质)为主要原料制备红矾钠
,含Al、Si氧化物等杂质)为主要原料制备红矾钠 的工艺流程如图。回答下列问题:
的工艺流程如图。回答下列问题:

(1) 中Fe元素的化合价
中Fe元素的化合价___________ ,焙烧的目的是将 转化为
转化为 并将Al、Si氧化物转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是
并将Al、Si氧化物转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是___________ 。
(2)滤渣2的成分___________ (填化学式)滤渣提纯后的用途___________ 。
(3)加入 酸化的作用是
酸化的作用是___________ (结合化学用语简述)。
(4)蒸发结晶时,过度蒸发将导致___________
(5)该小组用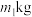 铬铁矿(
铬铁矿( 的质量分数60%)制备
的质量分数60%)制备 ,最终得到产品
,最终得到产品 ,产率为
,产率为___________ (列出计算式)
 ,含Al、Si氧化物等杂质)为主要原料制备红矾钠
,含Al、Si氧化物等杂质)为主要原料制备红矾钠 的工艺流程如图。回答下列问题:
的工艺流程如图。回答下列问题:
(1)
 中Fe元素的化合价
中Fe元素的化合价 转化为
转化为 并将Al、Si氧化物转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是
并将Al、Si氧化物转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是(2)滤渣2的成分
(3)加入
 酸化的作用是
酸化的作用是(4)蒸发结晶时,过度蒸发将导致
(5)该小组用
 铬铁矿(
铬铁矿( 的质量分数60%)制备
的质量分数60%)制备 ,最终得到产品
,最终得到产品 ,产率为
,产率为
您最近一年使用:0次
解题方法
8 . 一定条件下,利用R(g)制备M(g),反应为① ,过程中发生②
,过程中发生② 和③
和③ 两个副反应,反应历程如图所示。下列说法正确的是
两个副反应,反应历程如图所示。下列说法正确的是
 ,过程中发生②
,过程中发生② 和③
和③ 两个副反应,反应历程如图所示。下列说法正确的是
两个副反应,反应历程如图所示。下列说法正确的是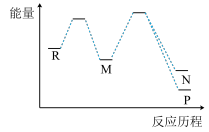
| A.反应③比反应①更快达到平衡 |
| B.温度越高,产物中M的纯度越高 |
| C.一定时间内,使用合适的催化剂可减少体系中P的含量 |
D.增大R的浓度,反应①②③的 增大, 增大, 减小 减小 |
您最近一年使用:0次
2023-12-02更新
|
430次组卷
|
4卷引用:寒假作业03 化学平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)
(已下线)寒假作业03 化学平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)广东省2024届普通高中毕业班高三上学期第二次调研考试化学试题2024届广东省茂名市化州市高三上学期第二次调研考试化学试题(已下线)化学(广东卷01)-2024年高考押题预测卷
9 . 对注射器[存在平衡: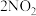 (红棕色)
(红棕色)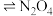 (无色)
(无色)  ]进行如下操作,下列说法正确的是
]进行如下操作,下列说法正确的是
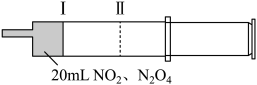
步骤1:活塞从Ⅰ处→拉至Ⅱ处
步骤2:活塞从Ⅱ处→推向Ⅰ处
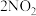 (红棕色)
(红棕色)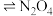 (无色)
(无色)  ]进行如下操作,下列说法正确的是
]进行如下操作,下列说法正确的是
步骤1:活塞从Ⅰ处→拉至Ⅱ处
步骤2:活塞从Ⅱ处→推向Ⅰ处
| A.步骤1注射器中颜色变深 |
B.步骤2注射器中颜色先变深后变浅,变浅的原因是消耗更多 |
C.若将活塞固定在I处,升高温度,注射器中颜色变深,则说明 >0 >0 |
D.当体系处于稳定状态时,混合气体中 的百分含量:Ⅰ>Ⅱ 的百分含量:Ⅰ>Ⅱ |
您最近一年使用:0次
名校
解题方法
10 . 合成氨工业中采用循环操作,主要是为了
| A.增大化学反应速率 | B.提高平衡混合物中氨的含量 |
| C.降低氨的沸点 | D.提高氮气和氢气的利用率 |
您最近一年使用:0次
2023-06-30更新
|
504次组卷
|
16卷引用:湖北省武汉市长虹中学2021-2022学年高二上学期10月月考化学试卷
湖北省武汉市长虹中学2021-2022学年高二上学期10月月考化学试卷山西省怀仁市2021-2022学年高二上学期期中化学试题人教2019版选择性必修一第二章 第四节 化学反应的调控 课后习题河北省石家庄市2021-2022学年高二上学期期末考试化学试题(已下线)2.4 化学反应的调控-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)新疆喀什地区疏附县第一中学2022-2023学年高二上学期期末考试化学试题(已下线)化学反应速率与化学平衡——课时7化学反应的调控(已下线)第08讲 化学反应的调控-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)陕西省西安市鄠邑区2022-2023学年高一下学期6月期末考试化学试题 广东实验中学越秀学校2023-2024学年高二上学期期中考试化学试题四川省遂宁市射洪中学校2023-2024学年高二上学期11月期中化学试题青海省西宁市大通县2023-2024学年高二上学期期末考试化学试题吉林省吉林市2022-2023学年高二上学期期中调研测试化学试题黑龙江省虎林市高级中学2022-2023学年高二上学期期中考试化学试题云南省玉溪市华宁县第二中学2021-2022年高二下学期开学考试化学试题贵州神贵阳市2023-2024学年清镇市博雅实验学校高二上学期第四次月考化学试卷



