名校
解题方法
1 . 一定压强下,向 密闭容器中充入
密闭容器中充入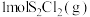 和
和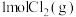 ,发生反应:
,发生反应: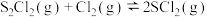 。
。 的消耗速率
的消耗速率 、
、 的消耗速率
的消耗速率 、温度
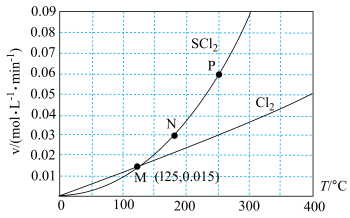
、温度 三者的关系如图所示。下列说法正确的是
三者的关系如图所示。下列说法正确的是
 密闭容器中充入
密闭容器中充入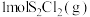 和
和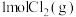 ,发生反应:
,发生反应: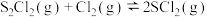 。
。 的消耗速率
的消耗速率 、
、 的消耗速率
的消耗速率 、温度
、温度 三者的关系如图所示。下列说法正确的是
三者的关系如图所示。下列说法正确的是
A.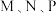 三点对应状态下,达到平衡状态的是 三点对应状态下,达到平衡状态的是 |
B.温度升高,平衡常数 增大 增大 |
C.保持其他条件不变,若投料改为通入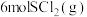 ,平衡时 ,平衡时 的体积分数增大 的体积分数增大 |
D.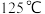 时,平衡时 时,平衡时 的消耗速率大于 的消耗速率大于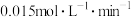 |
您最近一年使用:0次
名校
2 . 如图所示,甲容器容积固定不变,乙容器有可移动的活塞。甲中充入2mol SO2和1mol O2,乙中充入4mol SO3和1mol He,在恒定温度和相同的催化剂条件下,发生如下反应: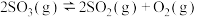 ,下列有关说法正确的是
,下列有关说法正确的是
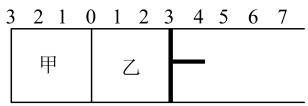
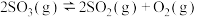 ,下列有关说法正确的是
,下列有关说法正确的是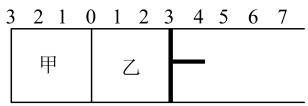
A.若活塞固定在6处不动,达平衡时甲乙两容器中的压强: |
B.若活塞固定在3处不动,达平衡时甲乙两容器中 的浓度: 的浓度: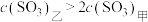 |
C.若活塞固定在3处不动,达平衡时甲乙两容器中 的体积分数: 的体积分数: |
D.若活塞固定在7处不动,达平衡时甲乙两容器中 的物质的量分数相等 的物质的量分数相等 |
您最近一年使用:0次
名校
解题方法
3 . 下列实验方案、现象和结论都正确的是
| 实验操作 | 现象 | 结论 | |
| A | 用玻璃棒蘸取新制氯水涂在pH试纸上 | pH试纸变红色 | 氯水显酸性 |
| B | 向酸性KMnO4和H2C2O4的混合溶液中 加入少量MnSO4(s) | 气泡迅速增多 溶液很快褪色 | MnSO4作催化剂 |
| C | 分别取5mL0.2mol/LNa2S2O3溶液和 10mL0.1mol/LNa2S2O3溶液于两支试管中 然后同时加入10mL0.1mol/LH2SO4溶液 | 产生等量浑浊 前者时间更短 | 增大Na2S2O3浓度 可以加快反应速率 |
| D | 对平衡体系2HI H2+I2(g)压缩容器 H2+I2(g)压缩容器 | 颜色加深 | 平衡正向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-09-17更新
|
263次组卷
|
3卷引用:浙江省海宁市高级中学2022-2023学年高二上学期10月月考化学试题
名校
4 . 工业上能利用甲烷重整制合成气 、
、 ,反应体系中主要反应如下:
,反应体系中主要反应如下:
主反应I.


副反应II.


已知在727℃时, 。
。
据此分析,下列判断错误的是
 、
、 ,反应体系中主要反应如下:
,反应体系中主要反应如下:主反应I.



副反应II.



已知在727℃时,
 。
。据此分析,下列判断错误的是
A.当体系中反应达到平衡时, |
B.727℃时,反应 的平衡常数 的平衡常数 |
| C.若反应体系为恒温体系,压缩容器容积,平衡时混合气体的平均摩尔质量增大 |
| D.若反应体系为恒温恒容体系,当气体的总压强不变时,反应达到平衡状态 |
您最近一年使用:0次
2023-09-01更新
|
280次组卷
|
2卷引用:安徽省合肥市第八中学2022-2023学年高三上学期12月月考化学试题
名校
5 . 常温下某同学将一定量的 充入注射器中后封口,测得拉伸和压缩注射器的活塞过程中气体透光率随时间的变化如图所示(已知气体颜色越深,透光率越小;
充入注射器中后封口,测得拉伸和压缩注射器的活塞过程中气体透光率随时间的变化如图所示(已知气体颜色越深,透光率越小;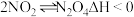 )。下列说法正确的是
)。下列说法正确的是
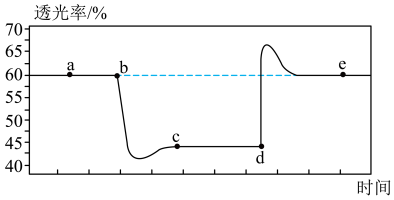
 充入注射器中后封口,测得拉伸和压缩注射器的活塞过程中气体透光率随时间的变化如图所示(已知气体颜色越深,透光率越小;
充入注射器中后封口,测得拉伸和压缩注射器的活塞过程中气体透光率随时间的变化如图所示(已知气体颜色越深,透光率越小;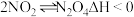 )。下列说法正确的是
)。下列说法正确的是
A. 点操作为压缩针管,因此 点操作为压缩针管,因此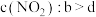 |
B. 点的操作为拉伸注射器到任意位置 点的操作为拉伸注射器到任意位置 |
C. 点平均相对分子质量与 点平均相对分子质量与 点相等 点相等 |
D.若注射器绝热,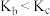 |
您最近一年使用:0次
2023-08-11更新
|
371次组卷
|
2卷引用:陕西西安市第八十三中学2023-2024学年高二上学期10月月考化学试题
6 .  可作大型船舶的绿色燃料,可由CO或
可作大型船舶的绿色燃料,可由CO或 制备。工业上用
制备。工业上用 制备
制备 的原理如下:
的原理如下:
反应1:
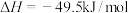
反应2:
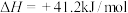 (副反应)
(副反应)
(1) ,该反应的
,该反应的
___________  。
。
(2)将 和
和 按
按 通入密闭容器中发生反应1和反应2,分别在
通入密闭容器中发生反应1和反应2,分别在 、
、 、
、 下改变反应温度,测得
下改变反应温度,测得 的平衡转化率(
的平衡转化率( )以及生成
)以及生成 、CO选择性(S)的变化如图(选择性为目标产物在总产物中的比率)。
、CO选择性(S)的变化如图(选择性为目标产物在总产物中的比率)。 下
下 随温度变化趋势的是曲线
随温度变化趋势的是曲线___________ (填“a”“b”或“c”)。
②随着温度升高,a、b、c三条曲线接近重合的原因是___________ 。
③P点对应的反应2的平衡常数
___________ (保留两位有效数字)。
④分子筛膜反应器可提高反应1的平衡转化率、且实现 选择性100%,原理如图所示。分子筛膜反应器可提高转化率的原因是
选择性100%,原理如图所示。分子筛膜反应器可提高转化率的原因是___________ 。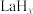 ,将带来系列技术变革。某小组据此设计了如下装置(如图),以电化学方法进行反应1。
,将带来系列技术变革。某小组据此设计了如下装置(如图),以电化学方法进行反应1。
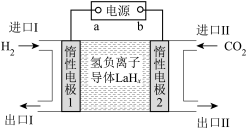
①电极a为电源的___________ (填“正极”或“负极”)。
②生成 的电极反应式为
的电极反应式为___________ 。
③若反应2也同时发生,出口Ⅱ为CO、 、
、 的混合气,且
的混合气,且 ,则惰性电极2的电流效率
,则惰性电极2的电流效率 为
为___________ (
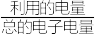 ×100%)。
×100%)。
 可作大型船舶的绿色燃料,可由CO或
可作大型船舶的绿色燃料,可由CO或 制备。工业上用
制备。工业上用 制备
制备 的原理如下:
的原理如下:反应1:

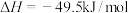
反应2:

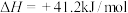 (副反应)
(副反应)(1)
 ,该反应的
,该反应的
 。
。(2)将
 和
和 按
按 通入密闭容器中发生反应1和反应2,分别在
通入密闭容器中发生反应1和反应2,分别在 、
、 、
、 下改变反应温度,测得
下改变反应温度,测得 的平衡转化率(
的平衡转化率( )以及生成
)以及生成 、CO选择性(S)的变化如图(选择性为目标产物在总产物中的比率)。
、CO选择性(S)的变化如图(选择性为目标产物在总产物中的比率)。
 下
下 随温度变化趋势的是曲线
随温度变化趋势的是曲线②随着温度升高,a、b、c三条曲线接近重合的原因是
③P点对应的反应2的平衡常数

④分子筛膜反应器可提高反应1的平衡转化率、且实现
 选择性100%,原理如图所示。分子筛膜反应器可提高转化率的原因是
选择性100%,原理如图所示。分子筛膜反应器可提高转化率的原因是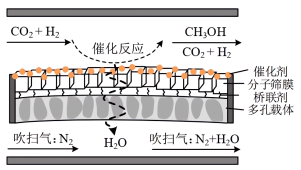
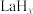 ,将带来系列技术变革。某小组据此设计了如下装置(如图),以电化学方法进行反应1。
,将带来系列技术变革。某小组据此设计了如下装置(如图),以电化学方法进行反应1。
①电极a为电源的
②生成
 的电极反应式为
的电极反应式为③若反应2也同时发生,出口Ⅱ为CO、
 、
、 的混合气,且
的混合气,且 ,则惰性电极2的电流效率
,则惰性电极2的电流效率 为
为
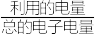 ×100%)。
×100%)。
您最近一年使用:0次
2023-06-03更新
|
704次组卷
|
5卷引用:湖南省宁乡市实验中学等多校联考2024届高三下学期一轮复习总结性考试(月考)化学试题
湖南省宁乡市实验中学等多校联考2024届高三下学期一轮复习总结性考试(月考)化学试题重庆市巴蜀中学校2023学年高三模拟预测化学试题(已下线)专题14 化学反应原理综合题-2023年高考化学真题题源解密(新高考专用)广西名校2023-2024学年高三上学期仿真卷(一)化学试题湖南省长沙市雅礼中学2023-2024学年高三上学期1月期末化学试题
名校
解题方法
7 . CH4和CO2联合重整能减少温室气体的排放。其主要反应为:
①CH4(g)+CO2(g) 2H2(g)+2CO(g)
2H2(g)+2CO(g)
②H2(g)+CO2(g) H2O(g)+CO(g)
H2O(g)+CO(g)
其他条件相同时,投料比n(CH4):n(CO2)为1∶1.3,不同温度下反应的结果如图。
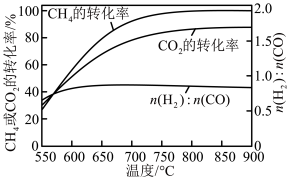
下列说法不正确 的是
①CH4(g)+CO2(g)
 2H2(g)+2CO(g)
2H2(g)+2CO(g)②H2(g)+CO2(g)
 H2O(g)+CO(g)
H2O(g)+CO(g)其他条件相同时,投料比n(CH4):n(CO2)为1∶1.3,不同温度下反应的结果如图。

下列说法
| A.550~600℃,升温更有利于反应①,反应①先达到平衡 |
| B.n(H2)∶n(CO)始终低于1.0,与反应②有关 |
| C.加压有利于增大CH4和CO2反应的速率但不利于提高二者的平衡转化率 |
| D.若不考虑其他副反应,体系中存在:4[c(CH4)+c(CO)+c(CO2)]=2.3[4c(CH4)+2c(H2)+2c(H2O)] |
您最近一年使用:0次
2023-03-31更新
|
1569次组卷
|
12卷引用:北京市第一○一中学2023-2024学年高三上学期10月月考化学试题
北京市第一○一中学2023-2024学年高三上学期10月月考化学试题北京市清华大学附属中学2023-2024学年高三上学期12月统练(六)化学试题北京市第八中学2023-2024学年高三上学期12月月考化学试题陕西省咸阳市实验中学2023-2024学年高二上学期段性检测(二)化学试题安徽省淮北市第一中学2023-2024学年高二上学期第三次月考化学试题北京市西城区2023届一模考试化学试题(已下线)专题15 化学反应速率和化学平衡(已下线)化学-2023年高考押题预测卷03(江苏卷)(含考试版、全解全析、参考答案、答题卡)江苏省南京师范大学附属中学2023届高三下学期5月模拟考试化学试题北京市十一学校2022-2023学年高二下学期期末考试化学试题北京市第六十六中学2023-2024学年高二上学期期中质量检测化学试题北京师范大学附属中学2023-2024学年高三上学期期中考试化学试题
名校
解题方法
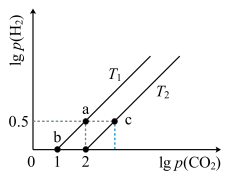
8 . 已知CH4(g)+CO2(g) 2CO(g)+2H2(g) △H>0。在密闭容器中充入等体积的反应物,测得平衡时CO2、H2的气体压强对数有如图所示关系,压强的单位为MPa。下列说法错误的是
2CO(g)+2H2(g) △H>0。在密闭容器中充入等体积的反应物,测得平衡时CO2、H2的气体压强对数有如图所示关系,压强的单位为MPa。下列说法错误的是
 2CO(g)+2H2(g) △H>0。在密闭容器中充入等体积的反应物,测得平衡时CO2、H2的气体压强对数有如图所示关系,压强的单位为MPa。下列说法错误的是
2CO(g)+2H2(g) △H>0。在密闭容器中充入等体积的反应物,测得平衡时CO2、H2的气体压强对数有如图所示关系,压强的单位为MPa。下列说法错误的是
A.a点时对应的Kp= (MPa) (MPa) |
| B.T1>T2 |
| C.c点对应的p(CO2)=1000MPa |
| D.当容器中CH4与CO的压强比为1∶2时,不能说明该反应达平衡状态 |
您最近一年使用:0次
2023-03-20更新
|
484次组卷
|
3卷引用:重庆市巴蜀中学校2023届高三适应性月考卷(七)化学试题
9 . 根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 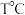 压缩装有 压缩装有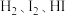 混合气体(已达平衡)的容器,气体颜色加深 混合气体(已达平衡)的容器,气体颜色加深 | 平衡向生成 的方向移动 的方向移动 |
B | 在硫酸钡沉淀中加入浓碳酸钠溶液充分搅拌后,取沉淀(已洗净)放入盐酸中,有气泡产生 |  |
C | 室温下将 晶体与 晶体与 晶体在小烧杯中混合,烧杯壁变凉 晶体在小烧杯中混合,烧杯壁变凉 | 该反应的 |
D | 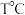 用 用 试纸测得 试纸测得 的 的 溶液 溶液 约为9, 约为9, 的 的 溶液 溶液 约为8 约为8 | 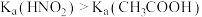 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-13更新
|
564次组卷
|
2卷引用:湖北省襄阳市第一中学2022-2023学年高二下学期3月月考化学试题
2023高三·全国·专题练习
名校
解题方法
10 . 工业上用丁烷催化脱氢制备丁烯: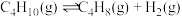 (正反应吸热),将丁烷和氢气以一定的配比通过填充有催化剂的反应器(氢气的作用是活化催化剂),反应的平衡转化率、产率与温度、投料比有关。下列判断不正确的是
(正反应吸热),将丁烷和氢气以一定的配比通过填充有催化剂的反应器(氢气的作用是活化催化剂),反应的平衡转化率、产率与温度、投料比有关。下列判断不正确的是
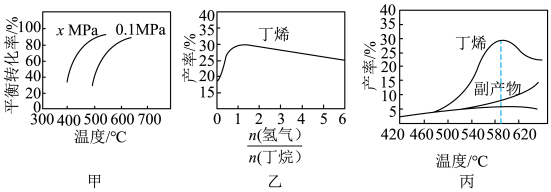
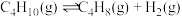 (正反应吸热),将丁烷和氢气以一定的配比通过填充有催化剂的反应器(氢气的作用是活化催化剂),反应的平衡转化率、产率与温度、投料比有关。下列判断不正确的是
(正反应吸热),将丁烷和氢气以一定的配比通过填充有催化剂的反应器(氢气的作用是活化催化剂),反应的平衡转化率、产率与温度、投料比有关。下列判断不正确的是
| A.由图甲可知,x小于0.1 |
B.由图乙可知,丁烯产率先增大后减小,减小的原因是氢气是产物之一,随着 增大,逆反应速率减小 增大,逆反应速率减小 |
C.由图丙可知,产率在 前随温度升高而增大的原因可能是温度升高平衡正向移动 前随温度升高而增大的原因可能是温度升高平衡正向移动 |
D.由图丙可知,丁烯产率在 后快速降低的主要原因是丁烯高温分解生成副产物 后快速降低的主要原因是丁烯高温分解生成副产物 |
您最近一年使用:0次



