名校
1 . 将BaO2放入密闭真空容器中,反应2BaO2(s) 2BaO(s)+O2(g)达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡不同
2BaO(s)+O2(g)达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡不同
 2BaO(s)+O2(g)达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡不同
2BaO(s)+O2(g)达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡不同 | A.保持体积和温度不变,充入一定量的氧气 | B.保持温度不变,缩小容器的体积 |
| C.保持体积不变,升高温度 | D.保持体积和温度不变,加入BaO2 |
您最近一年使用:0次
2017-10-22更新
|
351次组卷
|
6卷引用:河南省八市2017-2018学年高二上学期第一次质量检测化学试题
名校
2 . 合成氨对化学工业和国防工业具有重要意义。
(1)向合成塔中按物质的量之比l:4充入N2、H2进行氨的合成,图A为T℃时平衡混合物中氨气的体积分数与压强(p)的关系图。
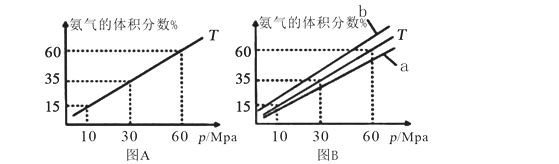
①图A中氨气的体积分数为15%时,H2的转化率为_______ 。
②图B中T=500℃,则温度为450℃时对应的曲线是_______ (填“a”或“b”)。
(2)合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为:CH4(g)+H2O(g) CO(g)+3H2(g) △H>0,一定温度下,在体积为2 L的恒容容器中发生上述反应,各物质的物质的量变化如下表:
CO(g)+3H2(g) △H>0,一定温度下,在体积为2 L的恒容容器中发生上述反应,各物质的物质的量变化如下表:
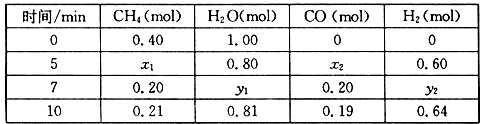
①分析表中数据,判断5 min时反应是否处于平衡状态?_____ (填“是”或“否”)。
②该温度下,上述反应的平衡常数K=_____________________ 。
③反应在7~10 min内,CO的物质的量减少的原因可能是____________ (填字母)。
a.减少CH4的物质的量 b.降低温度 c.升高温度 d.充入H2
④下列方法中可以证明上述反应已达平衡状态的是___________ 。
a.单位时间内生成3n mol H2的同时生成n mol CO
b.容器内压强不再变化
c.混合气体密度不再变化
d.混合气体的平均相对分子质量不再变化
e.CH4的质量分数不再变化
⑤已知碳的气化反应在不同温度下平衡常数的对数值(lgK)如下表:
则反应CO(g)+H2O(g) CO2(g)+H2(g)在900K时,该反应平衡常数的对数值(lgK)=
CO2(g)+H2(g)在900K时,该反应平衡常数的对数值(lgK)=_______ 。
(3)在容积可变的密闭容器中发生反应:mA(g)+nB(g) pC(g),在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如下表:
pC(g),在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如下表:
①当压强从2×105 Pa增加到5×105 Pa时,平衡______ 移动(填“正向、逆向或不”)。
②当压强为1×106 Pa时,此反应的平衡常数表达式为______________ 。
(1)向合成塔中按物质的量之比l:4充入N2、H2进行氨的合成,图A为T℃时平衡混合物中氨气的体积分数与压强(p)的关系图。

①图A中氨气的体积分数为15%时,H2的转化率为
②图B中T=500℃,则温度为450℃时对应的曲线是
(2)合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为:CH4(g)+H2O(g)
 CO(g)+3H2(g) △H>0,一定温度下,在体积为2 L的恒容容器中发生上述反应,各物质的物质的量变化如下表:
CO(g)+3H2(g) △H>0,一定温度下,在体积为2 L的恒容容器中发生上述反应,各物质的物质的量变化如下表:
①分析表中数据,判断5 min时反应是否处于平衡状态?
②该温度下,上述反应的平衡常数K=
③反应在7~10 min内,CO的物质的量减少的原因可能是
a.减少CH4的物质的量 b.降低温度 c.升高温度 d.充入H2
④下列方法中可以证明上述反应已达平衡状态的是
a.单位时间内生成3n mol H2的同时生成n mol CO
b.容器内压强不再变化
c.混合气体密度不再变化
d.混合气体的平均相对分子质量不再变化
e.CH4的质量分数不再变化
⑤已知碳的气化反应在不同温度下平衡常数的对数值(lgK)如下表:
| 气化反应式 | lgK | ||
| 700K | 900K | 1200K | |
| C(s)+H2O(g)=CO(g)+H2(g) | -2.64 | -0.39 | 1.58 |
| C(s)+2H2O(g)=CO2(g)+2H2(g) | -1.67 | -0.03 | 1.44 |
则反应CO(g)+H2O(g)
 CO2(g)+H2(g)在900K时,该反应平衡常数的对数值(lgK)=
CO2(g)+H2(g)在900K时,该反应平衡常数的对数值(lgK)=(3)在容积可变的密闭容器中发生反应:mA(g)+nB(g)
 pC(g),在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如下表:
pC(g),在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如下表:| 压强p/Pa | 2×105 | 5×105 | 1×106 |
| c(A)/mol•L-1 | 0.08 | 0.20 | 0.44 |
①当压强从2×105 Pa增加到5×105 Pa时,平衡
②当压强为1×106 Pa时,此反应的平衡常数表达式为
您最近一年使用:0次
2017-10-22更新
|
464次组卷
|
2卷引用:四川省成都市郫都区第一中学2017-2018学年高二上学期第一次月考化学试题
名校
3 . 利用催化技术可将汽车尾气中的 NO和 CO转变成CO2和N2,化学方程式:2NO(g)+2CO(g)  2CO2(g)+N2(g)。某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
2CO2(g)+N2(g)。某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
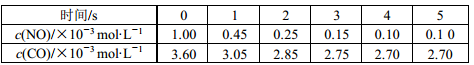
下列说法中不正确的是
 2CO2(g)+N2(g)。某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
2CO2(g)+N2(g)。某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
下列说法中不正确的是
| A.2 s内的平均反应速率 v(N2)=1.875×10-4 mol·L-1·s-1 |
| B.在该温度下,反应的平衡常数 K=5 |
| C.若将容积缩小为原来的一半, NO 转化率大于 90% |
| D.使用催化剂可以提高整个过程中 CO 和 NO 的处理量 |
您最近一年使用:0次
名校
4 . 下列反应不能用勒夏特例原理解释的是( )
| A.光照新制的氯水时 溶液的 pH逐渐减小 |
| B.锌与稀硫酸反应,加入少量硫酸铜反应速率加快 |
| C.可用浓氨水和氢氧化钠固体快速制取氨气 |
| D.增大压强,有利于SO2和O2反应生成 SO3 |
您最近一年使用:0次
2017-10-20更新
|
555次组卷
|
3卷引用:四川省成都市第七中学2017-2018学年高二上学期第一次月考化学试题
名校
5 . (1)在密闭容器中充入1molH2和1molI2,压强为P(Pa),并在—定温度下使其发生反应:H2(g)+I2(g)  2HI(g) △H<0。保持容器内气体压强不变,向其中加入1molN2,反应速率
2HI(g) △H<0。保持容器内气体压强不变,向其中加入1molN2,反应速率______ (填“变大”、“ 变小”或“不变”),平衡_________ 移动(填“向正反应方向”、“ 向逆反应方向”或“不”)。
(2)火箭残骸中存在红棕色气体,原因为:N2O4 2NO2(g) △H
2NO2(g) △H
①当温度升高时,气体颜色变深,则反应为_______________ ( “吸热”或“放热”)反应。
②T℃,将1molN2O4充入恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态是____________
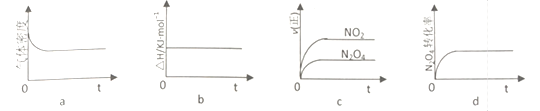
③T℃,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数___________ (填“增大”“ 不变”或“减小”)。
(3)已知 4HCl(g)+O2(g) 2Cl2 (g)+2H2O(g)中 2mol HCl被氧化,放出 57.8kJ 的热量,且部分化学键断裂示意图如下:
2Cl2 (g)+2H2O(g)中 2mol HCl被氧化,放出 57.8kJ 的热量,且部分化学键断裂示意图如下:

①写出该反应的热化学方程式___________________ 。
②断开1 mol H-O键与断开1 molH-C1键所需能量相差约为_________ kJ,H2O中H-O键比HCl中H-Cl键___________ (填“强”或“弱”)。
 2HI(g) △H<0。保持容器内气体压强不变,向其中加入1molN2,反应速率
2HI(g) △H<0。保持容器内气体压强不变,向其中加入1molN2,反应速率(2)火箭残骸中存在红棕色气体,原因为:N2O4
 2NO2(g) △H
2NO2(g) △H①当温度升高时,气体颜色变深,则反应为
②T℃,将1molN2O4充入恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态是
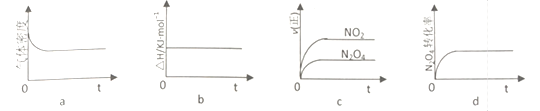
③T℃,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数
(3)已知 4HCl(g)+O2(g)
 2Cl2 (g)+2H2O(g)中 2mol HCl被氧化,放出 57.8kJ 的热量,且部分化学键断裂示意图如下:
2Cl2 (g)+2H2O(g)中 2mol HCl被氧化,放出 57.8kJ 的热量,且部分化学键断裂示意图如下:
①写出该反应的热化学方程式
②断开1 mol H-O键与断开1 molH-C1键所需能量相差约为
您最近一年使用:0次
名校
6 . 下列说法中,能说明化学平衡一定向逆反应方向移动的是
A.N2O4(g) 2NO2(g),改变某一条件后,气体颜色变浅 2NO2(g),改变某一条件后,气体颜色变浅 |
B.N2(g)+3H2(g) 2NH3(g),改变某一条件后,NH3的体积分数减少 2NH3(g),改变某一条件后,NH3的体积分数减少 |
C.H2(g)+I2(g) 2HI(g),单位时间内消耗H2和HI的物质的量之比等于1∶2 2HI(g),单位时间内消耗H2和HI的物质的量之比等于1∶2 |
D.2SO2(g)+O2(g) 2SO3(g),恒温恒压条件下,充入He 2SO3(g),恒温恒压条件下,充入He |
您最近一年使用:0次
名校
7 . —定条件下,在容积为10L的密闭容器中,将2molX和1molY进行如下反应:2X(g)+Y(g) Z(s),经1min达到平衡生成0.3mol的Z,下列说法正确的是
Z(s),经1min达到平衡生成0.3mol的Z,下列说法正确的是
 Z(s),经1min达到平衡生成0.3mol的Z,下列说法正确的是
Z(s),经1min达到平衡生成0.3mol的Z,下列说法正确的是| A.1min内,用Z表示平均反应速率为0.03mol·L-1·min-1 |
| B.将容器容积变为20L,Z的新平衡浓度将等于原平衡浓度的一半 |
| C.当X的体积分数不变时,则说明该反应达到平衡状态 |
| D.若温度和体积不变,往容器内增加1molX,Y的转化率将增大 |
您最近一年使用:0次
2017-10-11更新
|
413次组卷
|
2卷引用:安徽省六安市第一中学2017-2018学年高二9月月考化学试题
名校
8 . 已知一定温度下,2X(g)+Y(g)  mZ(g) ΔH=-a kJ/mol(a>0),现有甲、乙两容积相等且固定不变的密闭容器,在保持该温度下,向密闭容器甲中通入2 mol X和1 mol Y,达到平衡状态时,放出热量b kJ,向密闭容器乙中通入1 mol X和0.5 mol Y,达到平衡时,放出热量c kJ,且b>2c,则a、b、m的值或关系正确的是
mZ(g) ΔH=-a kJ/mol(a>0),现有甲、乙两容积相等且固定不变的密闭容器,在保持该温度下,向密闭容器甲中通入2 mol X和1 mol Y,达到平衡状态时,放出热量b kJ,向密闭容器乙中通入1 mol X和0.5 mol Y,达到平衡时,放出热量c kJ,且b>2c,则a、b、m的值或关系正确的是
 mZ(g) ΔH=-a kJ/mol(a>0),现有甲、乙两容积相等且固定不变的密闭容器,在保持该温度下,向密闭容器甲中通入2 mol X和1 mol Y,达到平衡状态时,放出热量b kJ,向密闭容器乙中通入1 mol X和0.5 mol Y,达到平衡时,放出热量c kJ,且b>2c,则a、b、m的值或关系正确的是
mZ(g) ΔH=-a kJ/mol(a>0),现有甲、乙两容积相等且固定不变的密闭容器,在保持该温度下,向密闭容器甲中通入2 mol X和1 mol Y,达到平衡状态时,放出热量b kJ,向密闭容器乙中通入1 mol X和0.5 mol Y,达到平衡时,放出热量c kJ,且b>2c,则a、b、m的值或关系正确的是| A.m = 4 | B.a = b | C.a <  | D.m < 3 |
您最近一年使用:0次
2017-10-11更新
|
346次组卷
|
3卷引用:河南省襄城高中2017-2018学年高二9月月考化学试题
9 . 已知某可逆反应在密闭容器中进行:A(g)+2B(g) 3C(g)+D(s) ΔH<0,如图中曲线a、b代表一定条件下该反应的进程。若使b曲线变为曲线a,可采取的措施是
3C(g)+D(s) ΔH<0,如图中曲线a、b代表一定条件下该反应的进程。若使b曲线变为曲线a,可采取的措施是
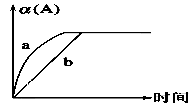
①增大A的浓度 ②缩小容器的容积 ③增大B的浓度 ④增大容器的容积 ⑤加入合适正催化剂
 3C(g)+D(s) ΔH<0,如图中曲线a、b代表一定条件下该反应的进程。若使b曲线变为曲线a,可采取的措施是
3C(g)+D(s) ΔH<0,如图中曲线a、b代表一定条件下该反应的进程。若使b曲线变为曲线a,可采取的措施是 
①增大A的浓度 ②缩小容器的容积 ③增大B的浓度 ④增大容器的容积 ⑤加入合适正催化剂
| A.① | B.②⑤ | C.④ | D.②③ |
您最近一年使用:0次
10 . 反应mX(g)+nY(g) pZ(g);在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是
pZ(g);在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是
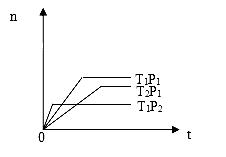
 pZ(g);在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是
pZ(g);在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是
| A.T1<T2,正向吸热 P1<P2 m+n<p | B.T1<T2,正向放热 P1>P2 m+n>p |
| C.T1>T2,正向吸热 P1<P2 m+n<p | D.T1>T2,正向放热P1<P2 m+n>p |
您最近一年使用:0次



