名校
解题方法
1 . 以Cu/ZnO/Al2O3为催化剂,乙醇直接合成乙酸乙酯过程中发生的可逆反应如下:
C2H5OH(g)=CH3CHO(g)+H2(g);ΔH=59kJ·mol-1
2CH3CHO(g)+H2O(g)=C2H5OH(g)+CH3COOH(g);ΔH=-86kJ·mol-1
CH3COOH(g)+C2H5OH(g)=CH3COOC2H5(g)+H2O(g);ΔH=-25kJ·mol-1
2C2H5OH(g)=C2H5OC2H5(g)+H2O(g);ΔH=-44kJ·mol-1
其他条件相同,将无水乙醇经预热气化后以一定流速通过装有催化剂的反应管,将出口处收集到的乙酸乙酯、乙醛、乙醚、乙酸、乙醇冷凝,测得部分有机物占全部有机物的质量分数与反应温度的关系如图所示。下列说法正确的是

C2H5OH(g)=CH3CHO(g)+H2(g);ΔH=59kJ·mol-1
2CH3CHO(g)+H2O(g)=C2H5OH(g)+CH3COOH(g);ΔH=-86kJ·mol-1
CH3COOH(g)+C2H5OH(g)=CH3COOC2H5(g)+H2O(g);ΔH=-25kJ·mol-1
2C2H5OH(g)=C2H5OC2H5(g)+H2O(g);ΔH=-44kJ·mol-1
其他条件相同,将无水乙醇经预热气化后以一定流速通过装有催化剂的反应管,将出口处收集到的乙酸乙酯、乙醛、乙醚、乙酸、乙醇冷凝,测得部分有机物占全部有机物的质量分数与反应温度的关系如图所示。下列说法正确的是

| A.在250~300℃范围,乙醇的转化率随温度的升高而减小 |
| B.在200~325℃范围,乙醇生成乙醚的反应均已到达平衡 |
| C.在300~325℃范围,出口处氢气的量随温度的升高而减小 |
| D.研发使用催化活性高的催化剂有利于提高乙酸乙酯的平衡产率 |
您最近一年使用:0次
2022-03-29更新
|
579次组卷
|
4卷引用:江苏省2022届高三下学期3月第一次调研测试化学试题
江苏省2022届高三下学期3月第一次调研测试化学试题江苏省响水中学2021-2022学年高二下学期第二次学情分析考试化学试题(已下线)秘籍07 化学反应速率及平衡图象剖析-备战2022年高考化学抢分秘籍(全国通用)(已下线)第七章 化学反应速率和化学平衡(测)-2023年高考化学一轮复习讲练测(全国通用)
名校
2 . 某化学小组同学研究温度和压强对反应速率和化学平衡的影响,测得化学反应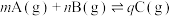
 中C的百分含量(C%)与时间(t)、温度(T)、压强(p)的关系如图所示。下列说法正确的是
中C的百分含量(C%)与时间(t)、温度(T)、压强(p)的关系如图所示。下列说法正确的是
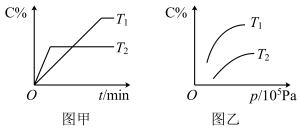
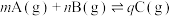
 中C的百分含量(C%)与时间(t)、温度(T)、压强(p)的关系如图所示。下列说法正确的是
中C的百分含量(C%)与时间(t)、温度(T)、压强(p)的关系如图所示。下列说法正确的是
A. 、 、 | B. 、 、 |
C. 、 、 | D. 、 、 |
您最近一年使用:0次
2023-10-15更新
|
492次组卷
|
4卷引用:江苏省常州市第一中学2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
3 . 1000K时,在密闭容器内发生反应:2NO2(g) 2NO(g)+O2(g) ΔH>0,下列图像与该反应体系相符的是
2NO(g)+O2(g) ΔH>0,下列图像与该反应体系相符的是
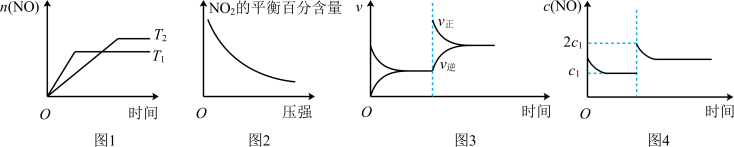
 2NO(g)+O2(g) ΔH>0,下列图像与该反应体系相符的是
2NO(g)+O2(g) ΔH>0,下列图像与该反应体系相符的是
| A.图1表示温度对反应的影响 | B.图2表示压强对物质平衡百分含量的影响 |
| C.图3表示恒容再充入NO2 | D.图4表示体积增大至原来的2倍 |
您最近一年使用:0次
2023-09-13更新
|
361次组卷
|
2卷引用:江苏省连云港市东海县石榴高级中学2022-2023学年高二上学期第一次学情测试化学试题
名校
4 . 碳热还原氧化锌反应可用于循环制氢。碳热还原氧化锌的主要反应如下:
反应I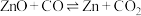 ;
;
反应Ⅱ
在不同容器中分别发生反应I、反应Ⅱ,不同压强(P1或P2)下分别达平衡时,两个反应中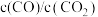 随温度变化的关系如图所示。下列说法正确的是
随温度变化的关系如图所示。下列说法正确的是
反应I
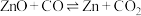 ;
;反应Ⅱ

在不同容器中分别发生反应I、反应Ⅱ,不同压强(P1或P2)下分别达平衡时,两个反应中
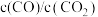 随温度变化的关系如图所示。下列说法正确的是
随温度变化的关系如图所示。下列说法正确的是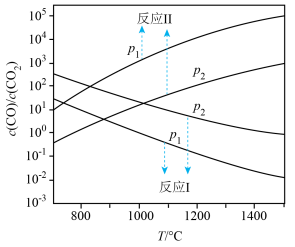
A.压强大小: |
B.在如图所示条件下,反应I可表示为  |
C.选择反应Ⅱ的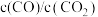 小于反应I的条件,将C与ZnO置于同一密闭容器中,碳热还原氧化锌反应能顺利进行 小于反应I的条件,将C与ZnO置于同一密闭容器中,碳热还原氧化锌反应能顺利进行 |
D.一定条件下将C与ZnO置于同一密闭容器中反应,当 时,增大 时,增大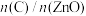 的值,可减少平衡时气体中 的值,可减少平衡时气体中 的含量 的含量 |
您最近一年使用:0次
2023-06-02更新
|
662次组卷
|
3卷引用:江苏省扬州市2023届高三下学期三模化学试题
名校
解题方法
5 . 二甲醚催化制备乙醇主要涉及以下两个反应:
反应Ⅰ:CO(g)+CH3OCH3(g) CH3COOCH3(g)△H1<0
CH3COOCH3(g)△H1<0
反应Ⅱ:CH3COOCH3(g)+2H2(g) CH3CH2OH(g)+CH3OH(g)△H2<0
CH3CH2OH(g)+CH3OH(g)△H2<0
在固定 CO、CH3OCH3、H2的原料比、体系压强不变的条件下,同时发生反应Ⅰ、Ⅱ, 平衡时各物质的物质的量分数随温度的变化如图所示。下列说法正确的是
反应Ⅰ:CO(g)+CH3OCH3(g)
 CH3COOCH3(g)△H1<0
CH3COOCH3(g)△H1<0反应Ⅱ:CH3COOCH3(g)+2H2(g)
 CH3CH2OH(g)+CH3OH(g)△H2<0
CH3CH2OH(g)+CH3OH(g)△H2<0在固定 CO、CH3OCH3、H2的原料比、体系压强不变的条件下,同时发生反应Ⅰ、Ⅱ, 平衡时各物质的物质的量分数随温度的变化如图所示。下列说法正确的是

| A.曲线 B 表示 H2的物质的量分数随温度的变化 |
| B.600 K 后升高温度,CH3COOCH3的物质的量分数降低原因是反应Ⅱ平衡右移 |
| C.测得 X 点 CH3CH2OH 的物质的量分数是 10%,则 X 点反应Ⅱ有:v 正>v 逆 |
| D.其他条件不变,延长反应时间能提高平衡混合物中乙醇含量 |
您最近一年使用:0次
2023-04-15更新
|
309次组卷
|
5卷引用:江苏省连云港市赣榆区2022-2023学年高二下学期4月期中考试化学试题
解题方法
6 . 优化焦炭水蒸气重整工艺可制得CO含量较低的氢燃料。0.1 MPa下,按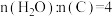 向容器中加入一定量的焦炭和水蒸气。体系中发生如下反应:
向容器中加入一定量的焦炭和水蒸气。体系中发生如下反应:
反应I:
 kJ⋅mol
kJ⋅mol
反应II:
 kJ⋅mol
kJ⋅mol
反应III:
 kJ⋅mol
kJ⋅mol
达到平衡时, 的产率和CO、
的产率和CO、 、
、 干态体积分数(
干态体积分数( )随温度变化如图所示。下列说法
)随温度变化如图所示。下列说法不正确 的是

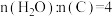 向容器中加入一定量的焦炭和水蒸气。体系中发生如下反应:
向容器中加入一定量的焦炭和水蒸气。体系中发生如下反应:反应I:

 kJ⋅mol
kJ⋅mol
反应II:

 kJ⋅mol
kJ⋅mol
反应III:

 kJ⋅mol
kJ⋅mol
达到平衡时,
 的产率和CO、
的产率和CO、 、
、 干态体积分数(
干态体积分数( )随温度变化如图所示。下列说法
)随温度变化如图所示。下列说法
| A.曲线B表示CO干态体积分数随温度的变化 |
| B.制备CO含量低的氢燃料应选择800℃左右的温度 |
C.800~1400℃,随温度升高 的产率降低,是因为温度升高对反应II的平衡转化率的影响大于对反应I平衡转化率的影响 的产率降低,是因为温度升高对反应II的平衡转化率的影响大于对反应I平衡转化率的影响 |
D.1200℃时,向平衡体系中通入水蒸气,再次达到平衡时 的值比原平衡的小 的值比原平衡的小 |
您最近一年使用:0次
名校
7 . 在恒容密闭容器中充入一定量的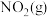 和
和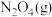 ,发生反应N2O4(g)⇌2NO2(g)
,发生反应N2O4(g)⇌2NO2(g)  ,体系中各物质的百分含量与温度的变化关系如图所示,
,体系中各物质的百分含量与温度的变化关系如图所示,

下列说法错误的是
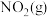 和
和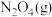 ,发生反应N2O4(g)⇌2NO2(g)
,发生反应N2O4(g)⇌2NO2(g)  ,体系中各物质的百分含量与温度的变化关系如图所示,
,体系中各物质的百分含量与温度的变化关系如图所示,
下列说法错误的是
A.曲线①表示 的百分含量 的百分含量 |
B. 的键能总和大于 的键能总和大于 的键能总和 的键能总和 |
C.若 点为反应平衡点,此时平衡常数 点为反应平衡点,此时平衡常数 |
| D.反应达到平衡后,往该容器中充入少量N2O4,N2O4转化率减小 |
您最近一年使用:0次
2021-11-03更新
|
130次组卷
|
2卷引用:江苏省江阴市华士高级中学2023-2024学年高二上学期12月学情调研化学(选修)试卷
名校
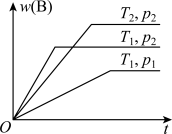
8 . 密闭容器中进行的可逆反应aA(g)+bB(g)⇌cC(g)在不同温度(T1和T2)及压强(p1和p2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示。下列判断正确的是( )

| A.T1<T2,p1<p2,a+b>c,正反应为吸热反应 |
| B.T1>T2,p1<p2,a+b<c,正反应为吸热反应 |
| C.T1<T2,p1>p2,a+b<c,正反应为吸热反应 |
| D.T1>T2,p1>p2,a+b>c,正反应为放热反应 |
您最近一年使用:0次
2020-05-08更新
|
392次组卷
|
25卷引用:江苏省南京市雨花台中学2020-2021学年高二年级上学期期末调研测试化学试题
江苏省南京市雨花台中学2020-2021学年高二年级上学期期末调研测试化学试题2016-2017学年新疆生产建设兵团二中高二上期中化学卷新疆呼图壁县第一中学2017-2018学年高二上学期期中考试化学试题新疆维吾尔自治区昌吉市第四中学2018-2019学年第一学期高二第一次月考化学试题内蒙古自治区翁牛特旗乌丹第一中学2018-2019学年高二上学期期中考试化学试题新疆自治区昌吉市第九中学2018-2019学年高二上学期第二次月考化学试题四川省宁南中学2018-2019学年高二下学期第一次月考化学试题山东省实验中学2020届高三第一次诊断性考试化学试题云南省玉溪市玉溪一中2019-2020学年高二上学期第一次月考化学试题(已下线)专题7.2 化学平衡状态 化学平衡移动(讲)-《2020年高考一轮复习讲练测》步步为赢 高二化学寒假作业:作业五 化学平衡的图像分析黑龙江省哈尔滨市第六中学2019-2020学年高二上学期期末考试化学试题甘肃省天水市甘谷第一中学2019-2020学年高二下学期开学考试化学试题湖北省新高考联考协作体2020-2021学年高二上学期期中考试化学试题贵州省毕节市七星关区毕节市实验高级中学2020-2021学年高二上学期期中考试化学试题重庆市朝阳中学高2020-2021学年高二上学期期中考试化学试题甘肃省永昌县第一高级中学2020-2021学年高二上学期期末考试化学试题广东省大埔县虎山中学2022-2023学年高三上学期1月期末考试化学试题河北省承德县第一中学2022-2023学年高一下学期期末考试化学试题北京市东直门中学2022-2023学年高二上学期期中考试化学试题北京工业大学附属中学2023-2024学年高二上学期期中考试化学试题四川省达州市宣汉县第二中学2023-2024学年高二上学期中期考试化学试题四川省内江市2025届第三中学高二上学期化学试卷四川省自贡市第二十二中学校2023-2024学年高二上学期期中考试化学试题上海市建平世纪中学2023-2024学年高二上学期阶段练习二 化学(等级)试题
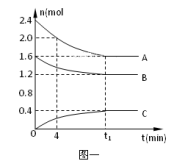
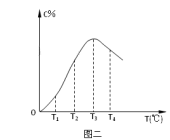
9 . 在10L密闭容器中,A、B、C三种气态物质构成了可逆反应体系;某温度时,A、B、C物质的量与时间的关系如图一,C的百分含量与温度的关系如图二。下列分析不正确的是


A.0~4 时,A的平均反应速率为0.01mol/(L·min) 时,A的平均反应速率为0.01mol/(L·min) |
B.该反应的平衡常数表达式为: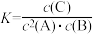 |
| C.由T1向T2变化时,v正>v逆 |
| D.此反应的正反应为吸热反应 |
您最近一年使用:0次
名校
解题方法
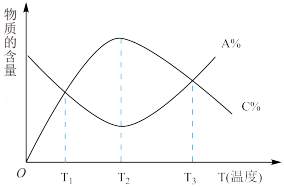
10 . 经一定时间后,可逆反应aA+bB cC中物质的含量A%和C%随温度的变化曲线如图所示。下列说法正确的是( )
cC中物质的含量A%和C%随温度的变化曲线如图所示。下列说法正确的是( )
 cC中物质的含量A%和C%随温度的变化曲线如图所示。下列说法正确的是( )
cC中物质的含量A%和C%随温度的变化曲线如图所示。下列说法正确的是( )
| A.该反应在T1、T3温度时达到化学平衡 |
| B.该反应在T2温度时达到化学平衡 |
| C.该反应的逆反应是放热反应 |
| D.升高温度,平衡会向正反应方向移动 |
您最近一年使用:0次
2020-08-19更新
|
393次组卷
|
42卷引用:2018版化学(苏教版)高考总复习专题七题型冲关--巧解平衡及速率图像题
2018版化学(苏教版)高考总复习专题七题型冲关--巧解平衡及速率图像题(已下线)2010年云南省昆明一中高三上学期第一次月考化学试题(已下线)2011届内蒙古包头一中高三第一次模拟考试(理综)化学部分(已下线)2011-2012学年辽南协作体高二上学期期中考试化学试卷(已下线)2012-2013学年吉林省实验中学高二上学期期末考试化学试卷(已下线)2012-2013福建省上杭一中高二上学期期中考试化学理试卷(已下线)2014-2015学年福建三明市一中高二上第一次月考化学试卷2015届山东省日照市高三12月校际联合检测化学试卷2015-2016学年湖北省荆州中学高二上第一次月考化学试卷2015-2016学年江西省临川一中高二上第一次月考化学试卷2015-2016学年山东省平度市高二上学期直升班抽考化学试卷2015-2016学年山东省青岛市平度市高二上学期教学质检化学试卷2015-2016学年江西省上高二中高二下4月月考化学试卷2015-2016学年江西省吉安市一中高二下学期期中化学试卷2015-2016学年安徽省合肥中科大附中高二下期中理科化学试卷2015-2016学年湖南东部六校高一下期中化学试卷2015-2016学年浙江省杭州二中高二下期中化学试卷2015-2016学年云南临沧一中高二下学期期末考试化学卷2017届山西省康杰中学高三上学期10月月考化学试卷2016-2017学年湖北省武钢三中高二上月考一化学卷2016-2017学年江西省宜春市奉新一中高二上月考一化学试卷2016-2017学年天津市武清区等五区县高三上学期期中考试化学试卷安徽省淮北市第一中学2016-2017学年高一下学期期中考试化学试题1安徽省阜阳市临泉县第一中学2016-2017学年高二下学期学科竞赛化学试题江西省临川第二中学2018届高三上学期第四次月考(期中)化学试题四川省成都石室中学2017-2018学年高二10月月考化学试题山东省枣庄市第三中学2017-2018学年高二第六学段学情调查(1月)化学试题【全国百强校】黑龙江省哈尔滨市第三中学校2018-2019学年高二上学期第一次阶段性测试化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二上学期10月月考化学试题河北省安平中学2019-2020学年高二上学期第一次月考化学试题(已下线)专题7.3 化学平衡常数 化学反应进行的方向(练)-《2020年高考一轮复习讲练测》重庆市云阳县2019-2020学年高二上学期期中考试化学试题湖南省长沙市第一中学2019-2020学年高二上学期第一次月考化学试题黑龙江省哈尔滨师范大学附属中学2019-2020学年高二10月月考化学试题江西省赣州市南康中学2020-2021学年高二上学期第二次大考化学试题山东省济宁市微山一中2020-2021学年高二上学期第一次月考化学试题安徽省定远县育才学校2020-2021学年高二上学期第二次月考化学试题天津市部分区2020-2021学年高二上学期期中考试化学试题河南省郑州市第一〇六高级中学2020-2021学年高二上学期11月考试化学试题广东省揭阳市揭西县河婆中学2020-2021学年高二上学期第二次月考化学试题湖南省祁东县育贤中学2022-2023学年高二上学期第一次月考化学试题安徽省太和县第八中学2021-2022学年高二上学期第一次月考化学试题



